晚期新生儿呼吸窘迫综合征珂立苏应用剂量的研究
扎西吉,王正岭,马凤美,吕文华
(青海省妇女儿童医院新生儿科,青海西宁810000)
晚期新生儿呼吸窘迫综合征珂立苏应用剂量的研究
扎西吉,王正岭,马凤美,吕文华
(青海省妇女儿童医院新生儿科,青海西宁810000)
目的探讨珂立苏应用剂量对晚期新生儿呼吸窘迫综合征的影响。方法选取2014年7月-2015年12月青海省妇女儿童医院收治的新生儿呼吸窘迫综合征患儿95例,依据随机数表法分为大剂量组和小剂量组,比较用药前、用药后1、6、12及24 h两组患儿血氧分压(PaO2)、动脉血二氧化碳分压(PaCO2)、肺泡动脉氧分压差[P(A-a)O2]、吸入氧体积分数(FiO2)、氧合指数(OI)、X线评分及相关指标。结果大剂量组48例,治愈25例,好转21例,无效2例,总有效率为95.83%;小剂量组47例,治愈20例,好转19例,无效6例,死亡2例,总有效率为82.98%。用药前,两组患儿的PaO2、PaCO2、P(A-a)O2、FiO2、OI、X线评分差异无统计学意义(P>0.05)。大剂量组患儿在用药后1 h PaO2迅速恢复,且在用药后6、12及24 h持续上升。小剂量组患儿PaO2亦有所升高,但用药后1 h变化幅度并不明显,用药后24 h PaO2水平仍低于大剂量组。给药后1 h内,两组患儿的PaCO2均有所下降,但变化并不明显,至用药后6 h,患儿PaCO2较用药前降低,且在用药后12和24 h内维持稳定状态。给药后1 h,大剂量组患儿P(A-a)O2降至200 mmHg左右,小剂量组患儿的平均P(A-a)O2为(274.18±44.16)mmHg,组间差异有统计学意义(P<0.05)。用药后6h,两组患儿的P(A-a)O2差值最大,至24 h后仍有较大差距。用药后1、6、12及24 h,两组患儿的FiO2均降低,组间差异无统计学意义(P>0.05)。给予大剂量珂立苏后,患儿OI在较短时间内(用药后1 h)迅速下降,接近正常水平,而小剂量组患儿至用药后12 h逐渐恢复正常。用药后12 h大剂量组患儿X线评分降低,同时小剂量组患儿X线评分虽低于用药前,但与同时间点大剂量组患儿比较,仍有较大差异(P<0.05)。结论大剂量珂立苏治疗呼吸窘迫综合征成效显著,能够有效改善新生儿血气指标,具有安全可靠、临床操作性高的特点。
珂立苏;剂量;呼吸窘迫综合征;并发症;X线评分
肺表面活性物质由肺泡上皮细胞分泌,肺表面活性物质分泌不足可导致肺泡塌陷,肺顺应性降低[1-2]。呼吸窘迫综合征是指肺部功能障碍,血管组织液体交换功能减退引起的肺含水量增加、通气血流比值失调,患者主要表现为呼吸困难、低氧血症[3-4]。一般情况下,呼吸窘迫综合征多发生在胎龄不足37周的新生儿群体中,且胎龄越小,出现呼吸窘迫综合征的风险越大。珂立苏即牛肺表面活性剂,是从健康的新生小牛肺部分离出的肺表面活性物质,主要用于新生儿呼吸窘迫综合征的临床治疗[5]。长期的临床应用表明,珂立苏用于治疗呼吸窘迫综合征具有治愈率高、严重并发症少的特点,多数患儿可通过珂立苏建立正常呼吸。近年来,有关珂立苏给药剂量的争议越来越大,国内外学者均对新生儿呼吸窘迫综合征的临床用药持谨慎态度。本研究给予新生儿呼吸窘迫综合征患儿不同剂量的珂立苏,通过比较不同剂量下新生儿血气指标变化,旨在明确珂立苏最佳给药剂量,现分析报道如下。
1 资料与方法
1.1 一般资料
选取2014年7月-2015年12月于青海省妇女儿童医院收治的新生儿呼吸窘迫综合征患儿95例,依据随机数表法分为两组。大剂量组48例,其中,男25例,女23例;胎龄33~38周,平均(35.1±1.4)周;出生体重1 849~2 356 g,平均(2 084±389)g;小剂量组47例,其中男26例,女21例;胎龄32~37周,平均(34.8±1.6)周;出生体重1 877~2 421 g,平均(2 109±427)g。两组患儿的胎龄、性别、出生体重等一般资料差异无统计学意义(P>0.05)。
纳入标准:①符合呼吸窘迫综合征诊断标准[6],并经X线确诊;②胎龄≥32周;③出生体重≤2500g;④出生后12 h内入院;⑤所有患儿家属均知情同意;⑥经本院伦理委员会批准同意。
排除标准:①先天性心脏病或畸形;②心血管系统异常;③合并有全身感染性疾病;④重症颅脑出血;⑤临床资料不完整。
1.2 方法
1.2.1 大剂量组所有患儿均进行气管插管,确定珂立苏(华润双鹤药业股份有限公司公司,国药准字H20052128)无变色后进行复温,轻轻振荡混匀,制成均匀混悬液。将100 mg/kg珂立苏经气管给药,并进行正压通气,促进药物弥散,并根据患儿情况选择呼吸机辅助通气。用药后密切观察患儿生命体征和症状,呼吸窘迫症状未得到有效缓解或病情加重时加用珂立苏,最多使用3次。
1.2.2 小剂量组小剂量组患儿给药种类、方式等均与大剂量组一致,剂量由100mg/kg调整为40mg/kg。
1.3 观察指标
分别于用药前、用药后1、6、12及24h使用5700全自动血气分析仪(Instrumentation Laboratory Co.公司)测定患儿PaO2、PaCO2、P(A-a)O2、FiO2水平,记录呼吸机参数计算OI值,分别于用药前、用药后12和24 h进行胸X线检查,并由2位以上专业医师进行X线结果判断,X线评分标准:0分,无呼吸窘迫综合征;1分,呼吸窘迫综合征Ⅰ级;2分,呼吸窘迫综合征Ⅱ级;3分,呼吸窘迫综合征Ⅲ级;4分,呼吸窘迫综合征Ⅳ级。观察并记录两组患儿用药后的辅助通气时间、氧疗时间、住院时间、呼吸困难时间、珂立苏使用次数及并发症发生情况。
1.4 统计学方法
采用SPSS 19.0统计软件进行数据分析,计量资料用t检验,计数资料用χ2检验,计量结果用重复测量方差分析,P<0.05为差异有统计学意义。
2 结果
2.1 两组患儿的临床疗效比较
大剂量组48例,治愈25例,好转21例,无效2例,总有效率为95.83%;小剂量组47例,治愈20例,好转19例,无效6例,死亡2例,总有效率为82.98%。见表1。
2.2 两组患者用药前后PaO2比较
用药前,两组患儿的PaO2差异无统计学意义(P>0.05)。大剂量组患儿在用药后1 h PaO2迅速恢复,且在用药后6、12及24 h持续上升。小剂量组患儿PaO2亦有所升高,但用药后1 h变化幅度并不明显,用药后24h PaO2水平仍低于大剂量组。见表2。
2.3 两组患者用药前后PaCO2比较
用药前,两组患儿的PaCO2差异无统计学意义(P>0.05)。给药后1 h内,两组患儿的PaCO2均有所下降,但变化并不明显,至用药后6 h,患儿PaCO2较用药前降低,且在用药后12和24 h内维持稳定状态。见表3。
2.4 两组患者用药前后P(A-a)O2比较
用药前,两组患儿的P(A-a)O2差异无统计学意义(P>0.05)。给药后1 h,大剂量组患儿P(A-a)O2降至200 mmHg左右,小剂量组患儿的平均P(A-a)O2为(274.18±44.16)mmHg,组间差异有统计学意义(P<0.05)。用药后6 h,两组患儿的P(A-a)O2差值最大,至24 h后仍有较大差距。见表4。
2.5 两组患者用药前后FiO2比较
用药前,两组患儿的FiO2差异无统计学意义(P>0.05)。用药后1、6、12及24 h,两组患儿的FiO2均降低,组间差异无统计学意义(P>0.05)。见表5。
2.6 两组患者用药前后OI比较
用药前,两组患儿的OI差异无统计学意义(P>0.05)。给予大剂量珂立苏后,患儿OI在较短时间内(用药后1 h)迅速下降,接近正常水平,而小剂量组患儿至用药后12 h逐渐恢复正常。见表6。
2.7 两组患者用药前后X线评分比较
用药前,两组患儿的X线评分差异无统计学意义(P>0.05)。用药后12 h大剂量组患儿X线评分降低,同时小剂量组患儿X线评分虽低于用药前,但与同时间点大剂量组患儿比较,仍有较大差异(P<0.05)。见表7。
2.8 两组患儿辅助通气时间、氧疗时间、住院时间、呼吸困难时间及珂立苏使用次数比较
大剂量组患儿的辅助通气时间、氧疗时间、住院时间、呼吸困难时间及珂立苏使用次数均低于小剂量组(P<0.05)。见表8。
2.9 两组患儿并发症发生率比较
大剂量组肺炎5例,肺出血2例,脑室出血5例,肺疾病6例,气胸1例;小剂量组肺炎11例,肺出血4例,脑室出血7例,肺疾病7例,气胸1例,两组患儿的肺炎、肺出血发生率差异有统计学意义(P<0.05)。见表9。
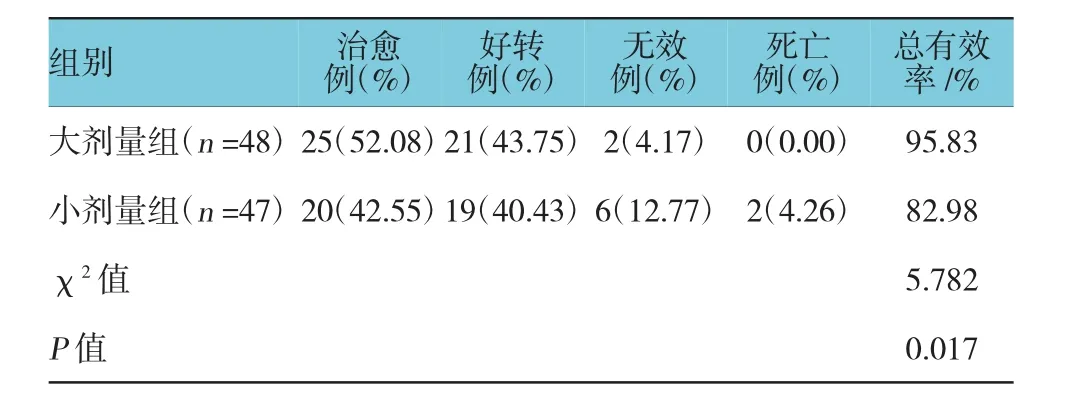
表1 两组患儿的临床疗效比较
表2 两组患者用药前后PaO2比较(mmHg,±s)

表2 两组患者用药前后PaO2比较(mmHg,±s)
组别用药后24 h大剂量组(n=48)58.32±12.6970.21±14.2572.06±12.1775.07±14.0276.63±13.76小剂量组(n=47)57.20±14.2862.09±13.3664.97±14.2866.17±12.6168.22±13.95 t值1.5422.1572.4792.0152.198 P值0.1370.0350.0140.0450.031用药前用药后1 h用药后6 h用药后12 h
表3 两组患者用药前后PaCO2比较(mmHg,±s)
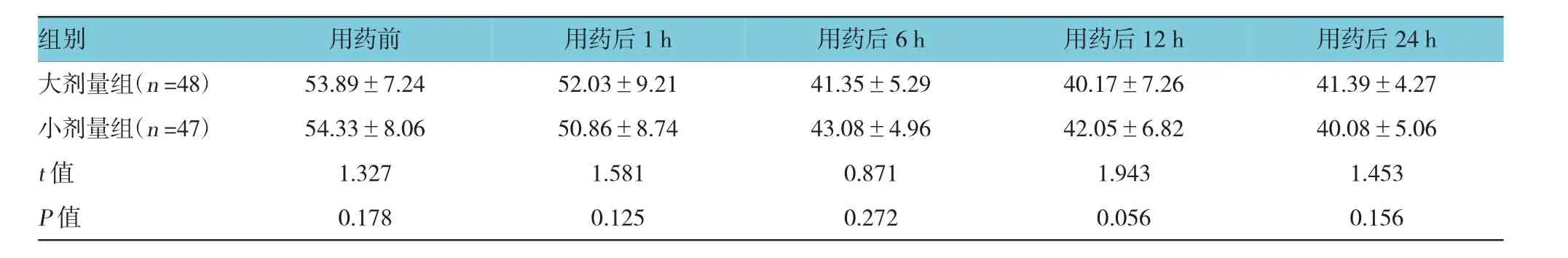
表3 两组患者用药前后PaCO2比较(mmHg,±s)
组别用药后24 h大剂量组(n=48)53.89±7.2452.03±9.2141.35±5.2940.17±7.2641.39±4.27小剂量组(n=47)54.33±8.0650.86±8.7443.08±4.9642.05±6.8240.08±5.06 t值1.3271.5810.8711.9431.453 P值0.1780.1250.2720.0560.156用药前用药后1 h用药后6 h用药后12 h
表4 两组患者用药前后P(A-a)O2比较(mmHg,±s)
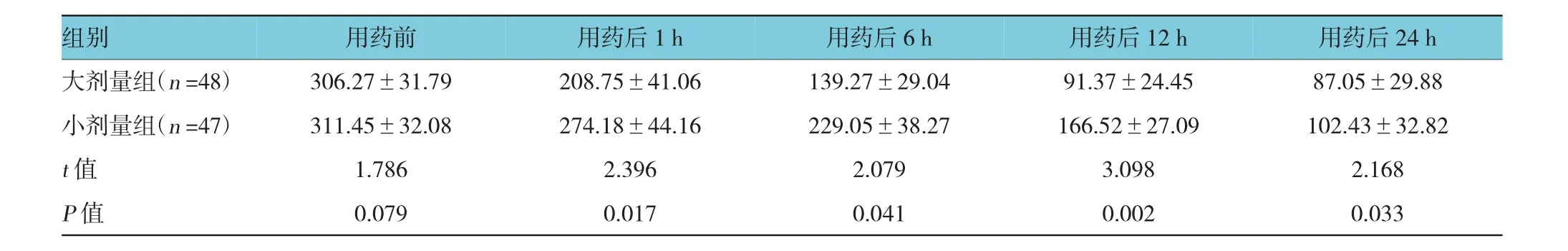
表4 两组患者用药前后P(A-a)O2比较(mmHg,±s)
组别用药后24 h大剂量组(n=48)306.27±31.79208.75±41.06139.27±29.0491.37±24.4587.05±29.88小剂量组(n=47)311.45±32.08274.18±44.16229.05±38.27166.52±27.09102.43±32.82 t值1.7862.3962.0793.0982.168 P值0.0790.0170.0410.0020.033用药前用药后1 h用药后6 h用药后12 h
表5 两组患者用药前后FiO2比较(%,±s)
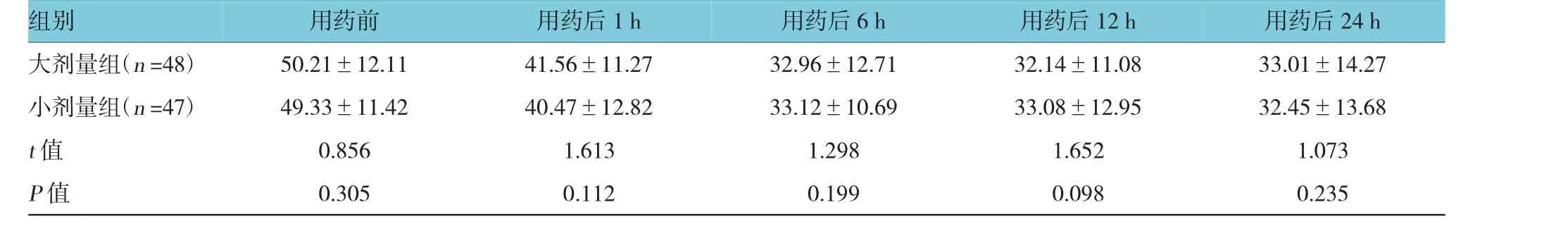
表5 两组患者用药前后FiO2比较(%,±s)
组别用药后24 h大剂量组(n=48)50.21±12.1141.56±11.2732.96±12.7132.14±11.0833.01±14.27小剂量组(n=47)49.33±11.4240.47±12.8233.12±10.6933.08±12.9532.45±13.68 t值0.8561.6131.2981.6521.073 P值0.3050.1120.1990.0980.235用药前用药后1 h 用药后6 h 用药后12 h
表6 两组患者用药前后OI比较(±s)

表6 两组患者用药前后OI比较(±s)
组别用药后24 h大剂量组(n=48)12.05±2.296.91±2.476.02±2.495.53±2.795.15±1.27小剂量组(n=47)11.96±2.458.25±3.967.48±3.626.85±3.146.34±2.08 t值1.7132.0932.8131.9722.306 P值0.0850.0380.0050.0490.021用药前用药后1 h用药后6 h用药后12 h
表7 两组患者用药前后X线评分比较(分,±s)
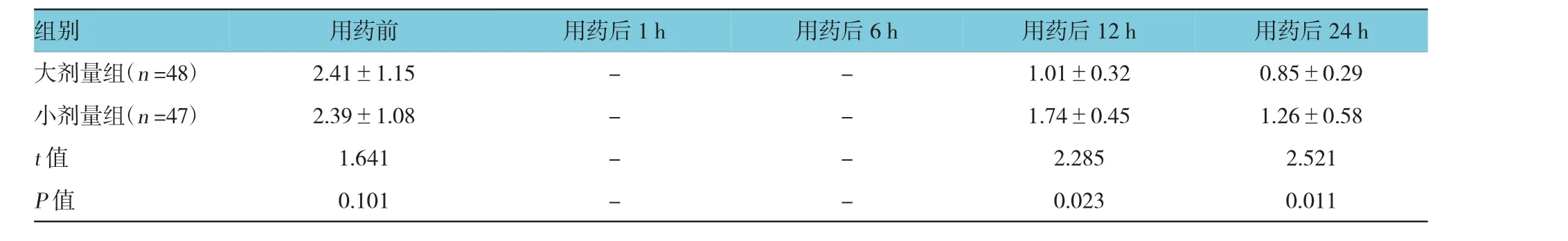
表7 两组患者用药前后X线评分比较(分,±s)
组别用药后24 h大剂量组(n=48)2.41±1.15--1.01±0.320.85±0.29小剂量组(n=47)2.39±1.08--1.74±0.451.26±0.58 t值1.641--2.2852.521 P值0.101--0.0230.011用药前用药后1 h用药后6 h用药后12 h
表8 两组患儿辅助通气时间、氧疗时间、住院时间、呼吸困难时间及珂立苏使用次数比较(±s)
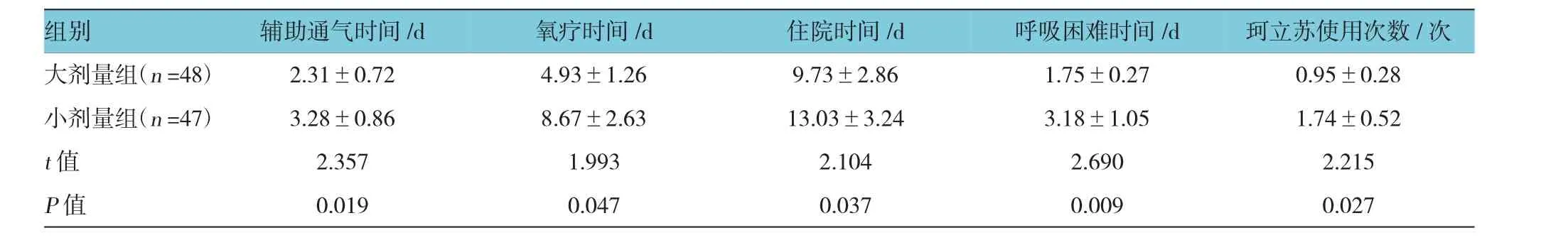
表8 两组患儿辅助通气时间、氧疗时间、住院时间、呼吸困难时间及珂立苏使用次数比较(±s)
组别珂立苏使用次数/次大剂量组(n=48)2.31±0.724.93±1.269.73±2.861.75±0.270.95±0.28小剂量组(n=47)3.28±0.868.67±2.6313.03±3.243.18±1.051.74±0.52 t值2.3571.9932.1042.6902.215 P值0.0190.0470.0370.0090.027辅助通气时间/d氧疗时间/d住院时间/d呼吸困难时间/d
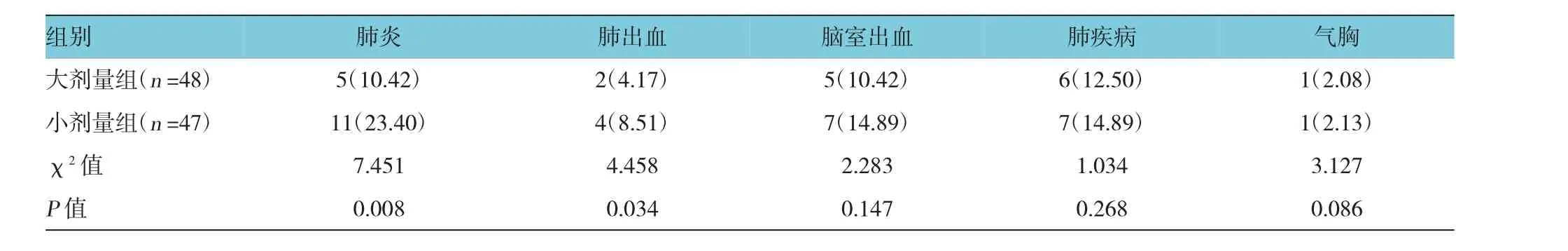
表9 两组患儿并发症发生率比较例(%)
3 讨论
JOHN借助膜天平确定了表面张力与气液界面表面积的关系,提出肺容积扩大时,肺表面张力升高,并首次将肺泡气液界面中具有降低肺表面张力作用的物质命名为“肺表面活性物质”。肺表面活性物质是一种复杂脂蛋白,主要成分为表面活性物质结合蛋白和二棕榈酰卵磷脂,分别占10%和60%左右,其主要生理功能包括:①维持肺泡容积稳定,避免肺泡萎缩;②降低肺部毛细支气管表面张力,降低毛细支气管阻塞或痉挛风险;③维持肺泡液体交换,避免发生肺水肿;④降低肺表面、肺毛细血管张力,增加肺通气量和肺顺应性,促进肺小动脉、肺泡扩张,保护肺泡上皮细胞[7-9]。与成人相比,新生儿尤其是早产儿肺泡发育不成熟,肺表面活性物质分泌不足,易导致肺毛细血管血流及淋巴回流减少,肺液清除速度降低,从而造成呼吸窘迫综合征。患有呼吸窘迫综合征的新生儿一般在出生后12 h内出现呼吸困难、呼吸衰竭等不良症状,且发病率、死亡率随着胎龄的减小而升高,是威胁早产儿生命健康的重要因素之一。珂立苏在新生儿呼吸窘迫综合征的临床应用中较为广泛,其安全性、有效性已得到国内外学者的一致认可[10-11]。但是现有文献中关于珂立苏剂量对治疗效果的影响的数据较少,临床上使用珂立苏治疗新生儿呼吸窘迫综合征尚无统一标准。本次研究对不同剂量下新生儿呼吸窘迫综合征患儿的血气指标、治疗后并发症等进行全面比较,结果如下。
研究数据显示,大剂量组治疗有效率高达95.83%,且无新生儿死亡,小剂量组总有效率为82.98%,出现2例死亡病例,提示大剂量珂立苏能够进一步提高新生儿呼吸窘迫综合征治愈率,降低临床死亡率。新生儿发生呼吸窘迫综合征的主要原因是缺乏肺表面活性物质,早在1980年,日本学者FUJIWARA首次通过小牛肺表面活性物质制剂治疗早产儿呼吸窘迫综合征,并获得成功,表明外源性肺表面活性物质能够有效治疗呼吸窘迫综合征。有报道称,新生儿呼吸窘迫综合征早期并无明显症状,不足以引起重视,但是该病进展迅速,发现时患儿症状已相当严重。因此,及时补充足量外源性肺表面活性物质可能是恢复患儿肺功能,挽救患儿生命的重要手段。大剂量珂立苏在新生儿呼吸窘迫综合征的临床治疗上有明显优势,这是因为足量珂立苏的注入能够延长药物半衰期,增加药效,对抢救急性呼吸衰竭新生儿更为有利。
目前,临床上常用的呼吸衰竭综合征诊断方法包括血液生化检查和X线检查,为了全面评估不同剂量对新生儿呼吸窘迫综合征的影响,本研究对两组患儿的血气指标进行定时检测。PaO2反映氧分子溶解于血液产生的压力,与细胞利用氧效能密切相关。新生儿表现出呼吸窘迫综合征的临床症状时,肺脏血管组织的液体交换功能已出现不同程度的损伤,此时患儿肺泡表面张力急速扩增,而进入肺部的空气很少,从而引发通气不良,造成PaO2降低[12-14]。本次研究对两组患儿给予不同剂量的珂立苏,其中大剂量组患儿在用药后1 h PaO2迅速恢复,且在用药后6、12及24h持续上升。小剂量组患儿PaO2亦有所升高,但用药后1 h变化幅度并不明显,用药后24 h PaO2水平仍低于大剂量组,可见在早期使用足量珂立苏能够迅速提高细胞利用氧效能,避免呼吸衰竭等不良后果。与PaO2不同,PaCO2反映的是肺泡的通气质量,是人体呼吸酸碱平衡的重要评定指标。这是因为,二氧化碳CO2弥散能力较强,肺泡中的CO2含量与血液基本持平,因此临床上可通过测定PaCO2判断肺泡通气情况。本次研究发现,给药后1 h内,两组患儿的PaCO2均有所下降,但变化并不明显,至用药后6 h,患儿PaCO2较用药前降低,且在用药后12和24 h内维持稳定状态。本研究认为,新生儿呼吸窘迫综合征患儿肺部功能减弱,CO2在较短时间内潴留,代偿作用无法及时调节,而当CO2含量超过某一水平时,机体呼吸中枢对PaCO2的调节作用基本暂停,由于此时患儿呼吸中枢对CO2的反应较弱,在给予珂立苏后其功能需要一段合理时间才能恢复,因此与PaO2比较,PaCO2的恢复期更长。P(A-a)O2是指肺泡氧分压与动脉血氧分压的差值,能够准确反映肺换气功能是否正常,较PaO2、PaCO2更为敏感。P(A-a)O2升高主要见于呼吸窘迫综合征、肺不张等急性肺疾病中,结合PaO2变化可判断肺部疾病进展情况,具体而言,当P(A-a)O2升高而PaO2未降低时,表明肺泡通气量明显增加,但当P(A-a)O2升高且PaO2降低时,患者肺部病变已严重影响氧合作用,出现氧弥散障碍。本组病例显示,用药前两组患儿的P(A-a)O2高达300 mmHg,表明新生儿呼吸窘迫综合征患儿肺部通气量明显不足,极易出现肺不张、呼吸衰竭等不良事件。给药后1h,大剂量组患儿P(A-a)O2降至200mmHg左右,小剂量组患儿的平均P(A-a)O2为(274.18±44.16)mmHg,组间差异有统计学意义(P<0.05)。用药后6 h,两组患儿的P(A-a)O2差值最大,至24 h后仍有较大差距,表明大剂量珂立苏在治疗新生儿呼吸窘迫综合征方面具有明显优势。OI是机体氧合作用的反映指标,研究证明,当OI值低于正常水平时,即便加大吸入气氧浓度仍无法有效纠正氧合作用,因此与PaO2相比,OI对呼吸窘迫综合征治疗效果的评估价值更为客观。结果显示,给予大剂量珂立苏后,患儿OI在较短时间内(用药后1 h)迅速下降,接近正常水平,而小剂量组患儿至用药后12 h逐渐恢复正常。X线检查对新生儿呼吸窘迫综合征的判断非常重要,X线下患儿两侧肺野透亮度下降,存在网状阴影及细小颗粒,肺不张进一步扩大时,肺野出现毛玻璃样改变,肺部呈现弥漫性浸润阴影[15-16]。为了在掌握胸片动态变化的同时降低X线照射对患儿的影响,仅在用药后12和24h进行X线复查。结果发现用药后12 h大剂量组患儿X线评分降低,同时小剂量组患儿X线评分虽低于用药前,但与同时间点大剂量组患儿比较,仍有较大差异。
另外数据显示大剂量组患儿治疗期间辅助通气时间、氧疗时间均高于小剂量组,表明与小剂量比较,大剂量珂立苏能够更为快速地帮助患儿肺部功能恢复,建立正常呼吸。由于大剂量珂立苏药效更强,作用时间更长,患儿呼吸窘迫综合征的临床症状能够在较短时间内得到有效缓解,从而缩短呼吸困难持续时间和住院时间。研究中发现,部分小剂量组患儿需要接受2、3次的药物注射才能取得良好的治疗效果,不仅延长住院时间,还对患儿自身免疫功能产生不利影响。因此,建议临床医师在确保患儿安全的前提下尽量使用100 mg/kg以上的剂量,以达到更好的治疗效果。珂立苏自研发成功起经历了长达18年之久的临床试验,其安全性得到了国内外学者的一致认可。即便如此,临床上给药过程中仍出现不良反应,其中由于气道阻塞引起的并发症占总体的33.33%,包括呛咳、呼吸暂停等。本次研究中,两组患儿均出现肺炎、脑出血、脑室出血、肺疾病、气胸等并发症,且肺炎、肺出血发生率的组间差异有统计学意义,表明大剂量珂立苏并不增加新生儿呼吸窘迫综合征并发症风险,有较高安全性。
综上所述,大剂量珂立苏治疗呼吸窘迫综合征成效显著,能够有效地改善新生儿血气指标,具有安全可靠、临床操作性高的特点。但是,除药物种类、给药剂量外,患儿体质量、胎龄、给药途径等均在一定程度上影响治疗效果,期待更严谨的实验研究,为珂立苏治疗新生儿呼吸窘迫综合征的最佳给药剂量、途径提供科学的参考依据。
[1]曹昕,周克兵.盐酸戊乙奎醚对多发伤致急性肺损伤患者血浆肺表面活性物质相关蛋白D、肿瘤坏死因子α和白细胞介素8水平的影响[J].中国现代医学杂志,2015,25(16):58-61.
[2]ISSAC M S M,ASHUR W,MOUSA H.et al.Genetic polymorphisms of surfactant protein D rs2243639,interleukin(IL)-1β rs16944andIL-1RN rs2234663inchronicobstructivepulmonary disease,healthy smokers,and non-smokers[J].Molecular Diagnosis&Amp,Therapy,2014,18(3):343-354.
[3]钱程,谷天祥,修宗谊,等.肺复张在体外循环心脏术后早期急性肺损伤-急性呼吸窘迫综合征患者的疗效观察[J].中国现代医学杂志,2013,23(6):69-72.
[4]KIM H S,LEE E S,CHO Y J.et al.Insufficient serum levels of antituberculosis agents during venovenous extracorporeal membrane oxygenation therapy for acute respiratory distress syndrome in a patient with miliary tuberculosis[J].ASAIO Journal,2014, 60(4):484-486.
[5]周家仍.固尔舒、珂立苏联合经鼻间歇正压通气治疗新生儿呼吸窘迫综合征的疗效比较[J].医学综述,2013,19(24):4597-4599.
[6]任雪云,王瑜,张伟伟,等.经鼻双水平正压通气和经鼻持续气道正压通气治疗早产儿呼吸窘迫综合征疗效观察[J].山东医药,2015, 4:69-71.
[7]杨一民.气管插管-肺表面活性物质-拔管后经鼻持续正压通气模式治疗新生儿呼吸窘迫综合征的临床疗效研究[J].中国全科医学,2013,16(10):1134-1136.
[8]李欣颖.新生儿呼吸窘迫综合征(N RDS)肺表面活性物质替代疗法的护理及效果观察[J].护士进修杂志,2015,30(15):1425-1427.
[9]赵有为,傅万海,覃晓菲,等.辅助通气方式对新生猪支气管肺泡灌洗液炎性因子及肺表面活性物质相关蛋白A的影响[J].中华实用儿科临床杂志,2013,28(6):411-413.
[10]郝明.固尔苏与珂立苏联合鼻塞型持续气道正压呼吸治疗新生儿急性呼吸窘迫综合征的效果研究[J].中国妇幼保健,2014,29(27): 4436-4438.
[11]葛标,张翔.珂立苏联合鼻塞持续气道正压呼吸治疗新生儿呼吸窘迫综合征疗效分析[J].安徽医药,2013,17(4):672-673.
[12]魏铭,钟强,甄海宁,等.乌司他丁联合连续性血液净化治疗急性呼吸窘迫综合征48例[J].医药导报,2015,34(7):910-913.
[13]廖积仁,刘玉婵,谭菁,等.经鼻同步间歇正压通气与经鼻持续正压通气治疗早产儿合并新生儿呼吸窘迫综合征的临床疗效研究[J].中华妇幼临床医学杂志:2014,10(4):511-515.
[14]孔令凯,孔祥永,李丽华,等.双水平正压通气和经鼻持续气道正通气在早产儿呼吸窘迫综合征INSURE治疗方式中应用的比较[J].中华妇幼临床医学杂志:电子版,2013,9(5):579-585.
[15]王小虎,姜红,牛世平,等.不同剂量牛肺表面活性物质治疗晚期早产儿呼吸窘迫综合征的临床研究[J].中国新生儿科杂志,2014, 29(1):43-45.
[16]程国涛.新生儿呼吸窘迫综合征临床及床头胸片分析[J].西部医学,2013,25(1):121-122.
(张西倩 编辑)
Study of Calsurf application dose for late neonatal respiratory distress syndrome
Xi-ji Za,Zheng-ling Wang,Feng-mei Ma,Wen-hua Lyu
(Department of Pediatrics,Qinghai Women and Children Hospital,Xining,Qinghai 810000,China)
ObjectiveTo investigate the effects of Calsurf application dose for late neonatal respiratory distress syndrome.MethodsNinety-five cases of neonatal respiratory distress syndrome in our hospital between July 2014 and December 2015 were selected,and divided into large-dose group and small-dose group according to a random number table.PaO2,PaCO2,P(Aa)O2,FiO2,OI and X line scores before treatment,1,6,12 and 24 h after treatment were compared between the two groups.ResultsAmong the 48 cases in the high-dose group,25 cases were cured, 21 cases were improved,2 cases did not get curative effect,the total effective rate was 95.83%;while among the 47 cases of the low-dose group,20 cases were cured,19 cases were improved,6 cases had no curative effect,2 cases died,the total efficiency was 82.98%.Before treatment,PaO2,PaCO2,P(Aa)O2,FiO2,OI or X ray score was not significantly different between the two groups(P>0.05).In the high-dose group PaO2rapid recovered 1 h after treatment,and continued to rise 6,12 and 24 h after treatment;in the small-dose group PaO2also increased,but the change was not obvious 1 h after treatment,PaO2level was still significantly lower than that in the high-dose group 24 h after treatment.PaCO2reduced in both groups within 1 h after administration,but the change was notobvious;6 h after treatment PaCO2was significantly lower than that before treatment and maintained stable 12 and 24 h after administration.P(Aa)O2dropped to about 200 mmHg in the high-dose group 1 h after administration,and in the low-dose group,the average P(Aa)O2was(274.18±44.16)mmHg,the difference was statistically significant (P<0.05).P(Aa)O2had the biggest difference between the two groups 6 h after drug intake,there was still big difference 24 h after treatment.After treatment for 1,6,12 and 24 h,FiO2in the two groups was significantly lowered,the difference between the groups was not statistically significant(P>0.05).After administration of high doses of Calsurf,OI decreased rapidly 1 h after treatment to nearly normal level,while in the low dose group OI gradually returned to normal after 12 h.X-ray scores were significantly reduced in the high-dose group 12 h after administration,while X-ray scores in the small-dose group were significantly lower than those before treatment but there were still big differences from those in the high-dose group at the same time point(P<0.05).ConclusionsLarge-dose Calsurf has remarkable effect on respiratory distress syndrome.It can effectively improve neonatal blood indicators,and has the advantages of safety,reliability and high clinical operability.
Calsurf;dose;respiratory distress syndrome;complication;X line score
R722.1
:B
10.3969/j.issn.1005-8982.2017.02.022
1005-8982(2017)02-0113-06
2016-01-11

