NOBIAS PA1螯合树脂富集——ICP-MS定量测定近海水体中的稀土元素
梁 杰, 何会军, 麻洪良, 杨士凤, 张 劲, 2
NOBIAS PA1螯合树脂富集——ICP-MS定量测定近海水体中的稀土元素
梁 杰1, 何会军1, 麻洪良1, 杨士凤1, 张 劲1, 2
(1. 中国海洋大学 海洋化学理论与工程技术教育部重点实验室, 山东 青岛 266100; 2. 富山大学 大学院地球环境生命, 日本 富山 9308555)
稀土元素是海洋中一类极为重要的地球化学过程的示踪剂, 但因其浓度多在pmol/kg数量级, 分析测试一直是难点, 为了使稀土元素在海洋研究中得到更广泛的应用, 必须对海洋中低浓度的稀土元素进行准确测量。本研究建立了NOBIAS PA1螯合树脂富集—ICP-MS法, 可以对近海的小体积水样中的稀土元素进行高准确度、高精密度分析。研究表明, 调节样品溶液pH为4.59~4.69、清洗溶液为6 mL 0.05 mol/L NH4AC、洗脱溶液为2 mL 1 mol/L HNO3时, 实验测试条件为最优。本方法对稀土元素的回收率在94%~106%, 检出限范围为0.001~0.424 pmol/kg, 分析精密度优于5%(=5)。本研究所建立的方法, 可用于河水、海水与河口盐度梯度区稀土元素的分析。
稀土元素; NOBIAS PA1 螯合树脂; 固相萃取; 小体积; 近海水样
稀土元素(REEs)是由原子序数57至71(La~Lu)的镧系元素和39号元素铱(Y)组成。由于具有特殊的4f电子结构, 稀土元素间离子半径差别不大, 晶体化学性质相似, 且随原子序数变化呈有规律的变化[1]。除铈(Ce)和铕(Eu)性质比较特殊, REEs通常是以正三价形态存在。Ce3+在氧化条件下易于转变成Ce4+, 并以CeO2的形式存在, 形成Ce异常。Eu3+则在还原条件下易于转变成Eu2+, 形成Eu异常。由于REEs独特性质的存在, 其具有比单个微量元素示踪体系更好的示踪性, 被广泛用于指示海洋生物地球化学过程[2-5]。如REEs在河口过程[6-8]以及颗粒物-水界面的生物地球化学行为的应用[9-11]以及进行物源示踪、水团示踪分析等[12-14]。我国近海存在着非常复杂的水团构成, 如在东海就存在黑潮、台湾暖流、长江冲淡水、黄海冷水团等多个水团的交互作用[15-18]。对如此众多的水团构成进行解析, 并估算其比例构成与变异等, 是研究我国近海生态系统演变及其对人类活动、与全球气候变化的响应的基础。REEs还具有“类同位素”性质, 特别适合于多水团的构成解析[19-20], 但目前, 这方面的研究在我国近海还非常少[21-23]。REEs分析手段上的不足一直是困扰相关研究开展的重要因素。
电感耦合等离子体质谱法(ICP- MS)可以进行多元素分析, 但由于海水中的REEs的浓度在pmol/kg数量级, 且盐的含量很高, 因此直接测定会导致仪器雾化器阻塞、背景高、质谱干扰等问题[24], 从而导致灵敏度降低、准确度变差。因此必须对海水中的REEs进行预处理[25-26]。
常用的REEs方法包括有机溶剂萃取法[27-28]、共沉淀法[29-31]、固相萃取法[32-34]和离子色谱法[35]等。Nozaki等[28]和Zhang等[32]以HDEHP和 H2MEHP混合溶剂萃取法富集海水中的稀土元素, 该方法缺点在于需大量样品、消耗大量有机溶剂及操作繁琐等。而固相萃取法是目前应用比较广泛的方法。研究者用到的固相萃取树脂包括碳纳米管[36-37], 螯合纤维[32-33]和螯合树脂[38-39]。NOBIAS PA1螯合树脂(简称NOBIAS)是近年逐渐被研究者广泛接受的树脂之一, 该树脂有乙二胺四乙酸铵(EDTriA)基团和亚氨二乙酸(IDA)基团, 可以与金属离子形成5个配位键, 因此具有很好的亲和性。水体中的REEs通过螯合树脂在封闭空间中络合, 避免了引进污染的可能性。NOBIAS对水体中的REEs有着极佳的吸附性, 且负载树脂上REEs易被1mol/L硝酸洗脱, 重复利用性高[25]。同时, 使用该树脂前不需要进行功能团络合, 这显著区别于其他树脂[24]。因此NOBIAS被广泛应用于海水中微量金属元素的富集[40-41]。
本文以NOBIAS螯合树脂富集–ICP-MS法对中国近海水体中的REEs进行了分析, 对富集、分离纯化以及测定过程中的参数进行了优化选择, 旨在建立可以用于河流、河口及海洋环境中REEs的快速、准确测定的分析方法。
1 实验方法与样品采集
1.1 仪器与试剂
本实验方法用到的仪器包括ICP-MS (Thermo Fisher iCap Qc, 美国); 电子天平(赛多利斯MSE225P- 000-DU, 德国); pH计(赛多利斯PB-10, 德国); 蠕动泵(兰格LEAD-2-88, 中国); 超纯水处理系统(Elix 10+Milli-Q Reference, 德国)。
实验过程中所用到的低密度聚乙烯(LDPE)瓶和其他器皿均在反王水(HNO3︰HCl=3︰1)和3%的HCl中先后浸泡24 h, Milli-Q水洗至中性后超净台内晾干。
分析过程中所用的试剂均为痕量金属级, 浓硝酸(HNO3, Fisher Scientific, 68%~70%); 冰醋酸(HAc, Fisher Scientific); 氨水(NH4OH, Fisher Scientific)。所使用的元素标准溶液均为美国Inorganic Ventures公司生产: 铑标准溶液 1 000 μg/mL, 2.5%硝酸介质; 铟标准溶液 1 000 μg/mL, 2%硝酸介质; 铼标准溶液 1 000 μg/mL, 3%硝酸介质; 稀土单标溶液1 000 μg/mL, 5%硝酸介质; 稀土混标溶液100 μg/mL, 7.14%硝酸介质。
各溶液均以Milli-Q水(18.2 MΩ/cm)配制, 2% HNO3: 用电子天平称取浓硝酸14.3 g, 然后加入Milli-Q水至500 g; 1 mol/L HNO3: 用电子天平称取浓硝酸8.99 g, 然后加入Milli-Q水至100 g; 1︰1 NH4AC缓冲溶液: 按HAc: NH4OH: H2O =4︰5︰9的比例(质量比)称取配制; 0.05 mol/L NH4AC缓冲溶液配制: 量取1︰1 NH4AC缓冲溶液4 mL并稀释至500 mL。混合稀土标准溶液, 参照大洋REEs的浓度[10, 13], 用1000 μg/mL的稀土单标溶液混合配制而成; 标准曲线序列分别为Y、La、Ce、Nd: 0, 0.01, 0.1, 0.5, 5, 10, 50 μg/L; Pr、Sm: 0, 0.01, 0.1, 0.5, 1, 5, 10 μg/L; Eu、Gd、Tb、Dy: 0, 0.01, 0.05, 0.1, 0.5, 1, 5 μg/L; Ho、Er、Tm、Yb、Lu: 0, 0.01, 0.03, 0.05, 0.1, 0.3, 0.5 μg/L。
用于条件实验的海水样品分别采自长江口淡水端和东海。以X-Niskin采水器采集水样, 在超净工作台内以0.4 μm Whatman PC滤膜过滤, 滤液以超纯级HCl酸化到pH<1.5, 保存待用。实验过程中, 以NH4AC缓冲溶液调节到设定的pH, 然后进行条件实验。需要注意的是本研究样品量和所用试剂匀均为万分之一天平取, 因此单位为pmol/kg。
1.2 NOBIAS PA1螯合树脂
本研究中所使用的NOBIAS PA1螯合树脂是由日本日立公司生产, 该树脂有乙二胺四乙酸铵(EDTriA)基团和亚氨二乙酸(IDA)基团[40]。REEs和NOBIAS PA1螯合树脂络合方式如图1所示。新树脂在使用前需用3 mol/L HNO3去除其中的无机杂质, 约可以预处理200个海水样品。

图1 NOBIAS PA1螯合树脂的官能团结构(修改自Biller, 2012年)
1.3 ICP-MS
REEs分析所使用的仪器为Thermo Fisher iCap Qc ICP-MS, 操作条件如表1所示。ICP-MS测定REEs时, 轻稀土元素与H和O形成的多原子离子LREEO+或LREEOH+, 会干扰质量数相等的中、重稀土元素, Ba形成的多原子离子BaO+或BaOH+, 对REEs尤其是Eu元素测量形成干扰[42]。实验中通过调节仪器的样品气流量、辅助气流量、射频功率等使REEs和Ba的氧化率小于2%。ICP-MS分析采用内标元素铑、铟、铼用来校正分析信号的漂移, 对基体效应有明显的补偿作用[43]。

表1 稀土元素测量时ICP-MS的操作条件
1.4 预处理过程
REEs预处理流程如图2所示, 实验在千级超净实验室中完成, 实验过程如下。
清洗实验系统: 使用5 mL 1 mol/L HNO3、60 mL Milli-Q水清洗管路和萃取装置, 然后用约5 mL 0.05 mol/L NH4AC缓冲溶液调节NOBIAS柱pH。
富集REEs: 将调节好pH的水样以一定流速通过图2的装置, 样品中的REEs被富集到NOBIAS树脂柱上。然后以0.05 mol/L NH4AC缓冲溶液将富集装置中残余的Ca2+、Mg2+清洗出来[25-26]。
洗脱和测量REEs: 以1 mol/L HNO3溶液将富集在萃取柱上的REEs洗脱下来。然后通过ICP-MS对REEs进行测量。
1.5 样品采集
样品采集于2015年8月16日至8月23日, 采样站位如图3所示。以X-Niskin采水器采集水样, 在超净工作台内以0.4 μm Whatman PC滤膜过滤, 滤液以超纯级HCl酸化到pH<1.5。X-Niskin采水器和滤膜均严格按照痕量金属元素采样要求(GEOTRACES)进行清洗和处理。

图2 稀土元素富集和洗脱过程(修改自Sohrin)
2 结果与讨论
2.1 实验条件的优化
2.1.1 样品pH的最优选择
样品pH是影响螯合树脂萃取效率的主要因素之一。以往的研究表明, 使用NOBIAS 树脂萃取法富集海水中的痕量金属(例如Co、 Ni、 Cu、Zn、 Cd和Pb), 调节样品pH在4.5~8.0的范围内, 具有很好的回收率[40]。本研究调节样品溶液(河水)的pH范围为3.5~6.0(图4a), 结果表明在pH为4~6范围内, REEs的回收率为90%以上。由于pH在4~4.5之间各REEs的回收率差异较大, 因此细化4.5至4.8区间样品的pH条件(图4b), 结果表明pH在4.59~4.69, NOBIAS 树脂柱对REEs的萃取效率比较高, 为94%~102%。而调节样品溶液pH低于4.59和高于4.69时, 萃取效率要低于93%。因此本研究选择调节样品pH为4.59~4.69。
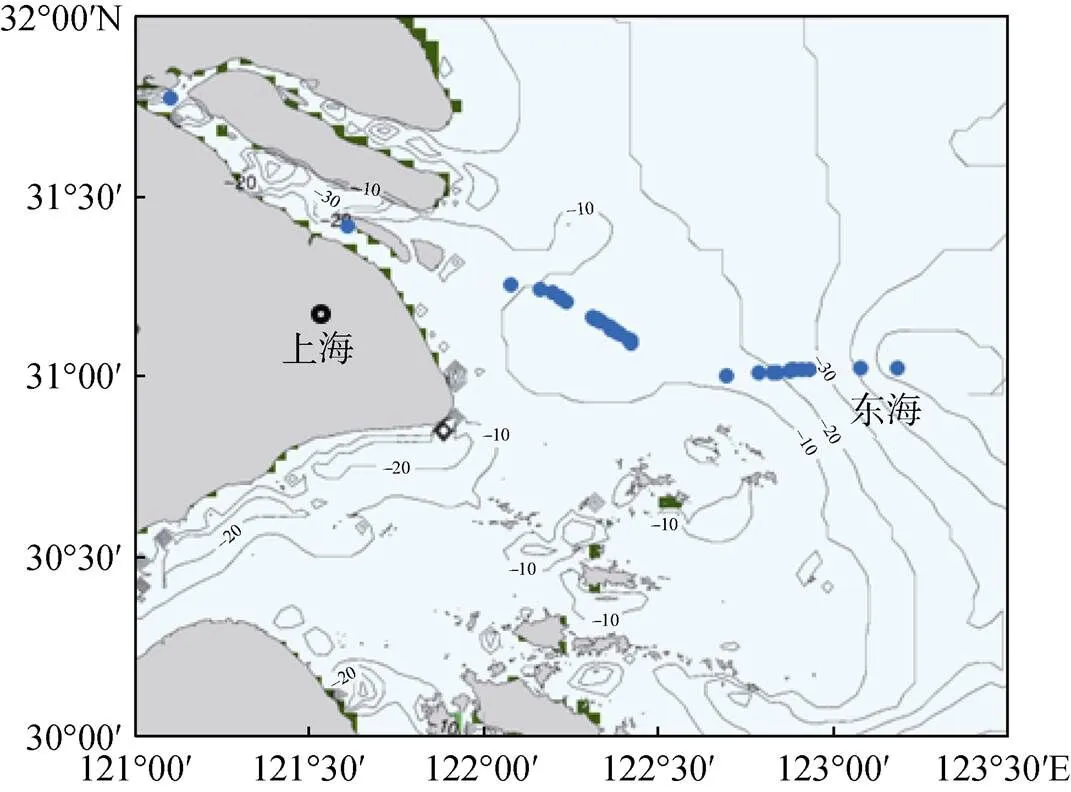
图3 长江口及其邻近东海海域的采样站位图

图4 不同样品溶液pH下NOBIAS 树脂对稀土元素的回收率
2.1.2 清洗液体积的选择
由于Mg2+、Ca2+在ICP中容易形成分子离子, 干扰REEs浓度的准确测定, 预处理过程中需要尽量去除样品中的Mg2+、Ca2+ [26]。为此以NOBIAS 树脂对样品中的REEs进行富集后, 需以适量的缓冲溶液将残留在萃取装置中的Mg2+、Ca2+清洗出来。本研究中, 选用东海水为实验对象, 对样品中的REEs进行富集后, 以不同体积0.05 mol/L NH4AC缓冲溶液对萃取装置进行了清洗。结果表明, 在清洗NH4AC缓冲溶液大于6 mL时, Mg2+、Ca2+的清除率非常高(图5)。

图5 清洗缓冲溶液体积量量对Mg2+、Ca2+去除率的影响
2.1.3 洗脱溶液体积的最优选择
本研究以1 mol/L HNO3溶液, 将螯合树脂中富集的REEs洗脱下来。样品REEs回收率随洗脱液体积的变化如图6所示。当洗脱液体积大于2 mL时, REEs回收率趋于稳定, 大于95%, 因此选择2 mL 1 mol/LHNO3溶液作为洗脱液。

图6 洗脱溶液量对稀土元素回收率的影响
2.2 方法的空白、检出限和精密度
对空白平行进行9次测定, 得到本方法的空白和检出限(3σ)如表2所示。大部分REEs的空白低于0.1 pmol/kg, 钇(Y)、镧(La)、铈(Ce)的空白稍高, 但大洋中Y、La、Ce和Dy的浓度分别为304、275、568和28.8 pmol/kg, 远高于本方法中Y(0.153 pmol/kg)、La(0.482 pmol/kg)、Ce(0.333 pmol/kg)和Dy(0.068 pmol/kg)的空白值。对取自海水端元的样品进行5次平行分析, REEs浓度为钇(Y)492 pmol/kg、镧(La)128 pmol/kg、铈(Ce)62.3 pmol/kg、镨(Pr)15.0 pmol/kg、钕(Nd) 63.4 pmol/kg、钐(Sm)13.2 pmol/kg、铕(Eu)3.31 pmol/kg、钆(Gd)19.6 pmol/kg、铽(Tb)2.90 pmol/kg、镝(Dy) 20.0 pmol/kg、钬(Ho)4.95 pmol/kg、铒(Er)15.6 pmol/kg、铥(Tm)2.13 pmol/kg、镱(Yb)12.4 pmol/kg、镥(Lu) 1.98 pmol/kg时, 方法的其相对标准偏差为如表2所示, 相对标准偏差均小于5%。

表2 空白平均值、检出限及样品相对标准偏差
2.3 方法的适用性
NOBIAS PA1螯合树脂和REEs的络合性主要取决于pH、离子强度以及样品中其他络合物的种类。尤其是Mg2+、Ca2+的存在会造成与稀土元素阳离子之间的竞争关系[26]。以本研究建立的分析方法, 在不同盐度条件下, 对水样中的REEs进行了分析, REEs的回收率(表3)与水样盐度间的关系如图7所示。结果表明, 在水样盐度0~34范围内, 本研究建立的分析方法对REEs的回收率在94%~106%。
3 长江口及其邻近海域的应用
以本研究所建立的分析方法, 对长江口及其邻近海域表层水体中的REEs成功进行了分析。REEs浓度随盐度的变化如图8所示。在河口低盐度区域, REEs浓度急剧降低。这很大程度上是由于有机胶体等发生絮凝作用附着到颗粒物上, 与胶体络合的REEs也会由溶解态清除出来, 使溶解态REEs浓度急剧降低[21]。盐度为5左右, 溶解态REEs的凸起峰, 可能为颗粒物解吸或其他源的输入[22]; 在盐度大于10后的区域内, 溶解态REEs浓度随盐度增加而增加, 是由于物理混合, 以及颗粒物部分溶解所致。
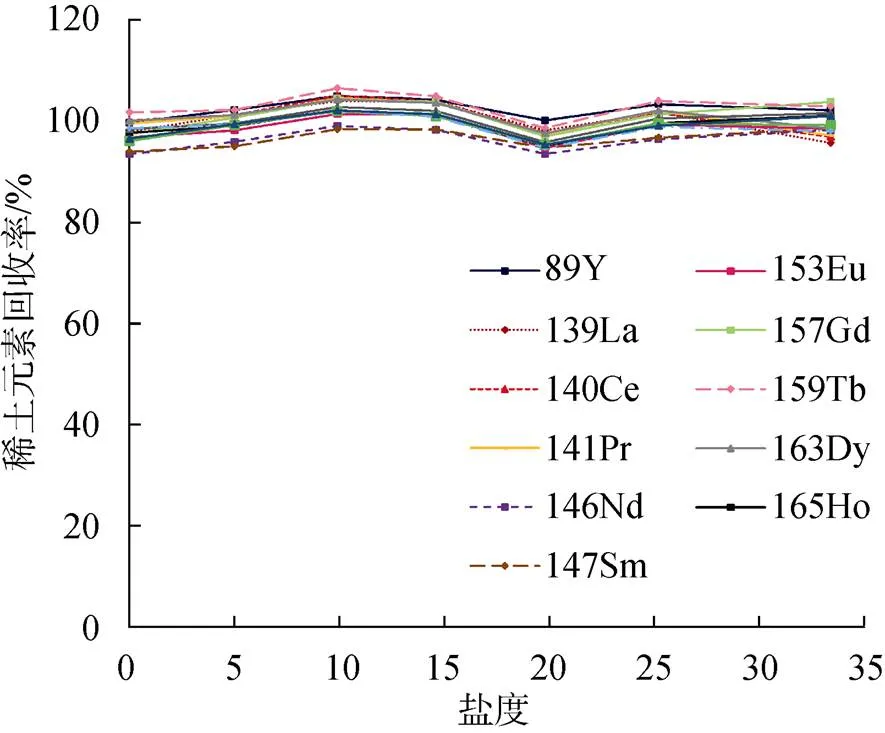
图7 盐度对稀土元素回收率的影响
图9为长江口不同盐度水样的溶解态REEs配分模式图。由图可知, 长江口水体混合过程中, 轻稀土和重稀土随盐度增加产生分异, 水体中重稀土元素与可溶性有机质以及无机阴离子络合形成稳定的络合物, 以小胶体形式存在于溶解态中, 而轻稀土元素与Fe、Mn、Al等金属氢氧化物胶体络合形成大胶体被吸附在颗粒物上[21], 分异程度随盐度增加而加深。

表3 盐度梯度样品稀土元素的回收率
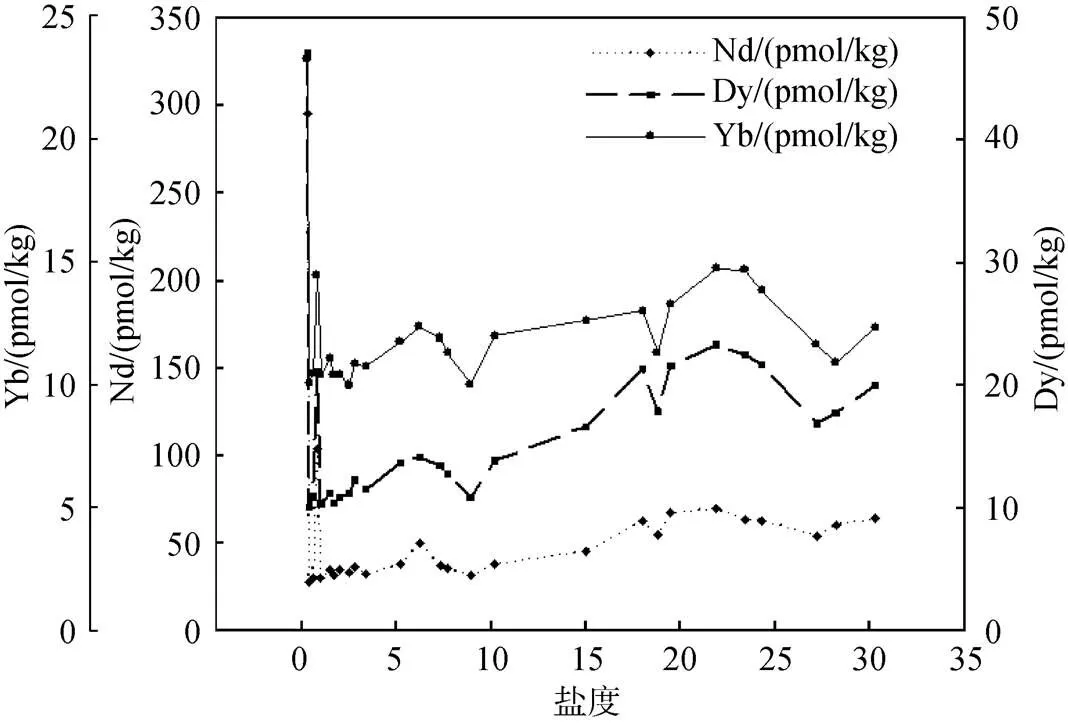
图8 长江口表层水体溶解态稀土元素随盐度梯度分布

图9 长江口表层水体PAAS标准化的溶解态稀土元素配分模式
4 结论
(1) NOBIAS PA1螯合树脂富集—ICP-MS法可以实现对近海水体中的REEs进行富集、分离纯化以及测定。本文建立的分析方法适用于河流、河口及海洋环境中REEs的快速、准确分析。该方法具有样品体积小、回收率高、空白低、检出限低和精密度好等优点。
(2) 以本研究所建立的NOBIAS PA1螯合树脂富集—ICP-MS法对长江口盐度梯度区水体样品中的REEs进行了分析, 结果表明REEs在长江口盐度梯度区具有系统性复杂的生物地球化学行为。在河水端元, 由于胶体絮凝作用, REEs浓度急剧降低; 在盐度5附近区域, 受颗粒物解吸或其他输入源的影响, 出现明显的浓度凸起峰; 在高盐度区域, 由于物理混合, 以及颗粒物部分溶解, 溶解态REEs浓度显著递升。
[1] 赵振华. 微量元素地球化学原理[M]. 北京: 科学出版社, 1997. Zhao Zhenhua. The geochemistry principle of trace element[M]. Beijing: Science Press, 1997.
[2] Hanson G N. Rare Earth Elements in Petrogenetic Studies of Igneous Systems[J]. Annual Review of Earth & Planetary Sciences, 1980, 8(1): 371-406.
[3] Banfield J F, Eggleton R A. Apatite replacement and rare earth mobilization, fractionation, and fixation during weathering[J]. Clays and Clay Minerals, 1989, 37(2): 113-127.
[4] Elderfield H, Upstill-Goddard R, Sholkovitz E R. The rare earth elements in rivers, estuaries, and coastal seas and their significance to the composition of ocean waters[J]. Geochimica et Cosmochimica Acta, 1990, 54(4): 971-991.
[5] Worrall F, Pearson D G. The development of acidic groundwaters in coal-bearing strata: Part I. Rare earth element fingerprinting[J]. Applied Geochemistry, 2001, 16(13): 1465-1480.
[6] Sholkovitz E R, Elderfield H. Cycling of dissolved rare-earth elements in Chesapeake bay[J]. Global Biogeochemical Cycles, 1988, 2(2): 157-176.
[7] Goldstein S J, Jacobsen S B. REE in the Great Whale River estuary, northwest Quebec[J]. Earth & Planetary Science Letters, 1988, 88(s 3–4): 241-252.
[8] Sholkovitz E R. The geochemistry of rare earth elements in the Amazon River estuary[J]. Geochimica Et Cosmochimica Acta, 1993, 57(10): 2181-2190.
[9] Sholkovitz E R. Chemical evolution of rare earth elements: Fractionation between colloidal and solution phases of filtered river water[J]. Earth & Planetary Science Letters, 1992, 114(1): 77-84.
[10] Takumi A, Eisaku I, Yoshinobu E, et al. Composition of rare earth elements in settling particles collected in the highly productive North Pacific Ocean and Bering Sea: Implications for siliceous-matter dissolution kinetics and formation of two REE-enriched phases[J]. Geochimica Et Cosmochimica Acta, 2011, 75(17): 4857- 4876.
[11] Akagi T. Rare earth element (REE)–silicic acid complexes in seawater to explain the incorporation of REEs in opal and the “leftover” REEs in surface water: New interpretation of dissolved REE distribution profiles[J]. Geochimica Et Cosmochimica Acta, 2013, 113(113): 174-192.
[12] Zhang J, Liu C Q. Major and rare earth elements in rainwater from Japan and East China Sea: natural and anthropogenic sources. Chem Geol[J]. Chemical Geology, 2004, 209(3): 315-326.
[13] Zhang J, Amakawa H, Nozaki Y. The comparative behavior of yttrium and lanthanides in the seawater of the North Pacific[J]. Geophysical Research Letters, 1994, 21(24): 2677-2680.
[14] Alibo D S, Nozaki Y. Rare earth elements in seawater: particle association, shale-normalization, and Ce oxidation[J]. Geochimica et Cosmochimica Acta, 1999, 63(3): 363-372.
[15] 吴晓丹, 宋金明, 李学刚. 长江口邻近海域水团特征与影响范围的季节变化[J]. 海洋科学, 2014, 38(12): 110-119. Wu Xiaodan, Song Jinming, Li xuegang. Seasonal variation of water mass characteristic and influence area in the Yangtze Estuary and its adjacent waters[J]. Marine Sciences, 2014, 38(12): 110-119.
[16] 赵瑞祥, 刘志亮. 台湾东北部黑潮表层水入侵东海陆架的季节变化规律[J]. 海洋科学, 2013, 37(7): 118- 123. Zhao Ruixiang, Liu Zhiliang. The seasonal variability of the Kuroshio surface water intrusion onto the East China Sea continental shelf derived from Argos drifter data[J]. Marine Sciences, 2013, 37(7): 118-123.
[17] Chen C T A, Wang S L. A salinity front in the southern East China Sea separating the Chinese coastal and Taiwan Strait waters from Kuroshio waters[J]. Continental Shelf Research, 2006, 26(14): 1636-1653.
[18] Zhang J, Liu S M, Ren J L, et al. Nutrient gradients from the eutrophic Changjiang (Yangtze River) Estuary to the oligotrophic Kuroshio waters and re-evaluation of budgets for the East China Sea Shelf[J]. Progress in Oceanography, 2007, 74(4): 449-478.
[19] Zhang J, Nozaki Y. Rare earth elements and yttrium in seawater: ICP-MS determinations in the East Caroline, Coral Sea, and South Fiji basins of the western South Pacific Ocean[J]. Geochimica Et Cosmochimica Acta, 1996, 60(23): 4631-4644.
[20] Zhang J, Nozaki Y. Behavior of rare earth elements in seawater at the ocean margin: a study along the slopes of the Sagami and Nankai troughs near Japan - ICP-MS determinations in the East Caroline, Coral Sea, and South Fiji basins of the western South Pacific Ocean[J]. Geochimica Et Cosmochimica Acta, 1998, volume 62(62): 1307-1317(11).
[21] 王中良, 刘丛强. 长江口水体混合过程中溶解态稀土元素分布特征[J]. 科学通报, 2000, 45(12): 1322- 1326. Wang Zongliang, Liu Congqiang. Distributions of dissolved rare earth elements during estuarine mixing at the Changjiang River mouth[J]. Chinese Science Bulletin, 2000, 45(12): 1322-1326.
[22] Wang Z L, Liu C Q. Geochemistry of rare earth elements in the dissolved, acid-soluble and residual phases in surface waters of the Changjiang Estuary[J]. Journal of Oceanography, 2008, 64(64): 407-416.
[23] Bai L L, Zhang J. Clarifying the Structure of Water Masses in East China Sea Using Low-Volume Seawater Measurement with Rare Earth Elements[J]. Advances in Geosciences, 2010, 18.
[24] 王美玲, Mitsuo Ito. NOBIAS chelate-PA1吸附剂固相萃取ICP-AES/ICP-MS测定高盐试样中的金属离子[C]// 2006全国核材料学术交流会论文集. 2006. Wang Meilin, Mitsuo Ito. Determination of metal ions in high-salt samples by ICP-AES/ICP-MS using Nobias-chelate PA1 adsorbent solid phase extraction[C]// Proceedings of the national academy of nuclear materials. 2006.
[25] Yoshiki S, Shouhei U, Seiji N, et al. Multielemental determination of GEOTRACES key trace metals in seawater by ICPMS after preconcentration using an ethylenediaminetriacetic acid chelating resin.[J]. Analytical Chemistry, 2008, 80(16): 6267-6273.
[26] Wang B S, Lee C P, Ho T Y. Trace metal determination in natural waters by automated solid phase extraction system and ICP-MS: The influence of low level Mg and Ca.[J]. Talanta, 2014, 128: 337-344.
[27] Shabani M B, Akagi T, Shimizu H, et al. Determination of trace lanthanides and yttrium in seawater by inductively coupled plasma mass spectrometry after preconcentration with solvent extraction and back-extraction[J]. Analytical Chemistry (Washington); (USA), 1990, 62: 24(24): 2709-2714.
[28] Nozaki Y, Alibo D S. Importance of vertical geochemical processes in controlling the oceanic profiles of dissolved rare earth elements in the northeastern Indian Ocean[J]. Earth & Planetary Science Letters, 2003, 205(3): 155-172.
[29] Piepgras D J, Wasserburg G J. Neodymium isotopic variations in seawater[J]. Earth & Planetary Science Letters, 1980, 50(1): 128-138.
[30] Greaves M J, Elderfield H, Klinkhammer G P. Determination of the rare earth elements in natural waters by isotope-dilution mass spectrometry[J]. Analytica Chimica Acta, 1989, 218(2): 265-280.
[31] Amakawa H, Sasaki K, Ebihara M. Nd isotopic composition in the central North Pacific[J]. Geochimica Et Cosmochimica Acta, 2009, 73(16): 4705-4719.
[32] Zhang T H, Shan X Q, Liu R X, et al. Preconcentration of Rare Earth Elements in Seawater with Poly (acrylaminophosphonic dithiocarbamate) Chelating Fiber Prior to Determination by Inductively Coupled Plasma Mass Spectrometry[J]. Analytical Chemistry, 1998, 70(18): 3964-3968.
[33] Wen B, Shan X Q, Xu S G. Preconcentration of ultratrace rare earth elements in seawater with 8-hydroxyquinoline immobilized polyacrylonitrile hollow fiber membrane for determination by inductively coupled plasma mass spectrometry[J]. Analyst, 1999, 124(4): 621-626.
[34] Fu Q, Yang L, Wang Q. On-line preconcentration with a novel alkyl phosphinic acid extraction resin coupled with inductively coupled plasma mass spectrometry for determination of trace rare earth elements in seawater[J]. Talanta, 2007, 72(4): 1248-1254.
[35] Haley B A, Klinkhammer G P. Complete separation of rare earth elements from small volume seawater samples by automated ion chromatography: method development and application to benthic flux[J]. Marine Chemistry, 2003, 82(82): 197-220.
[36] Liang P, Liu Y, Guo L. Determination of trace rare earth elements by inductively coupled plasma atomic emission spectrometry after preconcentration with multiwalled carbon nanotubes[J]. Spectrochimica Acta Part B Atomic Spectroscopy, 2005, 60(1): 125-129.
[37] Cho J, Chung K W, Man S C, et al. Analysis of rare earth elements in seawater by inductively coupled plasma mass spectrometry after pre-concentration using TSK™-HD-MW-CNTs (highly dispersive multi-walled carbon nanotubes)[J]. Talanta, 2012, 99: 369-374.
[38] Willie S N, Sturgeon R E. Determination of transition and rare earth elements in seawater by flow injection inductively coupled plasma time-of-flight mass spectrometry ☆[J]. Spectrochimica Acta Part B Atomic Spectroscopy, 2001, 56(9): 1707-1716.
[39] Kim I, Kim S, Kim G. Analytical Artifacts Associated with the Chelating Resin Extraction of Dissolved Rare Earth Elements in Natural Water Samples[J]. Aquatic Geochemistry, 2010, 16(4): 611-620.
[40] Biller D V, Bruland K W. Analysis of Mn, Fe, Co, Ni, Cu, Zn, Cd, and Pb in seawater using the Nobias- chelate PA1 resin and magnetic sector inductively coupled plasma mass spectrometry (ICP-MS)[J]. Marine Chemistry, 2012, s 130–131(1): 12-20.
[41] Hatje V, Bruland K W, Flegal A R. Determination of rare earth elements after pre-concentration using NOBIAS- chelate PA-1®resin: Method development and application in the San Francisco Bay plume[J]. Marine Chemistry, 2014, 160: 34-41.
[42] 曹心德, 尹明. 微波消解-电感耦合等离子体质谱法测定土壤中微量稀土元素[J]. 分析化学, 1999, 27(6): 679-683. Cao Xinde, Yin Ming. Determination of Trace Rare Earth Elements in Soils by Inductively Coupled Plasma-Mass Spectrometry After Microwave Digestion for Sample Preparation[J]. Chinese Journal of Analytical Chemistry, 1999, 27(6): 679-683.
[43] 胡圣虹, 林守麟, 刘勇胜, 等. 等离子体质谱法测定地质样品中痕量稀土元素的基体效应及多原子离子干扰的校正研究[J]. 高等学校化学学报, 2000, 21(3): 368-235. Hu Shenghong, Lin Soulin, Liu Yongsheng, et al. Studies on the Calibration of Matrix Effects and Polyatomic Ion for Rare Earth Elements in Geochemical Samples by ICP-MS[J]. Chemical Journal of Chinese Universities, 2000, 21(3): 368-235.
(本文编辑: 康亦兼)
Determination of REEs in the seawater adjacent to China using ICP-MS with a Nobias-chelate PA1 resin
LIANG Jie1, HE Hui-jun1, MA Hong-liang1, YANG Shi-feng1, ZHANG Jin1, 2
(1. Key Laboratory of Marine Chemistry Theory and Technology, Ministry of Education, Ocean University of China, Qingdao 266100, China; 2. Earth and Environmental System, University of Toyama, Toyama 9308555, Japan)
The concentration of rare earth elements (REEs) in seawater (pmol/kg) is generally estimated at the pmol/L level. As REEs are useful tools in the study of marine geochemistry, it is necessary to accurately determine their abundance in seawater. In this study, a highly sensitive and precise method is developed using the chelating resin Nobias-chelate PA1 in an offline preconcentration manifold. Magnetic sector detection using inductively coupled plasma mass spectrometry (ICP-MS) was used to analyze the REEs in coastal seawater samples. The optimal experimental parameters were determined when the pH ranges from 4.59–4.69, buffer volume is 6 mL, and elution volume is 2 mL. The detection limits of this method are 0.001 and 0.424 pmol/kg. The relative standard deviations (RSD) of the five replicate analyses of REEs in seawater were observed to be better than 5%. This method can be used to analyze REEs in rivers, estuaries, and seawater.
rare earth elements; NOBIAS-chelate PA-1; solid-phase extractions; small volume; the adjacent China seawater sample
Mar. 31, 2016
P734.2, P734.4
A
1000-3096(2017)10-0058-09
10.11759/hykx20160331006
2016-03-31;
2017-07-29
国家自然科学基金项目(41276071, 41530965)
[National Natural Science Foundation of China, No. 41276071, 41530965]
梁杰(1991-), 男, 山西交城人, 硕士研究生, 主要从事痕量元素生物地球化学研究, 电话: 0532-66782380, E-mail: liangjie19911009@ 163.com; 何会军, 通信作者, 电话: 0532-66782931, E-mail: he-hui- jun@163.com

