2011~2014年广州地区无偿献血者核酸检测结果分析
梁浩坚+汪传喜+许结仪+郑优荣+李仲平+蓝岚茵+林诗雅


[摘要]目的评估核酸检测技术应用于广州地区无偿献血者血液筛查的功效。方法采用Grifols公司(原诺华诊断公司)PROCLEIX TIGRIS全自动核酸检测分析系统和PROCLEIX ULTRIO HIV-1/HCV/HBVAssay核酸检测试剂,对2011年1月~2014年12月的1 146 740例无偿献血者血液标本进行HIV/HCV/HBV三项单人份核酸检测,同时采用血清学试剂进行HBsAg,HCVAb,HIVAb/Ag检测。对核酸检测单独反应性标本(血清学阴性,核酸检测反应性)进行鉴别试验以确定感染病毒种类。结果1146740例献血者血液标本,核酸检测的反应性比率为0.97%(10 645/1146 740),低于血清学HBsAg,HCVAb,HIVAbAg三项总的检测阳性率1.66%(19024/1146740)。在1114428例经血清学全项检测合格的标本中,单人份核酸检测共检出2457例核酸反应性样本,核酸单独反应性比率为0.22%;在2457例核酸单独反应性标本中,鉴别试验反应性的样本为718例,其中,HBV-DNA 711例,HCV-RNA4例,HIV-RNA 3例。核酸鉴别试验阳性率为29.22%(718/2457)。结论目前在广州地区输血传播疾病的残余风险主要还是输血感染HBV。核酸检测技术应用于血液筛查,将有助于缩短病原体检测的窗口期,降低输血残余风险,血清学和核酸检测两种方法互为补充,应同时使用以保障血液安全。
[关键词]核酸检测;血液筛查;输血风险;血液安全;转录介导扩增技术
输血相关传染病的预防和控制是全社会关注的焦点之一。2010年,国家卫生与计划生育委员会(原卫生部)确定在全国15家采供血机构开展核酸检测(NAT)试点工作,以进一步保证血液检测质量,提升我国无偿献血者血液检测水平。到目前NAT技术已经广泛运用于全国各地血站的血液筛检。该技术的检测灵敏度较ELISA检测方法高,能显著缩短病原体检测的窗口期,从而降低输血传播病毒的残余风险50%以上。但NAT技术从理论上并不能完全消除“窗口期”,国外已有经核酸检测后仍发生输血后感染的病例报道,包括HIV和HBV。本中心2010年11月正式将NAT技术应用于血液筛查项目中,对全部无偿献血者血液标本进行HBV DNA、HCV RNA和HIV RNA核酸检测。本研究通过对无偿献血者血液标本的常规血清学及核酸检测结果的分析,以评估核酸检测的检测功效,以及本地献血者人群的感染状况。现将检测结果报道如下。
1资料与方法
1.1一般资料
2011年1月~2014年12月,广州血液中心采集的无偿献血者血液标本1146740例。所有无偿献血者均符合现行的卫生部《献血者健康检查要求》(GB18467-2011)。血液采集后同时留取核酸检测标本和酶免检测标本管各一支。核酸检测标本采集、保存和处理等均严格按照卫生部核酸检测试点技术要求操作。
1.2主要仪器与试剂
核酸检测仪器:Grifols公司(原诺华诊断公司)PROCLEIX TIGRIS全自动核酸检测分析系统,试剂配置恒温箱(RPI)。试剂为PROCLEIXULTRIO Assay核酸联检试剂盒和核酸鉴别试剂盒(Discriminatory Assay)。核酸检测试剂批号:(593226,614952,624775,116153等)。血清学检测仪器:STAR全自动加样仪和全自动酶联免疫分析仪(FAME24/30)。ELISA检测主要试剂包括乙肝表面抗原试剂盒(法国梅里埃,批号B11FA,20110704;上海科华:批号201101031,201201011,201302011)、丙型肝炎抗体试剂盒(美国强生ORTHO:批号EXE187,EXE208;上海科华:批号201103011,201202031,201303011)及人类免疫缺陷病毒(HIVl/2)抗原抗体检测试剂盒(法国伯乐,批号1F0189,280213,3F0259;北京万泰,批号1201 10204,120121 120,12013 1022)。
1.3检测策略
血液标本采用血清学和NAT并行检测操作策略;对核酸检测单独反应性标本进行分项鉴别试验。
1.4检测方法
采用PROCLEIX TIGRIS 全自动核酸检测分析系统(TMA方法)对血液核酸标本进行单人份联合检测(HIV-1/HCV/HBV);对核酸检测单独反应性标本进行分项鉴别试验;核酸检测结果反应性结果由检测系统软件自动判定,其判定标准为样本的S/CO值≥1。采用两种不同厂家的ELISA试剂对献血者标本进行血清学HBsAg、HCVAb、HIVAgAb检测,严格执行说明书进行相关操作,通过阴阳性对照及室内质控品来控制试剂盒的质量和检测的有效性;血清学检测结果阳性的判定:样本OD≥cut off值。
1.5检测原理
Grifols核酸检测试剂是以转录介导的扩增(transcription-mediated amplification,TMA)技术原理来检测病毒核酸的方法。其检测基本原理是:利用特异性的目标捕获试剂和磁微珠分离纯化被检测病毒核酸分子,再通过TMA技术来扩增HBVDNA、HCV RNA和HIV-1 RNA(1型)的核酸片断,最后通过杂交保护(HPA)方法检测扩增产物。试剂中含有内标分子,用以监测整个反应过程,避免出现假阴性结果。
1.6统计学方法
采用SPSS17.0统计软件进行处理和分析,对计数资料进行x2检验,P<0.05为差异具有统计学意义。
2结果
2.1血清学与核酸检测结果的比较
对1 146 740例献血者血液标本,核酸检测的阳性检出率为0.97%,低于血清学(HBsAg,HCVAb,H1VAbAg三项之和)的检测阳性率1.66%,二者之间的差异具有统计学意义(x2=2128.4,P<0.05),见表1。
2.2核酸检测
4年中Grifols单人份核酸检测系统的总阳性率为0.97%,并且阳性率呈现逐年缓慢增加的趋势。在对每年的检测阳性率进行比较时,各年度间检测阳性率未见统计学意义(x2=2.442,P<0.05),见表2。
2.3血清学合格标本中核酸检测情况
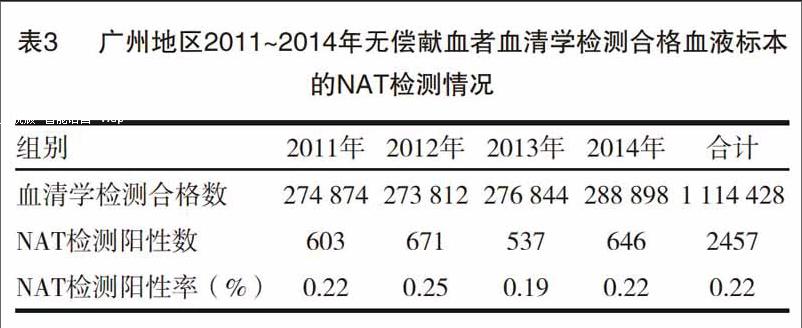
在1114428例血清学检测合格标本中,单人份核酸检测共检出2457例核酸反应性样本,核酸单独反应性比率为0.22%;在对每年检测阳性率进行比较时,各年度间血清学检测合格标本其NAT检测阳性率之间的差异具有统计学意义(x2=16.506,P<0.05),见表3。
2.4核酸鉴别结果
在2457例核酸单独反应性标本中,鉴别试验反应性的样本为718例,其中,HBV-DNA 711例,HCV-RNA 4例,HIV-RNA 3例,献血者中核酸单独阳性的样本大多属于HBV感染,HBV DNA鉴别阳性率与另外两者间的差异具有统计学意义(x2=2091.464,P<0.05)。核酸鉴别试验总阳性率为29.22%(718/2457)。见表4。
3讨论
目前,国内外应用于血液筛查的核酸检测技术主要有TMA及PCR两种。我中心使用的是Grills公司基于TMA技术的核酸检测试剂,对全部献血者样本进行单人份核酸检测。这种检测方法的灵敏度高,反应条件简单,扩增效率高,可以防止低拷贝的病毒阳性血液的漏检。其分析灵敏度为:HBVDNA 10.4IU/mL,HCV RNA 3.0IU/mL和HIV RNA45.0IU/mL。并且该方法的整个反应过程在1个试管中进行,因此也减少了污染发生的可能。本研究显示,广州地区无偿献血者血液标本的核酸阳性检出率明显低于酶免检测项目阳性检出率(P<0.05)。在所有因输血传播病毒项目检测不合格而淘汰的21481份标本中,血清学和NAT一致阳性的仅有8616份(占40.1%),而血清学单独阳性的有10408份(占48.5%),NAT单独阳性的有2457份(占11.4%)。对于这部分检测结果不一致的情况,一方面是由于血清学和核酸检测都存在检测的假阳性的可能,另一方面也说明了血清学和核酸检测二者具有的互补作用。因此在目前的技术条件下,血清学和核酸检测对献血者的筛查是缺一不可的。
在献血者血液筛查中引入核酸检测技术,其主要目的是检测出原有血清学检测可能漏掉的具有感染性的献血者样本。在本研究中的1114428份血清学检测合格标本中,单人份核酸检测共检测出反应性样本2475例,阳性检出率为0.22%(2457/1114428),结果明显高于大连和沈阳地区0.07%,这可能与各地区病毒流行率差异、检测样本数量、使用试剂差异,以及检测模式(单人份与多人份混样检测)不同有关。在对这些核酸单独阳性样本的鉴别检测中,共检出718例阳性结果,鉴别阳性检出率为29.22%。这个鉴别率与汪德海等报道的一致,而低于大连,杭州等地的数据。而出现核酸检测联检反应性,而鉴别试验全部为非反应性的原因可能有:(1)联检结果假阳性。这可能是由于酶免及核酸检测平行进行,检测人员若操作不规范,导致阳性标本的小范围污染,增加联检结果假阳性的可能;或由于检测试剂本身的非特异性反应。(2)鉴别试验的假阴性。如病毒浓度处于极低的浓度水平,由于病毒颗粒在血浆中的泊松分布,导致取样时未能吸取到带有病毒的样本;或可能是因不合适的储存条件,不良的运送,干扰物质的存在,导致样本中病毒的降解,也会造成鉴别试验假阴性的结果。由于我国乙肝的流行率相对较高,因此献血者中核酸单独阳性的样本大多属于HBV感染。而HBV感染,特别是隐匿性乙肝感染(OBI)的病毒浓度通常很低,因此出现上述低浓度样本的可能性很大。已有文章报道,对于不可鉴别的样本,采用其他核酸检测方法,或乙肝感染标志物(如乙肝核心抗体)进行检测时,部分样本仍然呈现阳性结果。提示这些不可鉴别的样本中存在一定比例的真阳性。
从结果中可以看出目前广州地区无偿献血者的HBV感染率较高,输血传播HBV残余风险明显高于HCV和HIV,从核酸鉴别试验数据分析,在718例鉴别阳性结果中,HBV DNA阳性711例,占99.03%。文献报道,HBV输血残余风险主要来自于血清转换前的窗口期、变异病毒株和隐匿性HBV感染3个方面。其中献血者中的HBV DNA单独阳性者大部分属于隐匿性HBV感染,表明输血残余风险主要来自于隐匿性HBV感染。本文检出HCV RNA 4例和HIV RNA 3例,其中HCV RNA及HIV RNA各一例送卫生部临检中心验证为阴性。另外2例HIV RNA因献血者联系电话注销,无法进行随访追踪,3例HCV RNA中2例经确证为阳性。在2015年鉴别试验中,又发现HIV RNA阳性2例,送惠州市中心血站作定量检测后确证为HIV阳性。经随访追踪献血者,一周后再进行检测,血清学及核酸检测均为阳性,因此确定该2例标本为HIV“窗口期”感染。
血清学检测的是抗原或抗体,NAT检测的是病毒核酸,核酸检测能从血清学检测阴性的标本中检出漏检的病毒感染者,是血清学检测的有力补充,我国许多城市自引入核酸检测后也多有这方面报道。在本研究中的1114428份血清学检测合格标本中,单人份核酸检测共检测出反应性样本2475例(0.22%),证实核酸检测的必要性。将NAT技术应用于血液筛查,可以显著降低因血清学漏检而导致的输血传播疾病的残余风险,进一步提高血液安全,以保障临床用血安全。

