微纤化纤维素及其制备技术的研究进展
高艳红,石瑜,田超,李群,刘玮哲
微纤化纤维素及其制备技术的研究进展
高艳红1,石瑜2,田超2,李群1,刘玮哲3
(1天津科技大学,天津市制浆造纸重点实验室,天津300457;2中国制浆造纸研究院,北京100102;3吉林晨鸣纸业有限责任公司,吉林吉林132000)
微纤化纤维素(MFC)是一种主要由植物纤维制备而得的可再生高分子材料,兼具天然纤维和纳米材料的特点。近年来,有关MFC制备、改性及应用方面的研究越来越多,然而制备成本高、干燥以及再分散等仍然是MFC规模化生产所不可回避的问题。为了更全面地加深对MFC及其制备技术发展现状的认识,本文首先探讨了MFC物化特性及其命名,然后介绍了MFC机械制备方法,包括高压均质处理、微射流处理、超细研磨处理、冷冻破碎处理和高强超声处理等,并对MFC机械制备存在的问题进行了分析。本文还介绍了MFC制备过程中的预处理方法,包括纤维素酶预处理、酸-碱抽提预处理、羧甲基化预处理、TEMPO氧化预处理、高碘酸盐氧化预处理等。最后对MFC在规模化生产及干燥过程中存在的问题进行了总结。
纳米材料;纤维素;微纤化纤维素;预处理;机械制备
纤维素是地球上储量最为丰富的天然可再生高分子化合物,所有的植物以及部分藻类、细菌和被囊动物均可以合成纤维素。据不完全统计,全球每年纤维素的合成量超过1.5×1012吨,而每年只有6×109吨纤维素被用于造纸、纺织、材料等行业[1],因此,如何进一步提高纤维素资源的利用率与利用价值是人们需要共同关注的问题之一。
1 纤维素
植物纤维从结构上看类似于“电缆”(如图1所示),由约36条纤维素分子链构成原细纤维(elementary fibrils),而不同种类植物纤维的原细纤维直径也不尽相同,一般在3~5nm左右[2],也有说在1.5~3nm左右[3]。需要说明的是,构成原细纤维纤维素分子链的准确数目至今没有得到实验的证实,而有关的研究也一直没有间断[4]。纤维素分子链中的每个葡萄糖单元含有3个游离羟基(如图2所示),其中C2、C3位上的游离羟基为仲醇羟基,C6位上的游离羟基为伯醇羟基。纤维素分子上游离羟基的存在,使得纤维素可以发生包括氧化、酯化、醚化、接枝共聚等多种化学反应,这为纤维素的改性利用提供了化学基础。纤维素分子链中C6位上的游离羟基反应活性较高,特别是在酯化反应中,而C2位游离羟基则在醚化反应中的反应活性较高。根据纤维素分子链的聚集状态,又形成了纤维素分子链有序排列的结晶区和无序排列的非结晶区。结晶区纤维素分子链有良好的取向性,分子链间排列紧密整齐,分子间结合力好,对纤维物理强度贡献较大,纤维素结晶区的密度约为1.59g/cm3。非结晶区纤维素分子链取向性较差,分子链间排列松弛无序,分子间结合力也较差,纤维素非结晶区的密度约为1.5g/cm3。通常结晶区纤维分布在原细纤维的内层,而非结晶区纤维存在于原细纤维的外层。若干原细纤维通过半纤维素的连接又构成了直径10~20nm左右、且具有网状结构的微细纤维(microfibrils)[5]。若干微细纤维又进一步构成细纤维(fibrils或fiber),针叶木细纤维长度一般在3mm左右,阔叶木细纤维长度一般在1mm左右。
2 纳米纤维素
按照ISO/TS 27687—2008[7]有关纳米纤维的定义,纤维任意两个维度尺寸相近(尺寸相差3倍以内),且均处于纳米尺度范围(1~100nm),而第三维度远大于其余维度(尺寸相差3倍以上)的纤维称之为纳米纤维。近年来,随着纳米技术的不断发展,各学科间的交叉和联系也越来越大,纳米纤维这一概念也不再局限于某一个单一学科,因此,有关纳米纤维素(nanocellulose,NC)的研究也随之兴起。目前纳米纤维素并没有统一或官方的准确定义,只是在很多文献报道中提到纤维素纤维三个维度之中任一维度处于纳米尺度范围(1~100nm)的纤维均可称之为纳米纤维素[8]。
纳米纤维素根据原料来源以及功能特性可以大致分为3个类别:纳米微晶纤维素(nanocrystal cellulose,NCC)、纳米纤化纤维素(nanofibrillated cellulose,NFC)以及细菌纳米纤维素(bacterial nanocellulose,BNC)[9],表1为纳米纤维素的一般尺寸。有关纳米纤维素的制备方法多种多样,且不断有新的方法被提出,因此,对纳米纤维素进行归类或者定义,应该主要考虑从纳米纤维素的特性出发。美国纸浆与造纸工业技术协会(TAPPI)[10]根据纳米纤维素的特性将其分了为两大类(如图3):纳米纤维(nanofiber)和纳米结构材料(nanostructure material),其中纳米纤维包括纤维素纳米晶体(cellulose nanocrystal,CNC)和纤维素纳米纤丝(cellulose nanofibril,CNF),纳米结构材料包括纤维素微晶体(cellulose micocrystal,CMC)和纤维素微纤丝(cellulose microfibril,CMF)
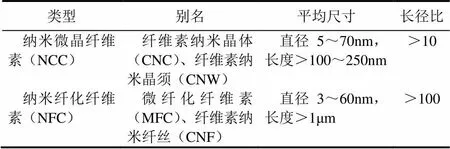
表1 纳米纤维素的一般尺寸[9]
2.1 纳米微晶纤维素
纳米微晶纤维素(nanocrystalline cellulose,NCC),通常也称作纤维素纳米晶体(cellulose nanocrystal,CNC)、纤维素纳米晶须(nanocrystal whiskers,CNW),是指以木材纤维、农林废弃物、被囊动物以及细菌纤维素等为原料,在一定温度和时间条件下,采用浓酸(55%~70%)水解处理而得的一种纳米尺寸、且具有刚性棒状结构的纤维素纤维。NCC典型直径在3~20nm之间。常用于NCC制备的酸主要有硫酸、盐酸、磷酸等,其中,有关硫酸用于制备NCC的研究最多。采用硫酸水解法制备NCC,由于在纤维表面引入了磺酸基(<0.3 mmol/g),使得纤维表面负电荷密度增大,一定程度上减轻了NCC悬浮液中纤维的絮聚和絮凝,增加了NCC悬浮液的稳定性,但是磺酸基的引入会使NCC纤维的热稳定性降低[11]。NCC在制备过程中保留了大部分的结晶区,因此具有较高的结晶度和纤维素纯度、高比表面积和高透明度的特点。不同的原料、不同的酸水解条件所制得的NCC结晶度、形态、尺寸也各不相同。因此,针对不同原料,相适应的NCC制备工艺也各不相同,加之酸水解过程中反应的均匀性等问题,所以很难制备出尺寸均一的NCC,这给NCC的应用造成了一定的阻碍。此外,由于NCC具有高吸水性和高反应活性的特点,使得NCC只能以浓度较低的悬浮液保存,并且需要添加分散剂和稳定剂来保持NCC悬浮液的稳定,以防止其聚集、沉淀。一般制备NCC的得率在30%~40%左右,虽然CHEN等[12]发现通过控制酸浓度可以使NCC的制备得率提高至70%,但是制备过程中仍然会产生大量的高浓废酸,而废酸的处理和利用无疑再一次增加了NCC的制备成本。不过近年来也出现了一些关于NCC废液及其副产物高值化利用的研究,这或许是补偿NCC制备成本一个很好的思路。
2.2 微纤化纤维素
纳米纤化纤维素(nanofibrillated cellulose,NFC),也称作微纤化纤维素(microfibrillated cellulose,MFC)或纤维素纳米纤丝(cellulose nanofibrils,CNF),是指以植物纤维为原料,通过机械处理得到的一种直径小于100nm的纤维素纤维。从形态上来看,NFC呈现出的是一种细长的丝状结构,具体来说,NFC应该是以原细纤维为主要结构单元的丝状结构,然而在NFC的制备过程中,所得到的NFC实际上并不是以单根丝状结构的形式呈现的,而是由纳米或微米纤丝缠绕、交织或连接而成的网状结构[13]。这可能与植物细胞壁的结构有关,因为构成细胞初生壁(如图4所示)的微细纤维是呈紊乱状或网状排列的,构成细胞次生壁的微细纤维是以螺旋结构聚集在一起的[5]。由于现有方法无法获得全部由单根原细纤维组成、且尺寸均一的NFC,因此与NCC相比,NFC的尺寸均一性更差,既包含单根原细纤维结构,又包含原细纤维束或微细纤维结构[14]。单根NFC纤维的直径一般在2~20nm之间,而不同种类植物纤维原料的原细纤维束或微细纤维直径通常在20~200nm之间[15],因此,从纤维尺寸上来讲,NFC这个名称并不能准确、全面表达纳米纤维素纤丝的全部特性,所以有关NFC的其他叫法也多种多样[6,8-9]:microfibril,microfibril aggregates,microfibrillar cellulose,nanofibril,nanofiber,nanofibrillar cellulose或 fibril aggregates等。此外,在有关表述NFC尺寸的文献中,都只提到获得了一种具有纳米尺寸的纤丝,然而具有这种尺寸的纤丝在整个NFC悬浮液纤维中所占的比例并未被普遍提及。IWAMOTO等[16]比较了多种TEMPO衍生物和类似物的氧化效率后发现,无论采用何种氧化物和氧化条件,经过一定程度的机械处理之后,所制得的NFC悬浮液中均存在未纤化完全的原细纤维束。此外,提高TEMPO氧化后纤维素的羧基含量,能够增加NFC悬浮液中纳米尺寸纤丝的得率,当氧化纤维素羧基含量达到1.18mmol/g时,经过机械处理之后,NFC悬浮液中具有纳米尺寸纤丝的得率能够上升至56.3%。考虑到过去有关这种类型纤维素纤维的表述都是以MFC的形式出现的,因此,基于以上原因,也为了避免混淆,本文将NFC和MFC统称为MFC。
3 微纤化纤维素的机械制备方法
MFC的制备通常是以高强度机械处理为主,辅以必要的预处理以降低机械处理的能耗,提高制备效率。机械处理方法包括高压均质处理、微射流处理、超细研磨处理、冷冻破碎处理、高强超声处 理等。
3.1 高压均质处理
高压均质处理的作用原理是利用往复泵向一个狭小的空间不断泵入浆料悬浮液,通过调压手柄调节空间内部浆料的压力,然后在高压高速的状态下将浆料从一狭缝中挤出,通过多次重复这一过程即可制得MFC,如图5(a)所示。通常高压均质处理物料质量分数在0.3%~3.0%左右[18],也有研究在物料质量分数高达7%的条件下进行高压均质处 理[6],均质压力在30~150MPa[19-20]之间,循环次数视原料种类和原料初始状态不同也有所差异,一般在1~30次左右[21-22]。高压均质过程中所产生的高剪切力会对纤维产生强烈的作用,使纤维表面分丝帚化,同时纤维尺寸也大幅度降低。此外,浆料在挤出的过程中所承受的压力会迅速降低,压力骤降所产生的“爆破”效果也会对纤维造成纤化和撕裂效果[23]。1983年,HERRICK和TURBAK等[24-25]以木材纤维为原料,首次采用高压均质机处理得到了一种黏度高并且稳定的凝胶状MFC。1985年,TURBAK等[26]首次对高压机均质处理制备MFC申请专利,并将之正式命名为微纤化纤维素(microfibrillated cellulose,MFC)。此后,不断有以不同种类植物纤维为原料,采用高压均质处理制备MFC的方法被报道:DUFRESNE等[27]以漂白马铃薯茎秆浆为原料,采用高压均质处理,在压力50MPa,温度90~95℃的条件下,循环15次制得直径为5nm的MFC;LEITNER等[19]以漂白甜菜茎浆为原料,采用高压均质处理在30MPa压力下,循环10~15次制得MFC;HABIBI等[28]以漂白仙人掌皮浆为原料,采用高压均质处理在压力50 MPa,温度低于95℃的条件下,循环15次制得直径2~5nm的MFC。
采用高压均质处理前,浆料悬浮液的浓度以及纤维的尺寸需要特殊控制,否则极易发生堵塞。通常的做法是在均质前对浆料进行机械预处理,对纤维进行预纤化和润胀,同时控制纤维尺寸,使其能够满足均质要求。KELLEY等[29-30]以漂白、未漂针叶木浆和漂白阔叶木浆为原料,采用Valley打浆机在2%的浆浓下打浆3 h,然后在55MPa、45℃、浆浓0.7%的条件下均质1~20个循环制备MFC,其中以漂白针叶木浆为原料制得的MFC直径为(79±20)nm,以漂白阔叶木浆为原料所制得的MFC直径为(69±16)nm,而以未漂针叶木浆为原料所制得的MFC直径为(85±21)nm。WANG和SAIN[31]以黄豆荚为原料,采用PFI磨浆机在标准条件下磨浆12000r/min,再通过一种改进的类似于均质机的仪器在50~100MPa的压力下,循环20次得到直径在50~100nm之间的MFC。IWAMOTO和NAKAGAITO等[32]以硫酸盐浆为原料,采用磨浆间隙0.1mm的盘磨机处理30次,然后再采用高压均质机循环处理30次,所得到MFC直径为50~100nm之间,长度为几微米。STELTE和SANADI[33]以两种商品针叶木浆和阔叶木浆为原料,采用机械预处理加高压均质处理的方式制备出了直径在10~25nm左右的MFC,他们发现机械预处理对针叶木浆比对阔叶木浆更有效,他们把出现这种现象的原因归结为两种浆在机械预处理的过程中纤维内部纤化和纤维外部纤化的程度有所差异,以及两种浆纤维素含量不同。在机械预处理过程中,纤维内部氢键发生断裂使得纤维内部发生纤化,而纤维外部纤化只是在机械预处理过程中,由于机械摩擦、挤压使纤维表面发生的纤化现象。AMIRALIAN等[18]以澳大利亚特有的一种牧草(triodia pungens)为原料,分别采用碱法蒸煮和次氯酸盐对其进行脱木素和漂白处理,最后采用高压均质处理,在浆浓0.3%,均质压力35MPa的条件下,在未经任何其他预处理或后处理的情况下,循环一次即得直径为(3.7±1)nm的MFC,据其称这是当前所有有关MFC制备的报道中,制备类似尺寸所需的均质处理条件最低的,甚至低于经过酶预处理或TEMPO氧化预处理后的浆料所制得的MFC。此外,AMIRALIAN等还以经有机溶剂法制得浆料为原料,采用高压均质处理制备MFC。他发现要制得同样尺寸的MFC,有机溶剂法所制得的浆料需要在35 MPa的压力循环至少3次,若要只循环1次,那么均质压力需要提高至150MPa。对于这种差别产生的原因,AMIRALIAN等认为是由于经过碱法蒸煮之后,浆料中半纤维素含量和木素含量较低,因此更有利于纤维的纤化。
磨浆处理也可以单独作为制备MFC的方法,KARANDE和BHARIMALLA等[34]以棉浆为原料,采用盘磨处理,磨浆间隙0.1mm左右,磨浆质量分数0.5%,磨浆循环30次。实验结果表明:经过盘磨处理30次后,纤维直径从25μm下降到约242nm左右,纤维结晶度和纤维素分子聚合度随着磨浆次数的增加均有较大程度的下降。KUMAR等[35]以漂白蔗渣浆、漂白针叶木和阔叶木浆为原料,采用PFI磨浆(10~12.5)×104r/min,制备出了直径为10~160nm的MFC。实验结果表明:在本实验条件下,相比针叶木浆,PFI磨浆处理对阔叶木浆和蔗渣浆效果更好,纤维也更容易分丝帚化,所制得的MFC直径也更小。
3.2 微射流处理
微射流处理的作用原理是通过一个增压泵将浆料悬浮液在高压状态下泵入一个细小的Z型管道(0.2~0.4mm)中,浆料在管道中受到高速剪切和巨大的撞击力作用,通过多次重复这一过程即可制得MFC,如图5(b)所示。通常微射流处理物料质量分数在0.7%~1.8%左右,微射流处理压力一般在69~207MPa不等[29],微射流处理循环次数一般在1[36]~30[32]次左右。有报道称微射流处理的剪切速率可以高达107s–1[37],此外,与高压均质处理相比,微射流处理一般在较高的压力条件下进行,所制得MFC直径更小,尺寸也更加均一。LEE等[36]以微晶纤维素为原料,采用微射流处理在137.9MPa的压力下制备MFC,考察了不同循环次数(1~20次)对MFC纤维形态的影响。实验结果表明:循环10~15次时,纤维长径比逐渐增加,而进一步循环至20次时,纤维出现絮聚现象,他们认为这是由于纤维比表面积增加以及MFC纤维表面羟基密度增加,导致纤丝之间的作用增强。FERRER等[38]以3种不同的棕榈果茎纤维为原料,采用PFI磨浆与微射流处理结合的方式制备MFC。实验结果表明:微射流处理制备的MFC,纤维形态较均一,且以本色浆为原料制得的MFC比以漂白浆为原料制得的MFC性能更加优良。尽管采用微射流处理制备的MFC性能优异,但是LAVOINE等[6]指出微射流处理所需循环次数较多、能耗过高,会对环境产生负面影响,因此较难规模化应用。
3.3 超细研磨处理
超细研磨处理的原理是通过磨石旋转产生高强剪切力,破坏纤维的细胞壁结构和氢键连接,从而实现纤维纤化及分离单根纤维的目的,如图5(c)所示。通常超细研磨处理物料质量分数在5%~10%左右[39],超细研磨转数控制在150~2500r/min左右,超细研磨循环次数一般在1~10次左右,循环次数过多不仅不会增加纤维的纤化效果,而且能耗会大大增加。WANG等[40]以漂白阔叶木浆为原料,采用超细研磨处理制备MFC,研究了不同研磨能耗
和时间对纤维结晶度和纤维素分子聚合度的影响。实验结果表明:研磨11h,磨浆能耗从5kWh/kg上升到30kWh/kg,纤维结晶指数从62%下降到40%,纤维素分子聚合度从850下降到550。此外,随着磨浆的进行,浆料温度升高,水分不断蒸发,浆浓从2%上升到3.2%,这使得磨浆能耗增加。HASSAN等[41]分别以稻草浆和蔗渣浆为原料,采用超细研磨与高压均质联用处理的方式制备MFC。他们发现在这一过程中,超细研磨处理能够起到纤维分丝帚化的作用,而高压均质处理能够使纤维尺寸变得更小、更均一。IWAMOTO等[42]以辐射松为原料,研究了不同超细研磨处理循环次数对纤维纤化程度及尺寸的影响。实验结果表明:研磨循环1~3次,纤维尺寸已经明显降低,循环5次时,大部分纤维直径已经介于20~50nm之间,而继续增加循环次数,纤维形态并没有进一步变化,因此,他推测超细研磨5次时,纤维的纤化已经完成。NAIR等[43]的研究也得到了类似结论,当研磨时间从2h增加到6 h,纤维形态并没有明显变化,但是研磨4h以后,纤维素分子聚合度明显降低,他指出这是因为超细研磨会导致纤维一定程度的降解,使得纤维结晶度和纤维素分子聚合度降低,并且会影响MFC的机械性能。HENRIKSSON等[44]认为纤维长度和纤维素分子聚合度之间具有很大的相关性,增加纤化程度会降低纤维长度,而长径比小的MFC所制成的片或膜与长径比大的纤维相比较脆且易碎。IWAMOTO等[42]的研究也证实,纤维在超细研磨处理过程中会发生降解,而纤维尺寸降到纳米级会对由其所制得的膜和复合材料的机械性能产生负面影响。
与高压均质处理和微射流处理相比,超细研磨机结构简单并且运行稳定,能够保证浆料悬浮液在相对较高的质量分数(2%~10%)下进行研磨处理,且不会发生浆料堵塞现象。在研磨处理前不需要对原料的尺寸进行控制,这是超细研磨处理的优点所在。但是,研磨过程中,磨石摩擦产生石粉混入浆料中会造成浆料污染,并且难以有效分离,因此,控制研磨条件以避免这一现象的发生是超细研磨处理需要考虑的问题之一。此外,超细研磨处理能耗较大也是需要关注的问题。
3.4 冷冻破碎处理
冷冻粉碎处理主要包括两部分,充分吸水润胀的纤维在液氮氛围中迅速冷冻结冰,使纤维细胞内的水形成冰晶,然后在高强度机械力的冲击之下,纤维细胞壁被破坏形成碎片,从而被分离出来。该法最早由DUFRESNE等提出,他们以甜菜渣为原料,采用冷冻粉碎加高压均质联合处理的方式制备MFC,然后用MFC铸膜并对其物理性能进行了评价。实验结果表明:MFC能够形成网状结构,有效提高了纤维素膜的弹性模量。此外DUFRESNE等[46]还指出果胶能够起到MFC纤维间黏结剂的作用,在干燥状态下能够增加MFC膜的杨氏模量,但在湿润状态下作用相反,而且果胶的存在不利于MFC的有效制备。ALEMDAR和SAIN[47]分别以麦草和豆荚为原料,采用冷冻粉碎、机械搅拌和高压均质联合处理的方式制MFC,其中以麦草为原料所制得MFC中大多数纤维直径在30~40nm之间,而以豆荚为原料所制得的MFC中纤维直径分布在20~120nm之间。不难看出,冷冻粉碎处理并不能作为一个单独的处理手段使用,而是通常作为预处理手段与其他机械处理方法联用制备MFC。
3.5 高强超声处理
高强超声处理是利用声波的声空化作用产生的强大机械震荡力分离纳米纤维的一种方法[48]。声波在液体中传播时,液体由于压力起伏会产生负压,在负压区液体结构缺陷处会产生微小空化气泡,当空化气泡由形成、膨胀到最后破裂时,会产生强烈的机械震荡力,极短的时间内会产生高达5000K高温,大约500MPa的高压,以及速度高达400km/h的微射流[49]。利用这种强烈的机械震荡力能够去除纤维S1层,使S2层发生变形、位移,润胀并发生纤化[50]。WANG和CHENG[51]采用高强超声处理制备MFC,研究了超声温度、时间、功率、浆料浓度、纤维尺寸、以及探针伸入浆料的长度等6个因素对纤维纤化程度的影响。实验结果表明:提高超声功率和升高温度有利于纤维纤化,而长纤维纤化程度较低,但是,浆料浓度过高、探针伸入浆料悬浮液中过深则不利于纤维纤化。CHEN等[52]分别以竹子、木材和麦草为原料,在20~25kHz,功率1000W条件下,超声处理30min制备纳米纤维素。实验结果表明:制得的MFC结晶度均超过60%,热降解温度超过330℃。AMIRALIAN等[18]以针叶木浆为原料,着重研究了超声振幅(功率)和时间对纤维纤化程度的影响,他们发现超声强度过高,MFC纤维结构发生破坏,纤维细胞壁发生滑动、位移,同时伴随着纤维极性增加(氢键),会导致MFC发生聚集和弯曲缠绕。虽然高强超声处理能够很容易得到纳米级的MFC,但是超声处理较不均匀,只有一小部分纤维能够得到有效纤化并形成凝胶,其余纤维仍为悬浮液状。
3.6 其他机械处理方法
UETANI等[17]为了观察MFC纤化现象,采用一种高速搅拌处理的方式制备MFC,他们发现采用这种方法制备的MFC尺寸并不均一,而且多数纤维并没有完全纤化。但是通过对比超细研磨处理发现,当纤维纤化程度相同时,高速搅拌对纤维的破坏程度较超细研磨小。
AMIRALIAN等[18]以针叶木浆为原料,比较了不同球磨转数和球磨时间对纤维尺寸的影响。实验结果表明:当球磨转数为3000r/min时,可以制得直径(8±2)nm,长度(341±100)nm的NCC,转数为1000r/min时,才能制得直径(8.7±4.8)nm,长度几微米的MFC。此外AMIRALIAN指出球磨时间对纤维形态的影响最大,但是球磨时间过长会造成纤维污染,因为球磨过程中纤维上的活性羟基会吸附金属离子,需要酸洗除去。
蒸汽爆破也可以作为制备纳米纤维素的一种方法,浆料悬浮液在高温高压的环境中维持一定时间,让高温蒸汽进入纤维内部,然后迅速泄压所产生的压降会形成“爆破”效果,直接作用于纤维表面及内部,从而使纤维分丝帚化。实验室规模的蒸汽爆破温度通常在200~250℃左右,为了提高蒸汽爆破的效果,在蒸汽爆破前通常需要对原料进行预处理[8]。
静电纺丝对于制备纳米纤维并不算一个新的方法,因为早已有采用静电纺丝的方式制备纳米纤维的实例,据称目前已有的文献中,已经有超过50种聚合物采用静电纺丝的办法,成功纺制得到了极细的纤维,直径最小可以达到3nm[53]。尽管如此,采用静电纺丝法,以植物纤维原料制备MFC的研究还很有限[6]。需要指出的是,静电纺丝法首先要将原料溶解在溶剂中或制成熔融态,只有黏弹性较好的材料才能纺制出细长的纳米纤维,通常同种原料不同溶剂所纺出的纳米纤维也不尽相同,因此,对于植物纤维原料来说,选择合适的纤维素溶剂和溶解条件至关重要。
4 能耗
尽管目前已有多个机构或组织对外宣布(如表2),已经能够实现批量制备MFC,也有很多文献提出了高效、低耗的MFC的制备方法。但是客观地讲,将MFC应用于一些低值的领域如纸和纸板的生产等,经济上仍不可行[8]。MFC纤维本身的形态和结构特点,使得单一的机械处理制备MFC的能耗过高。很多有关制备MFC的文献都提到了制备过程的能耗:LINDSTRÖM等[54]的报道指出,MFC的制备能耗超过30000kWh/t。ANKERFORS[55]的报道提到采用高压均质处理制备MFC的能耗约为27000kWh/t。ISOGAI等[56]的报道提到MFC的制备过程能耗高达700MJ/kg。SYVERUD等[13]的研究表明,采用高压均质处理,在压力1000bar,浆浓0.5%,循环均质一次的能耗接近10000kWh/t。ERIKSEN[57]的研究表明,MFC制备过程能耗甚至高达70000kWh/t。需要指出的是,单纯的横向比较机械处理制备MFC的能耗并没有太多意义,以高压均质处理制备MFC为例,能耗与设备型号、均质压力、浆浓、循环次数、流量等因素有关[8],因此,不同的制备条件所需的能耗也各不相同。此外,即使条件相同,但是所用原料的不同也必然导致能耗有所差异。尽管如此,单纯机械处理制备MFC的能耗较高这一事实是不可否认的,因此,开发低耗高效的MFC制备方法是解决MFC规模化制备及应用必须面对的问题之一。
在机械处理前对纤维原料进行预处理,可以有效降低后续机械处理的能耗。根据不同原料的纤维特性,采用相适宜的预处理方法,能够更大程度的暴露纤维表面的羟基,提高纤维的可及性,增加纤维内表面积,改变纤维结晶度,切断纤维分子内和分子间氢键,增加纤维的反应活性和加工性能[58]。ANKERFORS[55]的研究表明,采用酶或化学预处理,可以将MFC的制备能耗从20000~30000kWh/t降低到约1000 kWh/t,耗能降幅超过95%。ISOGAI等[59]的研究表明,采用化学预处理可以将MFC的制备能耗降低95%以上(从700MJ/kg降低至7MJ/kg)。由此不难发现,预处理是降低MFC机械制备能耗一个非常必要的手段。

表2 纳米纤维素中试概况[60]
5 微纤化纤维素的预处理方法
预处理可以显著降低MFC机械制备能耗,而根据预处理对纤维的作用方式不同,预处理方法又可分为非改性预处理和改性预处理,其中,非改性预处理主要包括生物酶预处理、酸-碱抽提预处 理、纤维素溶剂预处理;改性预处理主要包括羧甲基化预处理、乙酰化预处理、TEMPO氧化预处理、高碘酸盐氧化与氧化/磺化联用预处理等。
5.1 纤维素酶预处理
纤维素酶作为一类生物活性蛋白,可以特异性的水解纤维素,并使其转化为低聚糖甚至单糖,通常这一过程的发生需要3种酶协同作用,因此,纤维素酶是一种由3种酶所构成的复合酶的总称,包括内切葡聚糖酶、外切葡聚糖酶和纤维二糖酶(葡萄糖苷水解酶)。研究表明纤维素酶预处理能够有效降低MFC制备过程中机械处理的能耗[61],而这一过程只需要纤维素酶对纤维的部分结构进行改变而不是完全水解[62],因此,通常主要将单组分内切葡聚糖酶用于预处理制备MFC[8]。纤维素酶能够选择性地水解纤维素的非结晶区,对纤维素结构的破坏程度比酸水解小,这有利于后续机械处理得到高长径比和高度网络缠绕结构的MFC。PÄÄKKÖ等[63]认为纤维素酶预处理过程中,纤维纤丝束部分程度的瓦解破坏不但有利于机械处理过程中纤维的纤化,而且能够保留纤维原有的连接形式,依靠这种原有连接所形成的MFC网络结构要比仅仅依靠氢键所形成的网络结构物理强度更高,这为MFC应用于增强复合材料的强度性能提供了基础。HOEGER等[64]以实验室自制针叶木机械浆和商品针叶木漂白硫酸盐浆为原料,采用纤维素酶预处理与超细研磨处理联用的方式制备MFC。实验结果表明:虽然两种原料在相同超细研磨条件下耗能相同,但是两种原料化学成分的差异使得它们在研磨过程中纤维的纤化程度不同,通过对比两种原料制得的MFC的SEM图的异同,他们认为木素的存在不但会降低纤维素酶的作用效果,也会影响研磨过程中纤维的纤化程度。
纤维素酶预处理不仅能够有效降低MFC制备过程的能耗,而且预处理废液易于回用处理,是一种具有工业化应用前景的预处理方法。Innventia公司Lindström团队创建的全球首家MFC中试工厂就是采用的纤维素酶预处理[65]。芬兰VTT研究中心的HefCel项目开发了一种纤维素酶预处理技术,能够在浆浓20%~40%的条件下制备MFC,而且预处理过程产生的糖等副产物可以回收并进行高值化利用[66]。
5.2 酸-碱抽提预处理
BHATNAGAR和SAIN[67]最早采用酸-碱抽提预处理与机械处理相结合的方式制备MFC,他们以木材纤维、农业废弃物(秸秆、农作物的根茎等)为原料,先采用稀酸在50~90℃条件下对植物纤维进行酸水解,紧接着用质量分数不超过10%的碱液进行抽提,然后将抽提后的浆料在液氮氛围中冷冻,最后采用冷冻粉碎处理的方式制备MFC。此后ALEMDAR和SAIN等[47,68]对这一方法进行了改进,他们以麦草和大豆壳为原料,首先用17.5%的氢氧化钠溶液将麦草和大豆壳充分浸泡2h后用水洗净,这一步骤主要是为了让纤维充分润胀,增大纤维的比表面积,使之能够更好的酸水解;紧接着用1mol/L的盐酸在(80±5)℃的条件下对洗净后的浆料进行酸水解,水解结束后再用水将浆料充分洗涤,这一步骤主要是为了破坏低分子量多糖之间的连接,溶出半纤维素和果胶,达到分散纤维的目的。同时,这一过程还可以除去原料中的草酸钙,尤其是非木材原料,因为草酸钙的存在会影响均质效果;最后再用2%的氢氧化钠在60~80℃的条件下对浆料进行热碱抽提,抽提结束后用水将浆料洗至中性,这一步骤主要是为了破坏木素的结构,同时破坏木素与碳水化合物之间的连接,为了保护纤维在热碱抽提过程中不被过度氧化降解,少量的亚硫酸钠可以加入充当抗氧化剂。将酸-碱抽提预处理之后的浆料风干,然后将风干后的浆料置于液氮环境中冷冻,将冻干的浆料迅速用研钵捣碎,随后浸入大量的水中配置成一定浓度的悬浮液,再用高速分散机将浆料悬浮液分散,最后在30MPa的压力下,高压均质处理20个循环制得MFC,其中麦草MFC直径在10~80nm之间,大豆荚MFC直径在20~120nm之间。经过酸-碱抽提处理之后,大豆荚的半纤维素含量和木素含量分别从12.5%和18%下降到3.5%和2.5%,而纤维素含量从54%上升到94%,麦草和大豆荚纤维素的结晶度上升,且热稳定性也有所提高。值得一提的是,经过机械处理之后,麦草和大豆荚纤维的热稳定性会进一步提高。HAN等[69]以漂白木浆为原料,先用20%的氢氧化钠溶液对原料进行碱处理,再用48%的硫酸溶液对碱处理之后的浆料进行酸水解处理,最后采用微射流处理在压力207MPa的条件下,循环处理10次,制得直径(16±4)nm,且具有纤维素Ⅱ型结构的MFC悬浮液。
5.3 羧甲基化预处理
羧甲基化预处理可以在纤维表面引入负电荷,增加纤维之间的静电斥力,使纤维更易分散和裂解。如图6所示,与制备羧甲基纤维素(CMC)原理相同,羧甲基化预处理也是先将纤维与碱反应生成碱纤维素,再与氯乙酸反应完成羧甲基化。不同之处在于羧甲基化制备CMC和羧甲基化预处理的反应程度(纤维取代度)不同,因为取代度过高会造成纤维素降解,还会造成纤维素在羧甲基化后溶解。研究表明:当取代度达到0.07时,经过羧甲基化处理之后的纤维在水中就会呈现凝胶状[70],因此,控制反应程度是羧甲基化预处理的关键因素之一。WÅGBERG等[71]采用羧甲基化对亚硫酸盐针叶木浆进行预处理,预处理完成后采用微射流机在165MPa的压力下进行均质化处理,制得直径5~15nm,长1μm的棒状MFC悬浮液,此外,他们还发现MFC悬浮液中较高的无机盐浓度和较低的pH会使得MFC发生絮聚。EYHOLZER等[72]比较了羧甲基化处理置于均质前和均质后的区别,他指出在均质前进行羧甲基化预处理所制得的MFC比原浆及均质化后再羧甲基化处理制得的MFC纤维素结晶度低,尺寸也更小、更均一。TAIPALE等[73]的研究结果表明:羧甲基化预处理能够将后续微射流处理的能耗从5.5MWh/t降至2.2MWh/t。SIRÓ等[74]研究了多级均质对经羧甲基化预处理制得MFC性能的影响,他们指出采用羧甲基化预处理制得的MFC凝胶非常适合制备透明度高且具有良好氧阻隔性能的纤维素膜。
5.4 TEMPO氧化预处理
1983年,SEMMELHACK等[75]最早采用2,2,6,6-四甲基哌啶-氮氧化物(TEMPO)通过电解氧化的方式将伯醇羟基氧化成醛基和酮基。1984年,SEMMELHACK等[76]又以TEMPO为氧化剂,以氯化铜为催化剂,对烯丙醇和苯甲醇进行氧化后发现,大部分的氧化都发生在伯醇羟基。1987年,PIER LUCIO ANELLI等[77]以TEMPO为氧化剂,在二氯甲烷和NaClO的混合溶液中对伯醇羟基进行选择性氧化的研究,他们发现在0℃条件下,Br–离子为催化剂,大量的伯醇羟基在几分钟内就可被迅速氧化成醛基。1995年,DE NOOY等[78]首次采用TEMPO介质对聚多糖(淀粉等)进行氧化,并成功将淀粉葡萄糖单元C6位的伯醇羟基选择性氧化成羧基。ISOGAI等[79]最早采用TEMPO介质氧化体系对木质纤维原料进行预处理来制备MFC,采用这种预处理方式不仅可以有效降低后续机械处理的能耗,而且可以分离得到单根直径3~4nm的透明MFC凝胶。
在TEMPO/NaBr/NaClO氧化体系中,TEMPO和NaBr首先被溶于浆料悬浮液中,用NaOH溶液和HCl溶液调节pH在10~11之间,然后将一定浓度的NaClO溶液缓慢加入后反应开始发生,反应期间用一定浓度的NaOH溶液将pH控制在10或10.5,保证反应在一个恒定的pH下进行。如图7所示,在TEMPO/NaBr/NaClO氧化体系中,TEMPO作为催化剂,NaBr作为助催化剂,NaClO作为氧化剂,TEMPO被NaClO氧化后,反应后的氧化产物又可以将伯醇羟基选择性氧化成醛基,醛基进而再被氧化变为羧基,NaBrO和NaClO也一定程度参与醛基氧化为羧基的这一过程。以天然纤维素为原料,即使很剧烈的TEMPO氧化条件或较长的反应时间,氧化后浆料悬浮液中水溶性聚糖的含量也非常有限[79]。若以再生纤维素、丝光化纤维素为原料,则反应后浆料悬浮液会变澄清,这是因为氧化过程中会产生了大量水溶性的聚糖[56,79]。此外,半纤维素及木素的存在也会对TEMPO氧化过程造成影响:PÄÄKKÖNEN等[80]的研究表明,半纤维素的存在会降低TEMPO氧化效率,反应时间会从28min(木聚糖含量7.3%)延长至220min(木聚糖含量25.2%),高压均质处理后半纤维素会不均匀的分布在MFC纤维的表面,在MFC凝胶中形成“网络润胀”结构,这会增加纤维的保水能力,影响MFC凝胶的流变性能及脱水能力。若以机械浆为原料,由于原料中木素及半纤维素的存在,会消耗更多的NaClO,反应时间也会延长,且反应过程中半纤维素及木素会被NaClO氧化成水溶性物质。尽管以机械浆为原料,氧化纤维素得率只有40%左右,但是纤维素羧基含量仍然可以达到1.0~1.5mmol/g[81]。ISOGAI等[82-83]采用XRD研究氧化后纤维素的晶型结构时发现,经过TEMPO氧化后,纤维素的晶型仍然是纤维素Ⅰ型,因此,他认为TEMPO氧化只会发生在纤维素结晶区表面,不会在结晶区内部发生,氧化后纤维素的13C NMR谱图也证实了这一点。经过TEMPO氧化之后,MFC中微纤丝的直径会随着纤维素羧基含量的上升逐渐减小,而不同羧基含量的MFC的-电位相同,说明MFC微纤丝表面羧基密度相同[56],这可能是因为随着微纤丝直径逐渐减小,纤维比表面积增大,因此在纤维表面羧基密度相同的情况下,羧基含量升高,这也间接证明了TEMPO氧化只会发生在纤维素结晶区表面。采用TEMPO氧化预处理制备的MFC,其MFC微纤丝直径几乎为一常数,与原料种类关系不大,而微纤丝的长度及长度分布主要取决于TEMPO氧化条件及机械处理条件。在MFC的制备过程中,当氧化后MFC羧基含量超过0.8mmol/g时,就能得到透明的MFC凝胶,对于从未干燥的原料和干燥一次的原料,在TEMPO氧化预处理制备MFC的过程中差别并不大,只有当NaClO浓度用量低于3mmol/g时,两类原料之间的差别才会显现[56]。
研究表明,采用TEMPO/NaBr/NaClO氧化体系对纤维原料进行氧化预处理,氧化结束后纤维素分子的质均聚合度DPw会从380~1200下降至40~80[84-85],这主要是由于TEMPO/NaBr/NaClO氧化体系是在碱性条件下完成反应的,而氧化过程中产生的醛基会在碱性条件下发生β-烷氧基消除反应,造成纤维素分子链的断裂。此外,氧化过程中,纤维素分子糖苷键也会发生原位断裂,造成纤维素分子聚合度下降。采用TEMPO/NaBr/NaClO氧化体系,在氧化后的纤维素还会残余少量未反应的醛基,因此,采用铜乙二胺溶液测定氧化纤维素分子聚合度时,需要首先将未反应的醛基氧化成羧基,以避免在聚合度的测定过程中,醛基在碱性条件下发生β-烷氧基消除反应,造成聚合度的测定结果偏低[56]。
TEMPO/NaClO/NaClO2氧化体系能够有效避免氧化过程中纤维的降解,在这一氧化体系中,TEMPO和NaClO作为催化剂,NaClO2作为氧化剂,图8为TEMPO/NaClO/NaClO2氧化体系反应原理图。HIROTA等[86]以聚合度(DPv)680的再生纤维素纤维为原料,采用TEMPO/NaClO/NaClO2氧化体系在pH 4.8~6.8进行氧化,所得到的氧化纤维素分子的DPw超过490。通过研究反应后纤维素的NMR图发现,伯醇羟基几乎全被氧化成羧酸盐形式,有趣的是氧化后纤维素在酸性条件下较稳定,而在碱性条件下则会发生β-烷氧基消除反应而降解,这一特性恰恰与天然纤维素相反。尽管TEMPO/NaClO/NaClO2氧化体系能够很好地保留纤维素分子的聚合度,且氧化反应较完全,氧化后纤维素不会残余未反应的醛基,但是其对纤维素的氧化效率低于TEMPO/NaBr/NaClO氧化体系。
ISOGAI等[56]认为TEMPO氧化预处理在未来具有工业化应用的前景:首先,TEMPO氧化预处理制备的MFC微纤丝虽然直径在纳米级别,但是微纤丝长度仍处于微米级别,因此,氧化后纤维非常容易洗涤、脱水浓缩,这有利于其储存和运输。此外,TEMPO氧化预处理对原料的适应性好,因此不存在原料方面的问题。
5.5 高碘酸盐氧化预处理
高碘酸盐可以选择性切断纤维素分子链上葡萄糖单元C2—C3键,并将C2、C3位置上的游离羟基氧化成醛基,即双醛纤维素(DAC)。通过进一步的化学处理,醛基可以很容易的被转换成其它功能性基团:双醛纤维素上的醛基可以和伯胺反应生成亚胺,制备成的凝胶可以用于化妆品和食品领 域[87]。KIM和KUA等[88]将双醛纤维素上的醛基进一步氧化成羧基,并制备成一种水凝胶,用来作为离子交换色谱柱的填充物。
如图9所示,LIIMATAINEN等[21]以漂白桦木浆为原料,采用高碘酸盐氧化制备双醛纤维素,然后用亚氯酸钠氧化处理将醛基进一步氧化成羧基,在纤维素分子C2、C3位引入负电荷,最后用去离子水将氧化后的浆料配置成0.5%的浆料悬浮液,调节pH为7.5,然后在25~95MPa的压力下均质,直到浆料悬浮液变成均匀透明的MFC凝胶。实验结果表明:在不同氧化条件下,采用这种方式制备MFC的得率在51%~91%之间(其中,高碘酸盐氧化得率为91%~100%,亚氯酸钠氧化得率为66%~100%,高压均质得率为85%~100%),预处理后羧基含量高于0.38mmol/g,均质至多4个循环即可制得直径(25±6)nm的MFC凝胶,这一结果与采用TEMPO氧化相近。LIIMATAINEN认为在纤维素分子上引入负电荷可以增加纤维之间的静电斥力,同时破坏纤维素分子之间的氢键连接,此外,预处理过程中纤维的润胀及一定程度的降解对后续的纤维纤化处理也是有益的。为了研究高碘酸盐氧化和亚氯酸钠氧化预处理对高压均质处理的影响机制,LIIMATAINEN分别研究了均质前氧化纤维素浆料悬浮液的电解质浓度和pH对均质过程的影响,他发现增加电解质浓度会降低纤维素分子之间的静电斥力,使得均质循环的次数增加。在相同羧基含量的情况下,降低浆料悬浮的pH甚至会造成均质机的堵塞,这是因为随着pH的降低,纤维素分子上的羧基电离程度减小,纤维素分子之间的静电斥力降低。
如图10所示,LIIMATAINEN等[89]以漂白桦木浆为原料,采用高碘酸盐氧化制备双醛纤维素,然后再与偏亚硫酸钠(Na2S2O5)进行磺化反应,在纤维素分子C2、C3位引入磺酸基,最后用去离子水将氧化后的浆料配制成浓度为0.5%的浆料悬浮液,调节pH为7.0,然后在40~95MPa的压力下均质,直到浆料悬浮液变成均匀透明的MFC凝胶。实验结果表明:经过磺化处理之后,只有15%~30%的醛基能够转化成磺酸基,但磺酸基含量达到0.18mmol/g时,均质5次就可以得到直径10~60nm的透明MFC凝胶,而采用TEMPO氧化预处理后,浆料羧基含量需要达到0.8mmol/g才能达到类似效果。根据TSUGUYUKI等[82,84]的研究,MFC凝胶的透明度与纤维的宽度有很大关系,而采用TEMPO氧化法制得的MFC凝胶,通常为直径3~5nm的单根原细纤维。LIIMATAINEN认为冷冻干燥过程中纤维会发生聚集,造成采用场发射扫描电镜法测得的MFC凝胶的纤维宽度偏高,因此,采用高碘酸盐氧化-磺化预处理所制得的MFC凝胶的纤维实际宽度应小于10~60nm。当浆料磺酸基含量为0.51mmol/g时,均质3个循环即可得到透明的凝胶状MFC,而继续均质至5个循环,凝胶状的MFC会转变为透明液体状。LIIMATAINEN认为这是由于磺酸基含量高会更多的暴露微纤丝,在均质的过程中发生机械降解造成纤维长度下降。与其他预处理方法相比,高碘酸盐氧化-磺化预处理更加环保,因为高碘酸盐氧化后的废液只需收集并加入一定量的次氯酸钠就可以活化并且重新回用,而后续的磺化反应条件较低,且不会产生含卤化物的废水。需要指出的是,经过高碘酸盐氧化-磺化预处理之后,纤维素中还存在大量未反应的醛基,而醛基的存在极易造成纤维发生β-烷氧基消除化反应造成纤维的降解,尤其至在碱性条件下,因此,采用这种预处理方式制备MFC需要考虑残余醛基的处理问题[84]。
6 MFC干燥
无论是化学或是机械处理制备纳米纤维素均是在液体介质中进行。通常,经过预处理和机械处理制备得到的MFC悬浮液或凝胶浓度均较低。MFC浓度较低除了为保证MFC中纤维的高度分散状态、维持其纳米尺寸之外,现有方法无法在高浓状态下制备高度分散且具有纳米尺寸的MFC也是其浓度较低的主要原因之一。低浓度的MFC不仅会影响其应用,也会增加运输、储存成本。但是MFC在常规干燥过程中,水分在温度的作用下被过快的蒸发除去,会造成纤维之间不可逆的聚集(角质化),进而影响MFC的纳米尺寸及结构[90]。因此,对低浓度的MFC进行有效浓缩、干燥是MFC规模化制备及应用所面临的重大挑战之一[91]。
MFC悬浮液中水分的蒸发一般包括3个阶段:①干燥速率恒定,MFC悬浮液体积减小;②MFC悬浮液体积进一步减小,纤维流动性和扩散性降低,干燥速率第一次下降;③水分子向外部的传质速率低于水分子向液面的传质速率,干燥速率第二次下降。一旦MFC的干燥进入第三个阶段,MFC悬浮液中纤维之间的距离减小到一定程度后,纤维素分子间的羟基就会发生作用产生氢键,使得经过干燥后的MFC无法有效再分散[90]。MFC常用的干燥方法有烘箱干燥、冷冻干燥、喷雾干燥和超临界干燥。PENG等[92,93]分别采用上述四种干燥方法对MFC进行干燥,通过研究不同干燥方式对MFC尺寸、形态、热稳定性和结晶度的影响,比较了4种干燥方式各自的优缺点(见表3)。实验结果表明:经过超临界干燥之后,MFC仍能维持纳米尺寸,但是热稳定性和结晶度低;经过冷冻干燥之后,MFC呈膜状,其厚度仍处于纳米尺度,而热稳定和结晶度仅高于超临界干燥后的MFC;经过喷雾干燥后,MFC呈现颗粒状,其尺寸从纳米到微米间不等,热稳定性优于超临界干燥和喷雾干燥后的MFC。
7 结语
MFC是一种绿色的纤维素基可再生高分子材料,具有广泛应用于制浆造纸、食品包装、医药等多个领域的潜力。长久以来,能耗一直是制约MFC规模化制备的主要问题之一。随着多种预处理方法的提出,MFC的制备能耗得以有效降低,而且MFC的制备效率和品质也逐渐提高。然而,预处理方法的有效应用并没有显著降低MFC的制备成本,相反,一些预处理方法引入的化学药剂所带来的成本,甚至会高于机械法制备MFC的能耗成本。因此,从MFC制备成本和MFC产品品质的角度出发,开发适宜的、低成本的预处理技术,仍是MFC规模化制备所面临的主要问题。

表3 4种干燥方式比较[92-93]
MFC的制备过程通常是在液体介质中进行,对纤维原料预处理以及预处理后纤维的洗涤会产生大量废液,而这些废液无法直接排放,因此,需要对这些废液进行处理或利用以降低制备MFC的环境负荷。此外,对MFC产品的有效浓缩或干燥以及干燥后再分散,是MFC储存、运输以及应用所需考虑的又一个问题。因此,基于以上讨论,仍有许多工作需要开展以克服MFC规模化制备存在的问题。
[1] SIMON J,M LLER H,KOCH R,et al. Thermoplastic and biodegradable polymers of cellulose[J]. Polymer Degradation and Stability,1998,59(1):107-115.
[2] DIOTALLEVI F,MULDER B. The cellulose synthase complex:a polymerization driven supramolecular motor[J]. Biophys. J.,2007,92(8):2666-2673.
[3] ZHU H,FANG Z,PRESTON C,et al. Transparent paper:fabrications,properties,and device applications[J]. Energ. Environ. Sci.,2014,7(1):269-287.
[4] BESSUEILLE L,BULONE V. A survey of cellulose biosynthesis in higher plants[J]. Plant Biotechnol.,2008,25(3):315-322.
[5] KAMEL S. Nanotechnology and its applications in lignocellulosic composites,a mini review[J]. Express Polym. Lett.,2007,1(9):546-575.
公众号粉丝数量多且覆盖范围广,影响力大。便于公众号整合行业内资源,使信息传达更加便捷,集中管理更加容易。
[6] LAVOINE N,DESLOGES I,DUFRESNE A,et al. Microfibrillated cellulose——its barrier properties and applications in cellulosic materials:a review[J]. Carbohydrate Polymers,2012,90(2):735–764.
[7] German Version. Nanotechnologies——terminology and definitions for nano-objects——nanoparticle,nanofibre and nanoplate (ISO/TS 27687:2008)[S]. German Version:Vornorm DIN CEN ISO/TS,2008.
[8] OSONG S H,NORGREN S,ENGSTRAND P. Processing of wood-based microfibrillated cellulose and nanofibrillated cellulose,and applications relating to papermaking:a review[J]. Cellulose,2016,23(1):93-123.
[9] ABDUL KHALIL H P,DAVOUDPOUR Y,ISLAM M N,et al. Production and modification of nanofibrillated cellulose using various mechanical processes:a review[J]. Carbohydrate Polymer,2014,99:649-665.
[10] TAPPI. Proposed new TAPPI standard:Standard terms and their definition for cellulose nanomaterial [M]. TAPPI,2011.
[11] ROMAN M,WINTER W T. Effect of sulfate groups from sulfuric acid hydrolysis on the thermal degradation behavior of bacterial cellulose[J]. Biomacromolecules,2004,5(5):1671-1677.
[12] CHEN L,WANG Q,HIRTH K,et al. Tailoring the yield and characteristics of wood cellulose nanocrystals (CNC) using concentrated acid hydrolysis[J]. Cellulose,2015,(3):1753-1762.
[13] SYVERUD K,CHINGA-CARRASCO G,TOLEDO J,et al. A comparative study of Eucalyptus and Pinus radiata pulp fibres as raw materials for production of cellulose nanofibrils[J]. Carbohydrate Polymers,2011,84(3):1033-1038.
[15] SASSI J F,CHANZY H. Ultrastructural aspects of the acetylation of cellulose[J]. Cellulose,1995,2(2):111-127.
[16] IWAMOTO S,KAI W,ISOGAI T,et al. Comparison study of TEMPO-analogous compounds on oxidation efficiency of wood cellulose for preparation of cellulose nanofibrils[J]. Polym. Degrad. Stab.,2010,95(8):1394-1398.
[17] UETANI K,YANO H. Nanofibrillation of wood pulp using a high-speed blender[J]. Biomacromolecules,2011,12(2):348-353.
[18] AMIRALIAN N,ANNAMALAI P K,MEMMOTT P,et al. Isolation of cellulose nanofibrils from Triodia pungensdifferent mechanical methods[J]. Cellulose,2015,22(4):2483-2498.
[19] LEITNER J,HINTERSTOISSER B,WASTYN M,et al. Sugar beet cellulose nanofibril-reinforced composites[J]. Cellulose,2007,14(5):419-425.
[20] ZIMMERMANN T,BORDEANU N,STRUB E. Properties of nanofibrillated cellulose from different raw materials and its reinforcement potential[J]. Carbohydrate Polymers,2010,79(4):1086-1093.
[21] LIIMATAINEN H,VISANKO M,SIRVI J A,et al. Enhancement of the nanofibrillation of wood cellulose through sequential periodate–chlorite oxidation[J]. Biomacromolecules,2012,13(5):1592-1597.
[22] NAKAGAITO A N,YANO H. The effect of morphological changes from pulp fiber towards nano-scale fibrillated cellulose on the mechanical properties of high-strength plant fiber based composites[J]. Appl. Phys. A,2004,78(4):547-552.
[23] LPEZ-RUBIO A,LAGARON J M,ANKERFORS M,et al. Enhanced film forming and film properties of amylopectin using micro-fibrillated cellulose[J]. Carbohydrate Polymers,2007,47(3):249-278.
[24] HERRICK F W,CASEBIER R L,HAMILTON J K,et al. Microfibrillated cellulose:morphology and accessibility[J]. J. Appl. Polym. Sci.:Appl. Polym. Symp.(United States),1983,37:5039044.
[25] TURBAK A F,SNYDER F W,SANDBERG K R. Microfibrillated cellulose,a new cellulose product:properties,uses,and commercial potential[C]//NewYork:J. Appl. Polym. Sci.:Appl. Polym. Symp.(United States),1983-01-01.
[26] TURBAK A F,SNYDER F W,SANDBERG K R. Suspensions containing microfibrillated cellulose:US445272[P]. 1984-07-05.
[27] DUFRESNE A,DUPEYRE D,VIGNON M R. Cellulose microfibrils from potato tuber cells:processing and characterization of starch&ndash;cellulose microfibril composites[J]. J. Appl. Polym. Sci.,2000,76(14):2080-2092.
[28] HABIBI Y,MAHROUZ M,VIGNON M R. Microfibrillated cellulose from the peel of prickly pear fruits[J]. Food Chem.,2009,115(2):423-429.
[29] SPENCE K L,VENDITTI R A,ROJAS O J,et al. A comparative study of energy consumption and physical properties of microfibrillated cellulose produced by different processing methods[J]. Cellulose,2011,18(4):1097-1111.
[30] SPENCE K L,VENDITTI R A,HABIBI Y,et al. The effect of chemical composition on microfibrillar cellulose films from wood pulps:mechanical processing and physical properties[J]. Bioinformation,2010,101(101):5961-5968.
[31] WANG B,SAIN M. Dispersion of soybean stock-based nanofiber in a plastic matrix[J]. Polym. Int.,2007,56(4):538–546.
[32] IWAMOTO S,NAKAGAITO A N,YANO H,et al. Optically transparent composites reinforced with plant fiber-based nanofibers[J]. Appl. Phys. A,2005,81(6):1109-1112.
[33] STELTE W,SANADI A R. Preparation and characterization of cellulose nanofibers from two commercial hardwood and softwood pulps[J]. Indengchemres,2009,48(24):11211-11219.
[34] KARANDE V S,BHARIMALLA A K,HADGE G B,et al. Nanofibrillation of cotton fibers by disc refiner and its characterization[J]. Fibers & Polymers,2011,12(3):399-404.
[35] KUMAR A,SINGH S P,SINGH A K. Preparation and characterization of cellulose nanofibers from bleached pulp using a mechanical treatment method[J]. Tappi Journal,2014,13(5):25-31.
[36] LEE S Y,CHUN S J,KANG I A,et al. Preparation of cellulose nanofibrils by high-pressure homogenizer and cellulose-based composite films[J]. Journal of Industrial & Engineering Chemistry,2009,15(1):50-55.
[37] CHRISTIAN A,SUSANNA A,PETER J,et al. Nanoscale cellulose films with different crystallinities and mesostructures--their surface properties and interaction with water[J]. Langmuir,2009,25(13):7675-7685.
[38] FERRER A,FILPPONEN I,RODR GUEZ A,et al. Valorization of residual empty palm fruit bunch fibers (EPFBF)by microfluidization:production of nanofibrillated cellulose and EPFBF nanopaper[J]. Bioresour Technol.,2012,125C(12):249-255.
[39] TANIGUCHI T,OKAMURA K. New films produced from microfibrillated natural fibres[J]. Polym. Int.,1998,47(3):291-294.
[40] WANG Q Q,ZHU J Y,GLEISNER R,et al. Morphological development of cellulose nanofibrils (CNF) of a bleached eucalyptus pulp by mechanical fibrillation[J]. Cellulose,2012,19(5):1631-1643.
[41] HASSAN M L,MATHEW A P,HASSAN E A,et al. Nanofibers from bagasse and rice straw:process optimization and properties[J]. Wood. Sci. Technol.,2012,46(1-3):193-205.
[42] IWAMOTO S,NAKAGAITO A N,YANO H. Nano-fibrillation of pulp fibres for the processing of transparent nanocomposites[J]. Appl. Phys. A:Mater. Sci. Process,2007,89(2):461-466.
[43] NAIR S S,ZHU J Y,DENG Y,et al. Characterization of cellulose nanofibrillation by micro grinding[J]. Mol. Ecol. Notes,2006,6(1):90-92.
[44] HENRIKSSON M,ISAKSSON B P. Cellulose nanopaper structures of high toughness[J]. Biomacromolecules,2008,9(6):1579-1585.
[45] MATSUDA Y,HIROSE M,UENO K. Super microfibrillated cellulose,process for producing the same,and coated paper and tinted paper using the same:US6214163[P]. 2001-04-10.
[46] DUFRESNE A,CAVAILL J Y,HELBERT W. Thermoplastic nanocomposites filled with wheat straw cellulose whiskers. Part Ⅱ:Effect of processing and modeling[J]. Polym. Compos.,1997,18(2):198-210.
[47] ALEMDAR A,SAIN M. Biocomposites from wheat straw nanofibers:morphology,thermal and mechanical properties[J]. Composites Science & Technology,2008,68(2):557-565.
[48] CHENG Q,WANG S,RIALS T G. Poly(vinyl alcohol) nanocomposites reinforced with cellulose fibrils isolated by high intensity ultrasonication[J]. Composites Part A:Applied Science & Manufacturing,2009,40(2):218-224.
[49] 冯若. 声化学基础研究中的声学问题[J]. 物理学进展,1996,16(3):402-412.
FENG Ruo. the Acoustic problems in in fundamental study on sonochemistry[J]. ProgressinPhysics,1996,16(3):402-412.
[50] IWASAKI T,LINDBERG B,MEIER H. The effect of ultrasonic treatment on individual wood fibers[J]. Svensk Papperstidning,1962,65(20):795-816.
[51] WANG S,CHENG Q. A novel process to isolate fibrils from cellulose fibers by high‐intensity ultrasonication,part 1:process optimization[J]. J. Appl. Polym. Sci.,2009,113(2):1270-1275.
[52] CHEN W,YU H,LIU Y,et al. Isolation and characterization of cellulose nanofibers from four plant cellulose fibers using a chemical-ultrasonic process[J]. Cellulose,2011,18(2):433-442.
[53] HUANG Z M,ZHANG Y Z,KOTAKI M,et al. A review on polymer nanofibers by electrospinning and their applications in nanocomposites[J]. Composites Science & Technology,2003,63(15):2223-2253.
[54] AULIN C,GÄLLSTEDT M,LINDSTRÖM T. Oxygen and oil barrier properties of microfibrillated cellulose films and coatings[J]. Cellulose,2010,17(3):559-574.
[55] ANKERFORS M. Microfibrillated cellulose :energy-efficient preparation techniques and key properties[R].Stockholm:KTH Royal Institute of Technology,2012.
[56] ISOGAI A,TSUGUYUKI S,HAYAKA F. TEMPO-oxidized cellulose nanofibers[J]. Nanoscale,2010,3(1):71-85.
[57] ERIKSEN. The use of microfibrillated cellulose produced from kraft pulp as strength enhancer in TMP paper[J]. Nord. Pulp. Pap. Res. J.,2008,23(3):299-304.
[58] SZCZĘSNA-ANTCZAK M,KAZIMIERCZAK J,ANTCZAK T. Nanotechnology——methods of manufacturing cellulose nanofibres[J]. Fibres and Texitiles in Eastern Europe,2012,20(2):8-12.
[59] FUKUZUMI H,SAITO T,OKITA Y,et al. Thermal stabilization of TEMPO-oxidized cellulose[J]. Polym. Degrad. Stab.,2010,95(9):1502-1508.
[60] MILLER Jack. Nanocellulose:technology applications,and markets [C]//Vancouver,BC:TAPPI International Conference on Nanotechnology for Renewable Materials. 2014.
[61] HENRIKSSON M,HENRIKSSON G,BERGLUND L A,et al. An environmentally friendly method for enzyme-assisted preparation of microfibrillated cellulose (MFC) nanofibers[J]. Eur. Polym. J.,2007,43(8):3434-3441.
[62] MISSOUM K,BELGACEM M N,BRAS J. Nanofibrillated cellulose surface modification:a review[J]. Materials,2013,6(5):1745-1766.
[63] PÄÄKKÖ M ,VAPAAVUORI J,SILVENNOINEN R,et al. Long and entangled native cellulose I nanofibers allow flexible aerogels and hierarchically porous templates for functionalities[J]. Soft Matter,2008,4(12):2492-2499.
[64] HOEGER I C,NAIR S S,RAGAUSKAS A J,et al. Mechanical deconstruction of lignocellulose cell walls and their enzymatic saccharification[J]. Cellulose,2013,20(2):807-818.
[65] Innventia. Nanocellulose for the first time on a large scale[R]. Sweden:Innventia. 2011.
[66] QVINTUS Pia. Cellulose nanofibrils:overcoming challenges on the development of nanocellulose-based products [C]//Proceedings of the TAPPI International Conference on Nanotechnology for Renewable Materials,Atlanta,GA,2015 .
[67] SAIN M M,BHATNAGAR A. Manufacturing process of cellulose nanofibers from renewable feed stocks:US20080146701A1[P]. 2008-06-19.
[68] SAIN M M,BHATNAGAR A. Manufacturing of nano-fibrils from natural fibres,agro based fibres and root fibres:CA2437616A1[P]. 2005-02-04.
[69] HAN J Q,ZHOU C J,WU Y Q,et al. Self-assembling behavior of cellulose nanoparticles during freeze-drying:effect of suspension concentration,particle size,crystal structure,and surface charge[J]. Biomacromolecules,2013,14(5):1529-1540.
[70] WALECKA J A. An investigation of low degree of substitution carboxymethylcelluloses[J]. Georgia Institute of Technology,1956,
[71] WÅGBERG L,DECHER G,NORGREN M,et al. The build-up of polyelectrolyte multilayers of microfibrillated cellulose and cationic polyelectrolytes[J]. Langmuir the Acs Journal of Surfaces & Colloids,2008,24(3):784-795.
[72] EYHOLZER C,BORDEANU N,LOPEZ-SUEVOS F,et al. Preparation and characterization of water-redispersible nanofibrillated cellulose in powder form[J]. Cellulose,2010,17(1):19-30.
[73] TAIPALE T,ÖSTERBERG M,NYK NEN A,et al. Effect of microfibrillated cellulose and fines on the drainage of kraft pulp suspension and paper strength[J]. Cellulose,2010,17(17):1005-1020.
[74] SIRÓ I,PLACKETT D,HEDENQVIST M,et al. Highly transparent films from carboxymethylated microfibrillated cellulose:the effect of multiple homogenization steps on key properties[J]. J. Appl. Polym. Sci.,2011,119(5):2652–2660.
[75] SEMMELHACK M F,CHOU C S,CORTES D A. Nitroxyl-mediated electrooxidation of alcohols to aldehydes and ketones[J]. Jamchemsoc,1983,105(13):4492-4494.
[76] SEMMELHACK M F,SCHMID C R,CORTES D A,et al. Oxidation of alcohols to aldehydes with oxygen and cupric ion,mediated by nitrosonium ion[J]. Jamchemsoc,1984,106(11):3374-3376.
[77] ANELLI P L,BIFFI C,MONTANARI F,et al. Fast and selective oxidation of primary alcohols to aldehydes or to carboxylic acids and of secondary alcohols to ketones mediated by oxoammonium salts under two-phase conditions[J]. J. Org. Chem.,1987,52(12):2559-2562
[78] DE NOOY A E J,BESEMER A C,BEKKUM H V. Selective oxidation of primary alcohols mediated by nitroxyl radical in aqueous solution. Kinetics and mechanism[J]. Tetrahedron,1995,51(29):8023-8032.
[79] ISOGAI A,KATO Y. Preparation of polyuronic acid from cellulose by TEMPO-mediated oxidation[J]. Cellulose,1998,5(3):153-164.
[80] PÄÄKKÖNEN T,DIMIC-MISIC K,ORELMA H,et al. Effect of xylan in hardwood pulp on the reaction rate of TEMPO-mediated oxidation and the rheology of the final nanofibrillated cellulose gel[J]. Cellulose,2015,23(1):1-17.
[81] MAO L,LAW K,CLAUDE D,et al. Effects of carboxyl content on the characteristics of TMP long fibers[J]. Indengchemres,2008,47(11):3809-3812.
[82] TSUGUYUKI S,SATOSHI K,YOSHIHARU N,et al. Cellulose nanofibers prepared by TEMPO-mediated oxidation of native cellulose[J]. Biomacromolecules,2007,8(8):2485-2491.
[83] YOSHIDA Y,YANAGISAWA M,ISOGAI A,et al. Preparation of polymer brush-type cellulose β-ketoesters using LiCl/1,3-dimethyl-2-imidazolidinone as a solvent[J]. Polymer,2005,46(8):2548–2557.
[84] TSUGUYUKI S,MASAYUKI H,NAOYUKI T,et al. Individualization of nano-sized plant cellulose fibrils by direct surface carboxylation using TEMPO catalyst under neutral conditions[J]. Biomacromolecules,2009,10(7):1992-1996.
[85] TSUGUYUKI S,YOSHIHARU N,JEAN-LUC P,et al. Homogeneous suspensions of individualized microfibrils from TEMPO-catalyzed oxidation of native cellulose[J]. Biomacromolecules,2006,7(6):1687-1691.
[86] HIROTA M,TAMURA N,SAITO T,et al. Oxidation of regenerated cellulose with NaClO2catalyzed by TEMPO and NaClO under acid-neutral conditions[J]. Carbohydrate Polymers,2009,78(2):330-335.
[87] RINAUDO M. Periodate Oxidation of methylcellulose:characterization and properties of oxidized derivatives[J]. Polymers:Basel,2010,2(4):505-521.
[88] KIM U J,KUGA S,WADA M,et al. Periodate oxidation of crystalline cellulose[J]. Biomacromolecules,2000,1(3):488-492.
[89] LIIMATAINEN H,VISANKO M,SIRVI J,et al. Sulfonated cellulose nanofibrils obtained from wood pulp through regioselective oxidative bisulfite pre-treatment[J]. Cellulose,2013,20(2):741-749.
[90] ZIMMERMANN M V,BORSOI C,LAVORATTI A,et al. Drying techniques applied to cellulose nanofibers[J]. J. Reinf. Plast. Compos.,2016,
[91] BECK S,BOUCHARD J,BERRY R. Dispersibility in water of dried nanocrystalline cellulose[J]. Biomacromolecules,2012,13(5):1486-1494.
[92] PENG Y,GARDNER D J,HAN Y,et al. Influence of drying method on the material properties of nanocellulose Ⅰ:thermostability and crystallinity[J]. Cellulose,2013,20(5):2379-2392.
[93] PENG Y,GARDNER D J,HAN Y. Drying cellulose nanofibrils:in search of a suitable method[J]. Cellulose,2012,19(19):91-102.
Properties and preparation progress of microfibrillated cellulose:a review
GAO Yanhong1,SHI Yu2,TIAN Chao2,LI Qun1,LIU Weizhe3
(1Tianjin Key Laboratory of Pulp and Paper,Tianjin University of Science and Technology,Tianjin 300457,China;2China National Pulp and Paper Research Institute,Beijing 100102,China;3Jilin Chenming Paper Co.,Ltd.,Jinlin,132000,Jinlin,China )
Microfibrillated Cellulose(MFC)is a renewable macromolecular material derived from lignocellulosic fiber,which possesses the characteristic of natural cellulose and nanomaterials. Recently,many studies have been carried out in the preparation,modification,and application of MFC. However,its application is hampered by the high cost,dry methods and re-dispersability,especially in large scale production of MFC. To better understand the properties and progress of microfibrillated cellulose preparation,the characteristic and definition of MFC were firstly investigated,and the different mechanical preparation methods of MFC were discussed,including high pressure homogenization treatment,microfluidization treatment,ultrafine grinding treatment,cryocrushing treatment and high intensity ultrasonication treatment. Subsequently,the problems of mechanical preparation of MFC were analyzed. The pretreatment methods for MFC preparation were also presented,including cellulase pretreatment,alkaline-acid pretreatment,carboxymethylation pretreatment,TEMPO oxidation pretreatment,and periodate oxidation pretreatment. Finally,the problems existing in the preparation and dry process of MFC in large scale were summarized.
nanomaterials;cellulose;microfibrillated cellulose;pretreatment;mechanical preparation progress
TS727+.1
A
1000–6613(2017)01–0232–15
10.16085/j.issn.1000-6613.2017.01.030
2016-06-02;修改稿日期:2016-06-28。
天津市自然科学基金重点项目(16JCZDJC37700)。
高艳红(1988—),女,博士研究生。通讯作者:李群,教授,博士生导师,主要从事制浆清洁生产、植物纤维资源综合利用方面的研究。E-mail:liqun@tust.edu.cn。

