儿童心室辅助装置发展现状
孟凡,杨明,胡仁杰
1.上海交通大学 电子信息与电气工程学院 仪器科学与工程系,上海200240;2. 上海交通大学医学院附属上海儿童医学中心 心胸外科,上海200127
儿童心室辅助装置发展现状
孟凡1,杨明1,胡仁杰2
1.上海交通大学 电子信息与电气工程学院 仪器科学与工程系,上海200240;2. 上海交通大学医学院附属上海儿童医学中心 心胸外科,上海200127
编者按:作为心力衰竭治疗和等待心脏移植的重要手段,人工心脏辅助治疗心力衰竭患者的2年生存率已从早期的25%提高到目前的78%,接近于心脏移植的2年生存率。人工心脏辅助循环装置也已从早期的只能植入体表面积较大患者的容积式搏动血泵,转向体积较小、寿命更长的旋转平流血泵,甚至更进一步有望提供与血液不接触的直接心室辅助。目前人工心脏辅助研究的主要热点有儿童心室辅助、平流式血泵的搏动控制和人工心脏对血液破坏等,本专栏就以上内容为读者提供相关的研究进展。

栏目主编:杨明
杨明,上海交通大学电子信息与电气工程学院仪器科学与工程系教授。1985年本科毕业于东北重型机械学院检测技术专业,1990年研究生毕业于西安交通大学电测专业,1996年博士毕业于天津大学精密仪器及机械专业,1998年南京航空航天大学超声电机研究中心博士后出站。自2002起在英国利兹大学开始从事应用于人工心脏肌肉的超声器件研究,2005年回国工作以来,在包括国家自然基金科学仪器基础研究专款等国家自然基金和上海浦江人才计划和医疗器械科技支撑等的资助下,研制成功精密匹配搏动式人工心脏和非血液接触人工心脏辅助装置。其中搏动式血泵动态响应时间小于70 ms,尺寸已缩小到:直径60 mm,高度40 mm。目前已授权中国发明专利20余件,发表国际刊物论文20余篇。
越来越多的儿童心衰患者需要采用心室辅助装置进行移植过渡与心功能恢复治疗,而目前儿童用辅助装置的发展严重落后于成人辅助装置,临床选择非常有限。本文介绍了目前临床中使用的几种儿童用辅助装置以及国内外在该方面的研究进展。由于不同年龄儿童的生理参数差异以及儿童异于成人的某些特殊辅助需求,儿童心室辅助装置需要向多规格、小体积、搏动性、智能化等方向发展。
心室辅助装置;血泵;儿童
0 前言
目前小儿心脏病患者的人数在不断上升[1],其中发展为心力衰竭的人数也在不断提高,据统计每年约有15000例小儿心力衰竭被确诊,但由于手术水平的提高以及术后护理的改善,存活率在稳步上升。所有小儿心衰患者都具有低心排特征以及器官衰竭的潜在危险,其中约有10%~15%的患者需要机械辅助循环(Mechanical Circulatory Support,MCS)用以治疗[2]。对于此类危重病例,国外普遍采用辅助循环系统予以生命维持与心功能恢复,而由于经济条件以及医疗水平的限制,国内只有为数不多的医疗机构能够提供短期的心脏辅助循环治疗[3]。MCS分为体外膜肺氧合(Extracorporeal Membrane Oxygenation,ECMO)以及心室辅助装置(Ventricular Assist Devices,VAD),这两种装置在国内均已被用以小儿心功能不良的治疗[4]。ECMO在上世纪70年代中期被成功应用于临床,目前使用非常广泛技术相对成熟,多用于各种情况下的心肺功能支持,短期心室辅助以及急救。ECMO在辅助超过2周后血栓和出血等多种并发症的发生概率将大大升高,所以ECMO在应用于心室辅助时只能作为短期辅助以及配合药物的短期心功能恢复[5]。最早的VAD出现在上世纪60年代早期的美国,Liotta等将一个管状的心室辅助装置植入在左心房和降主动脉之间。VAD第一次成功应用于临床是DeBakey[6]在1967年采用一个VAD连接左心房和右锁骨下动脉对患者进行心功能辅助,该患者最后成功过渡到心脏移植。经过几十年的发展,VAD在成人辅助方面从装置的设计到医疗水平都取得了长足的进步,多种类型及不同特点的成人用VAD被研发出来并应用于临床,而由于儿童发生心衰的比例及数量都远小于成人,故儿童用VAD的市场相对较小,该领域的投入也相对较少,导致目前儿童用VAD的发展与儿童心室辅助的需求不相匹配,可用于临床的儿童用VAD选择非常有限,有相当一部分比例的儿童患者采用了成人用VAD进行辅助,但有数据显示,由于成人与儿童的生理参数不同,VAD的尺寸等其他参数也不尽相同,采用成人用VAD对体表面积较小的患者进行辅助,效果较差[7],而选择适合尺寸的VAD对儿童患者进行辅助则可以有效减少术后并发症的发生[8]。
1 辅助装置
心脏移植依旧是目前对于儿童心衰患者的最终的治疗手段,但由于供体严重不足,患者通常等待合适供体的时间较长,VAD能起到维持患者生命直到心脏移植的过渡作用[9],另外VAD还可以用于配合药物的心功能恢复治疗和终末期治疗。从辅助时间上看小儿VAD分为长期辅助型和短期辅助型,长期辅助型可以提供从几周到数月的辅助支持,短期辅助型则提供少于2周的心功能辅助[10]。图1是通常在选择辅助循环装置时的判断依据以及过程。
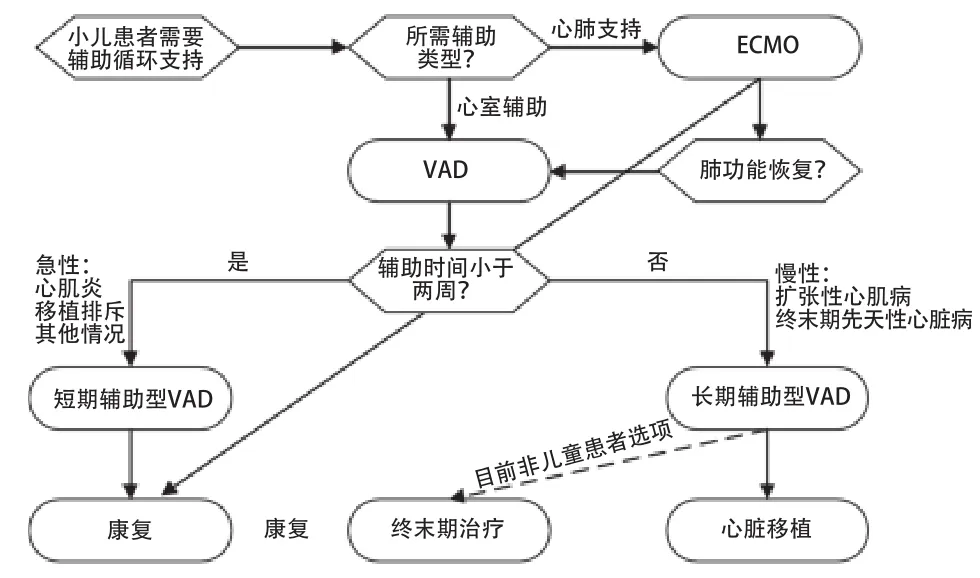
图1 辅助循环装置选择流程
另外,从泵体输出特性上分,小儿VAD又可分为搏动型与恒流型。搏动型主要指气动泵,原理主要为改变血腔容积对血液进行挤压再配合进出口瓣膜形成单向流动的搏动血流,Berlin Heart EXCOR即是一款临床使用的搏动型小儿VAD;恒流型主要分为离心泵和轴流泵,均通过高速旋转的叶片驱动血液,恒流泵不需要瓣膜,通常体积较搏动泵小。
1.1 长期辅助装置
Berlin Heart EXCOR(Berlin Heart Inc.,Berlin,Germany)是目前应用最广的长期辅助型儿童心室辅助装置,也是美国食品药品监督管理局(Food and Drug Administration,FDA)唯一批准的用于长期辅助的儿童心室辅助装置[5]。其主体为一个气动的搏动泵,主要由血腔以及连接在血腔上的进出口组成,进出口内分别安装了单向瓣膜,气动驱动器输出气流推动与血腔相连的推板,从而改变血腔容积实现血液的单向搏出[11]。Berlin Heart EXCOR具有适合不同年龄段儿童的不同尺寸的泵体,能够提供从10 mL到60 mL的每搏输出量,理论上可以用于最小体重为3 kg的婴儿[12]。另外它可以用于单心室辅助和双心室辅助。
Thoratec VAD(IVAD/PVAD,Thoratec Co., Pleasanton,CA,USA)其主体也是一款气动的搏动泵,最高可以输出7 L/min流量,每搏输出量为65 mL。IVAD可以植入,体积比作为体旁辅助的PVAD略小,IVAD也可以作为左心辅助、右心辅助以及双心室辅助。Thoratec VAD被FDA批准作为移植过渡使用[13],作为第一代VAD有将近30年的临床使用历史,可以用于体表面积较大的青少年。
HeartWare HVAD (HeartWare Systems,Framington,MA,USA)是第三代VAD,2012年被FDA批准可以作为心脏移植过渡使用。HVAD是一款体积较小,可以植入心包腔内的离心泵[14],曾辅助过最小体表面积为0.7 m2的患者,但有文献建议不要辅助体表面积<1.5 m2的患者[15]。
HeartMate II(Thoratec Co., Pleasanton,CA,USA)是一款被FDA批准用作心脏移植过渡和终点治疗的可植入轴流泵,其在全世界已经有超过一万例用于成人左心辅助的案例。HeartMate II的泵体体积非常小,重约290 g,长度7 cm,直径4 cm,无瓣膜,泵内仅有一个运动部件,这大大减小了泵的复杂性,同时提高了可靠性,它可以提供>2.5 L/min的流量,用于体表面积>1.4 m2的患者[16]。
另外,SynCardia全人工心脏(SynCardia Systems,Tucson,AZ,USA)是一款可植入的双心室辅助全人工心脏,被FDA批准可以作为移植过渡使用。其可提供最大9.5 L/min的搏动流输出,具有70 mL和50 mL每搏输出量的2种搏动泵,分别可以适用于体表面积>1.7 m2和1.2~1.7 m2的患者[17]。全世界目前有超过1200例的植入记录,根据最近的SynCardia数据显示,该全人工心脏有24例应用于先天性心脏病患者,其中6例为12~18岁的青少年。由于体积原因,该全人工心脏使用前要对患者的胸腔空间进行评估以判断是否适合植入[18]。
可以提供长期辅助的儿童VAD目前只有Berlin Heart,但其仍存在血栓等诸多并发症,且作为体旁辅助它的动力及控制系统体积较大,对患者的移动有很大限制,降低了患者的生活质量。所以在儿童长期心室辅助方面目前的选择还非常有限。
1.2 短期辅助装置
Jostra RotaFlow离心泵(MaQUET Cardiovascular,Wayne,NJ,USA)是一款可以用于儿童和成人的离心泵,其预充量为32 mL,可以提供最大10 L/min的流量。该泵由电磁式电机驱动,泵头内采用磁悬浮支持与单点机械支撑结合的方式支撑叶片旋转。通过磁悬浮支持方式可以减少叶片旋转时的机械摩擦及发热,从而减少溶血和机械磨损[19]。该泵常与氧合器配合使用,组成ECMO用于短时辅助[20],一般辅助时间不超过2周。
Thoratec PediMag(Thoratec Co., Pleasanton,CA,USA)PediMag是一款专为儿童设计的VAD,其离心泵泵头内采用全磁悬浮设计,叶片不受机械支撑与摩擦,因此PediMag比其他的离心泵在叶片旋转时产生更少的热量和血液破坏。其最大提供1.5 L/min流量[10],最小可以辅助支持体重为3 kg的病人,最大可适用于体表面积为1.3 m2的儿童,其作为ECMO的泵体已经在全世界大范围使用,通常辅助时间为2周内,最近几年其作为单独心室辅助泵的使用正在不断扩展[15]。
Tandem Heart(Cardiac Assist Inc.,Pittsburgh,PA,USA)是一个用于体旁辅助的离心泵,可以提供最大5 L/min的连续流量,预充量非常小(10 mL)。该泵可以经皮进行放置,其入口经过股静脉进入体内与左心房连接,出口与股动脉连接。FDA批准Tandem Heart可以用于体表面积>1.3 m2的患者作少于6 h的短时辅助。
此外,美国国家心肺和血液研究所在2010年启动了PumpKIN(Pumps for Kids,Infants and Neonates)项目,该项目主要进行FDA针对小儿辅助循环装置能够进入临床审批所需的前期研究及实验。项目共资助了4家合作单位分别研发4个辅助循环装置。目前该项目中仅有Jarvik Pediatric 2000(Jarvik Heart, Inc.,New York,USA)在不断优化并进入到临床前实验,有望最终进入临床,其他三个装置离临床使用还有较大的距离[21]。Jarvik Pediatric 2000是一款可以植入心室内部的轴流泵,其体积非常小,预充量仅有1 mL[10],其被验证比HeartMate II更适合植入,术中所需输血更少,拔管时间更短以及可以通过左胸骨切开术进行植入,这些特点都使得其更适合于儿童或者婴儿患者[22]。表1对目前常用的儿童心室辅助装置的基本参数进行了总结。
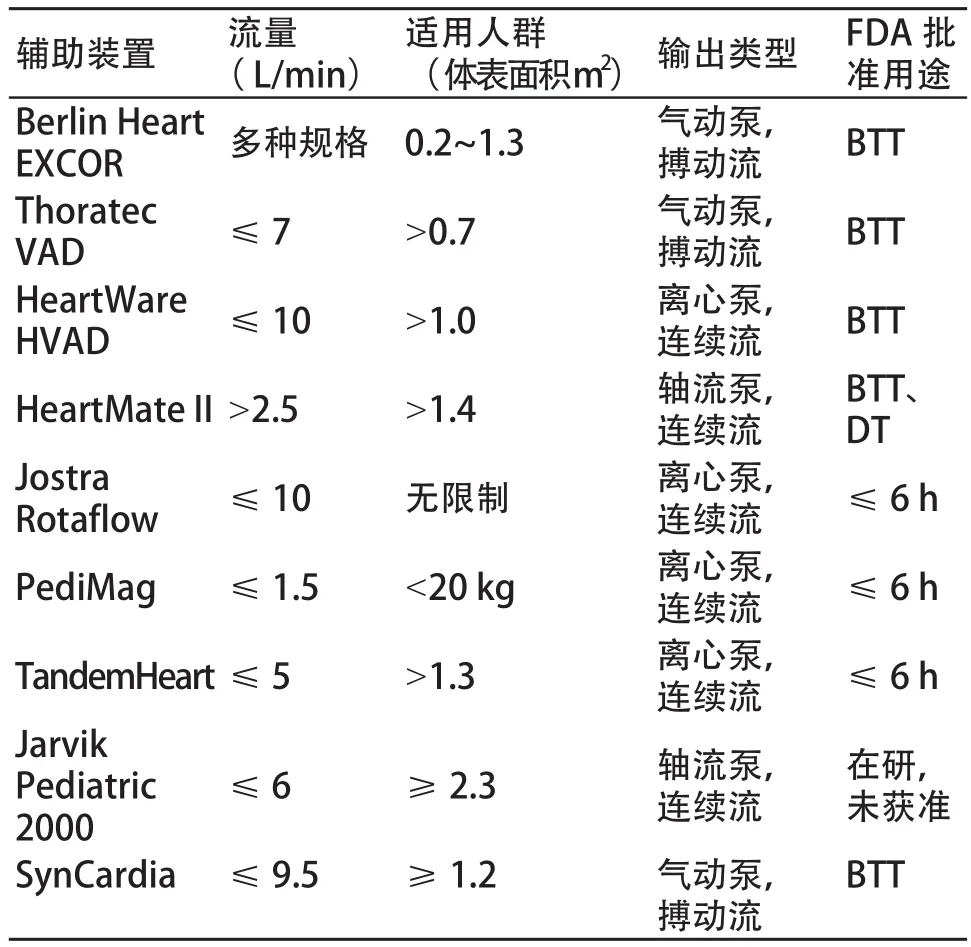
表1 常用儿童心室辅助装置的基本参数
1.3 国内研究现状
目前国内在儿童心室辅助装置研发方面还处于起步阶段,进行研究的机构较少,有一些项目还在研发阶段,没有能够进入临床使用的辅助装置,其中广东心血管病研究所根据成人用罗叶泵研制出一种每搏输出量20 mL的儿童用罗叶泵(图2a),该泵为一款气动搏动泵,泵体长148 mm,宽58 mm,高42 mm,采用隔膜将泵体分为气室腔与血室腔,配合进出口瓣膜形成单向血流。在该泵的动物存活实验中数只实验羊平均存活79.8 h[23-24]。另外,上海交大仪器科学与工程系自主研发出一款可用于儿童心室辅助的VAD,其主体为一款直径60 mm,高度40 mm的超声致动搏动泵(图2b),每搏输出量14 mL,最大输出平均压160 mmHg,最大输出流量3 L/min,平均压110 mmHg时输出流量可达2.0 L/min。

图2 国内儿童心室辅助装置
2 术后并发症
使用VAD进行治疗也同时存在神经、血液、肠胃以及免疫方面的一些并发症,其中某些方面是与血泵本身特性相关的。中风是其中非常危险的一种并发症,在搏动泵中发生概率较高。中风可能由出血和血栓引起,而其中血栓主要由血泵的表面凝血形成,临床发现搏动泵较恒流泵更易产生血栓,故采用搏动泵时需要更加复杂的抗凝治疗与管理[12]。
出血是另一个主要的并发症,主要发生在术后短期内。在Berlin Heart的对比试验中,体表面积<0.7 m2和0.7~1.5 m2的患者分别有42%和50%的概率发生术后出血[25]。几乎所有患者术后都需要抗凝治疗,而小儿抗凝药物的使用控制则呈现多样性且相对比较复杂[26]。有数据显示采用Berlin Heart EXCOR的病例中出现脑血管方面并发症的概率为30%,包括脑缺氧和脑出血,其中脑缺氧更为常见而脑出血危害更加严重[27]。脑血管并发症与抗凝治疗关系密切,多发生在术后抗凝治疗还没有起效之前,临床发现如配备专职抗凝医师会减少其发生概率[28]。故降低VAD所需的抗凝治疗等级可减少脑血管并发症的发生[29]。
另外,感染也是一种常见的并发症,多因长期住院和侵入式治疗产生,或接触VAD所需的电线、硬件、泵体包裹套等相关部产生。目前多采用抗生素及抗真菌药物治疗。
3 总结与展望
目前成人用VAD已发展比较成熟,而儿童用VAD发展还相对比较落后,临床可供选择的VAD非常有限。由于不同体表面积的儿童所需的辅助参数,如压力、流量等也不相同且儿童胸腔尺寸非常有限,故目前儿童心室辅助面临的最大问题是研制出不同输出参数的血泵以满足不同体表面积儿童的需要。由于儿童用VAD在临床中,主要用于心脏移植前的等待和心功能恢复治疗等,而搏动流可提高器官微循环灌注,故儿童较成人更需搏动流辅助。为避免并发症的发生,需要经常性地对人体血液循环进行检验,但对儿童进行抽血检验并不是一件容易的工作。因此,开发出具有自诊断功能儿童心室辅助装置尤其重要!综上所述,儿童用VAD需要向多规格、小体积、搏动性、智能化方向发展。
[1] Pirouz S,Matthew H,Rossano JW,et al.Characteristics and outcomes of heart failure-related intensive care unit admissions in children with cardiomyopathy[J].J Card Fail,2013,19(10):672-677.
[2] Rossano JW,Kim JJ,Decker JA,et al.Prevalence, morbidity, and mortality of heart failure-related hospitalizations in children in the United States:a population-based study[J].J Card Fail,2012, 18(6):459-470.
[3] Zhu DM,Wang W,Chen H,et al.Left ventricular assist device for pediatric postcardiotomy cardiac failure[J].ASAIO J,2006, 52(5):603-604.
[4] 王伟,朱德明,张蔚,等.儿童心脏辅助设备的使用[J].中国体外循环杂志,2010,8(3):176-179.
[5] Mascio CE.The use of ventricular assist device support in children: the state of the art[J].Artif Organs,2015,39(1):14-20.
[6] DeBakey ME.Left ventricular bypass pump for cardiac assistance: Clinical experience[J].Am J Cardiol,1971,27(1):3-11.
[7] Blume ED,Naftel DC,Bastardi HJ,et al.Outcomes of children bridged to heart transplantation with ventricular assist devices:A multi-institutional study[J].Circulation,2006,113(19):2313-2319.
[8] Husain SA,Wallis G,Fricker FJ,et al.Ventricular assist device implantation in the pediatric population:does pump size selection and associated hemodynamics impact outcomes[J]?ASAIO J,2008,54(5):474-478.
[9] Luo JM,Chou NK,Chi NH,et al.Pediatric heart transplantation bridged with ventricular assist devices[J].Transplant Proc,2010, 42(3):913-915.
[10] Lorts A,Zafar F,Adachi I,et al.Mechanical assist devices in neonates and infants[J].Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu,2014,17(1):91-95.
[11] Kirklin JK, Bennett Pearce F,Dabal RJ,et al.Mechanical circulatory support:strategies and outcomes in pediatric congenital heart disease[J].Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu,2014,17(1):62-68.
[12] O'Connor MJ,Rossano JW.Ventricular assist devices in children[J].Curr Opin Cardiol,2014,29(1):113-121.
[13] Yuki K,Sharma R,DiNardo J.Ventricular-assist device therapy in children[J].Best Pract Res Clin Anaesthesiol,2012,26(2):247-264.
[14] Padalino MA,Bottio T,Tarzia V,et al.HeartWare ventricular assist device as bridge to transplant in children and adolescents[J].Artif Organs,2014,38(5):418-422.
[15] Wilmot I,Lorts A,Morales D.Pediatric mechanical circulatory support[J].Korean J Thorac Cardiovasc Surg,2013,46(6):391-401.
[16] Mossad EB,Motta P,Rossano J,et al.Perioperative management of pediatric patients on mechanical cardiac support[J].Paediatr Anaesth,2011,21(5):585-593.
[17] Copeland JG,Smith RG,Arabia FA,et al.Cardiac replacement with a total artificial heart as a bridge to transplantation[J].N Engl J Med,2004,351(9):859-867.
[18] Morales DL,Zafar F,Gaynor JW,et al.The Worldwide Use of SynCardia Total Artificial Heart in Patients with Congenital Heart Disease[J].ISHLT,2013,32(4):S142.
[19] Loforte A,Pilato E,Martin Suarez S,et al.RotaFlow and CentriMag Extracorporeal Membrane Oxygenation Support Systems as Treatment Strategies for Refractory Cardiogenic Shock[J].J Card Surg,2015,30(2):201-208.
[20] Wang S,Evenson A,Chin BJ,et al.Evaluation of Conventional Nonpulsatile and Novel Pulsatile Extracorporeal Life Support Systems in a Simulated Pediatric Extracorporeal Life Support Model[J].Artif Organs,2015,39(1):E1-E9.
[21] Burns KM.Paediatric heart failure research:role of the National Heart, Lung, and Blood Institute[J].Cardiol Young,2015,25(S2):167-171.
[22] Sorensen EN,Pierson RN 3rd,Feller ED,et al.University of Maryland Surgical Experience With the Jarvik 2000 Axial Flow Ventricular Assist Device[J].Ann Thorac Surg,2012,93(1):133-140.
[23] 黄焕雷,祁周措,姚丽明,等.20 mL小儿罗叶泵的动物存活实验[J].北京生物医学工程,2012,31(3):251-257.
[24] 黄焕雷,肖学钧,刘鹏,等.小儿罗叶泵的研制[J].中国医疗设备, 2012,27(10):56-59.
[25] Fraser CD Jr.,Jaquiss RD,Rosenthal DN,et al.Prospective trial of a pediatric ventricular assist device[J].N Engl J Med,2012, 367(6):532-541.
[26] Moffett BS,Cabrera AG,Teruya J,et al.Anticoagulation Therapy Trends in Children Supported by Ventricular Assist Devices[J].ASAIO J,2014,60(2):211-215.
[27] Almond CS,Morales DL,Blackstone EH,et al.Berlin Heart EXCOR pediatric ventricular assist device for bridge to heart transplantation in US children[J].Circulation,2013, 127(16):1702-1711.
[28] Byrnes JW,Prodhan P,Williams BA,et al.Incremental Reduction in the Incidence of Stroke in Children Supported With the Berlin EXCOR Ventricular Assist Device[J].Ann Thorac Surg,2013,96(5):1727-1733.
[29] Miller JR,Lancaster TS,Eghtesady P.Current approaches to device implantation in pediatric and congenital heart disease patients[J].Expert Rev Cardiovasc Ther,2015,13(4):417-427.
Development Status of Ventricular Assist Devices in Children
MENG Fan1, YANG Ming1, HU Ren-jie2
1.Department of Instrument Science and Engineering, School of Electronic Information and Electrical Engineering, Shanghai Jiaotong University, Shanghai 200240, China; 2.Department of Cardiovascular and Thoracic Surgery, Shanghai Children's Medical Center, Shanghai Jiaotong University School of Medicine, Shanghai 200127, China
There has been an increased demand for using ventricular assist devices (VAD) as a bridge to transplant and myocardial recovery in children with end-stage heart failure. The development of pediatric VADs, however, has lagged behind the development of adult ventricular assist devices, which makes the clinical choices of VADs in pediatric care very limited. The purpose of this review is to describe several pediatric VADs in the clinical settings as well as to examine the research progress of VADs both at home and abroad. Because of the different physiological parameters of children of different ages groups, also because of the difference between children and adults, especially of the variances in the the demands of the pumping assistance, pediatric VADs need to developed into multi-modes characterized by small volumes, with pulsatile and intelligent action that emulates the heart.
ventricular assist devices; blood pump; children
R318.1
A
10.3969/j.issn.1674-1633.2016.01.004
1674-1633(2016)01-0016-05
2015-12-21
国家自然科学基金(81571831)。
杨明,教授,博士生导师。
通讯作者邮箱:myang@sjtu.edu.cn

