论海水中氯化钠浓度对挥发酚的影响
杨锡丹


摘要:用实验论证了海水中氯化钠浓度对挥发酚的影响,分析了该实验的试剂选用、标准系列电线的配制及实验原理,实验结果表明:氯化钠对挥发酚的影响并非普通的正比关系。
关键词:挥发酚;氯化钠;浓度;连续流动化学分析仪
中图分类号:X832
文献标识码:A 文章编号:1674-9944(2016)20-0040-03
1 引言
挥发酚指沸点在230℃以下的有毒物质,主要污染源为煤气洗涤、炼焦、合成氨、造纸、木材防腐和化工行业的工业废水。酚类为原生质毒,属于高毒物质,人体摄入一定量会出现急性中毒症状;长期饮用被酚污染的水,可引起头痛、出疹、瘙痒、贫血及各种神经系统症状[1]。因此,在常规水质监测中,挥发酚作为重要检测指标。现用实验做以下论证。
2 试剂、标准系列曲线的配制及实验原理
挥发酚标准溶液、曲拉通、磷酸、4-氨基安替比林、铁氰化钾、氢氧化钠、氯化钾、硼酸、氯化钠以及用于配制各种试剂的蒸馏水。
2.1 试剂选用
(1)50%曲拉通:准备一只50 mL量筒,准确量取50.0 mL曲拉通,用玻璃棒引流至100 mL烧杯中,蒸馏水稀释至100 mL,搅拌均匀,待用。
(2)挥发酚储备缓冲液:准确称取9.00 g硼酸、5.00 g氢氧化钠、10.00 g氯化钾于1000 mL烧杯中,蒸馏水稀释至1000 mL,搅拌均匀,待用。
(3)铁氰化钾溶液:准确称取0.35 g铁氰化钾至100 mL烧杯中,用上述配制的挥发酚储备缓冲液稀释至100 mL,用移液管移取1.00 mL上述50%曲拉通,搅拌均匀,待用。
(4)4-氨基安替吡啉溶液:准确称取0.10 g 4-氨基安替吡啉至100 mL烧杯中,用挥发酚储备缓冲液稀释至100 mL,移液管移取1.00 mL50%曲拉通,搅拌均匀,待用。
(5)挥发酚吸收试剂:准确量取100 mL挥发酚储备缓冲液至100 mL烧杯中,移取1 mL50%曲拉通,搅拌均匀,待用。
(6)挥发酚蒸馏试剂:准确量取160 mL磷酸入840 mL蒸馏水中,搅拌均匀,待用。
(7)人工海水:模拟海水[2],按照海水中氯化钠含量3.5%来计算,准确称取35.00 g氯化钠,加入适量蒸馏水在烧杯内初步混匀,玻璃棒引流至1000 mL容量瓶,用蒸馏水稀释至刻度线。
2.2 曲线配制
挥发酚[3]标准溶液浓度为500 mg/L,准确移取10.0 mL挥发酚标准溶液至250 mL容量瓶中,用蒸馏水定容至刻度线,摇匀,此时浓度为20 mg/L。从上述250 mL容量瓶中准确移取10.0 mL液体至100 mL容量瓶中,定容至刻度线,摇匀,此时浓度为2 mg/L(此为挥发酚使用液)。准备6个100 mL容量瓶,标记1~6,分别移取1.00 mL、2.00 mL、4.00 mL、6.00 mL、8.00 mL、10.0 mL至100 mL容量瓶,稀释至刻度线,摇匀。此时,标准曲线系列浓度为0.020 mg/L、0.040 mg/L、0.080 mg/L、0.120 mg/L、0.160 mg/L、0.200 mg/L。
2.3 实验原理
本方法采用的仪器为连续流动化学分析仪,在酸性条件下蒸馏,蒸馏物与碱性铁氰化钾和4-安吉安替吡啉来测定游离酚和取代酚,生成的红色反应物在505 nm下检测。
3 实验测定及分析
本次实验旨在验证,所以选取了两个点来做比较。
分别是①0.040 mg/L;②0.160 mg/L(标准曲线上的浓度点)。
其目的是更易于识别氯化钠浓度的大小对挥发酚所产生的有影响。
3.1 实验步骤
(1)准备10个100 mL容量瓶,移取相同体积的2.00 mg/L的挥发酚使用液2.00 mL。
(2)分别移入5.00 mL、10.0 mL、11.0 mL、12.0 mL、13.0 mL、14.0 mL、15.0 mL、16.0 mL、17.0 mL、18.0 mL人工海水至上述10个容量瓶中。
(3)用蒸馏水定容至刻度线。
3.2 结果确认
在加入5.00 mL、10.0 mL与11.0 mL人工海水的挥发酚峰形虽然没有发生过多变化,但是与0.040 mg/L的值已经有了明显的出入,此时浓度值为0.046 mg/L、0.055 mg/L和0.062 mg/L,并且随着海水浓度[4]的增加,挥发酚值变大。当加入12.0 mL人工海水,峰形发生了明显的变化,峰形直线上升,浓度值也逐渐增大,最终逐渐趋于平行,如表1。图1是与之对应的曲线图(横坐标是序号,纵坐标是测得的挥发酚浓度值)。
同样的,从表2、图2可看出,当挥发酚浓度为0.160 mg/L时,加入海水5.00 mL、10.0 mL、11.0 mL、12.0 mL后,挥发酚峰形并没有较大改变,此时测得挥发酚浓度分别为0.164 mg/L、0.172 mg/L、0.179 mg/L、0.183 mg/L,表明海水对挥发酚浓度有影响,但影响不大。当加入海水13.0 mL时,峰形改变较大,且加入的海水越多,峰形越为离谱,最终逐渐趋于温度。
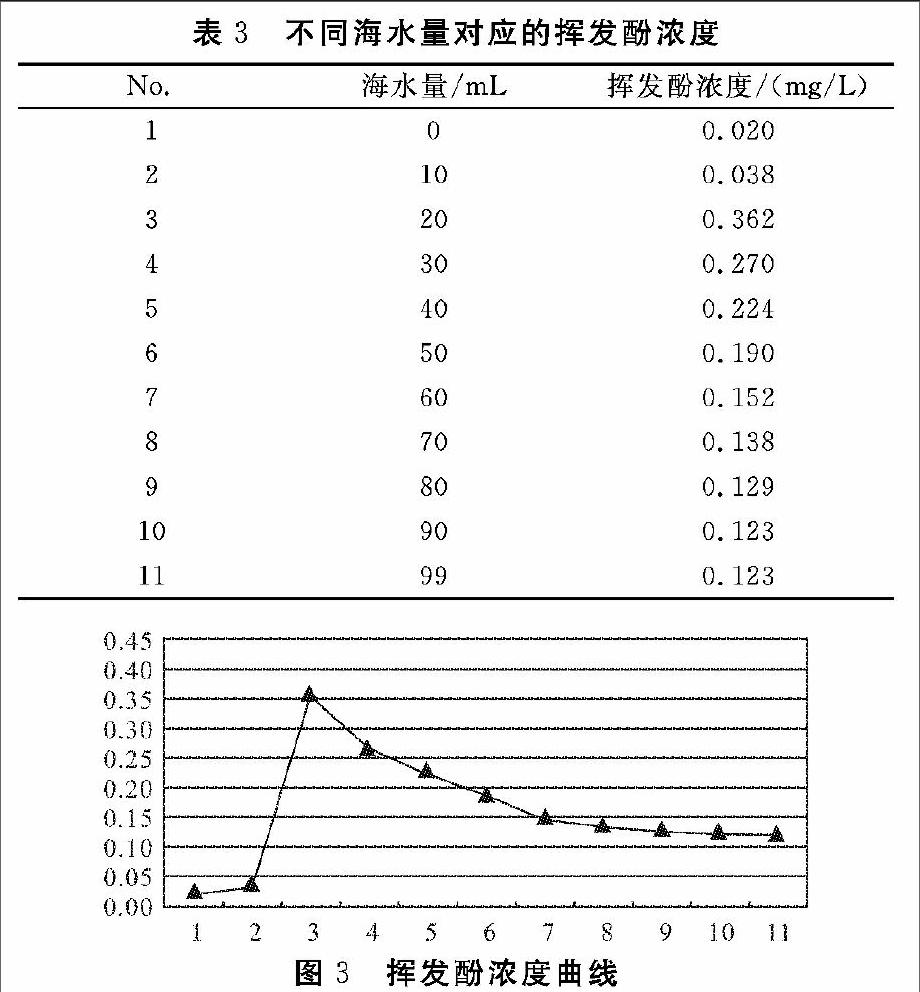
整个实验过程,并没有出现与镇海监测点时相同的U形峰,考虑到是否海水浓度不够大,同样采取两个点相比较的方法,选取曲线上的浓度点0.020 mg/L与0.080 mg/L。准备10个100 mL容量瓶,分别加入挥发酚使用液1.00 mL和海水10.0 mL、20.0 mL、30.0 mL、40.0 mL、50.0 mL、60.0 mL、70.0 mL、80.0 mL、90.0 mL、99.0 mL(相当于用海水定容至刻度线),分别用蒸馏水定容至刻度线,摇匀。结果显示,当加入20.0 mL海水时,出现U形峰。并且发现一个有趣的现象,随着海水浓度的增大,U形峰不高反低,且打点越来越低,并逐渐趋于稳定(表3,图3)。
相同的方法验证浓度点0.080 mg/L,出现同样的现象。结果显示当加入20.0 mL海水时,出现U形峰,此后,随着海水浓度的增加,U形峰不高反低。并逐渐趋于稳定(表4,图4)。
4 结论
也许影响挥发酚含量的因素不止氯化钠这一指标,还有很多很多因素,这有待于进一步研究认证[4~8]。此次论证结果表明氯化钠确实影响挥发酚含量的测定,但是并非氯化钠浓度越高,影响结果越大。
参考文献:
[1]周 丹.浅析水中挥发酚对人体危害及测定方法[J].中国建材科技,2014,(S2):221~222.
[2]陈金辉,肖靖泽,赵立晶,等.海水中挥发酚的在线蒸馏-流动注射分析[J].海洋环境科学,2011,30(1):102~104.
[3]莽丽琴,付志军,叶蓓蓓.影响测定水中挥发酚的几点因素[J].江西化工,2009(2):89~90.
[4]张志英,田大勇,王建安.水中余氯对检测挥发酚类化合物的影响[J].城镇供水,2002(2):20~21.
[5]杨明丽,陆嘉铭,徐琦玲.水中挥发酚检测方法初探[J].上海环境科学,2008(6):270~274.
[6]徐艳秋,郭洪超.探讨水中挥发酚的环境监测方法[J].北方环境,2013(3):132~133.
[7]刘亚苓,王玉娥,郝金枝.水中挥发酚的测定方法研究进展[J].理化检验(化学分册),2013(7):893~896.
[8]滕耀华.浅析水中挥发酚的环境监测方法[J].技术与市场,2012(4):97,99.

