静态顶空与顶空固相微萃取-气相色谱法测定食用油中正己醛含量比较
周玮婧,江小明,王 澍
(武汉食品化妆品检验所,湖北武汉 430000)
静态顶空与顶空固相微萃取-气相色谱法测定食用油中正己醛含量比较
周玮婧,江小明*,王 澍
(武汉食品化妆品检验所,湖北武汉 430000)
分别采用静态顶空(SHS)及顶空固相微萃取技术(HS-SPME)与气相色谱联用来分析食用油中的正己醛的含量。SHS中选用的提取温度和时间为130 ℃和15 min,HS-SPME中用85 μm Carboxen/PDMS萃取头,在130 ℃萃取15 min。通过同一浓度的标准溶液来比较两种方法的线性、精密度、准确度和检出限。结果表明:两种方法在0.00~1.00 μg/g范围内都具有良好的线性,标准曲线相关系数都在0.999以上,SHS法的结果稳定,重现性好,加样回收率为98.63%~100.02%,RSD为0.74%~2.92%,结果优于HS-SPME法。且SHS法的检出限(5.3 ng/g)也低于HS-SPME法(31.5 ng/g)。采用F检验和t检验分析统计两种方法的测定结果无显著性差异,综合比较来看,采用SHS法测定更合理准确,节约成本,在实验室分析油脂中正己醛含量的测定中可优先考虑SHS前处理法。
静态顶空,顶空固相微萃取,气相色谱,食用油,正己醛
油脂中脂肪酸容易受氧、水、光、热、微生物等的作用发生水解或氧化,发生酸败变质,分解为甘油和游离脂肪酸,或使脂肪酸中的不饱和链断开形成氢过氧化物和自由基,再依次形成短链脂肪酸、醛类、酮类等物质。这种酸败产生的大量自由基会促进机体衰老,产生的氢过氧化物具有潜在的致癌性,产生的异味挥发性产物能够危害人体健康[1-2]。正己醛是一种常见的挥发性油脂氧化分解产物,其含量在挥发性物质中所占的比例最大,正己醛虽然易挥发,但不容易进一步分解,有文献报道,可以通过分析醛类次级氧化分解小分子挥发性产物来评价油脂的氧化程度,油脂中己醛含量越高,氧化程度越大[3]。在深度氧化过程中,正己醛的测定比传统氧化评估指标更加可靠。油脂氧化程度的评价指标主要使用滴定法评价如酸价、碘值、过氧化值等一级产物,而对醛、酮类等氧化二级挥发性产物的分析与鉴定主要有高温裂解槽、动态顶空吸附-热脱附法、固相微萃取法、吹扫捕集法和静态顶空等预处理方法与气相色谱法结合的技术。其中静态顶空(SHS)法分析是一种非浓集型的气体分析方法,挥发性物质在顶空气相中达到一定的浓度时,即可进行分析;顶空-固相微萃取(HS-SPME)法是将萃取头置于顶空气体中一段时间,待平衡后将萃取头取出插入气相色谱进样口,热解吸涂层上吸附的物质[4-5]。这两种前处理方法均可避免在去除溶剂时引起挥发性物质的损失,也可降低共提取物引起的噪声,对于样品中微量挥发性有机物的分析,具有很高的灵敏度和更快的分析速度。目前已有文献报道采用静态顶空-气质法测定正己醛,且有出入境检验检疫行业标准《SN/T 3626-2013 出口食用油中正己醛含量的测定顶空固相微萃取气相色谱法》[6]测定油脂中的正己醛含量,但并未有报道关于使用静态顶空-气相色谱法测定正己醛含量以及这两种前处理方法的比较的资料。本文优化了SHS法与HS-SPME法两种技术结合气相色谱测定食用油中正己醛的分析条件,并对这两种方法进行比较,旨在为油脂的正己醛含量研究提供技术指导,探讨一种前处理简单易行的实验方法,从多方面评价食用油中脂类物质的氧化程度以及食用油的酸败程度。
1 材料与方法
1.1 材料与仪器
乙醚 分析纯,青岛精科仪器试剂有限公司;正己醛标准品,CAS:66-25-1,纯度97.7%,Dr. Ehrenstorfer。
Agilent 7890B气相色谱仪:配备毛细管柱分流/不分流进样系统,FID检测器;Agilent 7697A顶空进样器:配20 mL顶空瓶,聚四氟乙烯薄膜的胶塞密封垫;Supelco公司的固相微萃取装置:配85 μm Carboxen/PDMS(聚二甲基硅氧烷)纤维萃取头,磁力搅拌器,电子分析天平。
1.2 静态顶空-气相色谱分析
1.2.1 顶空条件 准确称取5 g试样(准确到0.0001 g)置于顶空瓶中,顶空瓶口加热温度130 ℃,定量管温度135 ℃,传输气路温度140 ℃,平衡时间15 min;增压时间0.15 min,进样时间1 min。
1.2.2 气相条件 色谱柱:HP-5毛细管色谱柱(0.25 μm,0.25 mm,30 m),载气:氮气(99.999%),流速:2.0 mL/min,进样口温度:240 ℃,分流比20∶1;检测器(FID):300 ℃,氢气:40 mL/min,空气:400 mL/min;进样体积:1 mL。柱温箱程序升温:40 ℃为初始温度,保持6 min,以5 ℃/min升温至60 ℃,不保留,继续以30 ℃/min升温至280 ℃,保持2 min。
1.3 固相微萃取-气相色谱分析
1.3.1 固相微萃取条件 准确称取5 g试样(准确到0.0001 g)置于20 mL的带有聚四氟乙烯密封塞的顶空瓶中,震荡溶解,加入转子。推出Carboxen/PDMS纤维萃取头(萃取头距样品表面约1 cm),萃取温度为130 ℃,时间为15 min。取出固相微萃取针迅速插入气相色谱进样口中,解吸3 min并进行色谱分析。纤维头在使用前先在GC进样口250 ℃处理40 min。
1.3.2 气相条件 参照静态顶空法的气相色谱条件,调整分流比1∶10,其余不变。
1.4 结果计算
1.4.1 正己醛标准曲线 用正己醛标准品和乙醚配制成100.0 mg/L的正己醛标准溶液,于(0~4 ℃冰箱中避光保存)。分别称量5 g(准确到0.0001 g)5个新榨的大豆油样品作为基底油,放入顶空进样瓶中。用微量注射器分别加入正己醛标准溶液(1、2.5、5、10、25、50 μL),含量分别为0.02、0.05、0.10、0.20、0.50、1.0 μg/g,用铝帽和密封垫密封后,小心涡旋震荡密封瓶,使物质充分混合。将配制好的标准溶液上机分析后,以正己醛含量(μg)为横坐标,峰面积(Pa)为纵坐标,绘制标准曲线。
1.4.2 样品处理与测定 准确称取5 g试样(准确到0.0001 g)置于顶空瓶中,放上硅橡胶密封垫和铝制钳口盖,用手动封盖器密封,在与绘制标准曲线相同的色谱条件下进行测定,根据标准曲线计算出样品中正己醛的含量。
2 结果与分析
2.1 样品前处理条件的确定
本文考察了不同平衡温度与平衡时间对静态顶空法分析灵敏度的影响,结果表明:随着平衡温度升高,体系中的蒸汽压相应增大,即气相中挥发性组分含量相应增高,正己醛峰面积响应值增加,有利于提高检测灵敏度[7]。但温度过高,使杂质的挥发量也增加,也容易使本底物质发生化学反应,甚至容易引起顶空系统泄漏,由于正己醛沸点为127.6 ℃,故实验中选用平衡温度为130 ℃。有资料显示,大部分挥发物在静态顶空条件下,组分在两相中分配通常在5~15 min可达到平衡,长时间受热可能导致油脂基质分解[8],故实验中选用平衡时间为15 min。在顶空-固相微萃取法分析中,参考SN/T 3626-2013的色谱条件进行实验,由于正己醛属于非极性物质,因此选择85 μm Carboxen/PDMS萃取头具有较好的提取效果,且由于15 min的萃取时间能够满足大多数分析物质的需要,参考静态顶空平衡条件,在130 ℃下吸附15 min,进行气相色谱分析。
2.2 采用两种前处理的色谱图比较
分别采用两种前处理方法富集食用油中的正己醛,经气相色谱分析后色谱图见图1。其中图1-a为采用HS-SPME法测定的油脂中正己醛加标(浓度为0.05 μg/g)色谱图,图1-b则是采用SHS法测定正己醛加标(浓度为0.05 μg/g)色谱图,如图所示,正己醛均能得到很好的分离,正己醛的理论塔板数分别为13269和39096。结果显示且在SHS法分析时,目标物质附近没有杂峰干扰,且正己醛色谱峰型尖锐,对称因子为1.09;而在HS-SPME法分析情况下正己醛峰型有拖尾,对称因子为0.85;但检测出的组分种类相对较多。综合分析可知,使用SHS法分析食用油中正己醛效果更为理想。

图1 油脂中正己醛的气相分析色谱图Fig.1 Chromatogram of the hexanal in edible oils
2.3 线性范围、检测限的比较
在基底油中加入己醛标准品,绘制标准曲线,SHS法与HS-SPME法测定正己醛,含量在0.00~1.00 μg/g范围内均呈良好的线性关系,回归方程分别为Y=655.749X-8.126,R2=0.9992和Y=728.134X-5.175,R2=0.9993,由此可见,两种方法线性关系良好,R2均能够达到0.999;但两种方法标准曲线的回归系数不同,SHS回归系数为655.749,而HS-SPME法的回归系数为728.134,说明SHS法的灵敏度优于HS-SPME法。在色谱分析中,以基线噪音的3倍所对应的浓度为方法的检出限,在本实验条件下SHS法测定正己醛的检出限为5.3 ng/g,而HS-SPME法测定正己醛的检出限为31.5 ng/g,高于SHS法。
表1 回收率实验结果
Table 1 Results of recovery test
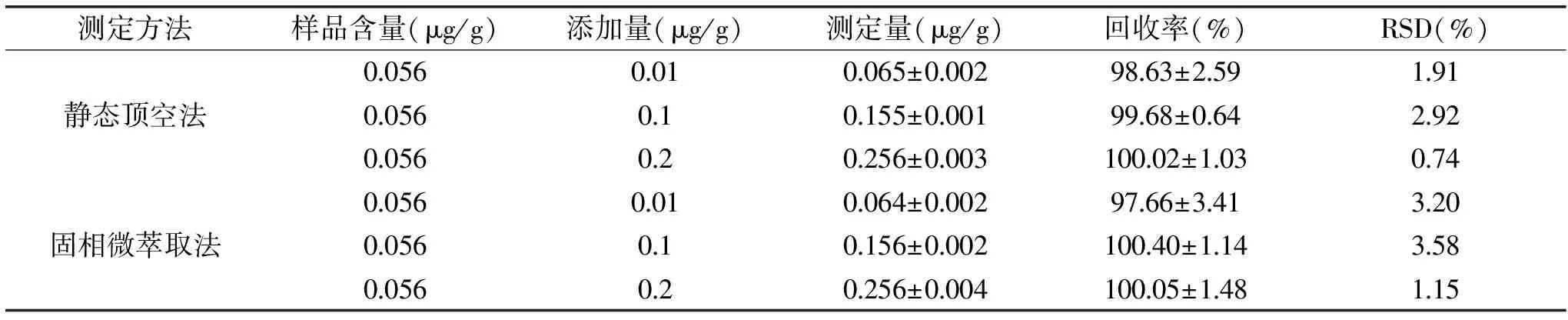
测定方法样品含量(μg/g)添加量(μg/g)测定量(μg/g)回收率(%)RSD(%)静态顶空法00560010065±00029863±2591910056010155±00019968±0642920056020256±000310002±103074固相微萃取法00560010064±00029766±3413200056010156±000210040±1143580056020256±000410005±148115
SHS法是采用亨利定律,在一定温度下,油脂中挥发性物质的检测成分即油液面上浓度对应气体压力平衡时密闭顶空瓶中的挥发气体成分,而固相微萃取是依照萃取头上涂层极性的差异有选择的富集挥发性物质,是对挥发性成分进行在线浓集,但存在着SPME纤维涂层选择性、使用寿命等方面的局限[12-13]。综合本研究来看,在分析油脂中正己醛等氧化产物时,采用SHS法测定油脂中正己醛含量能得到更准确的信息,而且SHS法有着简便快捷,自动化程度高、样品消耗量少、检测费用低等优点。因此,正己醛作为判定食用油氧化酸败程度的稳定指标,可以使用SHS法更适用于食用油中正己醛的含量测定,并为在实验室大批量检测油脂,进一步控制食用油质量,完善质量标准提供依据。
[1]谢笔钧.食品化学(第二版)[M].北京:科学出版社,2004,35-45.
[2]曹文明,王鑫,包杰,等.油脂氧化评价研究进展[J].粮食与油脂,2014,26(4):1-3.
[3]王志海,李玉振,宋世廉,等.大豆主要致腥成分之正己醛的快速直接气相色谱测定法[J].食品与发酵工业,1988(2):49-53.
[4]杨燕.济南市食用油中苯并芘、酸价及过氧化值的调查分析[D].济南:山东大学,2012.
[5]樊磊磊,刘乃强,张培毅.顶空气相色谱测定柴胡口服液中正己醛含量[J].中医研究,2015(9):76-78.
[6]SN/T 3626-2013,出口食用油中正己醛含量的测定顶空固相微萃取气相色谱法[S].
[7]张青龄,陈宜,黄建立.顶空气相色谱-质谱法分析大豆油中正己醛含量福建分析测试,2013(6):14-16.
[8]张金海.顶空气相色谱法测定咸鱼中正己醛含量样品前处理条件的优化[J].大连海洋大学学报,2015(4):216-220.
[9]葛兰波,冯彩英,郭立红,等.测定植物油制糕点变败新方法-液上气体法测定正己醛[J].中国公共卫生,1985,4(6):43-45.
[10]咸洋,周宇艳,程欲晓.静态顶空-顶空固相微萃取-气相色谱-质谱法检测食品用塑料包装材料中挥发性有机化合物残留量的适用性研究[J].理化检验-化学分册,2014,50(6):725-729.
[11]奚星林,陈捷,黄华军.顶空固相微萃取-气相色谱法检测食用油中的正己烷[J].食品科学,2003,24(12):97-98.
[12]宋秀华,李传荣,许景伟,等.静态顶空与固相微萃取法测定元宝枫叶片挥发物成分比较[J].山东农业大学学报:自然科学版,2014,45(5):670-674.
[13]王茜茜,李军明,王亚琴,等.静态顶空与顶空固态微萃取法测定云南野生干巴菌香气成分比较[J].食品工业科技,2011,11:174-180.
2.4 重复性比较
重现性反映了分析方法或测量系统存在的随机误差的大小,测试结果的随机误差越小,测试的精密度越高,重现性越好[9]。通常用相对标准偏差表示方法的重现性,取同一批次样品准确称取5 g(准确到0.0001 g),各制备7份样品,分别按SHS法与HS-SPME法进行7次重复实验,测得样品中正己醛含量的平均值分别为0.064 μg/g和0.063 μg/g。计算两种方法的标准偏差,SHS法所测数据RSD为0.40%,而HS-SPME法所测数据RSD为2.14%,结果表明两种方法正己醛含量测定重复性实验均可满足分析测试要求,但SHS法测定正己醛结果的重现性与稳定性优于SPME法。
2.5 精密度比较
精密称取同一批已知含量的样品(含正己醛0.056 μg/g)5 g(准确到0.0001 g)置顶空进样瓶中,迅速向瓶内分别添加低(0.01 μg/g)、中(0.10 μg/g)、高(0.20 μg/g)3个浓度标准溶液(n=5),分别按照SHS法和HS-SPME法测定食用油中正己醛含量,计算回收率。由表1可见,SHS法测定食用油样品不同水平的加样回收率为98.63%~100.02%,相对标准偏差为0.74%~2.92%;HS-SPME法测定食用油样品不同水平的加样回收率为97.66%~100.40%,相对标准偏差为1.15%~3.58%,两种方法测定样品的回收率和相对标准偏差均较理想,均能满足微量分析的要求,但总体来看SHS法分析结果优于HS-SPME法。
2.6 两种方法测定结果比较
选7种不同市售食用油样品,分别按照SHS法和HS-SPME法进行测定其正己醛含量,并用F检验和t检验分析统计两种不同方法测定结果是否有差异,结果见表2,统计量F=1.09小于显著水平α=0.05的F临界值5.050,两种测定方法结果方差无显著性差异;统计量t=0.0035小于显著水平α=0.05 的t双尾临界值为2.228,即两种不同分析方法结果无差异。两种测定方法的结果相近,但HS-SPME法的结果稍低于SHS法,可能是由于HS-SPME法的灵敏度低于SHS法,对测定结果造成一定影响[10]。
表2 两种分析方法结果比较(F检验和t检验)
Table 2 Compared to the result of two methods(Analysis of Variance and T Test)
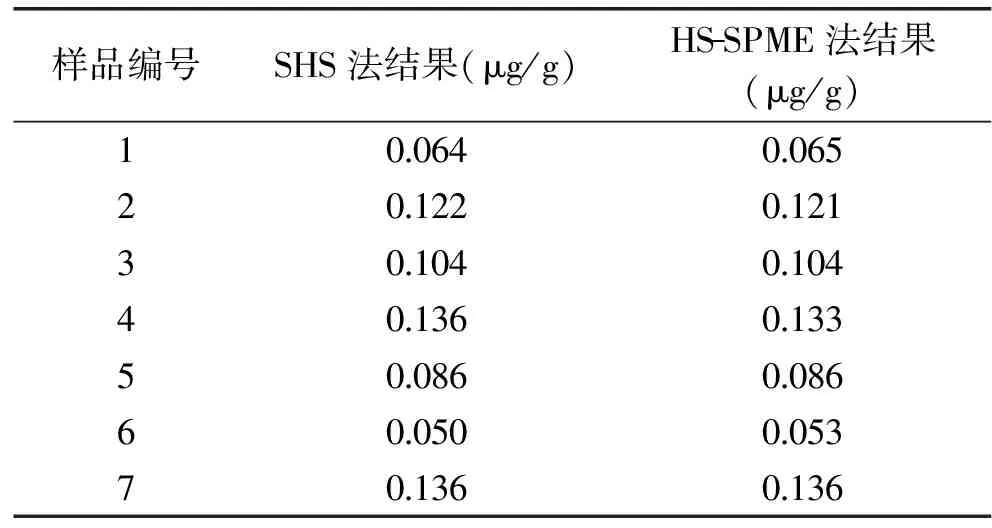
样品编号SHS法结果(μg/g)HS-SPME法结果(μg/g)100640065201220121301040104401360133500860086600500053701360136
注:方差分析F=1.09,显著水平α=0.05的F临界值为5.050;t 检验t=0.0035,显著水平α=0.05 的t 双尾临界值为2.228。
3 结论
为了更准确的测定食用油中正己醛的含量,为衡量油脂氧化提供实验依据,本文分析比较了测定食用油中正己醛的两种方法。通过分析数据可以看出,采用SHS法和HS-SPME法测定食用油中的正己醛含量准确可靠,方法学研究均符合要求[11],但SHS法的稳定性、准确度与灵敏度均优于HS-SPME法。
Comparison of determination of hexanal in edible oils by static headspace and headspace-SPME method
ZHOU Wei-jing,JIANG Xiao-ming*,WANG Shu
(Wuhan institute for food and cosmetic control,Wuhan 430000,China)
TwomethodsfordeterminationofhexanalinedibleoilswereanalyzedbyStaticHeadspace(SHS)andHeadspace-SolidPhaseMicroextraction(HS-SPME)respectively.Thehexanalwerequantitativelyanalyzedbythegaschromatography(GC).HS-SPMEandSHSwerecomparedintermsoflinearresponse,precision,accuracy,anddetectionlimit.Theresultsshowedthatbothtwomethodshadgoodlinearcorrelationbetween0.00and1.0μg/g,thecoefficientwereabove0.999.Atthesametime,theresultofSHShadgoodstability,reproducibilityandsamplerecoverywith98.63%~100.02%andRSDwas0.74%~2.92%,whichwasbetterthanthatoftheHS-SPME.AndthedetectionlimitofSHS(5.3ng/g)waslowerthanSPME(31.5ng/g).Therewerenosignificantdifferencebetweenthetwomethods,However,theSHSwasmorereliableandaccurate,itcouldbeconsideredastheoptimummethodfortheanalysisthecontentsofhexanalinedibleoilswhenappliedinthelab.
SHS;HS-SPME;GC;edibleoils;hexanal
2016-04-01
周玮婧(1985-),女,硕士,工程师,研究方向:食品安全,E-mail:elfinlife221@163.com。
*通讯作者:江小明(1970-),女,本科,高级工程师,主要从事食品分析方面的研究工作,E-mail:944703609@qq.com。
TS207.3
A
1002-0306(2016)19-0311-04
10.13386/j.issn1002-0306.2016.19.052

