LOP方案联合放疗治疗早期鼻型结外NK/T细胞淋巴瘤疗效及安全性研究
袁 斌,褚鸿亮,刘亚云,吴 涛
(贵州省肿瘤医院:1.血液科;2.淋巴瘤科,贵阳 550003)
LOP方案联合放疗治疗早期鼻型结外NK/T细胞淋巴瘤疗效及安全性研究
袁 斌1,褚鸿亮1,刘亚云1,吴 涛2
(贵州省肿瘤医院:1.血液科;2.淋巴瘤科,贵阳 550003)
目的 探讨LOP(门冬酰胺酶,长春新碱,地塞米松)方案化疗联合放疗治疗初治早期鼻型结外NK/T细胞淋巴瘤(ENKTL)的疗效及安全性。方法 回顾性分析该院86例分期为Ⅰ/Ⅱ期的早期ENKTL患者的临床资料,患者均接受LOP方案联合放疗,至少化疗4个疗程,并接受受累野放疗,根据放疗剂量分为两组,分别为DT 49~54 Gy组及DT 55~59 Gy组,放疗27~32次,中位随访39个月,评估疗效、3年总生存率(OS)。结果 (1)86例患者59例(68.60%)完全缓解(CR);18例(20.93%)部分缓解(PR);2例(2.33%)病情稳定(SD);7例(8.14%)疾病进展(PD);总反应率(ORR)89.53%;3年OS为90.70%;(2)放疗剂量49~54 Gy组和55~59 Gy组比较,ORR、3年OS差异无统计学意义;(3)放化疗常见不良反应为骨髓抑制、消化道症状、周围神经炎、肝功能损害、黏膜炎、皮炎及凝血功能异常,经积极对症处理后多数可恢复。结论 LOP方案联合放疗对早期ENKTL有效,放疗剂量49~54 Gy组和55~59 Gy组疗效无差异;放化疗不良反应多为轻至中度,该方案对早期ENKTL安全性较高。
淋巴瘤;NK/T细胞;化疗;放疗
鼻型结外NK/T细胞淋巴瘤(extranodal NK/T-cell lymphoma,nasal type,ENKTL)是非霍奇金淋巴瘤(NHL)的一个亚型,发病率有明显的地区差异性,西方国家的发病率不到全部淋巴瘤类型的1%,而在东亚及拉丁美洲国家,其发病率为7%~10%[1],好发于成年男性,男女比例为(2~3.6)∶1,患者中位年龄45岁。ENKTL与EB病毒(EBV)感染密切相关,几乎100%的病例可检出EB病毒的隐性感染。其临床表现无特异性,常以鼻塞、鼻部新生物、腭部溃疡等症状起病,病情易复发且对化疗药物容易产生耐药,具有极高的侵袭性,预后很差。目前,临床上已普遍接受化疗联合放疗治疗早期ENKTL,然而,对于ENKTL早期患者的最佳化疗方案仍在探寻中,SMILE(地塞米松,甲氨蝶呤,异环磷酰胺,左旋门冬酰胺酶及依托泊苷)、GELOX(吉西他滨,奥沙利铂及左旋门冬酰胺酶)等多药化疗方案在临床研究中得到应用[2-4]。Kwong等[2]采用SMILE方案治疗86例ENKTL患者,中期评价48例(56%)患者达到完全缓解,19例(22%)患者达到部分缓解,完成化疗后评价57例(66%)患者达到完全缓解,13例(15%)患者达到部分缓解,但57例(67%)患者出现3~4度血液学毒性,27例(31%)患者出现严重感染,36例(42%)患者出现3~4度血小板减少。Wang等[4]采用GELOX方案治疗27例ENKTL患者,2个周期化疗后,15例(55.6%)患者达到完全缓解,10例(37%)患者达到PR,2例(7.4%)患者获得疾病稳定,但70%以上患者出现1~2度血液学毒性,3~4度白细胞及血小板减少达到30%左右。ENKTL对放疗敏感,放疗近期疗效较好,但远期复发率高,而放疗联合化疗能否改善长期生存意见不一,放疗时机的选择及放疗剂量也存在争议,最近的临床研究显示在化疗前即开始放疗对于早期ENKTL患者的优势,另外,尚有临床研究采用“三明治”方案(CT+RT+CT)治疗ENKTL[5]。因此,治疗模式的选择对预后的影响值得探讨。笔者认为在完成化疗后再进行放疗,当化疗后患者达到完全缓解,后续放疗可采用相对低剂量放疗,以减少对正常组织损伤,且相对低剂量放量对于今后复发患者的2次放疗机会提供更多的空间,本研究分析86例早期ENKTL患者采用LOP方案联合放疗的疗效及安全性,以寻找适合患者的治疗方法。
1 资料与方法
1.1 一般资料 2008年3月至2015年7月本院血液科及淋巴瘤科收治ENKTL患者114例,纳入标准:(1)根据WHO淋巴瘤分类明确诊断为ENKTL;(2)原发灶位于鼻腔;(3)Ann Arbor分期Ⅰ~Ⅱ期;(4)初治患者;(5)东部肿瘤协作组(ECOG)体力评分0~2分;(6)接受LOP方案化疗联合受累野放疗。最终86例患者入选本研究,患者中位年龄52.15岁(15~84岁),其中男65例,女21例。48例(55.81%)患者有B症状(发热、盗汗、消瘦),多数患者ECOG体力状态评分0~2分,根据国际预后指数(IPI),72例患者为低危组。
1.2 治疗方法 86例患者接受LOP[左旋门冬酰胺酶(L-Asp) 6 000 U/m2静脉滴注(第1、3、5、7、9、11、13天);长春新碱 1.4 mg/m2(最大量2 mg)静脉推注(第1、8天);地塞米松 10 mg静脉滴注(第1~7天)方案化疗,门冬酰胺酶使用前,所有患者均使用50 U做皮试,1 h后观察,如出现过敏反应,使用培门冬酶(2 500 U/m2肌肉注射)代替;21 d为1个疗程;中性粒细胞绝对值大于1.5×109/L且血小板大于75×109/L时进行每周期化疗,如中性粒细胞或血小板低于上述标准时,化疗延迟3~7 d进行。所有患者接受至少4个周期化疗。
第4个周期化疗结束后3周开始受累野放疗(IFRT),照射范围包括筛窦、同侧上颌窦、蝶窦、鼻咽、鼻腔,视侵犯范围而定,放疗剂量根据剂量分为两组,分别为DT 49~54 Gy组和55~59 Gy组,总剂量分27~32次放疗,每天1次,每周5次。放疗过程中如出现以下一种以上情况,则延迟放疗直至毒性反应降至2度以下:4度白细胞或粒细胞缺乏,血小板低于25×109/L,任何3度以上的非血液学毒性,ECOG体力状态评分大于或等于3分。
1.3 近期疗效评价 患者入院后14 d内进行基础评估。治疗前评估包括病史、体格检查、全血细胞计数、血清乳酸脱氢酶、骨髓穿刺或活检、头颈部电子计算机断层扫描或磁共振以及胸、腹部、盆腔电子计算机断层扫描。根据淋巴瘤疗效标准,第2个周期化疗后或放疗前、后进行疗效评估,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)及疾病进展(PD),总反应率(ORR)为CR+PR的总和。
1.4 随访 随访截止日期为2015年7月31日。总生存时间(OS)指从进入临床实验起直至任何原因导致死亡的时间或最后随访时间。
1.5 统计学处理 应用SPSS19.0统计软件进行统计学分析,不同放疗剂量疗效对比采用χ2检验,生存时间采用寿命表法,不同放疗剂量患者3年OS比较采用Kaplan-Merei法,P<0.05为差异有统计学意义。
2 结 果
2.1 近期疗效 86例患者经2个周期化疗后CR 46例(53.49%),PR 24例(27.91%),SD 16例(18.60%),ORR 81.40%;放疗前CR 54例(62.79%),PR 22例(25.58%),SD 8例(9.30%),PD 2例(2.33%),ORR 88.38%;放疗后CR 59例(68.60%),PR 18例(20.93%),SD 2例(2.33%),PD 7例(8.14%),ORR 89.53%。放疗剂量49~54 Gy组40例,其中CR 28例(70.00%),PR 8例(20.00%),SD 1例(2.50%),PD 3例(7.50%),ORR 90.00%;放疗剂量55~59 Gy组46例,其中CR 31例(67.39%),PR 10例(21.74%),SD 1例(2.17%),PD 4例(8.70%),ORR 89.13%。两组CR、PR、SD、PD及ORR差异均无统计学意义(P>0.05)。
2.2 不良反应 化疗的主要不良反应为骨髓抑制、消化道反应、周围神经炎、肝功能不全以及凝血功能异常(低纤维蛋白原血症),放疗最常见的不良反应为黏膜炎及皮炎。多数不良反应为轻至中度,经对症处理后可恢复;低纤维蛋白原血症为使用L-Asp所致,纤维蛋白原最低值0.6 g/L,但无患者出现皮肤、黏膜及内脏出血,见表1。
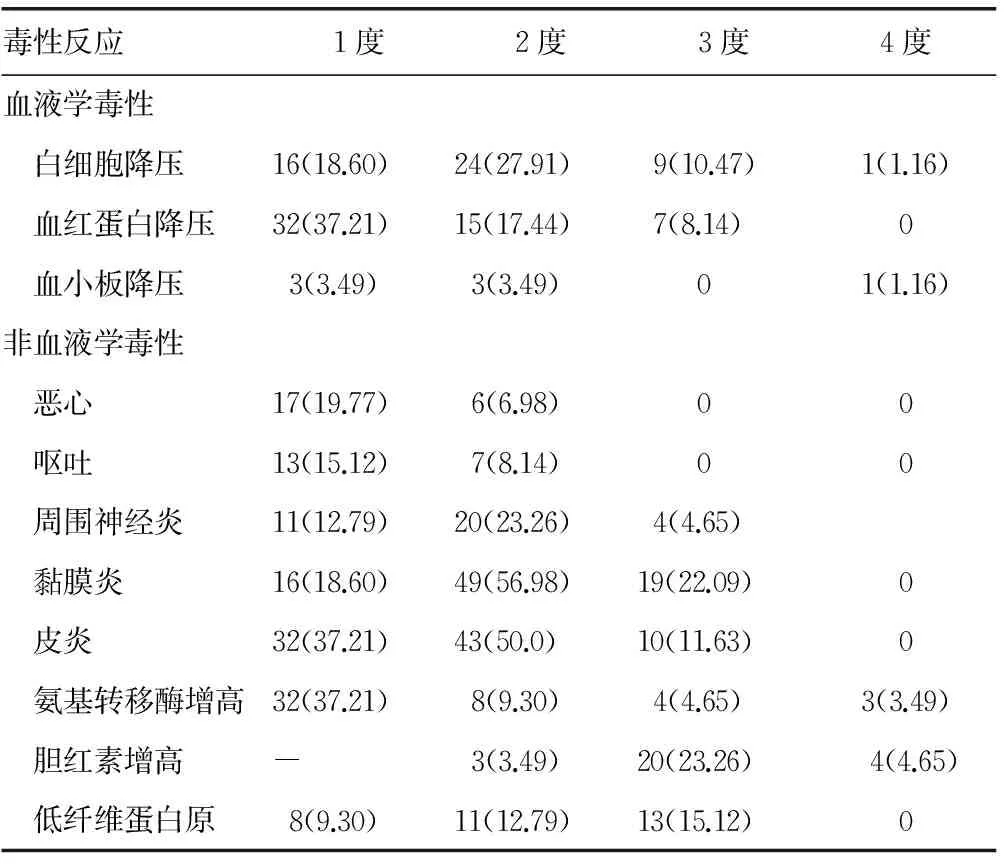
表1 常见毒性反应[n(%)]
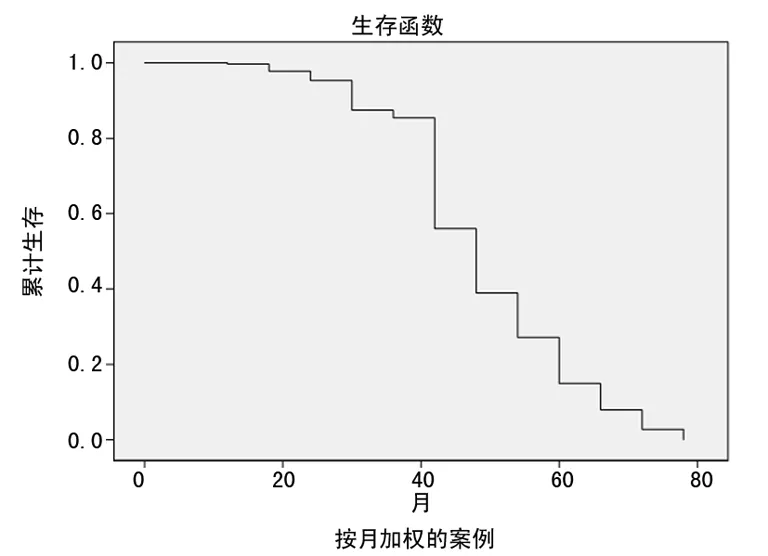
图1 86例ENKTL患者总生存曲线
2.3 总体生存情况 86例患者中生存67例,死亡11例,死亡原因主要为疾病复发或进展,仅1例患者死于化疗后肝衰竭。全组中位随访时间39个月(3~88个月),中位生存时间44.11个月(3~73个月),3年OS率90.70%,放疗剂量49~54 Gy组与55~59 Gy组3年OS差异无统计学意义(P=0.374),见图1、2。
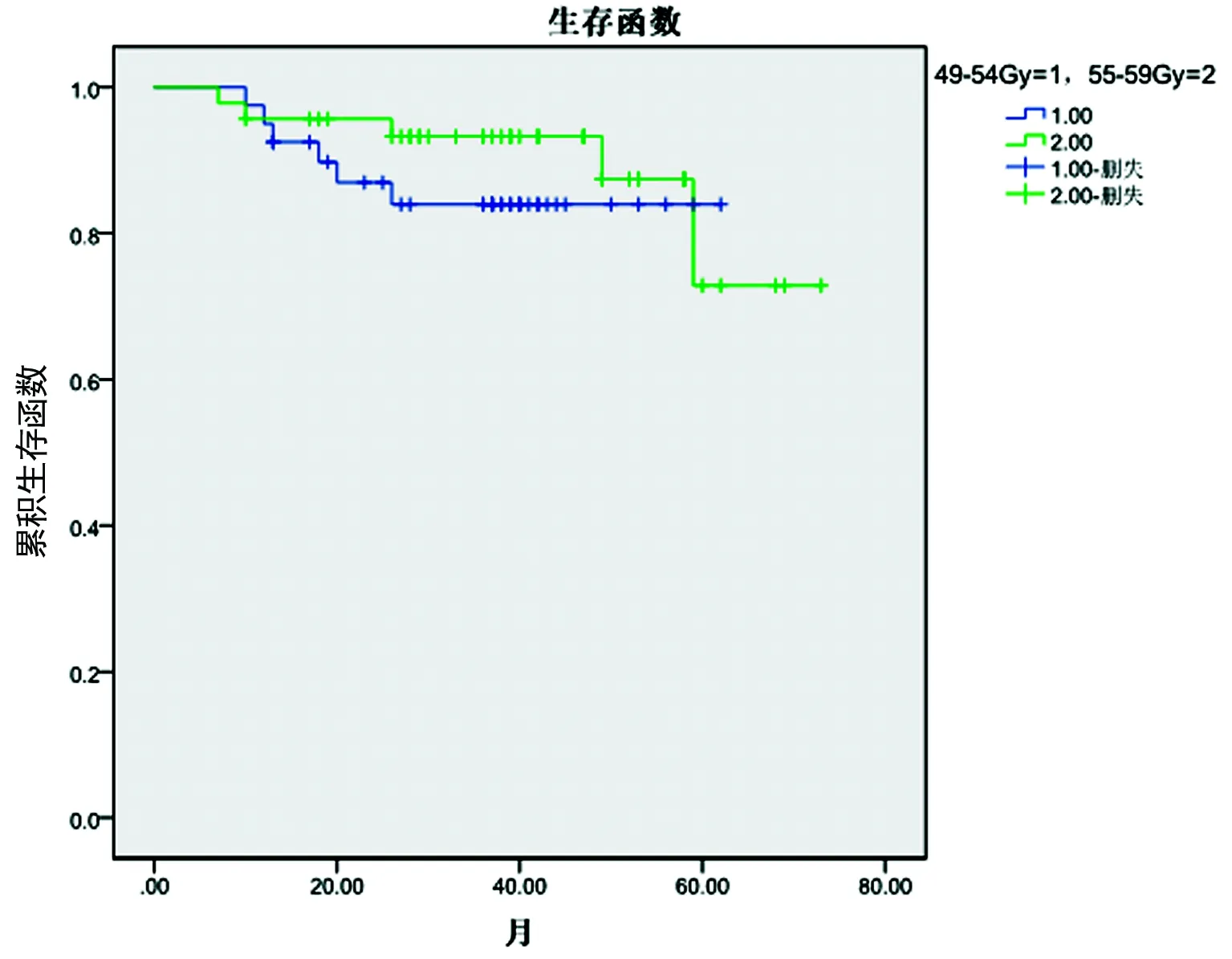
图2 不同放疗剂量对ENKTL患者生存的影响
3 讨 论
ENKTL是WHO造血与淋巴组织肿瘤分类中的一个独立类型,临床过程呈高度侵袭性,主要治疗方案为放疗、化疗、造血干细胞移植。对于早期ENKTL患者,有学者认为放疗联合化疗是治疗本病的标准方案[6-7]。
ENKTL对CHOP样常规化疗方案的不敏感可能与肿瘤细胞中过表达的多药耐药基因(MDR1)的编码产物P-糖蛋白有关[8];而L-Asp以其特殊的作用机制,可以水解血清中的天门冬酰胺,使得某些缺乏门冬酰胺合成酶的肿瘤细胞缺少必要的氨基酸,使DNA、RNA及蛋白质的合成受到抑制,从而发挥抗肿瘤作用。有体外研究表明门冬酰胺酶能够降低正常NK细胞的活性并能诱导肿瘤性NK细胞凋亡。近年来多家医院在治疗中总结含有门冬酰胺酶的化疗方案效果较好,Yong等[9]报道,对于CHOP方案无效的难治ENKTL患者使用含L-Asp的方案化疗可获得较高CR率;Zang等[10]报道采用L-Asp联合长春新碱及泼尼松组成的LOP化疗方案获得CR并维持2年以上;多个回顾性研究及临床实验亦证实L-Asp显著改善了ENKTL患者的疗效[1,4,11-14]。本组86例早期ENKTL患者采用LOP方案化疗联合放疗,CR 59例(68.60%),PR 18例(20.93%),ORR 89.53%,3年OS率90.70%,与多家医院研究结果相符,说明以L-Asp为基础的LOP方案对于早期ENKTL患者是有效的化疗方案。
早期ENKTL的适宜放疗剂量是目前存在争议较大的一个问题。多项大宗回顾性研究报道50~55 Gy照射剂量取得了较好的局部控制率,45~50 Gy的剂量与较高的局部复发率有关[15-18];韩宝林[19]综合多中心对放疗剂量的研究,认为对于ENKTL,放疗剂量应高于50 Gy;但过高的放疗剂量(≥60 Gy)并不能进一步提高生存率,反而会增加放疗并发症的发生概率。本组患者放疗剂量在49~59 Gy之间,分为49~54 Gy与55~59 Gy两组进行对比,CR、PR、SD、PD、ORR及3年OS差异无统计学意义,同文献报道相符。
本组患者在治疗过程中最常见的不良反应为骨髓抑制、消化道反应、周围神经炎、肝功能不全以及凝血功能异常(低纤维蛋白原血症)、黏膜炎及皮炎;多数不良反应为轻至中度,经对症处理后可恢复,仅1例患者因肝衰竭死亡;低纤维蛋白原血症为使用L-Asp常见的不良反应,但无患者出现严重出血导致死亡。说明LOP方案联合放疗对于早期ENKTL是一种安全性较高的治疗选择。
目前,已有多个治疗早期ENKTL的化疗方案,如LOP、SMILE、GELOX、CHOP-L等。Jiang等[1]采用LOP联合放疗的“三明治”疗法,CR率80.8%,PR率7.7%,2年OS及PFS分别为88.5%和80.6%;Kwong等[2]采用SMILE方案化疗后CR率66%,PR率15%,估计5年OS率为44.9%±12.5%,4年无病生存(DFS)率为63.7%±16.2%;Wang等[4]采用GELOX联合放疗后CR率74.1%,PR率22.2%,2年OS及PFS均为86%;Lin等[11]采用CHOP-L方案联合放疗,CR率81.6%,PR 2.6%,ORR 84.2%,2年OS,PFS及DFS分别为80.1%,81%和93.6%,然而,尚无研究证实本病最佳的化疗方案。本研究提示LOP方案对于早期ENKTL有较好的疗效,4疗程LOP方案化疗后放疗前CR率62.79%,PR率25.59%,ORR 88.38%,联合放疗后CR 68.60%,PR率20.93%,ORR 89.53%,3年OS 90.7%,与上述方案疗效相似,但相对其他方案,LOP方案所致的血液学毒性较SMILE、GELOX及CHOP-L方案低,尤其是3~4度血液学毒性明显低于其他化疗方案,安全性高。为了能够延长本病的生存期,还需要进行多中心较大数量病例的临床研究。
[1]Jiang M,Zhang H,Jiang Y,et al.Phase 2 trial of “sandwich” L-asparaginase,vincristine,and prednisone chemotherapy with radiotherapy in newly diagnosed,stage IE to IIE,nasal type,extranodal natural killer/T-cell lymphoma [J].Cancer,2012,118(13):3294-3301.
[2]Kwong YL.SMILE for natural killer/T-cell lymphoma:analysis of safety and efficacy from the Asia Lymphoma Study Group [J].Blood,2012,120(15):2973-2980.
[3]Yang Y,Yuan Z, Jian ZC,et al.Risk-adapted therapy for early-stage extranodal nasal-type NK/T-cell lymphoma:analysis from a multicenter study [J].Blood,2015,126(12):1424-1432.
[4]Wang L,Wang Z,Chen X,et al.First-line combination of gemcitabine,oxaliplatin,and L-asparaginase (GELOX) followed by involved-field radiation therapy for patients with stage IE/IIE extranodal natural killer/T-cell lymphoma [J].Cancer,2013,119(2):348-355.
[5]Zhang L,Jiang M,Xue L,et al.Five-year analysis from phase 2 trial of "sandwich" hemoradiotherapy in newly diagnosed,stage IE to IIE,nasal type,extranodal natural killer/T-cell lymphoma [J].Cancer Med,2016,5(1):33-40.
[6]Kim SJ,Kim WS.Treatment of localized extranodal NK/T cell lymphoma,nasal type [J].Int J Hematol,2010,92(5):690-696.
[7]Yamaguchi M.Current and future management of NK/T-cell lymphoma based on clinical trials [J].Int J Hematol,2012,96(5):562-571.
[8]Wang B,Li XQ,Ma X,et al.Immunohistochemical expression and clinical significance of P-glycoprotein in previously untreated extranodal NK/T-cell lymphoma,nasal type [J].Am J Hematol,2008,83(10):795-799.
[9]Yong W,Zheng W,Zhu J,et al.L-asparaginase in the treatment of refractory and relapsed extranodal NK/T-cell lymphoma,nasal type [J].AnnHematol,2009,88(7):647-652.
[10]Zang J,Li C,Luo SQ,et al.Early radiotherapy has an essential role for improving survival in patients with stage Ⅰ-Ⅱ nasal-type of NK/T cell lymphoma treated with L-asparaginase-containing chemotherapy--a single institution experience[J].Ann Hematol,2015,94(4):583-591.
[11]Lin N,Song Y,Zheng W,et al.A prospective phase Ⅱ study of L-asparaginase-CHOP plus radiation in newly diagnosed extranodal NK/T-cell lymphoma,nasal type [J].J Hematol Oncol,2013,6(1):44.
[12]Jaccard A,Gachard N,Marin B,et al.Efficacy of L-asparaginase with methotrexate and dexamethasone (AspaMetDex regimen) in patients with refractory or relapsing extranodal NK/T-cell lymphoma,a phase 2 study[J].Blood,2011,117(6):1834-1839.
[13]Yamaguchi M,Kwong YL,Kim WS,et al.Phase II study of SMILE chemotherapy for newly diagnosed stage IV,relapsed,or refractory extranodal natural killer(NK)/T-cell lymphoma,nasal type:the NK-Cell Tumor Study Group study [J].J Clin Oncol,2011,29(33):4410-4416.
[14]Gao Y,Huang H,Cai Q,et al.Efficacy and safety of pegasparagase with gemcitabine and oxaliplatin in patients with treatment-naive,refractory extranodal natural killer/T-cell lymphoma:a single-centre experience [J].Blood (ASH Annual Meeting Abstracts),2013,122:642.
[15]Wang B,Liu JJ,Ma X,et al.Combined chemotherapy and external beam radiation for stage IE and IIE natural killer T-cell lymphoma of nasal cavity [J].Leuk Lymph,2007,48(2):396-402.
[16]Wu X,Li P,Zhao J,et al.A clinical study of 115 patients with extranodal natural killer/T-cell lymphoma,nasal type [J].Clin Oncol,2008,20(8):619-625.
[17]聂大红,谢方云,李济时,等.早期鼻腔NK/T细胞淋巴瘤治疗方法和预后分析[J].中国放射肿瘤学杂志,2010,19(5):315-319.
[18]Huang MJ,Jiang Y,Liu WP,et al.Early of up-front radiotherapy improved survival of localized extranodal NK/T-cell lymphoma,nasal type in the upper acrogigestive tract [J].Int J Rad Oncol Biol Phys,2008,70(2):166-174.
[19]韩宝林.早期鼻腔NK/T细胞淋巴瘤放疗模式的研究现状[J].白血病·淋巴瘤,2012,10(21):636-637.
Study on efficacy and safety of LOP regimen plus radiotherapy for trteating early stage of nasal type extranodal NK/T cell lymphoma
YuanBin1,ChuHongliang1,LiuYayun1,WuTao2
(1.DepartmentofHemotology;2.DepartmentofLymphoma,GuizhouProvincialTumorHospital,Guiyang,Guizhou550003,China)
Objective To investigate the efficacy and safety of L-asparaginase,vincristine,and dexamethasone (LOP) regimen chemotherapy(CT) combined with radiotherapy (RT) for treating early stage of nasal type extranodal NK/T cell lymphoma.(ENKTL).Methods The clinical data of 86 inpatients with stage Ⅰ/Ⅱ of early nasal type ENK/TL in our hospital were retrospectively analyzed.Theses cases were treated by LOP regimen CT with at least 4 treatment courses combined with RT,moreover receiving the field RT.All cases were divided into two groups according to RT dose:DT=49-59 Gy and DT=55-59 Gy,27-32 times,and the median follow up lasted for 39 months.Then the efficacy and 3-year overall survival (OS) were evaluated.Results (1) In 86 cases,5 9 cases (68.60%) got complete responses (CR);18 cases (20.93%) got partial responses (PR) ;2 cases (2.33%) were in stable disease (SD);7 cases(8.14%) were in progress of disease (PD);the overall response rate (ORR) was 89.53%;the 3-year OS was 90.70%.(2)In the comparison between the RT dose DT=49-54 Gy and DT=55-59 Gy,ORR and 3-year OS had no statistical difference.(3) The common adverse reactions of CT and RT were bone marrow suppression,digestive tract symptoms,peripheral neuritis,liver function damage,mucositis,dermatitis and coagulation function abnormality,majority could be recovered by active symptomatic treatment.Conclusion The LOP regimen combined with RT has an effective in treating early stage of nasal type ENKTL,there is no difference in the efficacy between the RT dose DT=49-54 Gy and DT=55-59 Gy;the adverse reactions of CT and RT are mild to moderate,so this regimen has high safety for early stage of ENKTL.
lymphoma;NK/T cell;chemotherapy;radiotherapy
袁斌(1979-),本科,主治医师,主要从事血液疾病方面的研究。
论著·临床研究
10.3969/j.issn.1671-8348.2016.31.013
R825.5
A
1671-8348(2016)31-4360-03
2016-03-03
2016-07-17)

