阿德福韦酯联合方案治疗失败的慢性乙型肝炎患者换用替诺福韦酯优化治疗效果分析
陈 兴 尤 旭 李向永
(1阳江市公共卫生医院感染科,广东 阳江 529500;2南方医科大学第三附属医院检验科,广东 广州 510630;3中山大学附属第三医院感染科,广东 广州 510633)
·临床研究·
阿德福韦酯联合方案治疗失败的慢性乙型肝炎患者换用替诺福韦酯优化治疗效果分析
陈 兴1*尤 旭2李向永3
(1阳江市公共卫生医院感染科,广东 阳江 529500;2南方医科大学第三附属医院检验科,广东 广州 510630;3中山大学附属第三医院感染科,广东 广州 510633)
目的:分析对阿德福韦酯(Adefovir dipivoxil,ADV)为基础的联合方案治疗失败的慢性乙型肝炎患者换用替诺福韦酯(Tenofovir disoproxil fumarate,TDF)优化治疗的长期疗效及安全性。方法:回顾性评价替诺福韦酯优化治疗50例对阿德福韦酯联合方案治疗失败患者的疗效及安全性。结果:50例患者年龄23.0~51.0(35.0±17.3)岁。基线平均血清HBV DNA水平为(4.8±1.6)log IU/mL。48例HBeAg阳性(96.0%)。50例患者中,ADV)联合拉米夫定(Lamivudine, LAM)、联合替比夫定替比夫定(Telbivudine,LdT)、联合恩替卡韦恩替卡韦(Entecavir,ETV)治疗失败的患者分别有17(34.0%)例、14(28.0%)例、19(38.0%)例。治疗失败后换用TDF优化治疗,经过24.0~192.0(102.0±47.3)周治疗,不同时间点的病毒学应答率为12周38.0%,24周70.0%,36周77.1%,48周87.2%,60周83.7%,72周85.7%,84周92.1%,96周90.3%,108周95.8%,ALT复常率为12周34.0%,24周44.0%,36周54.2%,48周57.9%,60周62.9%,72周66.7%,84周71.3%,96周77.0%,108周82.8%。48例基线HBeAg阳性患者中,有5例(10.4%)发生HBeAg血清学转换。随访期间,6例患者出现病毒学突破,其中3例(2例TDF单药,1例TDF + ETV治疗)患者未能达到病毒学应答。没有严重不良事件发生。结论:对ADV为基础的联合治疗方案治疗失败的慢性乙型肝炎患者,换用TDF是一种安全、有效的优化治疗方案。
慢性乙型肝炎;联合治疗;阿德福韦酯;替诺福韦酯
慢性乙型肝炎患者长期服用核苷(酸)类似物(Nucleos(t)ide analogues,NUCs)的目的是有效地抑制乙型肝炎病毒(HBV)DNA至极低甚至检测不到的水平,防止疾病进展为肝硬化、肝癌[1]。然而,长期服用NUCs而产生的耐药、患者依从性差、不规范治疗等因素是发生治疗失败的主要因素。许多治疗失败患者即使选用阿德福韦酯(Adefovir dipivoxil,ADV)为基础的联合方案(包括ADV联合拉米夫定(Lamivudine, LAM)、ADV联合替比夫定(Telbivudine,LdT),ADV联合恩替卡韦(Entecavir,ETV),仍有部分患者治疗24周后仍然无法获得病毒学应答,甚至出现病毒学突破,即治疗失败。而对于使用ADV为基础的联合方案治疗失败患者的再治疗方案目前仍不明确。替诺福韦酯(Tenofovir disoproxil fumarate,TDF)不但强效、低耐药[2-3],且与核苷类似物(LAM、ADV、LdT)无交叉耐药,对ADV耐药的患者仍然有效,所以广泛应用于治疗失败后的优化治疗[4-6]。本文主要探讨对ADV为基础的联合方案治疗失败的慢性HBV感染者,换用TDF为优化治疗方案的疗效及其安全性。
1 资料与方法
1.1 一般资料
本研究为回顾性临床队列研究。选自2008年1月~2015年1月在本院感染科长期规范随访的慢性乙型肝炎患者50例。所有慢性乙型肝炎诊断均符合2005年版及2010年版《中国慢性乙型肝炎防治指南》标准[7,8]。50例患者中,男性43例(86.0%),年龄23.0~51.0(35.0±17.3),BMI为19.1~27.4(23.1±3.23),有乙肝家族史者25例(50%),肝硬化3例(6%),肝癌1例(2%)。ALT水平 13~893(93±170.3)U/L,HBV DNA水平3.4~6.7(4.8±1.6)log10IU/mL,HBeAg阳性患者48例(96%),既往采用LAM联合ADV、LdT联合ADV、ETV联合ADV三种治疗方案患者分别有17例(34%)、14例(28%)、19例(38%),上述联合治疗方案治疗失败后采用TDF、TDF联合ETV优化治疗的分别有41例(82%)、9例(18%)。
1.2 治疗方法
所有研究对象对ADV为基础的联合方案发生疗效均欠佳,予以换用TDF优化治疗。接受300 mg/d TDF单药或TDF联合ETV(0.5 mg/d)。血常规、肝肾功能、肌酸激酶、HBV DNA(最低检测值为100 IU/mL)和HBsAg、HBeAg等血清学检测在基线及以后每3个月检测一次。同时每6个月肝胆胰脾彩超检查1次,并在每次血液检测时收集2 ml血液样本以备未来评估。每次随访时都要对患者仔细体格检查,并报告任何不良事件。
1.3 疗效判断
主要终点是使用替诺福韦酯,患者达到病毒学应答(HBV DNA检测不到,< 100 IU/ml)的累积发生率。次要终点是HBeAg消失和血清学转换,丙氨酸氨基转移酶(ALT)复常,以及安全性和耐受性。
1.4 统计学分析
2 结 果
2.1 TDF抗病毒疗效
对ADV为基础的联合方案治疗失败的患者,换用TDF优化治疗,经过24~192(102±47.3)周治疗,不同时间点的病毒学应答率为12周38.0%,24周70.0%,36周70.1%,48周87.2%,60周83.7%,72周85.7%,84周92.1%,96周90.3%,108周95.8%。(见图1)。随访期间,6例患者出现病毒学突破,其中5例采用TDF单药治疗,1例TDF联合ETV治疗。6例病毒学突破的患者中,3例(2例为采用TDF单药治疗,1例为TDF联合ETV治疗)未能达到病毒学应答。
2.2 生化和血清学反应
对ADV为基础的联合方案治疗失败的患者,换用TDF优化治疗,ALT复常率为12周34.0%,24周44.0%,36周53.0%,48周57.9%,60周62.9%,72周65.5%,84周71.3%,96周77.0%,108周82.8%(见图2)。48例基线HBeAg阳性的患者中,经过中位数为84(60~108)周的随访后,5例(10.4%)患者发生HBeAg血清转换。在72周、84周、96周、108周的HBeAg/HBeAb累积血清学转换率分别2.5%、7.9%、11.2%、14.6%。
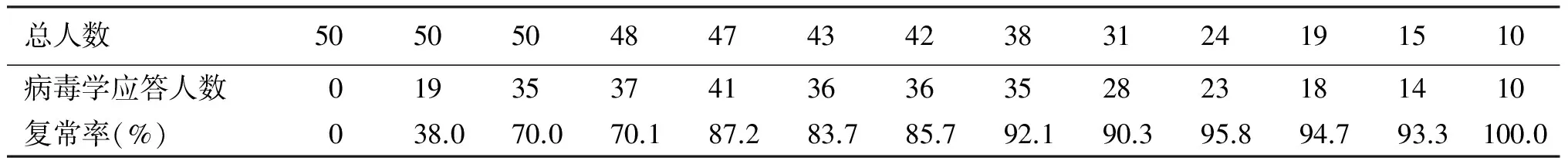
表1
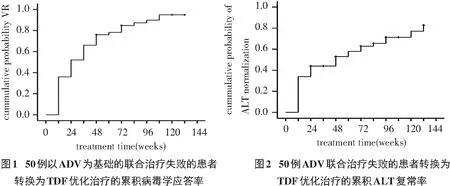
表2

总人数50505048474342383124191510ALT复常人数017222627272827242017149复常率(%)034.044.054.257.962.966.771.377.082.889.593.390.0
2.3 安全性分析
在研究过程中没有报告严重不良事件的报道。5例患者基线血清肌酸激酶高于正常参考范围(24~184 IU/L)。患者减少运动量,肌酸激酶逐渐恢复正常。另外,随访过程中只有1例服用TDF联合ETV的患者出现血清肌酐轻微升高,波动在128~146 μmol/L,在未更改抗病毒方案的情况下,血清肌酐可逐渐恢复到正常水平。
3 讨 论
本研究回顾性分析了对于ADV为基础的联合治疗方案治疗失败的患者,予长期TDF优化治疗,结果显示,可使大部分联合治疗失败患者在生化学、病毒学、血清学方面明显获益。TDF优化治疗108周时,累积ALT复常率高达80%(n=40),HBV DNA不可测率达94%(n=47),HBeAg/HBeAb转换率达14.6%(n=7)。
TDF不但对初始使用核苷(酸)类似物的患者显现出强效抑制HBV DNA复制及良好的耐受性,而且对多药经治的患者同样如此[9,10]。德国的一项研究显示[5],3年的TDF单药治疗,初始核苷(酸)类似物治疗及核苷(酸)类似物经历的患者HBV DNA不可测率分别高达91%、96%。另一项研究显示,对于核苷(酸)类似物经历的患者,TDF单药治疗22个月出现持续病毒学应答的患者可以达到84.9%[11]。据一项研究介绍,29例对之前LAM治疗失败或者LAM序贯ETV治疗的患者,经TDF 18个月的单药治疗,HBV DNA不可测率达到80%以上[6],在LAM耐药、ADV耐药、ETV耐药患者,累积病毒学应答率分别为82.8%,81.4%,和84.1%[12]。Zhang Q等[13]研究发现,ADV联合ETV疗效欠佳的患者,24周、48周、96周累计病毒学应答率分别达到52.6%、84.2%、94.7%,而ADV联合LAM、ADV联合LdT、ADV联合ETV三组之间的累积病毒学应答率无统计学差异(P=0.229)。本研究中,对于ADV为基础的联合治疗方案治疗失败的患者,转换TDF优化治疗24周、48周、96周、108周的累积病毒学应答率分别为52%、76%、89.8%和94.9%,与上述研究结果相似。所以,依照本研究长期随访的研究结果及国内外的其他类似研究结果,对ADV为基础的联合方案治疗失败的患者,转换为TDF优化治疗是值得推荐的。
总之,对ADV为基础的联合方案治疗失败的患者来说,转换为TDF治疗是一种安全、有效的优化治疗策略。
[1] Liaw YF,Kao JH,Piratvisuth T,et al.Asian-Paci?c consensus statement on the management of chronic hepatitis B: a 2012 update[J]. Hepatol Int,2012,6(4):809-810.
[2] Chen HL,Lee CN,Chang CH,et al.Efficacy of maternal tenofovir disoproxil fumarate in interrupting moter-to-infant transmission of hepatitis B virus[J]. Hepatology,2015,62(2):375-386.
[3] Kitrinos KM,Corsa A,Liu Y,et al.No detectable resistance to tenofovir disoproxil fumarate after 6 years of therapy in patients with chronic hepatitis B[J]. Hepatology,2014,59(2):434-442.
[4] Batirel A,Guclu E,Arslan F,et al.Comparable efficacy of tenofovir versus entecavir and predictors of response in treatment-naive patients with chronic hepatitis B:a multicenter real-life study[J]. Int J Infect Diis,2014,28:153-159.
[5] Petersen J,Heyne R,Mauss S,et al.Effectiveness and Safety of Tenofovir Disoproxil Fumarate in Chronic Hepatitis B:A 3-Year Prospective Field Practice Study in Germany[J]. Dig Dis Sci,2015,[Epub ahead of print].
[6] Kozielewicz D,Halota W,Wietlicka-Piszcz M,et al.Tenofovir rescue therapy in chronic hepatitis B patients who failed previous nucleoside analogue treatment[J]. Hepatol Int,2015,10(2):302-309.
[7] 中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南 (2010年版)[J]. 中国预防医学杂志,2011,12(1):1-15.
[8] 中华医学会肝病学分会,中华医学会感染病学分会,慢性乙型肝炎防治指南〔J〕.中华传染病杂志,2005.23(6):421-431
[9]Ayaz C,Celen MK,Dal T,et al.Tenofovir disoproxil fumarate treatment in HbeAg-positive patients[J]. Infez Med,2015,23(1):31-35.
[10] Kim BG,Jung SW,Kim EH,et al.Tenofovir-based rescue therapy for chronic hepatitis B patients who had failed treatment with lamivudine, adefovir,and entecavir[J]. J Gastroenterol Hepatol,2015,30(10):1514-1521.
[11] Lo AO,Wong VW,Wong GL,et al.Efficacy of tenofovir switch therapy for nucleos(t)ide-experienced patients with chronic hepatotis B[J]. Aliment Pharmacol Ther,2015,41(11):1190-1199.
[12] Lee S,Park JY,Kim do Y,et al.Prediction of virologic response to tenofovir mono-rescue therapy for multidrug resistant chronic hepatitis B[J]. J Med virol,2016,88(6):1027-1034.
[13] Zhang Q,Han T,Nie CY,et al. Tenofovir rescue regimen following prior suboptimal response to entecavir and adefovir combination therapy in chronic hepatitis B patients exposed to multiple treatment failures[J]. J Med Virol,2015,87(6):1013-1021.
Efficacy of tenofovir disoproxil fumarate switch therapy in chronic hepatitis B for suboptimal response to adefovir-based combination therapy
Chen Xing1*,You Xu2, Li Xiangyong3
(1Department of Infectious Diseases, Pubic Health Hospital of YangJiang, Guangdong 529500, China;2Department of Clinical Laboratory,The Third Affiliated Hospital of Southern Medical University,Guangzhou 510630,China;3Department of Infectious Diseases, The Third Affiliated Hospital, Sun Yat-sen University, Guangzhou 510630, China)
*Correspondingauthor:Email:LXY2005123@126.com
Objective:To analyze the efficacy and safety of tenofovir disoproxil fumarate (TDF) switch therapy in chronic hepatitis B patients for suboptimal response to adefovir(ADV)-based combination therapy in real life. Methods:To evaluate the efficacy and safety of TDF switch therapy in 50 chronic hepatitis B patients after suboptimal response to ADV-based combination therapy. Results:The median follow-up duration was 102 weeks (24~192 weeks) and median age was 35 years (range, 23 to 51). The mean serum HBV DNA level was 4.8±1.6 log IU/mL at baseline. 48 patients were HBeAg-positive (96%). 17(34%), 14(28%), 19(38%)patients was treated by prior lamivudine(LAM) plus ADV, telbivudine(LdT) plus ADV, ETV plus ADV, respectively. The cumulative probability of achieving virological response at 12, 24, 36, 48, 60, 72, 84, 96, and 108 weeks were 38.0%, 70.0%, 77.1%, 87.2%, 83.7%, 85.7%, 92.1%, 90.3%, 95.8%, respectively.The cumulative probability of normal ALT at 12, 24, 48, 60, 72, 84, 96 and 108 weeks were 34.0%, 44.0%, 54.2%, 57.9%, 62.9%, 66.7%, 71.3%, 77.0%, 82.8%. HBeAg seroconversion occured in 5 of 48 patients(10.4%). During the follow-up, 6 patients suffered from virological breakthrough, of whom 3 (2 cases was treated with TDF, and 1 case with TDf +ETV) failed to achieve virological response.No serious adverse event was reported. Conclusion:TDF switch therapy is an effective and safe for chronic hepatitis B patients with suboptimal response to ADV-based combination therapy in real-life.
chronic hepatitis B; combination therapy; adefovir; tenofovir
10.3969/j.issn.2095-9664.2016.04.11
R575.1
A
2095-9664(2016)04-0039-04
2016-07-14)
*通讯作者:Email: LXY2005123@126.com

