表征Y分子筛Brönsted酸中心强度的结构参数
袁 帅, 龙 军, 赵 毅, 田辉平, 刘宇键, 许 昀, 代振宇
(中国石化 石油化工科学研究院, 北京 100083)
表征Y分子筛Brönsted酸中心强度的结构参数
袁 帅, 龙 军, 赵 毅, 田辉平, 刘宇键, 许 昀, 代振宇
(中国石化 石油化工科学研究院, 北京 100083)
采用量子力学方法研究了具有不同Brönsted酸强度的Y分子筛酸中心的结构特性,计算了O—H键长(dO—H)、H的Mulliken电荷(qH)、O—H伸缩振动频率(νO—H)、∠Si—O—Al、分子轨道能量等结构参数,并探讨了这些结构参数与分子筛酸强度的对应关系。研究表明,dO—H、qH、νO—H、∠Si—O—Al与分子筛Brönsted酸强度并不呈严格的对应关系,而酸性羟基O—H的反键轨道能量(EO—H*)与酸强度存在良好的对应关系,EO—H*越低,Brönsted酸性越强。因为EO—H*越低,O—H反键轨道越容易被电子填充;反键轨道被电子填充后,体系能量升高,O—H键越容易被破坏,越容易给出H+,从而Brönsted酸性越强。因此,提出可以用EO—H*表征Y分子筛Brönsted酸强度,补充和完善了表征分子筛酸强度的结构参数。
分子筛; 酸强度; 结构参数; 分子轨道能量
(ResearchInstituteofPetroleumProccessing,SINOPEC,Beijing100083,China)
Y分子筛作为一种重要的微孔酸性催化材料在石油炼制与化学工业催化剂中起着非常重要的作用,其催化特性与Brönsted酸强度密切相关。Y分子筛Brönsted酸起源于骨架中四面体位置的Si原子被Al原子取代,为保持电荷平衡在Si—O—Al的桥氧位置上补偿1个H,该H表现出一定正电荷,当H从分子筛上解离出来形成H+,即表现出Brönsted酸性。国内外很多学者从实验和理论两方面对分子筛的酸性进行了较全面而深入的研究和总结[1-5]。在分子筛酸性研究中多用脱质子能(EDP)[4-5]作为酸强度的理论量度。EDP表示分子筛酸中心解离出H+所需的能量,EDP数值越大,表示分子筛解离出H+越困难,酸强度越小,反之表示酸强度越大。EDP与其结构密切相关,分子筛酸中心的一些结构参数也被用来表征Brönsted酸强度,或者初步判断Brönsted酸强度的相对大小。O’Malley等[6]认为,酸性O—H键长(dO—H)、H的Mulliken电荷(qH)、O—H伸缩振动频率(νO—H)可作为表征分子筛酸强度的结构参数。Redondo等[7]在研究ZSM-5分子筛酸性时得到的结论是,∠Si—O—Al可以用来表征分子筛酸强度。这些参数在一定范围内与分子筛酸强度具有较好的对应关系,但在某些情况下与酸强度并不吻合,表明分子筛酸强度与结构参数间的关系尚需进一步深入研究。
笔者构建了不同酸强度的Y分子筛酸中心模型,采用量子力学方法计算了它们的酸强度(EDP)。在研究现有参数(dO—H、qH、νO—H、∠Si—O—Al)与分子筛酸强度关系的基础上,首次研究了酸性O—H反键轨道能量(EO—H*)与酸强度的关系,寻找分子筛酸强度与结构间的内在关联,尝试提出新的结构参数更准确表征分子筛的酸强度。
1 Y分子筛酸中心模型和计算方法
1.1 模型的构建
Y分子筛的Brönsted酸强度与nSi/nAl密切相关[8]。模型中酸性O—H周围Al原子数目的变化,即nSi/nAl的变化会引起酸强度的改变;相同nSi/nAl下,Al原子排布方式不同,酸强度也会有所差异。根据这些原则,构建了具有不同nSi/nAl及同一nSi/nAl但Al排布不同的Brönsted酸中心模型。
(1) 利用Y分子筛的晶胞构建包含2个超笼的分子筛孔道模型。在两超笼连接处即十二元环上取1个Si原子替换为Al原子,并在与Al相连的O上补偿1个H,得到Y分子筛Brönsted酸的孔道模型。(2) 以Al—OH为中心向外扩展2个SiO4截取片段,构成14T的Si13Al1原子簇模型A。(3) 原子簇的边界用H饱和,H指向分子筛的原晶格O原子方向。固定Si—H键长0.147 nm[9]。构建酸中心模型过程示意图见图1。将Si13Al1模型A中某个T位的Si原子替换为Al原子,为保持电荷平衡要在与该Al相连的O上补偿1个H原子,可构建获得Si12Al2酸中心模型B。按照类似的步骤,在Si12Al2酸性中心模型的基础上构建Si11Al3模型C,在Si11Al3酸性中心模型的基础上构建Si10Al4模型D和E。
构建的酸中心模型见图2。由于它们具有不同的nSi/nAl或者同一nSi/nAl下Al排布不同,因此它们具有不同的酸强度。
1.2 计算方法
在Material Studio软件的Dmol3模块进行DFT计算。采用基于密度泛函理论中的广义梯度近似法GGA和DNP基组对所有模型进行结构优化。计算
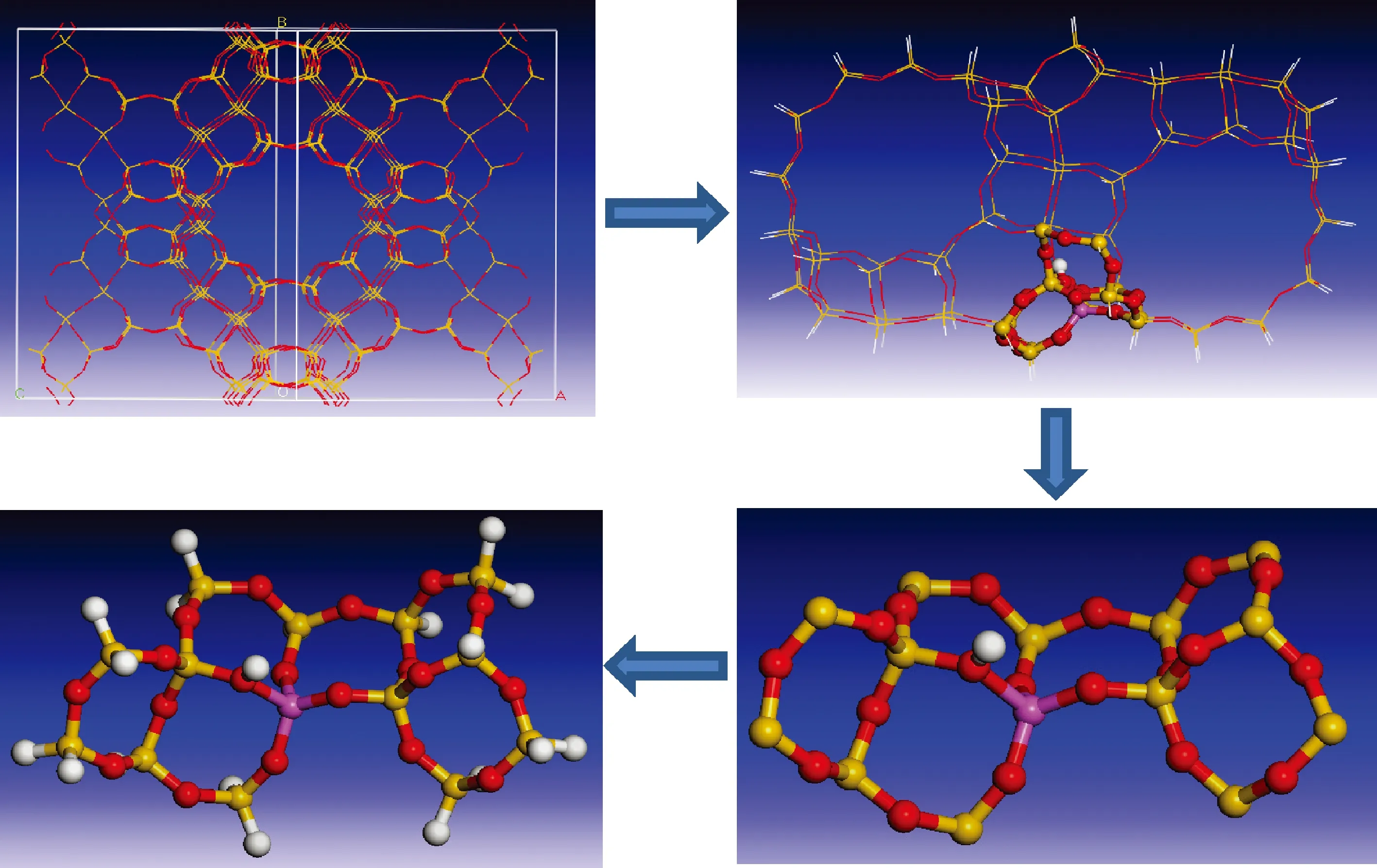
图1 构建Y分子筛酸中心模型过程示意图

图2 构建的A、B、C、D、E酸中心模型
过程中,将模型中的边界H原子固定在晶体结构坐标位置上,固定Si—H键长0.147 nm,其它内部原子松弛。对酸中心模型优化、计算、分析可获得分子筛酸中心模型不同的结构参数。
分子筛酸性研究中常以脱质子能(EDP)作为Brönsted酸强度的量度。EDP表示从分子筛结构中移走1个酸性质子所需要的能量,可由式(1)计算。
EDP=EA--EAH(AH=H++A-)
(1)
式(1)中,EAH和EA-分别为分子筛酸中心的能量和酸中心脱去质子后的能量。根据该式,酸中心EDP越大,酸性羟基O—H提供质子的能力越弱,酸强度越小;EDP越小,酸中心提供H+的能力越强,酸强度越大。
2 结果与讨论
计算了建立的不同酸中心模型的EDP,结果列于表1。
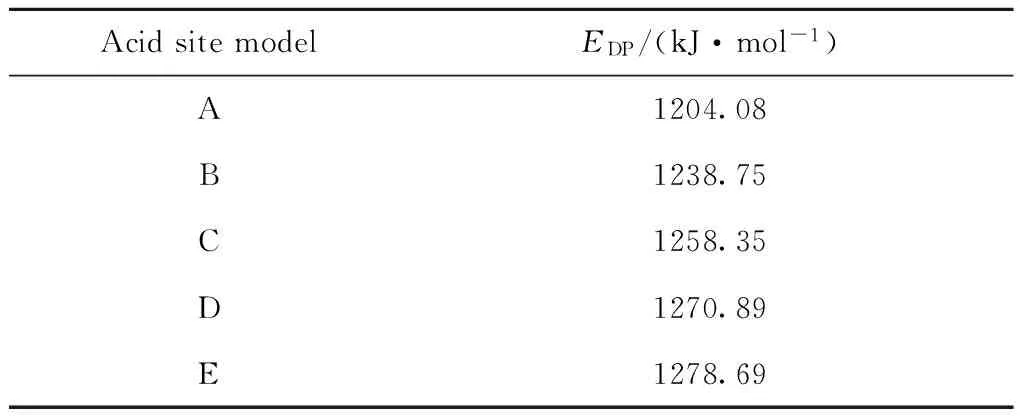
表1 建立的酸中心模型的EDP
从表1可知,A、B、C、D、E 5个酸中心模型的EDP数值依次增加,表明它们的酸强度呈降低趋势。从A到E的EDP差距74 kJ/mol,酸强度分布范围较宽。A、B、C、E间具有较明显的酸强度梯度,这主要是由于酸中心NNN(Next nearest neighbor)位置分布Al原子数目越多(nSi/nAl越低),酸中心强度越低[10],EDP就越大。模型D与E酸中心NNN位置上Al原子数量相同,只是Al排布位置不同,酸强度略有差别,EDP差距仅为8 kJ/mol。
为研究分子筛酸强度与一些结构参数的对应关系,计算了A、B、C、D、E模型酸中心的dO—H、qH、νO—H、∠Si—O—Al结构参数[6-7],结果列于表2。
由表2可知,虽然A、B、C、D、E的EDP有较明显变化,但是dO—H变化极小,仅0.0003 nm。一般认为,dO—H越大,O—H越容易解离出H+,酸性越强。B、C、D、E基本符合这个规律,但模型A酸中心强度最大,dO—H却不是最大。
A、B、C、D、E的H的Mulliken电荷(qH)变化范围也较小。一般认为,qH越大,O—H中的H的离子性越强,O—H越容易发生异裂释放出H+,酸性越强。A的EDP最小,酸性最强,qH也最大,但其他模型并不符合此规律。这可能是由于,qH大表示O—H间电子云更偏向于O,至于能否解离出H+还与O—H周围的骨架原子构成的整体环境有关。赵亮等[11]认为,在多Al原子取代的分子筛中,酸性H的电荷不能作为表征酸性强弱的参数。
A、B、C、D、E的O—H伸缩振动频率(νO—H)变化范围较大。一般认为,νO—H越小,O—H
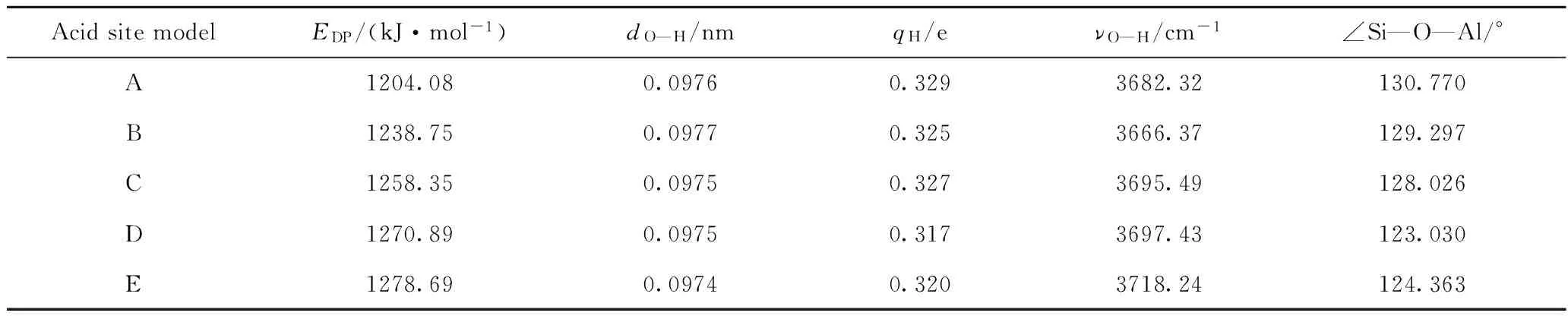
表2 建立的酸中心模型的结构参数
越弱,H+越容易解离,酸性越强。这个规律对A、B、C、D、E也不完全适用。Lo等[12]的研究结果也表明,EDP与dO—H和νO—H不存在明显的对应关系,而νO—H与dO—H具有很好的对应关系(见表2),即dO—H越大,νO—H越低。dO—H和νO—H主要与短程共价作用相关[13],仅考虑了较少的骨架原子的影响。
∠Si—O—Al考虑的骨架原子范围稍大。A、B、C、D、E基本上符合∠Si—O—Al越大,酸性越强的规律,其中D、E的酸强度比较接近,∠Si—O—Al没能有效区别。Zhou等[14]认为,∠Si—O—Al增大会使O—H周围晶体结构上的张力变小,从而使νO—H降低,利于H+的释放,提高酸强度。但∠Si—O—Al与酸强度内在关联尚难以从化学角度解释。
综上所述,dO—H、qH、νO—H、∠Si—O—Al与EDP具有一定的关联性,一定范围内可以作为酸强度的量度,并且这些参数从酸中心结构出发更加直观且易于获得;但在一些条件下,比如酸强度差距较小时,这些参数的变化范围确实极小,无法区分不同酸中心模型间的差异。这可能由于这几个参数主要考虑O—H周围近程共价作用的影响,而EDP还与酸中心长程作用力有关[14];也有可能由于这几个参数不是影响酸强度的本质因素,而仅是影响酸强度本质因素的外在表现。
由此设想,若有能表达O—H处于分子筛整体骨架中的结构参数,并且可以从化学角度解释其与酸强度的内在关系,可能会成为表征酸强度更准确的结构参数。前线分子轨道能量能够作为表达 O—H处于分子筛整体骨架中的结构参数,并且有可能从化学角度解释与酸强度的关系。为此计算了不同酸中心模型的HOMO轨道能量(EHOMO)、LUMO轨道能量(ELUMO)、前线分子轨道的能量差(ELUMO-EHOMO),考察它们与酸强度的关系,结果列于表3。模型A、E的HOMO轨道分布示于图3,LUMO轨道分布示于图4。
HOMO轨道具有给出电子的性质,与分子(酸性中心模型整体看作1个分子)的碱性相关。一般认为,EHOMO越高,给电子能力越强或者碱性越强。由表3可以判断,酸性中心模型D、E、C、B、A的L碱性由高到低依次降低,似乎与表示酸强度大小的EDP无直接对应关系。分析各分子的HOMO轨道分布可以看出表现碱性的活性位主要是骨架O原子,并且一般是离酸性O—H距离较远的骨架O原子(见图3)。王中学等[15]采用密度泛函方法研究了SBA-15分子筛簇模型的前线分子轨道性质。研究认为,O原子是L碱性或者还原性的活性位。总之HOMO轨道能量与酸强度无直接关系。

表3 不同酸中心模型的前线分子轨道能量及能量差

图3 模型A、E的HOMO轨道分布

图4 模型A、E的LUMO轨道分布
LUMO轨道具有得到电子的性质,与分子的酸性相关。一般认为,LUMO轨道能量越低,接受电子的能力越强或者L酸性越强。由表3可以判断, L酸性由高到低的酸性中心模型顺序为D、B、A、 C、 E,也与EDP无直接对应关系。王中学等[15]的研究同样没有发现LUMO轨道能量与对应的酸中心的EDP存在对应关系。这是因为LUMO轨道并不总是分布在所研究的某一酸性O—H的周围,如图4中E的LUMO轨道分布在分子的其他位置上。
前线分子轨道的能量差ELUMO-EHOMO反映一个分子是否容易被激发,其值越小,越容易被激发,反应活性越强,由此判断,构建的酸性中心模型的反应活性由高到低顺序为D、E、B、C、A。与酸中心的EDP顺序不一致。赵亮等[11]研究了128T的ZSM-5分子筛模型的ELUMO-EHOMO,认为ELUMO-EHOMO随分子筛模型硅/铝比的降低而降低,分子筛的活性增强,催化性能增强,但是与酸中心模型的EDP关联也不明显。
综上所述,由于前线轨道反映的是分子整体的性质,多数情况下与所研究的酸性O—H的关系并不明显,因此不能成为表征酸强度的结构参数。
考虑到分子的空轨道具有接收电子的性质,与分子的酸性相关。而整个分子的LUMO轨道由于并不围绕在酸性O—H周围,导致LUMO轨道与酸性O—H的酸强度关联性不强。因此,酸性O—H 未被电子填充的分子轨道——O—H反键轨道可能与酸性O—H的酸强度密切相关。
原子轨道通过线性组合成分子轨道时,轨道数目不变,轨道能级改变[16];2个能级相近的原子轨道组合成分子轨道时,低于原子轨道能级的称为成键轨道,高于原子轨道能级的称为反键轨道,等于原子轨道能级的称为非键轨道。分子筛酸性O—H的分子轨道能级如图5所示。分析图5可知,H的1s电子与O的2p电子通过线性组合形成分子轨道时,形成1个能级低于原子轨道能级的成键轨道σ和1个能级高于原子轨道能级的反键轨道σ*。成键轨道σ中含有1对自旋相反的电子,分别来自H和O,而反键轨道σ*是空轨道。计算了O—H反键轨道的能量EO—H*,考察其是否与EDP存在对应关系,结果列于表4。
由表4可知,酸性O—H的反键轨道能量EO—H*与EDP存在明显对应关系,EO—H*能量越高,
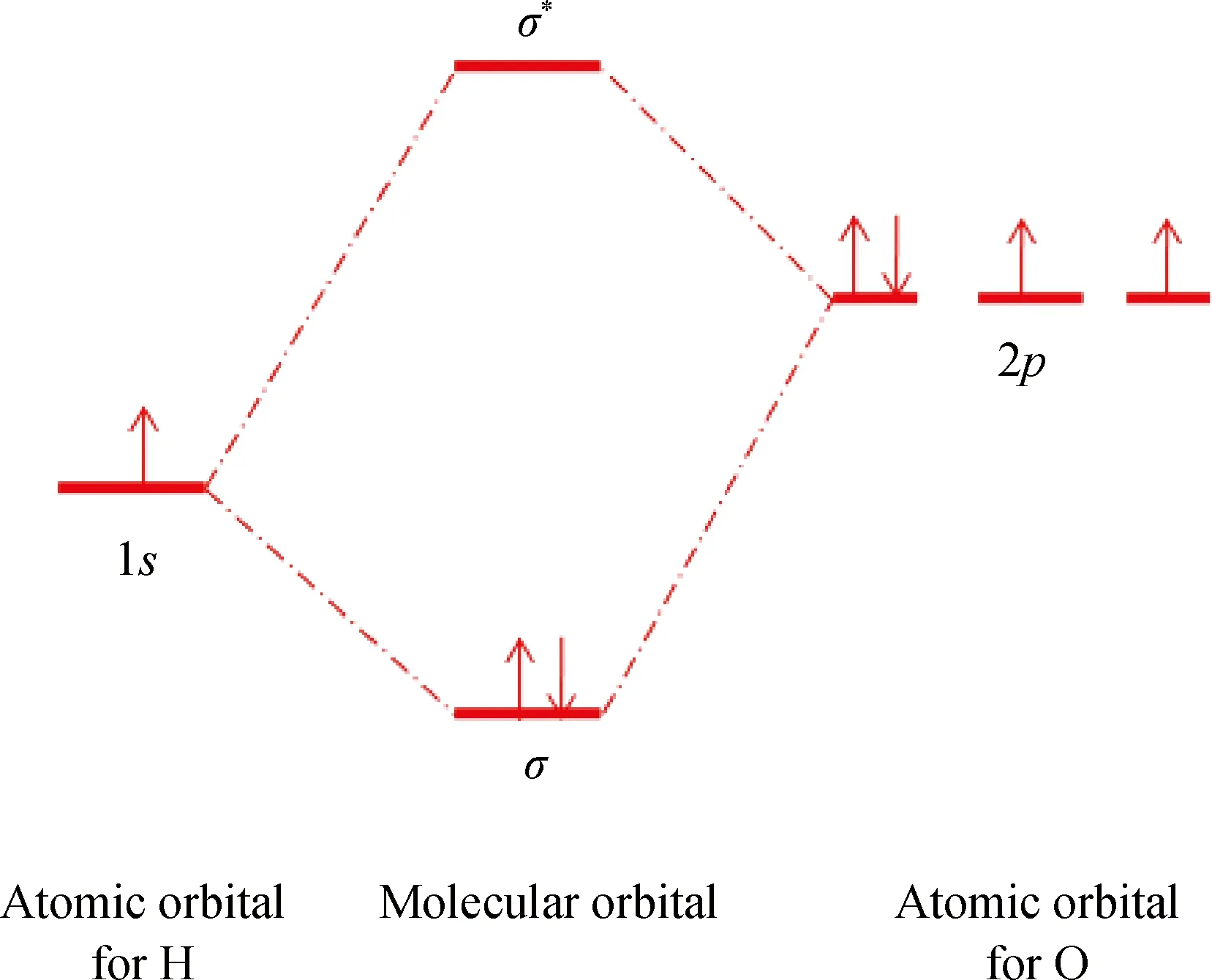
图5 酸性中心O—H的分子轨道示意图
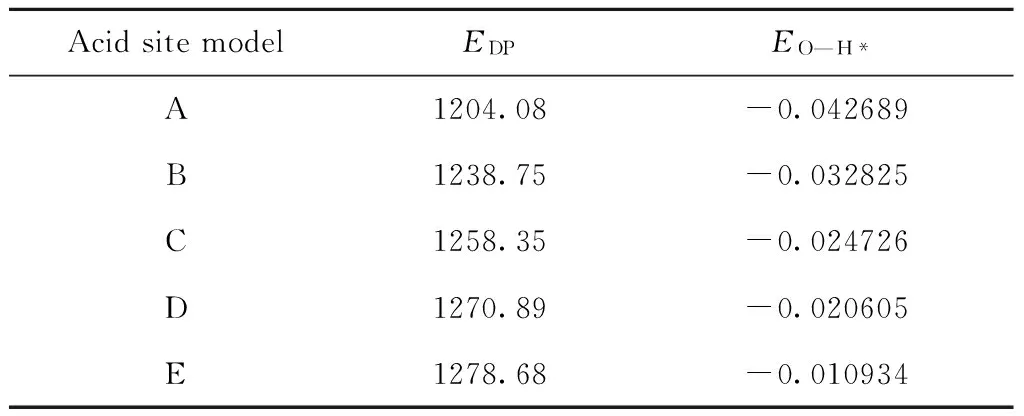
表4 不同酸中心模型的酸性O—H反键轨道能量EO—H*
由于反键轨道σ*是空轨道,具有接受电子的能力。当反键轨道上填入电子,会一定程度与成键作用抵消,使两原子间的化学键强度降低[16]。结构化学中键级的概念,即键级等于1/2(成键电子数—反键电子数),也同样表达了反键轨道中一旦流入电子会降低化学键的强度。由此分析,当酸性O—H的反键轨道σ*一旦填上电子,成键轨道σ的作用将被削弱,酸性H将变得容易解离。EO—H*能量越低表明电子越容易流入反键轨道σ*,成键作用越容易被削弱,键级越容易降低,酸性H越容易解离,表示从酸中心中解离出酸性H所需要的能量(解离能)的EDP也降低。这是EO—H*与EDP存在关系的内在原因。
综上所述,EO—H*与EDP数据上具有对应关系,且能够从本质上阐明二者之间的内在关联,因此EO—H*可以用来表征酸强度,丰富和完善了表征分子筛Brönsted酸强度的结构参数。
3 结 论
(1) 分子筛O—H键长(dO—H)、质子H的Mulliken电荷(qH)、O—H伸缩振动频率(νO—H)、∠Si—O—Al等结构参数对表征Brönsted酸强度存在一定局限,前线分子轨道能量及其能量差与酸强度关系也不明显。酸中心分子轨道能量中的O—H反键轨道能量(EO—H*)与分子筛Brönsted酸强度存在对应关系,即EO—H*能量越低,EDP越小,Brönsted酸性越强。
(2) 从本质上阐明了EO—H*与EDP之间的内在关联。EO—H*能量越低,电子越容易流入反键轨道σ*,成键作用越容易被削弱,酸性H越容易解离,EDP数值越小。
(3) 提出可以用EO—H*表征分子筛Brönsted酸强度,补充和完善了表征分子筛Brönsted酸强度的结构参数。
[1] 郑安民, 黄信炅, 王强, 等. 固体核磁共振技术在固体酸催化剂表征及催化反应机理研究之应用进展[J].催化学报, 2013, 34(3): 436-491.(ZHENG Anmin, HUANG Xinjiong, WANG Qiang, et al. Progress in development and application of solid-state NMR for solid acid catalysis[J].Chinese Journal of Catalysis, 2013, 34(3): 436-491.)
[2] 喻志武, 郑安民, 王强, 等. 固体核磁共振研究固体酸催化剂酸性进展[J].波谱学杂志, 2010, 27(4): 485-515.(YU Zhiwu, ZHENG Anmin, WANG Qiang, et al. Acidity characterization of solid acid catalysts by solid-state NMR spectroscopy: A review on recent progresse[J].Chinese Journal of Magnetic Resonance, 2010, 27(4): 485-515.)
[3] 邬忠琴, 郑安民, 杨俊, 等. NMR探针分子表征分子筛酸性的理论研究[J].波谱学杂志, 2007, 24 (4):501-509.(WU Zhongqin, ZHENG Anmin, YANG Jun, et al. Characterization of acidity of zeolites by NMR probe molecules: A theoretical investigation[J].Chinese Journal of Magnetic Resonance, 2007, 24(4): 501-509.)
[4] MOHAMED E, MICHIHISA K, MOMOJI K, et al. Periodic density functional investigation of Brønsted acidity in isomorphously substituted chabazite and AlPO-34 molecular sieves[J].Microporous and Mesoporous Materials, 2004, 71(1-3): 51-56.
[5] UWE E, MARTIN B, JOACHIM S. Predicting absolute and site specific acidities for zeolite catalysts by a combined quantum mechanics/interatomic potential function approach[J].Journal of Physical Chemistry B, 1997, 101(48): 10035-10050.
[6] PADRAIG O’MALLEY J, DWYER J. An ab initio quantum chemical investigation on the effect of the magnitude of the T-O-T angle on the Brönsted acid characteristics of zeolites[J].Journal of Physical Chemistry, 1988, 92(10): 3005-3007.
[7] ANTONIO R, JEFFREY H P. Quantum chemical studies of acid sites in zeolite ZSM-5[J].Journal of Physical Chemistry, 1993, 97(45): 11754-11761.
[8] BARTHOMEUF D. Aluminium topological density and correlations with acidic and catalytic properties of zeolites[C]//Studies in Surface Science and Catalysis, 1988, 38:178-186. Amsterdam: Elsevier Science Publisher.
[9] SUN Yingxin, YANG Jing, ZHAO Lifeng, et al. A two-layer ONIOM study on initial reactions of catalytic cracking of 1-butene to produce propene and ethene over HZSM-5 and HFAU zeolites[J].Journal of Physical Chemistry C, 2010, 114(13): 5975-5984.
[10] WANG Na, ZHANG Minhua, YU Yingzhe. Distribution of aluminum and its influence on the acid strength of Y zeolite[J].Microporous and Mesoporous Materials, 2013, 169(1): 47-53.
[11] 赵亮, 吴玉坤, 高杉, 等. ZSM-5分子筛硅铝比与其催化性能关系的量子化学研究[J].分子科学学报, 2010, 26(2): 86-91.(ZHAO Liang, WU Yukun, GAO Shan, et al. Quantum chemistry research on the relationship between Si/Al ratios and catalysis activities of ZSM-5 zeolites[J].Journal of Molecular Science, 2010, 26(2): 86-91.)
[12] CYNTHIA L O, BERNHARDT L T. Density-functional theory characterization of acid sites in chabazite[J].Journal of Catalysis. 2004, 227(1): 77-89.
[13] BRAND H V, CURTISS L A, ITON L E. Ab initio molecular orbital cluster studies of the zeolite ZSM-5 1 Proton affinities[J].Journal of Physical Chemistry, 1993, 97(49): 12773-12782.
[14] ZHOU Danhong, BAO Ying, YANG Mingmei. DFT studies on the location and acid strength of Brönsted acid sites in MCM-22 zeolite[J].Journal of Molecular Catalysis A: Chemical, 2006, 244 (1-2): 11-19.
[15] 王中学, 王大喜, 赵震, 等. SBA-15分子筛羟基结构性质及其催化活性的理论研究[J].无机化学学报, 2012, 28(1): 88-96.(WANG Zhongxue, WANG Daxi, ZHAO Zhen, et al. Structure and catalytic properties of the SiOH groups on SBA-15 molecular sieve: A density functional theory study[J].Chinese Journal of Inorganic Chemistry, 2012, 28(1): 88-96.)
[16] 周公度, 段连运. 结构化学基础(第四版)[M].北京: 北京大学出版社, 2008: 79-84.
The Structure Parameters for Brönsted Acid Site Strength of Y Zeolite
YUAN Shuai, LONG Jun, ZHAO Yi, TIAN Huiping, LIU Yujian, XU Yun, DAI Zhenyu
The quantum mechanics method was applied to investigate the structure characteristics of Y zeolite with different Brönsted acid strength. The structural parameters, such as O—H bond distance (dO—H), H Mulliken charge (qH), O—H stretching vibration frequency (νO—H), Si—O—Al angle and molecular orbital energy, were calculated. The relationship between these structural parameters and Brönsted acid strength was discussed. The results showed that there were poor correlations betweenqH,dO—H,νO—Hor Si—O—Al angle and B-acidity, however, there was a better correlation between anti-bonding orbita energy (EO—H*) and B-acidity. The lower theEO—H*, the stronger the B-acidity. An anti-bonding orbit with lowerEO—H*was more easily filled with electron, due to which the energy of the system would rise up to cause the O—H bond broken to give H+, thus the B-acidity would be stronger. On this basis,EO—H*was put forward to characterize Brönsted acid strength of Y zeolite, which would be a good complement to the structure parameters for acid site strength of Y zeolite.
zeolite; acid strength; structural parameters; molecular orbital energy
2015-11-06
国家自然科学基金项目(U1463209)资助
袁帅,男,博士,从事催化裂化催化剂及作用机理研究;Tel: 010-82368981;E-mail: yuanshuai.ripp@sinopec.com
1001-8719(2016)06-1083-07
O641
A
10.3969/j.issn.1001-8719.2016.06.001

