海藻酸钠/壳聚糖包覆尿素微球的制备及其缓释行为
余晓华,颜永斌,郑科旺,黄明军,覃彩芹
(1.湖北工程学院 生物质资源转化利用湖北省协同创新中心,湖北 孝感 432000;2.湖北大学 生命科学学院,湖北 武汉 430062)
海藻酸钠/壳聚糖包覆尿素微球的制备及其缓释行为
余晓华1,2,颜永斌1*,郑科旺1,黄明军1,2,覃彩芹1
(1.湖北工程学院 生物质资源转化利用湖北省协同创新中心,湖北 孝感 432000;2.湖北大学 生命科学学院,湖北 武汉 430062)
利用壳聚糖及羧甲基壳聚糖与海藻酸钠作为载体材料对尿素进行缓释,确定包膜型尿素的最佳制备方案。以壳聚糖、海藻酸钠为基材,尿素为芯材,氯化钙、戊二醛为复合交联剂,采用一步法和两步法制备包膜尿素。通过扫描电镜对包膜尿素微观结构进行表征,采用静水浸泡法对包膜尿素的缓释效果进行测试,最终得到较佳的制备工艺条件。结果表明:当羧甲基壳聚糖与海藻酸钠的配比为2:8,尿素含量为10%~20%,交联剂浓度为3%时,尿素的缓释效果最佳。
壳聚糖;海藻酸钠;尿素;缓控释肥
随着化肥在农业领域的广泛使用,其带来的诸多负面影响也日益突出,氮肥的大量施用引起了资源浪费、农产品品质下降、生态环境恶化等问题[1-2]。为了解决肥料损失严重的问题,目前主要是采用传统调控技术和实时实地进行氮肥管理、农田养分精准管理和缓释肥等措施。其中缓释肥是通过延缓延长肥料时效来提高利用率,目前可以大致分为三种:具有有限水溶性的合成型微溶态缓/控释肥料、包裹材料缓/控释肥料和包膜缓/控释肥料[3]。缓释肥虽然能够有效解决肥料利用率,但考虑到其生产成本较高,因此其在市场上占有率为0.15%,主要用在一些经济价值比较高的作物上[4-5]。在稳产、增产的前提条件下,利用资源丰富的可生物降解的控释材料来促进化学肥料的高效利用,减少生产中化学肥料的投入使用,实现农产品产量与质量安全、农业生态环境保护相协调的可持续发展,同时降低农业生产成本,促进农民节本增收。
壳聚糖是除纤维素以外的第二大天然资源,主要来源于虾、蟹的壳提取物,具有良好的生物相容性、生物可降解性,广泛应用于食品、医药卫生、农业等领域[6-7]。相关研究表明,以壳聚糖作为缓释肥料的包覆材料能够有效的提高肥料的利用率,改善肥料对农作物的作用效果[8]。壳聚糖作为缓释载体材料符合绿色环保的发展观念,壳聚糖在降解的同时可以释放出所含有的C、N元素,起到改良土壤、植物生长调节剂、生物微肥等作用[9]。
考虑到壳聚糖有聚阳离子的电解质特性,而海藻酸钠有聚阴离子的电解质特性,本实验利用两者在静电作用下能形成壳聚糖-海藻酸钠聚电解质复合膜[10-11]的特点,采用两种不同的壳聚糖,分别与海藻酸钠作用,对尿素进行包膜制备,得到两种缓释肥。同时,探究了不同变量下这两种缓释肥的包覆率与载药率,最终确定缓释尿素的最佳制备方案。
1 材料与方法
1.1 材料
壳聚糖(脱乙酰度92%),浙江澳兴生物科技有限公司;羧甲基壳聚糖,利用壳聚糖与氯乙酸在碱性条件下进行化学反应自制[12];海藻酸钠、尿素、醋酸、浓硫酸、无水乙醇、对二甲氨基苯甲醛、无水氯化钙、戊二醛(25%),分析纯,国药集团化学试剂有限公司。
1.2 海藻酸钠/壳聚糖包覆尿素微球的制备
1.2.1 海藻酸钠/壳聚糖包覆尿素微球的制备
将一定量的壳聚糖(CS)加入2% (v/v) 的醋酸溶液,搅拌使其溶解,配制成2%(w/v)的壳聚糖醋酸溶液;同时,将海藻酸钠溶于水配制成1%(w/v)海藻酸钠水溶液。按一定的比例将尿素(UREA)加入到海藻酸钠水溶液中,搅拌使其混合均匀。然后,将海藻酸钠尿素混合液匀速滴入到浓度为2%(w/v)的氯化钙/戊二醛复合交联剂,取出微球并浸泡于CS溶液, 0.5 h后置于35 ℃真空干燥,即得到黄色海藻酸钠/壳聚糖包覆尿素微球。
1.2.2 海藻酸钠/羧甲基壳聚糖包覆尿素微球的制备
将一定量的羧甲基壳聚糖(CMCS)溶于蒸馏水中配置成2%的CMCS溶液,将一定量的海藻酸钠溶于水配制成1%(w/v)海藻酸钠水溶液,按一定的比例加入尿素(UREA),搅拌使其混合均匀。然后,将羧甲基壳聚糖海藻酸钠尿素混合液匀速滴入到浓度为2%(w/v)的氯化钙/戊二醛复合交联剂中。交联反应一段时间后,取出微球,用蒸馏水冲洗三遍,35 ℃真空干燥,即得到黄色的海藻酸钠/壳聚糖包覆尿素复合微球。
1.3 海藻酸钠/壳聚糖包覆尿素微球的性能分析
1.3.1 海藻酸钠/壳聚糖包覆制备尿素微球的SEM测试
壳聚糖包覆尿素微球的表面形貌通过日本 JEOLJSM-6510扫描电子镜(SEM)进行分析,扫描前在样品表面真空喷金,加速电压25 kV。
1.3.2 海藻酸钠/壳聚糖包覆尿素微球的溶胀率测试
将干燥的微球浸泡于蒸馏水中24 h,使其充分溶胀,利用溶胀前后微球的重量计算其溶胀率:
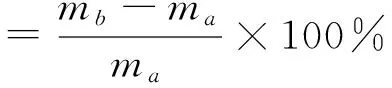
式中:ma为干燥微球的重量;mb为溶胀后样品重量。
1.3.3 海藻酸钠/壳聚糖包覆尿素微球的包封率测试
标准曲线制作:准确称取0.1 g尿素配制成1 mg/mL尿素标准液,置于4 ℃条件下存放。分别移取1、2、3、4、5、6、7、8、9、10 mL的尿素标准液于25 mL容量瓶,同时分别加入10 mL PDAB显色剂的用量、4 mL的2.0 moL/L硫酸溶液,用去离子水定容,摇匀后静置10 min。在422 nm处测吸光度,用去离子水为空白实验。根据尿素浓度和吸光度绘制出标准曲线并进行线性拟合,得到校正方程为y=566.1x+2.391(R2=0.996)。 待包膜尿素静置24 h后,将其破碎。将搅碎的包膜尿素置于水中24 h,取1 mL液体测其吸光度(422 nm),代入标准曲线方程:y=566.1x+2.391(R2=0.996),算出溶液中的尿素质量m1。利用实验中记录的数据算出10.0 g包膜尿素对应的尿素加入量m2,尿素的包封率W计算公式如下:W=[m1/m2]×100%
1.3.4 海藻酸钠/壳聚糖包覆尿素微球的缓释测试
采用静水浸泡法[13-14],取干燥后的包膜尿素10.0 g放在一定规格烧杯中加入40 mL水,放于恒温箱中,温度设定为25 ℃。隔一段时间取1 mL的浸泡液,时间梯度定为1 h、2 h、3 h、6 h、12 h、24 h。将1 mL浸泡液倒入25 mL的容量瓶中,加入10 mL的PDAB显色剂、4 mL的2.0 moL/L硫酸溶液,最后用去离子水定容至25 mL,同时配制一组未加尿素的空白组溶液作为参照。根据标准曲线算出溶液中的尿素释放量,从而计算一定时间内养分的溶出量。
2 结果与讨论
2.1 海藻酸钠/壳聚糖包覆制备尿素微球的SEM图谱分析
图1为海藻酸钠/壳聚糖包覆尿素微球的微观结构图。由图1可知,干燥后复合微球呈干瘪收缩状,这与崔红华等[15]海藻酸钠/壳聚糖葫芦素微球的研究结果一致。海藻酸钠/壳聚糖包覆尿素微球中CS直接附着于微球表面形成相对致密的膜结构,水分子不易通过,肥料难以释放,养分缓释效果差。由于微球的制备过程,从而造成两者在形貌与结构强度上的差异。
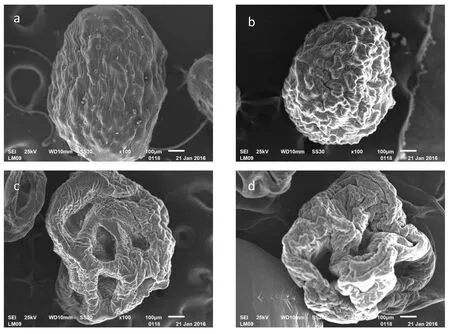
注:图(a)、(b)均为海藻酸钠/壳聚糖包覆尿素微球;图(c)、(d)海藻酸钠/羧甲基壳聚糖包覆尿素微球。
2.2 海藻酸钠/壳聚糖包覆尿素微球的溶胀率
材料透水性的好坏可以用复合微球干燥前后的溶胀率评定,具体数据见表1和表2。
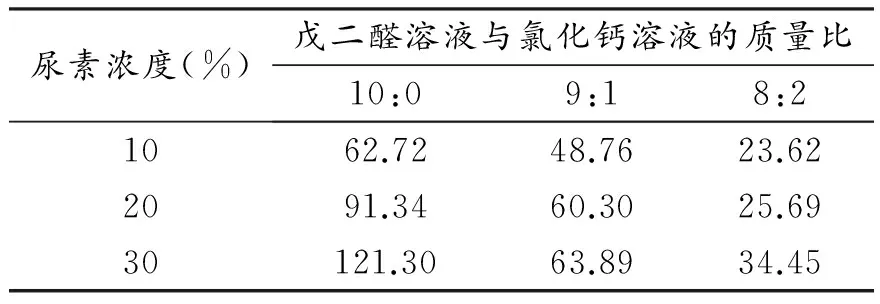
表1 海藻酸钠/壳聚糖复合微球的溶胀率
从表1中可知,相同尿素浓度下,随着交联剂戊二醛含量的增加,微球的溶胀率随之减小。实验表明,交联剂氯化钙含量增加,交联程度越高,交联度的提高使得膜紧实度提高,自由体积减小,水及肥料分子从自由体积空隙透过膜变得困难,从而使膜外的水难以进入膜内;在交联剂配比一样的情况下,尿素的含量越高,其微球溶胀率也越高,这是因为尿素中含有两个氨基,氨基作为负电子基团能和水分子间形成氢键,水从膜外透过膜层进入膜内的过程是一个氢键位置不断改变的过程,膜材料与水分子间的这种相互作用,使得水分很容易透过膜层,因而在适量范围内尿素含量越高其微球溶胀率越高。

表2 海藻酸钠/羧甲基壳聚糖复合微球的溶胀率
从表2可知,海藻酸钠的含量越高,微球的溶胀率越低。这是由于海藻酸钠的羧基与壳聚糖壳聚糖氨基之间存在静电相互作用,当壳聚糖与海藻酸钠的配比越接近时,包膜层的结构越复杂,膜更加紧密,因此实验中滴定成球时,膜内部的水难以透过,保水性能越好;而当壳聚糖-海藻酸钠的配比相同时,尿素含量越高,微球溶胀率越高,这与壳聚糖/海藻酸钠的原因一样。
对比发现,同等条件下尿素含量越高,微球的溶胀率也越高。羧甲基壳聚糖相较与壳聚糖而言,其保水性能较好,这与两者的分子间作用力和结构的差异性有关。研究表明,由于壳聚糖分子量大小的差异性,其在成膜过程中分子间作用力大小不同。壳聚糖分子量越高其分子链越长,链与链相互交缠,相互作用力也随之增强,使得其结构致密,从而使小分子物质不易通过,渗透性差。羧甲基壳聚糖作为改性后的壳聚糖,其引入的亲水性羧甲基基团与水分子之间形成的氢键作用,可以提高其微球溶胀率。
2.3 海藻酸钠/壳聚糖包覆尿素微球的尿素包封率
对比表3与表4可知,羧甲基壳聚糖-海藻酸钠包膜尿素的包封率更高,这可能与包膜层结构有关,包膜层越紧密尿素扩散出膜层的溶出量也就越少。实验发现尿素包封率整体不高,这可能与成膜的反应时间有关,如搅拌的速度、温度的控制、缓释的条件等。
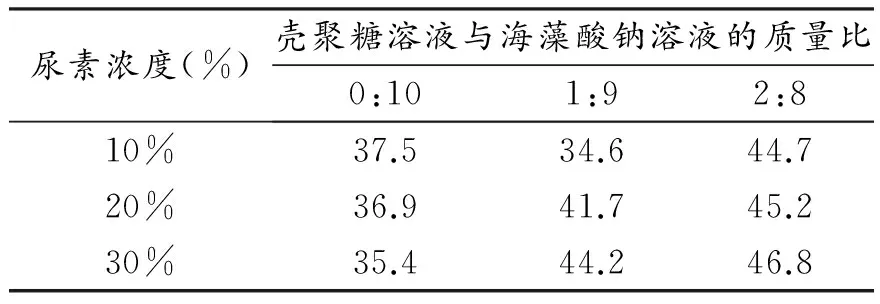
表3 海藻酸钠/壳聚糖-复合微球的尿素包封率

表4 海藻酸钠/羧甲基壳聚糖-复合微球的尿素包封率表
2.4 海藻酸钠/壳聚糖包覆尿素微球释放效果研究
缓控释肥的养分释放过程一定程度上与包膜材料的透水性有关,水透过包膜层进入肥料内部过快,肥料中的养分释放速率大,肥料养分的前期抑制释放性能差。根据缓控释肥的国家标准:肥料浸泡24 h后养分释放量不低于总质量分数的15%,即为缓控释肥。采用紫外分光光度计得到样品待测液不同时段的吸光度,将得到的数据带入校正方程y=566.1x+2.391(R2=0.996),可得到相应时间的尿素缓释量,具体结果如图2所示。
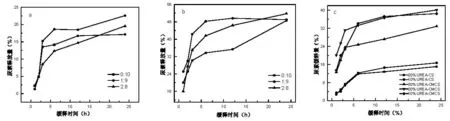
注:(a)为羧甲基壳聚糖组尿素含量为10%、不同CS-Alg配比的尿素缓释情况;(b)为壳聚糖组尿素含量为20%、不同CS-Alg配比的尿素缓释情况;(c)为两种壳聚糖不同尿素含量的尿素缓释情况
由图2可知,聚合物包膜结构与交联剂造成了水扩散与膜内溶胀率的不同,水分透过包膜层的净透出率越大,养分释放得越快。尿素含量的高低对壳聚糖-海藻酸钠包膜尿素的缓释量影响不明显。壳聚糖与海藻酸钠作用形成的包膜层结构不够紧密,且尿素中的氨基为亲水基团,因此尿素含量越高,膜内保留的水分越多,尿素溶解越多,随着膜内外的浓度差变大,养分释放加快。而羧甲基壳聚糖-海藻酸钠包膜尿素的膜层紧密,因此尿素含量的高低对尿素溶出速率影响不大。
由图2(a)和(b)可知,羧甲基壳聚糖-海藻酸钠包膜尿素相对于壳聚糖-海藻酸钠包膜尿素而言,其缓释效果明显要好,更加接近缓控释肥的国家标准。原因主要是羧甲基组聚合物分子量更大,聚合物成膜性更好,机械强度增大,包膜更加完整,且膜的结构更加致密。由于分子量越高,聚合物的结构越为紧凑,水及肥料分子不易通过,养分缓释效果更好。Raban等[16]认为包膜肥料主要通过扩散机制将养分释放到土壤中的,扩散驱动力是养分浓度梯度或压力梯度。当施用这种包膜肥料后,土壤或基质中的水分进入膜内溶解包裹的养分,并在扩散驱动力的作用下扩散到膜外,可以在3~12个月的时间里持续不断地释放养分。
对比图2(a)、图2(b)与图2(c)可知,在缓释开始的几个小时内尿素的溶出速率较大,而后溶出速率较为平缓。这是由于包膜型尿素的释放过程主要分为两个阶段,第一个阶段为水分进入膜内溶解尿素,尿素扩散至膜层表面;第二个阶段为尿素从膜层表面扩散到水中。由于在制备包膜尿素过程中有部分尿素未完全包裹进去附着在膜表面,因而在尿素缓释初期膜表面的尿素最先溶出,这部分的尿素溶出速率较快,然后是膜里面的尿素溶解扩散过程,这一阶段的溶出速率较慢。
3 结论
本实验以不同的壳聚糖与海藻酸钠为缓释材料,利用其良好的成膜性以及它们间的静电作用,对尿素进行物理包埋,在交联剂作用下制备出了干燥后平均粒径为1 mm左右的球形缓释尿素。通过对微球溶胀率的测定、微观结构的表征、尿素包封率以及缓释效果的研究的测定,最终确定出最佳的制备方案为:羧甲基壳聚糖与海藻酸钠的配比为2:8,尿素含量为10%~20%,交联剂的质量分数为3%。
[1] 裴瑞杰,胡述晓,孙天洲,等.缓控释肥料的研究与应用现状[J].中国农业信息,2015(8):62-65.
[2] 王月祥.缓/控释肥料的研究现状及进展[J].化工中间体,2010,4(3):5-9.
[3] 闫湘,金继运,何萍,等.提高肥料利用率技术研究进展[J].中国农业科学,2008,41(2):450-459.
[4] 王茹芳,张夫道,刘秀梅,等.胶结型缓释肥在小麦上应用效果的研究[J].植物营养与肥料学报,2005,11(3):340-344.
[5] 翟军海,高亚军,周建斌.控释/缓释肥料研究概述[J].干旱地区农业研究,2002,20(1):45-48.
[6] Berkland C, Kipper M J, Narasimhan B, et al. Microsphere size, precipitation kinetics and drug distribution control drug release from biodegradable polyanhydride microspheres[J].Journal of Controlled Release,2004,94(1):129-141.
[7] Szczubialka K Zomerska K,Karewicz A,et al.Novel drug carrier-Chitosan gel microspheres with covalently attached nicotinic acid[J].Journal of Controlled Release,2006,116(2):13-15.
[8] 王恩文,鲍莹.壳聚糖在农业中的应用研究[J].现代农业科技,2012(10):24-25.
[9] 马鹏鹏.甲壳素及其衍生物在农业生产中的应用[J].植物生理学报,2001,37(5):475-478.
[10] Ribeiro A J, Silva C, Ferreira D, et al. Chitosan-reinforced alginate microspheres obtained through the emulsification/internal gelation technique[J].European Journal of Pharmaceutical Sciences, 2005, 25(1):31-40.
[11] Shen J,Fatehi P,Ni Y.Biopolymers for surface engineering of paper-based products [J].Cellulose,2014,21(5):3145-3160.
[12] Wang Z,Yan Y,Yu X,et al.Protective effects of chitosan and its water-soluble derivatives against lead-induced oxidative stress in mice[J].International Journal of Biological Macromolecules,2015,83:442-449.
[13] 杨相东,曹一平,江荣风,等.几种包膜控释肥氮素释放特性的评价[J].植物营养与肥料学报,2005,11(4):501-507.
[14] 张玉凤,曹一平,陈凯.膜材料及其构成对调节控释肥料养分释放特性的影响[J].植物营养与肥料学报,2003,9(2):170-173.
[15] 崔红华,李超英,李敏,等.海藻酸钠-壳聚糖微球制备及质量评价研究[J].长春中医药大学学报,2011(5):844-846.
[16] Shaviv A,Raban S,Zaidel E.Modeling controlled nutrient release from polymer coated fertilizers:diffusion release from single granules [J].Environmental Science & Technology,2003,37(10):2251-2256.
(责任编辑:熊文涛)
Sodium Alginate/Chitosan Coated Urea Preparation of Microspheres and Its Slow Release Behavior
Yu Xiaohua1,2,Yan Yongbin1*,Zheng Kewang1,Huang Mingjun1,2,Qin Caiqin1
(1.TheCollaborativeInnovationCenterofHubeiProvinceForBiomassConversionandUtilization,HubeiEngineeringUniversity,Xiaogan,Hubei432000,China;2.SchoolofLifeScience,HubeiUniversity,Wuhan,Hubei430062,China)
Using chitosan and carboxymethyl chitosan and sodium alginate as carrier materials for slow-release urea, the optimal preparation method was determined for coated urea type. With chitosan and sodium alginate as the main raw material, urea as core material,calcium chloride and glutaraldehyde as crosslinking agent, one-step and two-step method were used for the preparation of chitosan, sodium alginate composite microspheres. By scanning electron microscope to observe the coating of urea, the slow release effect of coated urea was tested by still water immersion method, and the optimum preparation conditions were obtained. The results showed that when the ratio of carboxymethyl chitosan and sodium alginate was 2:8, the urea content was 10%~20%, the concentration of crosslinking agent was 3%, and the effect of urea was the best.
chitosan; alginate; urea; controlled-release fertilizer
2016-08-27
国家自然科学基金面上项目(31371750)
余晓华(1992- ),女,湖北黄石人,湖北工程学院生物质资源转化利用湖北省协同创新中心硕士研究生。
颜永斌(1975- ),男,湖北仙桃人,湖北工程学院生物质资源转化利用湖北省协同创新中心副教授,博士,本文通信作者。
TS201.25
A
2095-4824(2016)06-0010-05

