固体酸催化合成1,4-丁二醇二丙烯酸酯动力学
崔文岗,马海霞,骆军容,张明伟,梁世伟,高明明,李稳宏
1.西北大学化工学院,陕西 西安 710069;
2.第四军医大学校务处,陕西 西安 710032
固体酸催化合成1,4-丁二醇二丙烯酸酯动力学
崔文岗1,马海霞1,骆军容2,张明伟1,梁世伟1,高明明1,李稳宏1
1.西北大学化工学院,陕西 西安 710069;
2.第四军医大学校务处,陕西 西安 710032
对1,4-丁二醇与丙烯酸在固体超强酸SO42-/TiO2-SnO2作用下,催化合成1,4-丁二醇二丙烯酸酯的反应动力学进行研究。考察了固体超强酸催化作用下1,4-丁二醇、丙烯酸以及体系水含量对初始反应速率的影响,以Elay-Rideal机理为理论基础,建立了固体超强酸SO42-/TiO2-SnO2为催化剂合成工艺的动力学模型。实验数据和模型计算结果的比较表明,该模型精确度良好,实验验证模型预测值与实验值相对偏差小于 5%,为1,4-丁二醇二丙烯酸酯合成工艺的优化提供了依据。
1,4-丁二醇二丙烯酸酯 1,4-丁二醇 丙烯酸 固体超强酸
丙烯酸酯是一类重要的有机化工产品,目前约有超过100种特种丙烯酸酯,其产量却只及通用丙烯酸酯的5%左右[1-3]。生产丙烯酸酯的传统工艺一般采用液体酸作为催化剂,存在三废高、能耗高等环境问题。如何在保证原有生产效率的前提下,有效减少排放和消耗,成为了丙烯酸酯行业发展的方向[4],许多研究者将目光聚集到固体酸上面。目前研究的主要方向为固体杂多酸、固体超强酸以及负载型有机酸催化剂。
1,4-丁二醇与丙烯酸在固体超强酸催化的条件下发生的酯化反应,涉及到非均相双分子反应机理。非均相双分子反应机理包括Langmiur-Hinshelwood和Elay-Rideal机理[5]。本工作以SO42-/TiO2-SnO2固体酸为催化剂催化合成1,4-丁二醇二丙烯酸酯的酯化反应进行动力学研究。建立固体酸催化反应的动力学模型,通过实验和数学方法求解动力学参数,并对模型进行了验证。
1 实验部分
1.1 实验原理
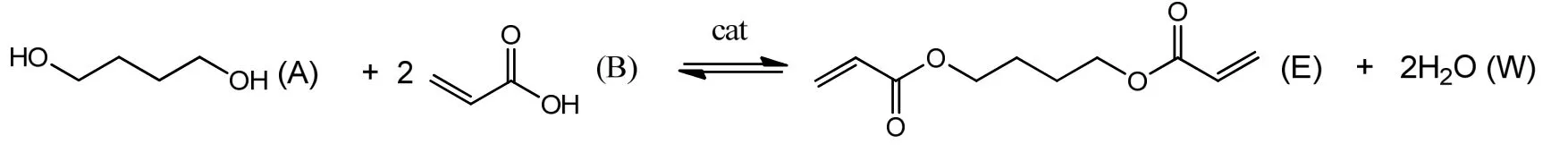
1,4-丁二醇与丙烯酸反应是一个可逆反应,反应式如下所示。该反应为SN2反应,在催化剂的作用下,1,4-丁二醇作为亲核试剂进攻丙烯酸上的羰基,经历取代-消除历程完成反应,其中催化剂可使羰基碳更为缺电子而有利于醇与它发生亲核加成而促进目标产物的生成。
1.2 实验过程及方法
根据前人的研究成果[6-9],本工作的研究将在无外扩散和孔扩散影响的情况下进行。将0.2 mol的1,4-丁二醇加入三口烧瓶,先后加入5%对固体酸催化剂和1%对苯二酚,在600 r/min转速下先后加入一定量的丙烯酸和50%甲苯,加热到135 ℃开始反应并计时,到4 h时停止反应,半小时取样一次用于分析:酯含量根据 HB/FG03-2009《辐射固化用多官能度丙烯酸酯单体纯度(酯含量)的测定》的方法进行检测;反应体系中的1,4-丁二醇的含量采用气相色谱外标法进行测定。
2 结果与讨论
2.1 原料和水含量对反应速率的影响
在1,4-丁二醇1.905 mol/L,固体酸催化剂质量含量为5%,对苯二酚质量含量1%,甲苯质量含量50%条件下,考察了不同温度下各组分浓度对初始反应速率的影响,结果见图1~图3。
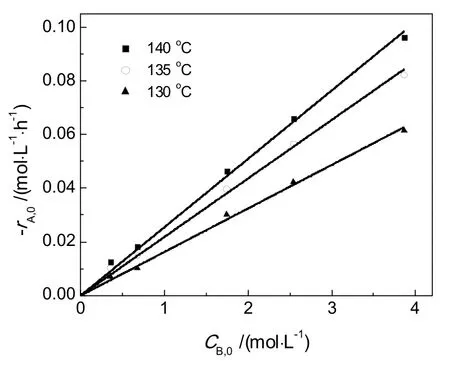
图1 不同丙烯酸浓度下的初始速率Fig.1 The initial reaction rate at different concentrations of acrylic acid
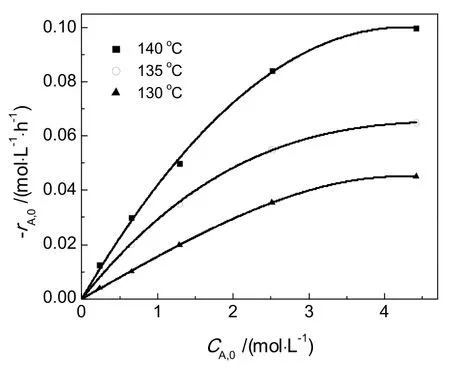
图2 不同1,4-丁二醇浓度下的初始速率Fig.2 The initial reaction rate at different concentrations of 1,4-butanediol
图1所示为不同丙烯酸浓度下初始反应速率变化情况,可以看出,不同反应温度下初始反应速率对丙烯酸浓度变化均为直线;随着初始酸含量的增加,初始反应速率呈线性增大。图2结果表明,1,4-丁二醇浓度对初始反应速率的影响呈曲线关系,在低浓度醇含量范围内,随着醇浓度增大初始反应速率呈线性增加,在高浓度醇含量范围内,随着酸浓度增加,初始反应速率增长幅度不断收窄,趋于恒定。而在相同条件下,随着初始水含量的增大,初始反应速率不断下降,如图3所示。
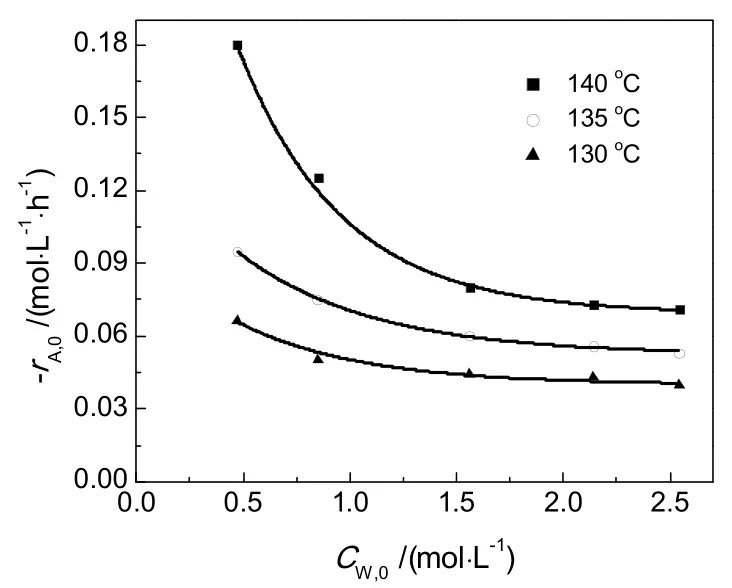
图3 体系初始含水量对初始反应速率的影响Fig.3 The influence of initial water content on the initial reaction rate
2.2 动力学模型的建立
通过以上实验可知,随着反应体系中1,4-丁二醇浓度的增加,初期反应速率呈线性增大,随着时间的延长,速率增长幅度不断收窄,说明1,4-丁二醇吸附在催化剂表面形成吸附态参与反应,随着1,4-丁二醇浓度增加,其吸附速率成为速率控制步,导致反应速率增长放缓。而反应速率随着体系中丙烯酸浓度的不断增加而呈线性增大,说明丙烯酸是以游离态参与反应的。根据以上分析可知,酸醇酯化反应合成1,4-丁二醇二丙烯酸酯的反应机理符合Eley-Rideal模型。即吸附在固体酸催化剂表面上的1,4-丁二醇醇分子与本体溶液中的丙烯酸分子发生酯化反应。与此同时,水分子对催化剂的吸附会对酯化反应的进行起到阻碍作用,而根据相关研究[8-10],可以忽略携水剂甲苯和生成物丙烯酸酯的吸附作用。
根据以上结论,反应速率表达式可以表示为:
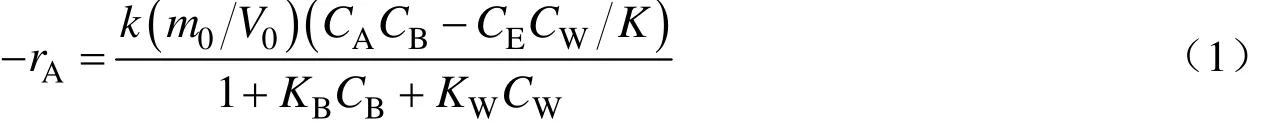
由于在反应初始阶段没有酯生成,因此式(1)可简化为:

根据实验数据,将不同温度下的-rA,0与CA,0作图,得到如图1所示的直线,斜率为。
通过式(2)变形得到

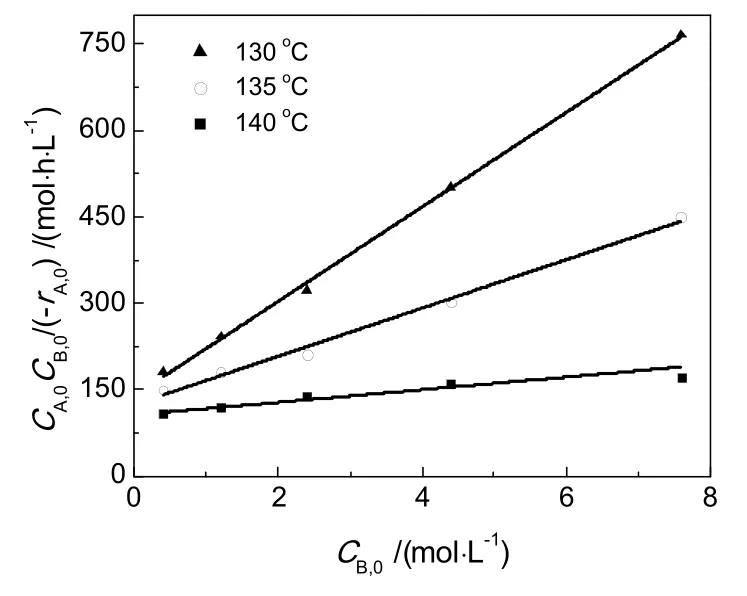
图4 CA,0CB,0/(-rA,0)-CB,0在不同温度下的拟合直线Fig.4 The fit line of CA,0CB,0/(-rA,0)-CB,0under different temperatures
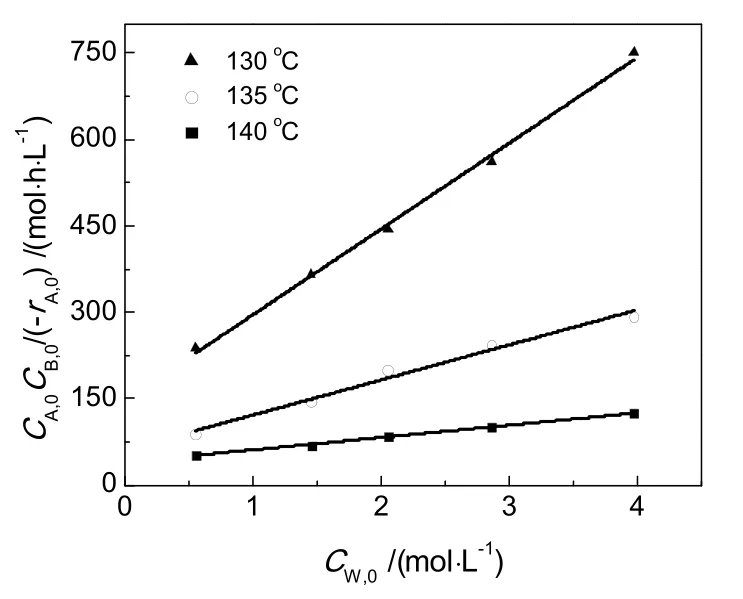
图5 CA,0CB,0/(-rA,0)-CW,0在不同温度下的拟合直线Fig.5 The fit line of CA,0CB,0/(-rA,0)-CW,0under different temperatures
为考察水浓度对反应的阻碍作用,将式(1)变形,由于反应初始阶段没有生成物,得到:

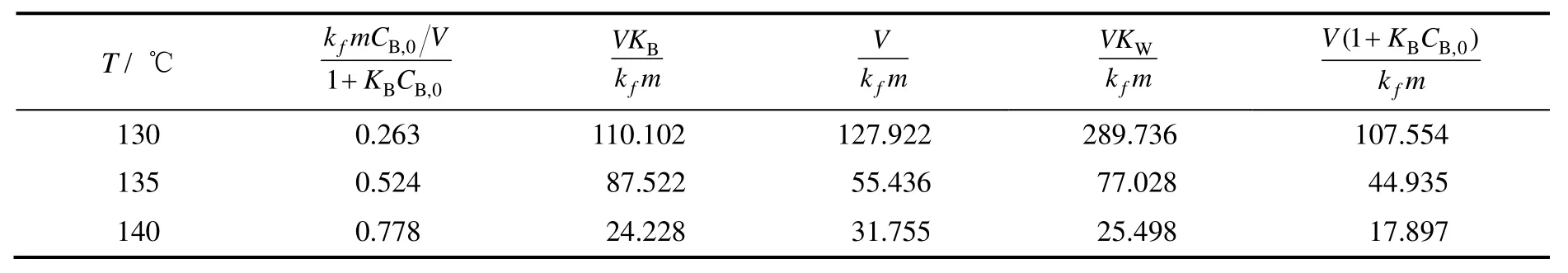
表1 拟合得到的斜率和截距值Table 1 The fitting values of slope and intercept
利用平均法[11]求解以上方程组,得到在不同温度下的kf,KB,KW的取值,见表2。

表2 不同温度下的kf, KB, KW取值Table 2 The values of kf, KB, KWat different temperatures
根据表2中所列的动力学常数值,利用Arrenius方程拟合得到反应温度与常数kf,KB,KW的关系式,如下所示:

根据式(1),反应速率可以以丙烯酸的反应速率表示,则可以得到式(9):
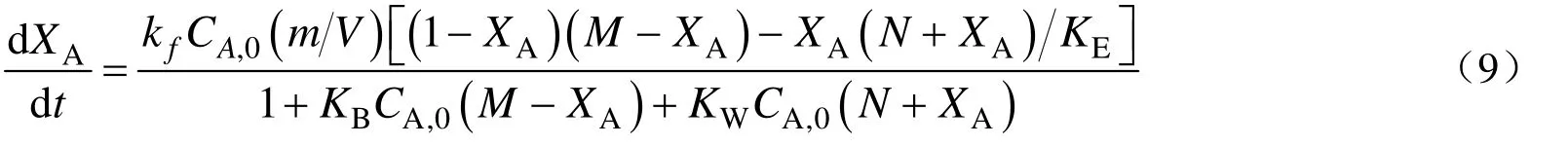
2.3 动力学模型的验证
利用尤格-库塔法对式(9)进行数值积分,得到XA与t的关系式,在酸醇比2.2:1,温度135 ℃,对苯二酚 1%,甲苯 50%的实验条件下,实验值与计算值见图6。
由图6可见,计算值与实验值相对偏差不大于5%,说明该模型精确度良好,能很好地预测实验结果,从而能够指导进一步实验研究。
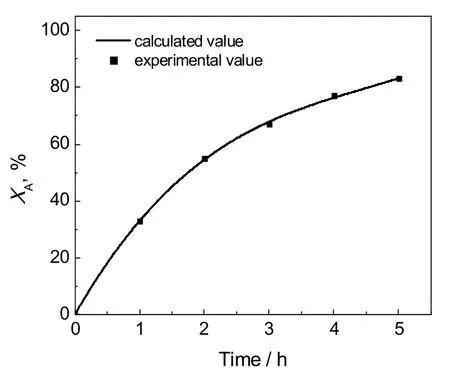
图6 计算值与实验值对比结果Fig.6 The comparison of the calculated and experimental values
3 结 论
a)1,4-丁二醇与丙烯酸直接酯化合成 1,4-丁二醇二丙烯酸酯的反应过程是一个二级可逆反应;建立SO42-/TiO2-SnO2固体酸催化合成1,4-丁二醇二丙烯酸酯的动力学模型;
b)固体酸催化合成1,4-丁二醇二丙烯酸酯的反应机理符合Eley-Rideal模型,即溶液中的1,4-丁二醇分子与吸附在固体酸表面的丙烯酸分子发生反应,通过进一步实验建立了动力学模型,并通过实验和数学方法求解,通过实验验证模型预测值与实验值相对偏差在5%以内,说明模型精确度良好。
符号说明
CA,0——1,4-丁二醇初始浓度,mol/LK——反应平衡常数
Ci——在本体溶液中的浓度,mol/LKi——吸收平衡常数
k1——正向速率常数,mol/hm——固体酸催化剂质量
kf——正向反应速率常数M——1,4-丁二醇某时刻的质量,g
N——生成物的总量V——体系总体积,L
r——反应速率,mol/hXAe——1,4-丁二醇平衡转化率,%
t——反应时间,hXA——1,4-丁二醇某时刻的转化率,%
[1] 王沛熹, 罗丽宏. 丙烯酸(酯)制备、应用进展及市场趋势 [J]. 化工科技市场, 2001, 24(4):15-18. Wang Peixi. Luo Lihong. Preparation, application and market trend of acrylic acid (ester) [J]. Chemical Technology Market, 2001, 24(4):15-18.
[2] 杜茂平, 毛君绒, 曾 睿. 丙烯酸酯涂料改性研究现状及发展趋势 [J]. 涂装与电镀, 2006, (5):11-14. Du Maoping, Mao Junrong, Zeng Rui. Present status and developmental trend of modifying acrylate coating [J]. Coatings Painting & Electroplating, 2006, (5):11-14.
[3] 张翼鸿. 世界丙烯酸化工新进展 [J]. 现代化工, 1997, (7):9-12. Zhang Yihong. New progress of acrylic acid production in the world [J]. Modern Chemical Industry, 1997, (7):9-12.
[4] Xu J, Shi W. Progress in radiation curing marketing and technology [J]. J Coat Techno, 2002, 74(928):67-72.
[5] 陈诵英. 催化反应工程基础 [M]. 北京: 化学工业出版社, 2011: 136-139.
[6] 毛东森, 卢冠忠, 陈庆龄, 等. 负载型氧化物固体超强酸催化剂的制备及应用 [J]. 化学通报, 2001, 64(5):278-284. Mao Dongsen, Lu Guanzhong, Chen Qingling, et al. Preparation and application of supported oxide solid super acid catalyst [J]. Chemistry, 2001, 64(5):278-284.
[7] 杨师棣, 汤发有. 固体超强酸SO42-/ZrO2-TiO2催化合成丙烯酸异丁酯 [J]. 精细石油化工, 2001, (1):6-9 Yang Shidi, Tang Fayou. Catalytic synthesis of isobutyl acrylate by solid super acid SO42-/ZrO2-TiO2solid super acid [J]. Speciality Petrochemicals, 2001, (1): 6-9.
[8] Darge O, Thyrion F C. Kinetics of the liquid phase esterification of acrylic acid with butanol catalysed by cation exchange resin [J]. J Chem Technol Biotechnol, 1993, 58(4):351-355.
[9] Dassy S, Wiame H, Thyrion F C. Kinetics or the liquid phase synthesis and hydrolysis of butyl lactate catalysed by cation exchange resin [J]. J Chem Technol Biotechnol, 1994, 59(2):149-156.
[10] Choi J, Hong W H, Chang H N. Reaction kinetics of lactic acid with methanol catalyzed by acid resins [J]. Int J Chem Kinet, 1996, 28(1):37-41.
[11] 王金福. 化工应用数学分析 [M]. 北京: 化学工业出版社. 2006: 251.
Kinetics of Catalytic Synthesis of 1,4-Butanediol Diacrylate over SO42-/TiO2-SnO2Solid Acid
Cui Wengang1, Ma Haixia1, Luo Junrong2, Zhang Mingwei1, Liang Shiwei1, Gao Mingming1, Li Wenhong1
1. School of Chemical Engineering, Northwest University, Xi’an 710069, China
2. General Affairs Department, Fourth Military Medical University, Xi’an 710032, China
The 1,4-butanediol diacrylate was synthesized and its reaction kinetic model was studied using 1,4-butanediol and acrylic acid catalyzed by solid superacid SO42-/TiO2-SnO2. The effects of the concentration of acrylic acid, 1,4-butanediol and water on the initial reaction rate have also been investigated. Based on Elay-Rideal mechanism, the kinetic model for the solid super acid catalyst synthesis process has been established and proved to be validated though the experiments and mathematical methods. The results showed excellent accuracy of the experimental verification model. The relative errors between the values predicted by the model and those from the actual experiment was less than 5% which provided good predication for optimization of the synthesis process of 1,4-butanediol diacrylate.
1,4-butanediol diacrylate; 1,4-butanediol; acrylic acid; solid superacid
TE624.4
A
1001—7631 ( 2016 ) 01—0055—05
2015-08-10;
2015-10-20。
崔文岗(1991—),男,硕士研究生;马海霞(1974—),女,教授,通讯联系人。E-mail:mahx@nwu.edu.cn。

