琥珀酸去甲文拉法辛缓释微丸胶囊的制备及微丸体外释药研究
陈 才,何 芳,龙 锐(重庆医科大学附属第一医院药学部,重庆 400016)
琥珀酸去甲文拉法辛缓释微丸胶囊的制备及微丸体外释药研究
陈 才*,何 芳,龙 锐#(重庆医科大学附属第一医院药学部,重庆 400016)
目的:制备琥珀酸去甲文拉法辛(DVS)缓释微丸胶囊,并对微丸体外释药特性进行研究。方法:采用醇溶上药法制备DVS微丸,并进行微丸质量评价及粉体学性质研究。用乙基纤维素和羟丙甲基纤维素作为包衣材料,流化床包衣制备DVS缓释微丸,干燥后装入肠溶空心胶囊中,制得缓释微丸胶囊。考察缓释微丸的体外释药特性、不同干燥时间(1~24 h)和人工胃液对其释药的影响。结果:DVS微丸和DVS缓释微丸的膜表面均光洁、有散在分布的小孔。DVS微丸中DVS的含量为19.56%(RSD=0.53%,n=10),上药率为94%,堆密度为0.792 1 g/ml,圆整度为7.84°,休止角为21.3°。DVS缓释微丸经不同时间干燥后的释药差异无统计学意义(P>0.05),经人工胃液处理3 h后累积释放度降低;DVS缓释微丸释药规律符合一级动力学过程。结论:本方法成功制成具有缓释作用的DVS缓释胶囊,且制备过程中可不进行干燥。
琥珀酸去甲文拉法辛;缓释微丸;流化床包衣;体外释药;制备
抑郁症是一种以持久且显著的情感低落、思维缓慢、认知功能受损、精神运动性迟缓为主要特征的心境障碍。2013年世界卫生组织(WHO)的统计结果表明,世界范围内的抑郁症和恶劣心境者的发病率高达12.8%[1]。其中重度抑郁症(Major depressive disorder,MDD)在美国和全世界范围内的发病率分别为16%~17%和3%~17%,已成为全世界范围内第四大致残因素,预计至2020年将继缺血性心血管疾病后,成为第二大致残因素[2]。然而,目前临床上仍无治疗效果可预测、效率较高和缓解率较好的抗抑郁药。
琥珀酸去甲文拉法辛(Desvenlafaxine succinate,DVS)是首个美国FDA批准上市,用于治疗重度抑郁症的选择性5-羟色胺-去甲肾上腺素再摄取抑制剂(Serotonin-norepinephrine reuptake inhibitors,SNRIs)[3],其作用机制与盐酸文拉法辛类似,能高效、选择性地抑制对突触前膜5-羟色胺和去甲肾上腺素的再摄取,具有耐受性强、安全性好、口服生物利用度高等特点[4]。DVS在50~400 mg/d的剂量范围内,药动学呈线性分布[5],治疗MDD有效且耐受性较好[6-9]。DVS血浆蛋白结合率为30%,表观分布容积为3.4 L/kg。临床研究表明,约45%的DVS以原型通过尿液排泄,其余的主要经Ⅱ相反应葡萄糖醛酸化而生成葡萄糖醛酸结合物,经肾脏排泄,小部分在肝脏中经细胞色素P450(CYP)3A4代谢生成氮氧双去甲基文拉法辛[10]。目前,DVS在美国上市的为缓释制剂,每日只需口服1次,国内还没有DVS的相关剂型上市。为了满足国内患者的需求,本研究采用微丸包衣技术制备DVS缓释胶囊,并进行体外释放度研究,以开发符合《中国药典》规定的、工艺简单且具有自主知识产权的DVS缓释胶囊。
1 材料
1.1 仪器
UV-2401型紫外-可见分光光度计(日本岛津公司);A-120-CSi型电子天平(西班牙Cobos公司);Mini-Glatt型流化床(德国Glatt公司);3号胶囊填充板(重庆朗斯制药机械有限公司);S4800型扫描电镜(日本Hitachi公司);TCL-16型高速台式离心机(上海安亭科学仪器厂)。
1.2 药品与试剂
DVS对照品(中国食品药品检定研究院,批号:100005-201406,纯度:100%);DVS原料药(重庆康刻尔制药有限公司,批号:130501,纯度:99.9%);蔗糖丸芯(上海卡乐康包衣技术有限公司,批号:A1302);肠溶空心胶囊(浙江绍兴康可胶囊有限公司,批号:20140216);乙基纤维素(EC,上海Colorcon公司,批号:69010682);羟丙甲基纤维素(HPMC,日本旭化成株式会社,批号:CW1201);聚乙烯吡咯烷酮K30(PVP K30,上海伯奥生物科技有限公司,批号:20130305);聚乙二醇6000(PEG6000,四川瀚华药用辅料公司,批号:1201121);奎二酸二丁酯(DBS,国药集团化学试剂有限公司);DVS缓释胶囊(自制,批号:20130601、20130602、20130603,规格:每粒50 mg);其余试剂均为分析纯。
2 方法与结果
2.1 DVS缓释微丸胶囊的制备
2.1.1 DVS微丸的制备 采用醇溶上药法制备DVS微丸。首先将PVP K30和NaCl完全溶解于去离子乙醇中,在搅拌条件下,将DVS溶于乙醇溶液中。蔗糖丸芯作为空白载体,采用Mini-Glatt型流化床底喷装置将乙醇溶液包裹至空白蔗糖丸芯表面[11-12]。制备DVS微丸的处方:空白蔗糖丸芯200 g,DVS 77 g,PVP K30 100 g,NaCl 1.8 g,95%乙醇2 000 ml。DVS微丸的工艺参数:进风容积75~100 m3/h,进风温度55℃,物料温度45~60℃,喷雾压力2.2 bar,插入喷嘴直径1.2 mm,流速2.5 ml/min。
2.1.2 DVS缓释微丸胶囊的制备 将PEG6000和HPMC分别加入去离子水中,搅拌使其完全溶解。将EC加入乙醇中,静置过夜使其完全溶解。然后在搅拌条件下,将水溶液加入乙醇溶液中,搅拌至呈澄清的乙醇水溶液。在搅拌条件下,将DBS加入乙醇水溶液中,搅拌4 h。采用Mini-Glatt型流化床底喷装置将乙醇水溶液均匀包裹至DVS微丸表面,制得DVS缓释微丸。流化床中干燥,然后置于肠溶空心胶囊中,制得DVS缓释微丸胶囊[11-12]。制备DVS缓释微丸的处方:DVS微丸350 g,EC 20 g,PEG6000 5 g,HPMC 50 g,DBS 3 ml,乙醇800 ml,去离子水100 ml。DVS缓释微丸的工艺参数:进风容积90~110 m3/h,进风温度50℃,物料温度35~45℃,喷雾压力2.0 bar,插入喷嘴直径1.2 mm,流速2.5 ml/min。
2.2 方法学考察
2.2.1 标准曲线的绘制 精密称取DVS对照品20.0 mg,置于100 ml量瓶中,加入适量的0.9%NaCl溶液溶解并定容至刻度,摇匀后作为贮备液。分别精密量取适量贮备液,加入0.9% NaCl溶液,制成含DVS分别为10、20、40、60、80、100 μg/ml的对照品溶液,在282 nm波长处检测吸光度(A)。以A对质量浓度(c)进行线性回归,得回归方程为A=0.009 4c+0.007 7(r=0.998)。结果表明,DVS检测质量浓度的线性范围为10~100 μg/ml。
2.2.2 回收率试验 精密称取DVS原料药适量(约相当于DVS标示量的50%、80%、100%)各3份,按“2.1”项下方法制成缓释微丸,加入适量的0.9%NaCl溶液稀释后,于282 nm波长处测定吸光度,根据回归方程计算得相应质量浓度,再计算低、中、高质量浓度供试品的平均回收率分别为100.24%、99.55%、100.89%,RSD分别为1.25%、1.05%、1.33%(n=3)。
2.2.3 稳定性试验 按“2.1.2”项下方法制备DVS缓释微丸,加入0.9%NaCl溶液稀释后,放置0、2、4、6、8、12、24 h测定吸光度。结果显示,吸光度的RSD=0.73%(n=7)。
2.2.4 精密度考察 精密量取适量“2.2.1”项下的DVS对照品贮备液于量瓶中,分别稀释成低、中、高质量浓度(40、50、60 μg/ml)的对照品溶液,于282 nm波长处测定吸光度。同日内测定6次,考察日内精密度;每天1次,连续测定6 d。考察日间精密度。结果显示,低、中、高质量浓度对照品溶液吸光度的日内RSD分别为0.77%、0.82%、0.46%(n=6),日间RSD分别为1.07%、0.82%、0.94%(n=6)。
2.3 药物含量测定
取DVS微丸研细,精密称取适量(约相当于DVS 5 mg),置于100 ml量瓶中,加少0.9%NaCl溶液,超声20 min,冷却至室温,再加0.9%NaCl溶液释至刻度,摇匀后水系滤膜过滤。取续滤液适量,于282 nm波长处测定吸光度,根据回归方程计算DVS微丸中DVS的含量。
2.4 DVS微丸的质量评价及粉体学性质的研究[13]
2.4.1 含量均匀度 分别称取10批次的DVS微丸适量,按“2.3”项下方法测定微丸中DVS的含量,考察微丸的含量均匀性。结果显示,10批次样品DVS的含量分别为19.62%、19.54%、19.66%、19.52%、19.44%、19.70%、19.44%、19.66%、19.41%、19.60%,平均含量为19.56%,RSD=0.53%(n=10)。结果表明主药含量均匀度较好。
2.4.2 上药率 上药率是指微丸中实际药物含量与理论含量的比值。根据含量均匀度检测结果可知,上药丸心实际药物含量为19.56%。按照“2.1.1”项下方法制备得到上药微丸370 g,计算DVS含量=370×19.56%=72.4 g,上药率=上药量/处方量×100%=72.4/77×100%=94%。结果表明DVS微丸上药率高、药物损失量小。
2.4.3 堆密度 称取一定质量(m)的微丸,置于100 ml量筒内,上下振动至体积不再发生变化,测定其体积(V),测定3次。按堆密度(d)=m/V计算,结果d=0.792 1 g/ml(n=3)。
2.4.4 圆整度 将一定数量的微丸置一平板上,将平板一侧抬起,测量在微丸开始滚动前倾斜平面与水平面的夹角,即为圆整度(φ)。φ越小,微丸的圆整度越好。结果,微丸的φ=7.84°(n=3)。
2.4.5 流动性 休止角(α)大小可反映微丸的流动性,同时又可间接反映其圆整度。采用固定漏斗法,微丸自漏斗上自由落下,在半径为r的圆盘上形成堆集体,测定堆集体的高度(h),α=arctan h/r。α≤30°为自由流动,α越小,流动性越好。结果,微丸的α平均值为21.3°(n=3)。
综上可见,DVS微丸圆整性和流动性都较好,可用于包衣。通过扫描电镜观察优化处方后制得的缓释微丸的表面形态,可见DVS微丸和DVS缓释微丸的膜表面光洁,有散在分布的小孔。DVS微丸和DVS缓释微丸的电镜扫描图见图1。

图1 DVS微丸和DVS缓释微丸的电镜扫描图Fig 1 Electron microscope scanning of DVS pellet and DVS sustained-release pellet
2.5 体外释放试验
取DVS缓释微丸,采用转篮法测定,以0.9%NaCl溶液900 ml为释放介质,转速为100 r/min。经1、2、4、6、8、10、12、18、24 h分别取释放液10 ml,同时补加等量释放介质,释放液经水系滤膜过滤,取适量续滤液作为供试品溶液。精密称取DVS对照品适量,加0.9%NaCl溶液制成质量浓度为50µg/ml的溶液,作为对照品溶液。取上述溶液在282 nm波长处测定吸光度,计算累积释放度。
2.6 热处理时间对DVS缓释微丸胶囊体外释药的影响
在60℃恒温箱中,将DVS缓释微丸分别放置1、2、4、6、8、10、12 h后取出,按“2.5”项下方法进行体外释放试验,测定吸光度,计算累积释放度,绘制释放曲线。结果显示,热处理不同时间对DVS缓释微丸的累积释放度无明显影响(P>0.05),因此,流化床中的干燥时间选择1 h。热处理不同时间对DVS缓释微丸释药的影响见图2。
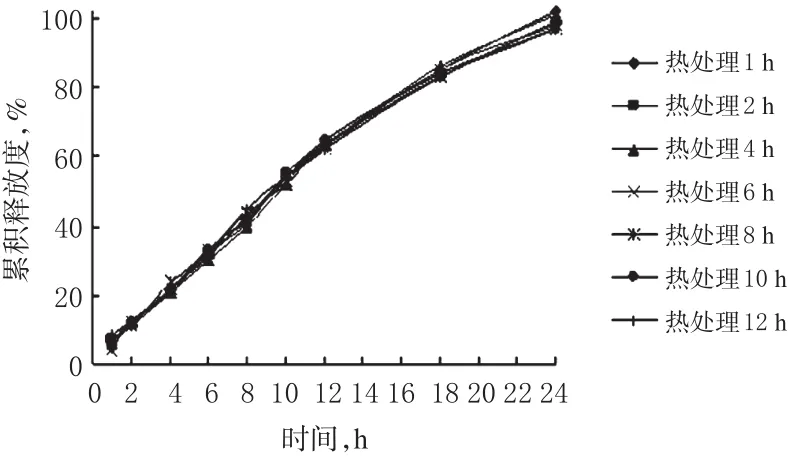
图2 热处理不同时间对DVS缓释微丸释药的影响Fig 2 Effects of drying time on drug release of DVS sustained-release pellets
2.7 模拟胃酸对DVS缓释微丸体外释药的影响
在开始体外释放试验前,分别将DVS缓释微丸于人工胃液(0.1 mol/L的HCl溶液)中浸泡1、2、3 h,然后再置于900 ml 0.9%NaCl溶液中,按“2.5”项下方法进行体外释放试验。考察其在0.9%NaCl溶液中24 h内的释放行为,分别在1、2、4、6、8、10、12、18、24 h测定吸光度。DVS缓释微丸经人工胃液处理不同时间后的释药曲线见图3。
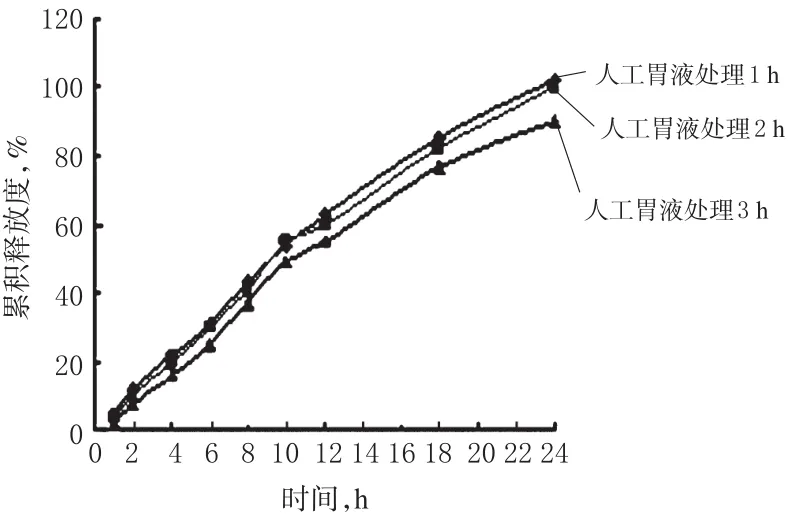
图3 DVS缓释微丸经人工胃液处理不同时间后的释药曲线Fig 3 Release curves of DVS sustained-release pellets after treated with artificial gastric juice for different time
由图3可知,与“2.6”项下热处理1 h的释放曲线比较,DVS缓释微丸在人工胃液中处理1、2、3 h时的累积释放度稍有所下降。常见口服药物在胃中的停留时间为0.5~3 h,为了防止胃液对微丸中药物释放速度和释放量的影响,故将DVS缓释微丸装于肠溶空心胶囊中。
2.8 DVS缓释微丸体外释药机制考察
对DVS缓释微丸的体外释放试验数据分别按照零级、一级和Higuchi释药动力学方程进行拟合,结果表明,DVS缓释微丸的体外释药过程符合一级动力学方程,即药物的释放速率呈浓度依赖性。DVS缓释微丸体外释曲线拟合结果见表1(表中C为累积释放度,t为释放时间)。

表1 DVS缓释微丸体外释曲线拟合结果Tab 1 Fit results of release curves in vitro of DVS sustainedrelease pellets
3 讨论
与片剂等剂型相比较,微丸属于多剂量剂型。制备过程是将一个剂量的药物几乎均匀地分散至上百个微丸,因此,偶有单个微丸的破损不会导致大的释药量的变化。胃空速率等生理因素不易影响微丸的药物释放速率,且微丸能更均匀地分布至胃肠道,故微丸具有良好的疗效重现性[13]。
在处方优化过程中,采用单因素筛选法对EC用量、HPMC用量、PEG6000用量、DBS用量、包衣增质量等因素进行了考察。试验结果表明,增加EC的量会延迟药物从微丸中释放;增加HPMC的量会导致药物初始释放的时间延迟,并且释放速率增加;加入适量PVP K30和PEG6000以控制并调节释药速率,其用量越大,药物从微丸中释放的速率越快;增塑剂DBS经4 h搅拌后包衣膜的稳定性最好;包衣增质量越大,释药速度越慢。最后,综合以上各因素的试验结果,获得最佳处方。
不同热处理时间对DVS缓释微丸中药物释放的影响无显著性差异(P>0.05),说明在包衣过程中药物和高分子聚合物之间无相互作用。
另外也优化了流化床的工艺参数,以无黏连、无静电现象和进液速度快为标准进行优化,筛选了雾化压力、物流温度、进气流量、进风温度以及进液速度等参数,其中雾化压力和物料温度两个参数尤其重要,最后获得本试验的最优工艺参数。
经流化床制得的缓释微丸具有缓释特征。本研究为DVS缓释制剂的制备生产提供了试验基础。
[1] Dennis CL,Dowswell T.Interventions(other than pharmacological,psychosocial or psychological)for treating antenatal depression[J].Cochrane Database Syst Rev,2013,7(7):6 795.
[2] Patten SB,Kennedy SH,Lam RW,et al.Canadian Network for Mood and Anxiety Treatments(CANMAT)clinical guidelines for the management of major depressive disorder in adults.I.classification,burden and principles of management[J].Affect Disord,2009,117(Suppl 1):S5.
[3] 孟江平.抗抑郁新药琥珀酸去甲文拉法辛的研究进展[J].中国药房,2012,23(10):927.
[4] Nichols AI,Fatato P,Shenouda M,et al.The effects of desvenlafaxine and paroxetine on the pharmacokinetics of the cytochrome P450 2D6 substrate desipramine in healthy adults[J].J Clin Pharmacol,2009,49(2):219.
[5] Kamath J,Handratta V.Desvenlafaxine succinate for major depressive disorder:a critical review of the evidence [J].Expert Rev Neurother,2008,8(12):1 787.
[6] Tourian K,Wang Y,Ii Y.A 10-month,open-label evaluation of desvenlafaxine in Japanese outpatients with major depressive disorder[J].Int Clin Psychopharmacol,2013,28(4):2 016.
[7] Liebowitz MR,Tourian KA,Hwang E,et al.A doubleblind,randomized,placebo-controlled study assessing the efficacy and tolerability of desvenlafaxine 10 and 50 mg/day in adult outpatients with major depressive disorder [J].BMC Psychiatry,2013,13(1):94.
[8] Thase ME,Kornstein SG,Germain JM,et al.An integrated analysis of the efficacy of desvenlafaxine compared with placebo in patients with major depressive disorder[J]. CNS Spectr,2009,14(3):144.
[9] Clayton AH,Kornstein SG,Rosas G,et al.An integrated analysis of the safety and tolerability of desvenlafaxine compared with placebo in the treatment of major depressive disorder[J].CNS Spectr,2009,14(4):183.
[10] Nichols AI,Richards LS,Behrle JA,et al.The pharmacokinetics and safety of desvenlafaxine in subjects with chronic renal impairment[J].Int J Clin Pharma Th,2011,49(1):3.
[11] 米丹凤,张志荣,赵越,等.扎托布洛芬缓释胶囊的制备及体外研究[J].四川大学学报:医学版,2010,41(1):166.
[12] 鱼江,封家福,肖隆祥,等.伊拉地平缓释胶囊的制备工艺及体外释药研究[J].药物分析杂志,2015,35(3):512.
[13] 张立超,全山丛,胡晋红,等.阿魏酸钠缓释小丸的制备及体外释药特性[J].中成药,2006,28(10):1 414.
(编辑:邹丽娟)
Study on Preparation of Desvenlafaxine Succinate Sustained-release Pellets Capsules and Drug Release in vitro of Pellets
CHEN Cai,HE Fang,LONG Rui(Dept.of Pharmacy,the First Affiliated Hospital of Chongqing Medical University,Chongqing 400016,China)
OBJECTIVE:To prepare Desvenlafaxine succinate(DVS)sustained-release pellets capsules,and to investigate the release property in vitro of pellets.METHODS:The pellets containing DVS were prepared by alcohol solution.The quality and micromeritics of DVS pellets were studied.Using ethylcellulose(EC)and hydroxypropyl methyl cellulose(HPMC)as coating materials,DVS sustained-release pellets were prepared by fluid-bed,and then put into enteric hollow capsule.The release property in vitro of DVS sustained-release pellets,and the effects of different drying time(1-24 h)and artificial gastric juice on drug release were investigated.RESULTS:DVS pellets and DVS sustained-release pellets were smooth and had scattered ostiole in surface.The content of DVS in DVS pellets was 19.56%(RSD=0.53%,n=10),and drug-loading rate was 94%;bulk density was 0.792 1 g/ ml;roundness degree was 7.84°;angle of repose was 21.3°.There was no statistical significance in the difference of drug release for DVS sustained-release pellets after dried for different time(P>0.05),and accumulative release rate decreased 3 h after treated with artificial gastric juice;the release regularity of DVS sustained-release pellets fitted to first-order kinetic equation.CONCLUSIONS:DVS sustained-release capsules are prepared successfully by this method,and can be not dried during preparation.
Desvenlafaxine succinate;Sustained-release pellet;Fluid-bed coating;Drug release in vitro;Preparation
R943
A
1001-0408(2016)31-4436-04
2016-05-25
2016-07-02)
*药师。研究方向:新药设计与合成、药物新剂型。电话:023-89012410。E-mail:175508404@qq.com
#通信作者:主管药师,博士。研究方向:医院药学。电话:023-89012410。E-mail:lrzj820@aliyun.com
DOI 10.6039/j.issn.1001-0408.2016.31.34

