CuO/AC@SiO2的制备及对H2S的深度脱除
许 芳,朱玉婵,魏少楠,宋 翔,李永清,任占冬
(1.武汉轻工大学 化学与环境工程学院,湖北 武汉 430023;2.海军工程大学 舰船工程系,湖北 武汉 430033)
废气处理
CuO/AC@SiO2的制备及对H2S的深度脱除
许 芳1,朱玉婵1,魏少楠1,宋 翔1,李永清2,任占冬1
(1.武汉轻工大学 化学与环境工程学院,湖北 武汉 430023;2.海军工程大学 舰船工程系,湖北 武汉 430033)
采用模板法在CuO外包裹一层具有介孔结构的SiO2,制备了CuO/AC@SiO2。采用X射线衍射仪对CuO/AC@SiO2的结构和催化活性位点进行了表征。通过固定床气固吸附实验,研究了CuO/AC@SiO2对H2S的吸附脱除性能。表征结果显示,CuO是催化氧化H2S的活性中心,被氧化成Cu2O后吸附脱除H2S的性能下降。实验结果表明:CuO/AC吸附H2S时的有效穿透时间为117 min,CuO/AC@SiO2的有效穿透时间提高到141 min,CuO/AC@ SiO2对H2S的吸附性能明显提高;以Cu(NO3)2为前驱体的CuO/AC@SiO2对H2S的吸附量高于以Cu(AC)2为前驱体;在Cu(NO3)2为前驱体、m(正硅酸乙酯)∶m(CuO/AC)=0.7、吸附温度为90 ℃的最佳条件下,CuO/AC@ SiO2对H2S的吸附量达17.40 mg/g。
硫化氢;CuO/AC@SiO2;介孔结构;有效穿透时间;前驱体;吸附量
众所周知,在许多工业生产过程中都会产生H2S气体。它是一种急性剧毒物质,浓度较高时,直接吸入会致人死亡。H2S在空气中的最高允许质量浓度为10 mg/m3。但在工业生产中,当H2S质量浓度大于3 mg/m3时就会引起管道腐蚀;当H2S质量浓度大于1 mg/m3时会使大多数金属氧化物和金属催化剂发生不可逆的中毒。早期脱除H2S采用克劳斯法,但脱除效果不令人满意。采用活性炭
(AC)、分子筛等多孔材料物理吸附H2S的方法不能完成深度脱除。目前采用最多是过渡金属氧化物催化氧化吸附法,常用的金属氧化物有CuO、ZnO、FeO、MnO2和MgO等[1-8],其脱除效果与氧化物本身的禁带宽度有关,禁带宽度越小,脱除效果越好。CuO的禁带宽度较小,表现出更好的吸附效果[9-15]。以AC、分子筛等多孔材料作为金属氧化物的载体[16-22],一方面可以增加金属氧化物的分散度,提高其利用率;另一方面,多孔材料本身可以依靠表面丰富的孔结构进行物理吸附,拓展其低温吸附H2S的能力[23]。
本工作采用模板法在CuO外包裹一层具有介孔结构的SiO2,从而保护内层的CuO晶体颗粒,减少聚集、覆盖和流失等现象发生。制备了CuO/AC@ SiO2,并通过固定床气-固吸附实验考察CuO/AC@ SiO2对H2S的吸附脱除效果。利用X射线衍射仪对CuO/AC@SiO2的结构和催化活性位点进行了表征。在此基础上进一步考察CuO制备前驱体、正硅酸乙酯(TEOS)用量和吸附温度对吸附脱除效果的影响。
1 实验部分
1.1 试剂和材料
十六烷基三甲基溴化铵(CTAB)、氨水、TEOS、乙醇、氢氧化钾、Cu(NO3)2、Cu(AC)2:均为分析纯。AC:20~40目。H2S标准气体:质量浓度100 mg/m3,N2为平衡气。
1.2 CuO/AC的制备
将AC用蒸馏水洗涤、过滤,置于马弗炉中,400 ℃活化12 h。将活化后的AC用蒸馏水、氢氧化钾溶液洗涤,120 ℃下烘干,备用。取2 g上述AC,加入到12 mL浓度为0.2 mol/L的Cu(NO3)2溶液中,浸渍、搅拌24 h,120 ℃下烘干。再将试样置于马弗炉中,400 ℃氧化2 h,降至室温,用球磨机研细,使其粒径在500~1 000 nm范围内。
1.3 CuO/AC@SiO2的制备
称取0.8 g上述CuO/AC固体粉末加入到装有75 mL乙醇和10 mL蒸馏水的锥形瓶中,再加入0.527 2 g CTAB和7.6 mL氨水(质量分数为25%),密封,室温下磁力搅拌30 min,放慢搅拌速率后逐滴加入0.2~1.0 mL TEOS,使m(TEOS)∶m(CuO/AC)为0.23~1.17,继续搅拌2 h后,过滤并用蒸馏水和乙醇分别洗涤3次,干燥后置于马弗炉中,并以5 ℃/min的升温速度升至400 ℃,煅烧2 h,得到CuO/AC@ SiO2。
1.4 试样的表征
采用Shimadzu公司XRD-7000型X射线衍射仪对试样进行表征,CuKα射线源,管电流30 mA,管电压40 kV,扫描范围2°~10°和30°~90°,扫描速率2~4(°)/min。采用 Shimadzu公司EDX-720型 X射线荧光光谱(XRF)仪分析试样组成。
1.5 吸附性能实验
余额宝社区服务点,其概念来自于美国等西方金融发达国家的“社区银行”,其中的“社区”并不是一个严格界定的地理概念,既可以指一个省、一个市或一个县,也可以指城市或乡村居民的聚居区域。凡是资产规模较小、主要为经营区域内中小企业和居民家庭服务的地方性小型提供购买余额宝购买服务、转出服务以及收益查看服务的服务点都可称为余额宝社区服务点。
固定床气-固吸附实验:将钢瓶中的H2S标准气体与空气通过流量计通入混气室,混合气由底部通入吸附柱,尾气由吸附柱顶部排出,并经碱液吸收后排放。吸附柱直径为6 mm,高度为10 cm。吸附柱内装填0.25 g CuO/AC@SiO2吸附剂,吸附温度控制在30~90 ℃,H2S气体流量为300 mL/min,空气流量为16 mL/min,氧气体积分数为1.1%。采用北京劳保所科技发展有限公司的气体检测器和气体检测管检测H2S含量。吸附过程中有效穿透时间(t,min)的计算是以气体中H2S质量浓度超过5 mg/m3为突破点,吸附量(q,mg/g)(按式(1)计算。

式中:ρ为气体质量浓度,mg/m3;ν为气体流量,mL/min;m为吸附剂质量,g。
2 结果与讨论
2.1 CuO/AC@SiO2的表征
CuO/AC@SiO2的XRD谱图见图1。由图1(a)可见:CuO/AC@SiO2谱线衍射峰的位置与单斜晶系CuO(标准卡05-0661)的晶型结构基本一致;在35.5°和38.7°处的衍射峰对应CuO的(-111)和(111)晶面;在48.8°,53.4°,58.3°,61.5°,66.2°,68.1°处的衍射峰对应CuO的(-202)、(020)、(202)、(-113)、(-311)和(220)晶面;在36.4°处强度较弱的衍射峰对应的是未完全氧化而形成的Cu2O的(111)晶面。
由图1(b)还可以看出,在26.6°,50.1°,59.9°处的衍射峰对应于外层SiO2的(101)、(112)和(211)晶面,可以进一步判断外层SiO2具有介孔材料的特征。通过 Scherrer 公式,对CuO(111)晶面衍射峰进行拟合,计算得到其粒径为9.8 nm。另外,通过 XRF 检测可知,CuO负载量为6.4%(w)。
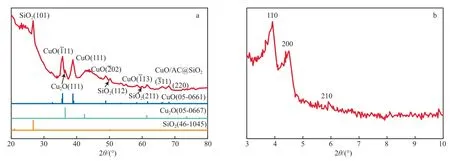
图1 CuO/AC@SiO2的XRD谱图
2.2 CuO/AC@SiO2对H2S的吸附性能
当吸附温度为90 ℃时,CuO/AC@SiO2和CuO/AC对H2S的吸附性能见图2。由图2可见,CuO/AC的有效穿透时间为117 min,而CuO/AC@SiO2的有效穿透时间则提高到141 min,吸附性能明显提高。CuO/AC@SiO2对H2S的吸附量达16.92 mg/g。外层包覆介孔SiO2层可对内层CuO纳米粒子起到保护作用,防止在吸附脱除H2S过程中CuO纳米粒子发生聚集和流失。同时介孔SiO2层具有规则的孔道结构,可以为催化反应传质过程提供合适的通道。
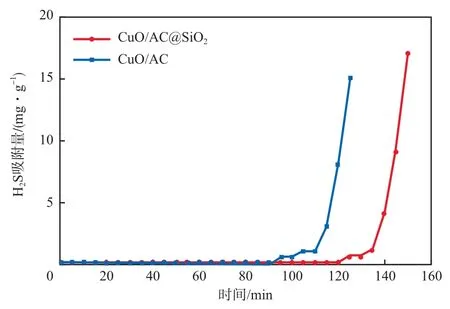
图2 CuO/AC@SiO2和CuO/AC 对H2S的吸附性能
失活前后CuO/AC@SiO2的XRD谱图见图3。由图3可见:失活前后SiO2的衍射峰基本没有发生改变,说明吸附脱除H2S过程中外壳结构保持良好;但在图中方框所标识的区域内,失活后CuO的衍射峰强度明显降低,Cu2O的衍射峰强度明显增加,说明CuO是催化氧化H2S的活性中心,当CuO被还原成Cu2O时吸附性能降低。而这种吸附性能的降低与金属氧化物催化剂禁带宽度有关,文献报道禁带宽度越小,吸附能力越强,氧化反应越容易发生[15]。CuO禁带宽度为1.7 eV,Cu2O禁带宽度为2.2 eV,所以当CuO被部分还原为Cu2O时,吸附脱除H2S的性能下降。另外,CuO是n型半导体,H2S为施电子气体,其氧化吸附会使CuO的费米能级增加,逸出功降低,电导率升高,易于在其表面更进一步吸附。而Cu2O为p型半导体,不利于H2S吸附,使吸附脱除H2S性能降低。
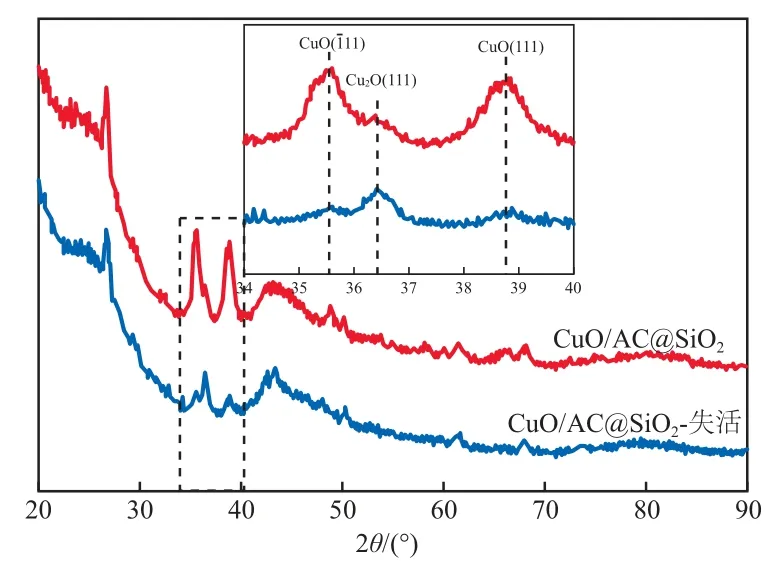
图3 失活前后CuO/AC@SiO2的XRD谱图
分别采用Cu(NO3)2和Cu(AC)2两种前驱体制备CuO/AC@SiO2,在吸附温度为90 ℃时,以Cu(NO3)2为前驱体的CuO/AC@SiO2对H2S的吸附量达18.84 mg/g;而以Cu(AC)2为前驱体的CuO/AC@ SiO2对H2S的吸附量仅为9.00 mg/g。故本实验选择Cu(NO3)2为前驱体较适宜。
不同前驱体吸附剂的XRD谱图见图4。

图4 不同前驱体吸附剂的XRD谱图
由图4可见,以Cu(NO3)2为前驱体时,所制备的氧化物以CuO为主,伴有少量的Cu2O;而以Cu(AC)2为前驱体时,所制备的氧化物以Cu2O为主。如前文所述,CuO比Cu2O具有更好的吸附脱除H2S的能力,所以Cu(NO3)2为前驱体制备的CuO/AC@SiO2吸附脱除H2S的效果更好。
2.4 TEOS加入量的影响
在Cu(NO3)2为前驱体、吸附温度为90 ℃时,TEOS加入量对H2S吸附量的影响见图5。由图5可见:随着TEOS用量的增加,CuO/AC@SiO2对H2S的吸附量先增加后减小;当m(TEOS)∶m(CuO/AC)=0.7时,吸附量最大,达17.40 mg/g。这是因为,当TEOS加入量较小时,形成外壳SiO2层厚度较薄,不能起到保护作用;当TEOS加入量过大时,外壳SiO2层过厚,存在较大的传质阻力,使吸附性能降低。故本实验选择m(TEOS)∶m(CuO/AC)=0.7较适宜。
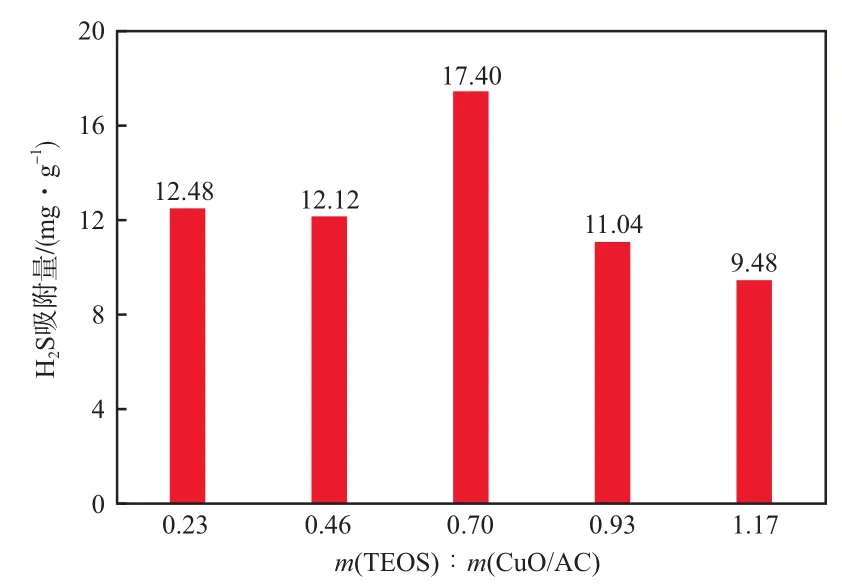
图5 TEOS加入量对H2S吸附量的影响
不同TEOS加入量的CuO/AC@SiO2的XRD谱图见图6。由图6可见:随着TEOS加入量的增加,SiO2的(101)晶面的衍射峰逐渐增强,说明外壳SiO2层厚度增加;而CuO的(-111)晶面和(111)晶面的衍射峰强度和比例基本没有变化,说明外层SiO2层厚度的变化未影响内层CuO颗粒。
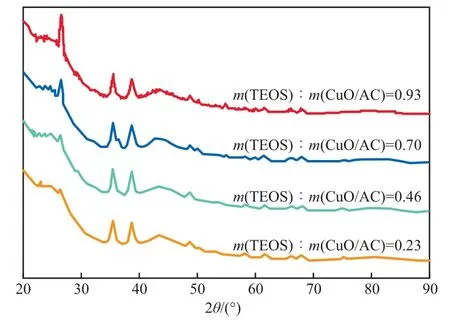
图6 不同TEOS加入量的CuO/AC@SiO2的XRD谱图
2.5 吸附温度的影响
在Cu(NO3)2为前驱体、m(TEOS)∶m(CuO/AC)=0.7的条件下,吸附温度对H2S吸附量的影响见图7。由图7可见:吸附温度为20~60 ℃时,随着吸附温度升高,H2S吸附量逐渐下降,推测在低温范围内主要发生物理吸附,物理吸附是放热反应,温度越高,吸附效果越差;吸附温度高于60℃时,随着吸附温度升高,H2S吸附量明显上升,说明此时发生了化学吸附,化学吸附是一个吸热过程,温度升高有利于提高反应速率,有利于提高吸附效果;当吸附温度升高至90 ℃时,吸附量达17.40 mg/g。故本实验选择吸附温度90 ℃较适宜。

图7 吸附温度对H2S吸附量的影响
3 结论
a)CuO外包裹一层具有介孔结构的SiO2,可保护内层的CuO晶体颗粒,减少聚集、覆盖和流失等。CuO/AC吸附H2S时的有效穿透时间为117 min,CuO/AC@SiO2的有效穿透时间提高到141 min,CuO/AC@SiO2对H2S的吸附性能明显提高。
b)CuO是催化氧化H2S的活性中心,其失活后会被氧化成Cu2O,Cu2O吸附脱除H2S的性能下降。以Cu(NO3)2为前驱体的CuO/AC@SiO2对H2S的吸附量高于以Cu(AC)2为前驱体的CuO/AC@SiO2对H2S的吸附量。
c)在Cu(NO3)2为前驱体、m(TEOS)∶m(CuO/AC)=0.7、吸附温度为90 ℃的最佳条件下,CuO/AC@SiO2对H2S的吸附量达17.40 mg/g。
[1]Fan Huiling,Sun Ting,Zhao Yanpeng,et al.Threedimensionally ordered macroporous iron oxide for removal of H2S at medium temperatures[J].Environ Sci
Technol,2013,47:4859-4865.
[2]连娜,陈树江,田琳,等.菱镁矿浮选尾矿浆液的烟气脱硫性能[J].化工环保,2014,34(1):81-83.
[3]Palma V,Barba D.H2S purification from biogas by direct selective oxidation to sulfur on V2O5-CeO2structured catalysts[J].Fuel,2014,135:99-104.
[4]Wang Xiaohui,Sun Tonghua,Yang Ji,et al.Lowtemperature H2S removal from gas streams with SBA-15 supported ZnO nanoparticles[J].Chem Eng J,2008,142:48-55.
[5]Hong Yong Son,Zhang Z F,Cai Z P,et al.Deactivation kinetics model of H2S removal over mesoporous LaFeO3/MCM-41 sorbent during hot coal gas desulfurization[J].Energy Fuels,2014,28:6012-6018.
[6]Kante K,Nieto-Delgado C,Rangel-Mendez J R,et al.Spent coffee-based activated carbon:Specifi c surface features and their importance for H2S separation process[J].J Hazard Mater,2012,201/202:141-147.
[7]Zheng Xianrong,Bao Weiren,Chang Liping,et al.Interaction among metal components of Zn-Mn-Cubased sorbents prepared by high-pressure impregnation method and its effect on the removal of H2S from hot coal gas[J].Energy Fuels,2012,26:3393-3398.
[8]Mayernick A D,Li R,Dooley K M,et al.Energetics and mechanism for H2S adsorption by ceria-lanthanide mixed oxides:Implications for the desulfurization of biomass gasifi er effl uents[J].J Phys Chem C,2011,115:24178-24188.
[9]Rodriguez J A,Maiti A.Adsorption and decomposition of H2S on MgO(100),NiMgO(100),and ZnO(0001)surfaces:A fi rst-principles density functional study[J].J Phys Chem B,2000,104:3630-3638.
[10]Nguyen-Thanh D,Bandosz T J.Activated carbons with metal containing bentonite binders as adsorbents of hydrogen sulfi de[J].Carbon,2005,43:359-367.
[11]Micoli L,Bagnasco G,Turco M.H2S removal from biogas for fuelling MCFCs:New adsorbing materials[J].Int J Hydrogen Energ,2014,39:1783-1787.
[12]Rezaei S,Tavana A,Sawada J A,et al.Novel copperexchanged titanosilicate adsorbent for low temperature H2S removal[J].Ind Eng Chem Res,2012,51:12430-12434.
[13]Skrzypski J,Bezverkhyy I,Heintz O,et al.Low temperature H2S removal with metal-doped nanostructure ZnO sorbents:Study of the origin of enhanced reactivity in Cu-containing materials[J].Ind Eng Chem Res,2011,50:5714-5722.
[14]Seema P,Behler J,Marx D.Adsorption of methanethiolate and atomic sulfur at the Cu(111)surface:A computational study[J].J Phys Chem C,2013,117:337-348.
[15]Ozaydin Z,Yasyerli S,Dogu G.Synthesis and activity comparison of copper-incorporated MCM-41-type sorbents prepared by one-pot and impregnation procedures for H2S removal[J].Ind Eng Chem Res,2008,47:1035-1042.
[16]闫春燕,伊文涛,李法强.TiO2/AC复合催化剂光催化降解布洛芬[J].化工环保,2014,34(3):281 -286.
[17]Ren Zhandong,Quan Shanshan,Zhu Yuchan,et al.Purifi cation of yellow phosphorus tail gas for the removal of PH3on the spot with fl ower-shaped CuO/AC[J].RSC Adv,2015(5):29734-29740.
[18]Wang Jiancheng,Qiu Biao,Han Lina,et al.Effect of precursor and preparation method on manganese based activated carbon sorbents for removing H2S from hot coal gas[J].J Hazard Mater,2012,213/214:184-192.
[19]Nguyen-Thanh D,Bandosz T J.Activated carbons with metal containing bentonite binders as adsorbents of hydrogen sulfi de[J].Carbon,2005,43:359-367.
[20]Wang Xueqian,Wang Fei,Chen Wei,et al.Adsorption of carbon disulfide on Cu/CoSPc/Ce modified activated carbon under microtherm and micro-oxygen conditions[J].Ind Eng Chem Res,2014,53:13626-13634.
[21]Sakanishi K,Wu Zhiheng,Matsumura A,et al.Simultaneous removal of H2S and COS using activated carbons and their supported catalysts[J].Catal Today,2005,104:94-100.
[22]Ikenaga N,Ohgaito Y,Matsushima H,et al.Preparation of zinc ferrite in the presence of carbon material and its application to hot-gas cleaning[J].Fuel,2004,83:661-669.
[23]Bagreeva A,Katikanenib S,Parabb S,et al.Desulfurization of digester gas:Prediction of activated carbon bed performance at low concentrations of hydrogen sulfi de[J].Catal Today,2005,99:329-337.
(编辑 祖国红)
Preparation of CuO/AC@SiO2and deep removal of H2S
Xu Fang1,Zhu Yuchan1,Wei Shaonan1,Song Xiang1,Li Yongqing2,Ren Zhandong1
(1.School of Chemistry and Environmental Engineering,Wuhan Polytechnic University,Wuhan Hubei 430023,China;2.Department of Warship Engineering,Naval University of Engineering,Wuhan Hubei 430033,China.)
CuO/AC@SiO2was prepared by coating a layer of mesoporous SiO2on CuO with template method.The structure and catalytic active site of CuO/AC@SiO2were characterized by XRD.The adsorption capability of CuO/AC@ SiO2to H2S was studied by gas-solid adsorption experiment in fi xed bed reactor.The characterization results indicate that CuO is the active center for H2S catalytic oxidation,and when CuO is reduced to Cu2O,the H2S removal effect is decreased.The experimental results show that:The effective penetration time of CuO/AC and CuO/AC@SiO2is 117min and 141min respectively,so the adsorption capability of CuO/AC@SiO2to H2S is obviously improved;The adsorption capacity of CuO/AC@SiO2using Cu(NO3)2as precursor is higher than that using Cu(AC)2;Under the optimum conditions of using Cu(NO3)2as precursor,m(tetraethyl orthosilicate)∶m(CuO/AC)=0.7 and adsorption temperature 90 ℃,the H2S adsorption capacity of CuO/AC@SiO2is 17.40 mg/g.
hydrogen sulfide;CuO/AC@SiO2;mesoporous structure;effective penetration time;precursor;adsorption capacity
TQ 126.316
A
1006-1878(2016)02-0200-05
10.3969/j.issn.1006-1878.2016.02.015
2015-10-14;
2015-11-20。
许芳(1979—),女,湖北省广济市人,硕士,实验师,电话 15071021315,电邮 x5460f@163.com。联系人:任占冬,电话 18986001481,电邮 renzhandong@163.com。
湖北省自然科学基金项目(2012FFB04803);武汉轻工大学科研项目(2012Y05)。

