阿片类药物在癌痛治疗的剂量滴定与转换
王术江综述,李伟彦审校
·综 述·
阿片类药物在癌痛治疗的剂量滴定与转换
王术江综述,李伟彦审校
疼痛是恶性肿瘤常见的并发症之一,严重影响患者的生活质量,阿片类药物是临床治疗癌痛的首选药物,因个体差异,常需进行剂量滴定与转换才能维持在疗效和安全性上获得最佳。
阿片类药物;剂量滴定;转换
癌痛是肿瘤患者最常见的主要症状,尤其是中晚期的肿瘤患者,从生理、心理、精神等多个方面严重影响患者的生活质量。癌痛是一种复杂的疼痛,其疼痛具有持续时间长,进行性加重且个体化差异大等特点,每个患者对疼痛的耐受程度及病情的不同阶段都不尽相同。癌痛因为对患者的影响大,已引起广泛重视,随着治疗新药的推出及治疗手段的多样化,癌痛已经得到及时、有效的控制。世界卫生组织(WHO)在1986年提出了简单有效的三阶梯止痛方法,经过检验实践,这种方法已经得到了一致认可,阿片类药物是目前治疗癌痛的普遍手段。WHO在2000年提出“对于中重度癌痛患者,阿片类止痛药具有无可取代的地位”[1-3]。采用阿片类药物相对其他药物治疗癌痛具有诸多优势:① 可以充分、迅速地对疼痛进行控制;② 可以确定药物合理治疗的剂量;③ 可以确保不同阿片类药物间及剂型转换的平稳过渡;④ 可以全程掌握患者疼痛的解救量;⑤ 其品种多、止痛作用强、器官毒性作用小,用药量无“天花板效应”。由于阿片类药物的使用存在较大的个体差异,故常需进行剂量滴定,获得最佳的用药剂量,并及时有效的转换以维持达到止痛的最大能效。阿片类药物的剂量滴定主要指征:① 未满意控制的中、重度癌痛;② 未用过阿片类药物的患者;③ 经弱阿片药物治疗失败的患者;④ 正在服用强阿片药物的患者;⑤ 剧烈疼痛患者。只有规范化的处理疼痛,才能持续有效地缓解疼痛,最大限度的减轻患者的心理负担,控制患者的躯体症状(药物不良反应),最大限度地提高生活质量。本文对阿片类药物常用及最新的药物剂量滴定及转换作综述如下。
1 阿片类药物的剂量滴定
肿瘤患者的镇痛需要个体化治疗,根据不同患者的疼痛程度以及药物的不同剂量,先行剂量滴定,快速获知满意镇痛日需阿片的剂量。通常用短效阿片类药物短时间内有效控制疼痛,并计算出前24 h内用药的总量,转换成等效剂量的控缓释片,以维系患者的镇痛治疗,使镇痛的疗效与患者的个体耐受达到最佳的平衡。目前国内外临床实践中常用的几种阿片类药物的剂量滴定如下。
1.1 吗啡滴定 吗啡是WHO推荐的强激动药代表药物,《美国国立综合癌症网络(NCCN)成人癌痛指南》、《欧洲姑息治疗学会阿片类药物癌痛治疗指南》,以及我国的《癌症疼痛诊疗规范》在关于癌症疼痛滴定的细则中,均把吗啡作为既往未使用过阿片类药物患者的标准初始治疗药物。作为中重度癌痛的首选药物,有无创、简单、价格低、安全可靠、止痛效果确切、快速缓解疼痛等优势,广泛应用于临床疼痛的治疗,可使85%的中重度慢性疼痛得以缓解。吗啡要通过静脉、皮下、口服途径给药。吗啡主要分即释和控缓释制剂两种。一是即释吗啡,主要的滴定方案是:第一天固定量=吗啡控释片5~10 mg,每4 h口服一次;解救量=2.5~5 mg,每2~4 h根据疼痛评估口服。第二天总固定量=前日总固定+前日总解救量(总固定量分6次口服,即每4 h口服);解救量=当日总固定量的10%。依法逐日调整剂量至疼痛≤3分,改用等效剂量控释吗啡。既往对于癌痛患者首先要即释吗啡口服治疗,近几年,人们对阿片类药物的认识渐深及认同其治疗的效果,一些新的治疗手段及药物开始用于癌痛患者的滴定,比如美国的NCCN《成人癌痛治疗指南》推荐使用静脉或皮下途径对患者进行药物滴定,特别是无法吞咽或有阿片类药物肠道吸收障碍的患者[4]。曾有人研究显示,静脉吗啡滴定较口服吗啡起效更快,能安全有效地为癌痛患者提供快速的解救治疗,但不良反应基本相当。即释吗啡也有一些不足:比如中、重度疼痛控制稳定时往往滴定周期较多,往往需要3个周期以上,对患者的评估及药物的换算过于频繁,对患者的依从性和医护人员的工作量受影响。第二种控释吗啡,口服等时等量释放, 反复给药无药物蓄积作用,不受食物、pH、胃肠蠕动影响,持续时间8~12 h,给药间隔时间绝不能<8 h。滴定方案:第一天滴定,固定量=吗啡控释片10~30 mg,每12 h口服一次,解救量=吗啡即释片2.5~5 mg,每2~4 h根据疼痛评估口服一次。第二天滴定,总固定量=前日总固定量+前日总解救量(总固定量分2次口服,即每12 h),解救量=当日总固定量的10%。依法逐日调整剂量至疼痛≤3分,Klepstad等[5]则比较了等量的即释吗啡与控释吗啡在轻中度癌痛患者的疗效差别。结果显示:两者治疗效果总体差异无统计学意义,但控释吗啡能够更快地滴定此类患者。短效阿片类药物的代表即释吗啡,基本上可以使疼痛在48 h内缓解,它的口服剂型每4 h给药的滴定方式是以其药代动力学创立的,目的是通过剂量滴定探索,简化疼痛效果评估和加快剂量的调整。目前无论国内还是国外都沿用了这一初始滴定的方法,美国NCCN采用的静脉或口服吗啡按需给药的方式进行初始剂量滴定。是选择“按时给药”还是“按需给药”来达到治疗癌痛的最佳效果,目前来说无统一定论,有待下一步的临床试验研究。吗啡在镇痛的同时可对肿瘤细胞的生长和转移产生影响,其机制可能与抑制自然杀伤细胞活性等有关[6]。WHO已将医疗用吗啡的消耗量作为衡量一个国家治疗癌症疼痛水平的标准之一,发达国家人均消耗吗啡量为22.2 mg,发展中国家人均消耗量为0.337 mg,我国人均消耗仅0.13 mg[7]。
1.2 芬太尼滴定 芬太尼也是强阿片类药物代表药物,它的临床应用有多种剂型,透皮贴剂(多瑞吉)是癌痛治疗中最常用的芬太尼制剂,主要用于对阿片类药物耐受的慢性癌痛,并且短效的阿片类药物对癌痛控制良好,对不稳定的经常需要剂量调整的癌痛不建议使用。作为透皮吸收的贴剂,可同时透过血脑屏障。而且肿瘤患者常合并肝、肾功能不全,对此类患者的止痛效果确切,对肝、肾功能影响小,长期用药无蓄积。常用的芬太尼透皮贴剂的滴定方案。第一天:固定量=芬太尼透皮贴剂25 μg/h贴皮同时口服即释吗啡10 mg 每4 h×2次,解救量=吗啡即释片2.5~5 mg,每2~4 h根据疼痛评估口服一次。第4天(72 h后),第二贴=第一贴剂量+日解救量×1/2,解救量=当日固定量的10%。NCCN成人癌痛指南(2015.V2)指出:从口服吗啡换用芬太尼透皮贴剂的比例:2 mg/d口服吗啡=1 μg/h芬太尼透皮贴剂(但不适用于芬太尼透皮贴剂换用口服吗啡)。文献资料分析芬太尼透皮贴剂使用显示:与吗啡口服缓释剂相比,芬太尼透皮贴剂便秘等不良反应的发生率更低,对改善患者躯体功能,减少患者负面情绪,提高患者的生活质量更有优势,无创及不良反应发生率低,患者更加偏好选择芬太尼透皮贴剂。卫生部2007年8月颁布的《麻醉药品和精神药品规范化临床应用和管理》指出若患者有吞咽困难、严重呕吐或胃肠梗阻,可以首选芬太尼透皮贴剂或其它直肠栓剂等。而国外最新研发的芬太尼制剂是应用于爆发痛,如即释剂型芬太转化黏液型,主要包括口腔含片、贴片、舌下含片,鼻腔喷剂,尤其适合爆发痛,作用时间短而迅速,一般不推荐用于阿片类药物未耐受患者。
1.3 羟考酮滴定 羟考酮也是一种强阿片激动剂,其缓释制剂作为口服制剂,是国内三阶梯治疗最常用的用药,是临床中、重度癌痛的一线药物。为u受体特异性配体,伴有部分k受体激动剂,由于其对多种阿片受体都有活性,故对神经性癌痛是非常好的选择,而吗啡则不能。羟考酮生物利用度比吗啡高,镇痛效果是吗啡同等剂量的1.5倍,具有镇痛疗效好,不良反应小,作用时间长等优势,与控缓释吗啡具有相似的效应和便捷,而且受年龄、肾功能的影响较小尤其是老年人更安全。羟考酮同样分即释和缓释制剂两种,临床中一般应用缓释制剂,Salzman等[8]分析关于羟考酮缓释片及即释片在癌痛滴定中的研究发现,即释和缓释羟考酮在癌痛滴定中没有差别,两者均具有良好的镇痛作用。而羟考酮缓释片有缓释和速释的兼容作用,即释部分服用后迅速释放而发挥止痛的作用,缓释部分平稳释放后,发挥镇痛的稳定作用,这样减少了患者的服用次数,也有利于患者服药的依从性,而且使用方便,简单易掌握。缓释羟考酮的滴定方案,第一天:固定量=羟考酮缓释片5~15 mg 每12 h口服一次,解救量=吗啡即释片 2.5~5 mg, 每2~4 h根据疼痛评估口服一次。第二天:总固定量=前日总固定量+前日总解救量的10%。
1.4 替利定滴定 替利定是最新研发的人工合成的强阿片类药,该药在欧美国家已经广泛应用,在中国刚起步,其本身不具镇痛作用,通过肝脏代谢为去甲替利定。去甲替利定是阿片u受体的特异激动剂[9],后者进一步代谢成非活性代谢物双去甲替利定,最后以代谢物从肾脏排泄。替利定主要的优势是起效快,10 min就可起效,而且镇痛效果与吗啡相当,每50 mg替利定与10 mg吗啡的镇痛效果等效,但安全性比吗啡高,产生身体依赖性的潜力远低于等剂量的吗啡,产生精神依赖性的潜力与等剂量的吗啡相当[10]。主要的滴定方案是:第一天固定量=替利定50~100 mg,每4 h口服一次;解救量=25~50 mg,每4~6 h根据疼痛评估口服一次。第2天总固定量=前日总固定量+前日总解救量(总固定量分4次口服,即每6 h),解救量=当日总固定量的10%。依法逐日调整剂量至疼痛≤3分,改用等效剂量控释阿片。近几年,替利定的世界临床医疗用量的增加趋势大大超过其他各种阿片镇痛药[11]。而国内临床研究及详实的资料还有待一步完善,找到适合国人的药动力学特征以指导临床的合理应用很有必要。
2 阿片类药物滴定后的转换及维持治疗
根据美国食品药物管理局(FDA) 的规定,阿片类药物耐受患者是指服用至少以下剂量药物者:口服吗啡60 mg/d,芬太尼透皮贴剂25 μg/h,羟考酮30 mg/d,口服氢吗啡酮8 mg/d,口服羟吗啡酮25 mg/d,或等效剂量其他阿片类药物,持续1周或更长时间。对于不符合上述阿片类药物耐受定义的患者,阿片类药物剂量未达到上述标准并持续1周或更长时间的患者,仍作为未使用过阿片类药物的患者。不同患者在同等癌痛条件下所需镇痛药物的剂量是不同的,故需要按照一定的方法从小剂量开始逐步增加剂量以尽快控制癌痛,这一过程被称为阿片类药物的初始剂量滴定[12]。初始剂量滴定应根据患者类型和一般情况选择合适剂量,以吗啡为例,口服速释吗啡正常成人初始剂量10 mg,年老体弱者5 mg,静脉或皮下速释吗啡正常成人3mg,年老体弱者2 mg。后续剂量应根据疼痛评估疗效调整,数字评分法 (NRS)疼痛评分增加,剂量增加100%;评分不变,增加50%;NRS4~6分重复上一次剂量(增加25%);NRS1~3分,维持目前有效剂量。当癌痛控制,24 h所需的阿片类药物剂量稳定后,应将短效制剂更换为控缓释制剂进行维持,以控制慢性持续性疼痛。通常在经过2~3个周期后,大多数患者可以取得满意的止痛效果,如果4个周期效果不满意,应重新对疼痛进行全面的评估,调整治疗方案。如将口服滴定改为静脉滴定;考虑特殊疼痛综合征;如有给与辅助镇痛治疗;甚至进行阿片类药物的转换。其理论基础是阿片类药物之间存在作用时效的区别及疗效和不良反应的不完全交叉耐受[13]。为减少毒副作用,并达到最佳的疗效,一些学者建议所用替代药物的初始剂量应低于等效剂量表的预期转换剂量,尽量考虑到等效剂量转化时等效剂量的不同药物间“等效”但不“等毒”。如Ackerman等[14]的一项研究显示,对于65岁以上的患者,口服羟考酮时便秘发生率是芬太尼透皮贴剂的7倍。研究显示,由于个体差异,阿片类药物的生物利用度不同,如硫酸吗啡可达15%~64%,而羟考酮的生物利用度大于50%,故口服硫酸吗啡与羟考酮等效剂量比例可由至少1∶1至2∶1不等[15],而患者口服硫酸吗啡转换为美沙酮的比值也在1∶1到4∶1。在癌性疼痛治疗的初始阶段与维持转换期是不同的[16]。在阿片类药物维持治疗常见的问题主要是:不良反应及晚期合并症控制经验不足;药物转换比较随意,转换剂量不准确;同时使用两种长效阿片药物;剂量调整过于谨慎或盲目追求大剂量等。剂量滴定过程中,没有任何一种阿片类药物适合所有患者,药物的增加剂量以安全的方式进行,在疗效和不良反应的相互平衡中的止痛剂量,改善癌痛患者的舒适度、功能和安全。阿片类药物在使用中应注意:①出现中度以上疼痛应早期应用,用足剂量,经常根据病情调整剂量;②应重视对药物不良反应的预防,根据患者情况选择不良反应少的药物;③疼痛加剧时要增加单次药物剂量,而不要增加给药次数;④接受即释吗啡治疗者可于睡前将剂量加倍,以防痛醒;⑤控释片不可碾碎应用;⑥应用时应有疼痛强度及剂量滴定的记录。常用的阿片类药物的等效剂量转换表[17]见表1。
3 爆发痛的处理及阿片类药物治疗
爆发痛是指患者的基础性疼痛在按时服用阿片类药物得以满意控制时,所出现的短暂而剧烈的疼痛[13]。常是急性加重的疼痛,或与活动、体位等相关,有的出现在给药期间末。
表1 几种阿片类药物等效剂量滴定
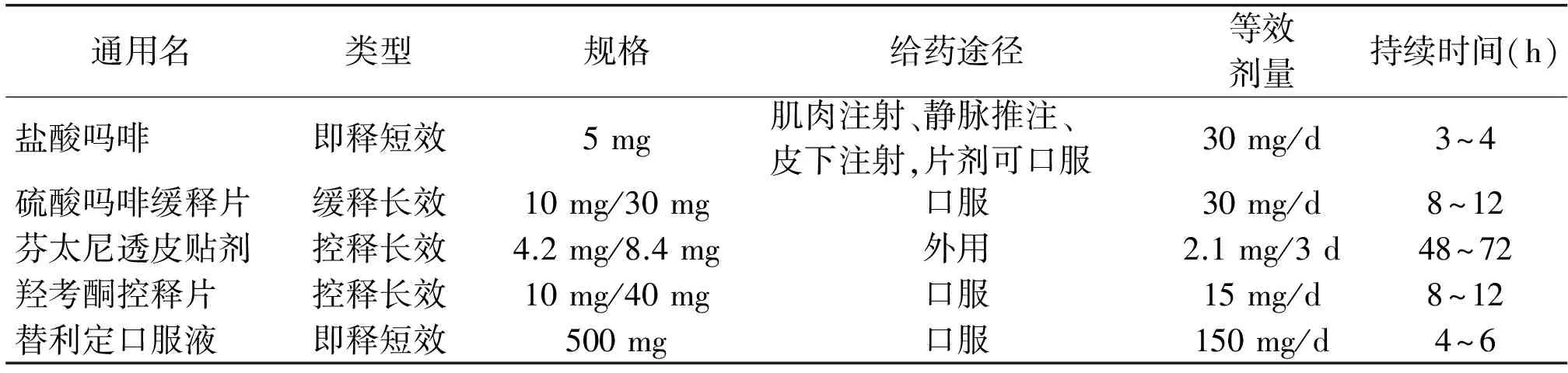
通用名类型规格给药途径等效剂量持续时间(h)极量限制盐酸吗啡即释短效5mg肌肉注射、静脉推注、皮下注射,片剂可口服30mg/d3~4无硫酸吗啡缓释片缓释长效10mg/30mg口服30mg/d8~12无芬太尼透皮贴剂控释长效4.2mg/8.4mg外用2.1mg/3d48~72无羟考酮控释片控释长效10mg/40mg口服15mg/d8~12无替利定口服液即释短效500mg口服150mg/d4~6一般不超600mg
一般可分为3种类型:突发型、自发型和镇痛药物剂量不足型。其会影响患者的睡眠、限制了患者的活动,降低了患者的生存质量。阿片类药物是治疗爆发痛的首选,胃肠道外部的治疗途径是治疗爆发痛很重要的手段,如皮下、静脉、黏膜、患者自控镇痛(PCA)、经皮、介入等。当然要了解痛的类型和性质,对内在的病因要进行直接的治疗,血管堵塞、神经压迫、骨折、感染等可能是内在的病因。短效阿片类药物的解救为24 h口服剂量(mg)的10%~20%,需时每小时给药,如果患者经常需要按需给予阿片类药物,或按时给药的阿片类药物剂量在峰效应或给药结束时无法缓解疼痛,可增加缓释阿片类药物的剂量,尽量选择维持时间长的长效药物。2011年的欧洲肿瘤内科科学会指南提出[18]:如果每天治疗爆发痛在4次以上,推荐背景用药选择缓释剂型的阿片类药物。因此,新的治疗药物、药物剂型及选择新的滴定方式,对于提高治疗的效率,控制癌痛尤其是爆发痛有非常重要的意义。对于爆发痛或者难治性癌痛的患者,无法达到镇痛的效果,按照三阶梯镇痛治疗的原则, PCA、鞘内输注系统给药等都是很好的控制方法。PCA滴定是比较有效的滴定方法[19], 患者的费用明显比对照组低,而且对照组可以明显的降低视觉模拟评分法(VAS)评分[20]。它可以根据患者的疼痛情况及按压的次数,及时调整药物的剂量,使药物维持在一个有效的水平,持续镇痛。但使用相对不便,操作起来比较复杂,尤其是对基层医院,限制了其应用,难以大范围的推广。
疼痛控制是世界性难题,多种因素影响或导致癌痛治疗不足,需要医护人员、患者和社会等多方共同努力。 阿片类镇痛药是目前治疗癌痛的普遍手段,明显提高了患者的生活质量。当然,阿片类药物的滴定也有诸多不良反应,最常见的不良反应有便秘、头晕、恶心、呕吐、嗜睡等。这就要求在临床应用中个体剂量滴定与维持并进,即既能控制癌痛而又无不可接受的不良反应的发生。为确保有效镇痛并使创伤最小,口服给药是阿片类药物最简单和安全的方式。随着新药的研发及治疗手段的多样化,镇痛的效果不断提高,不良反应逐步减少, 多种医学模式多种治疗手段成为癌痛治疗的新方向,即联合使用作用机制不同的镇痛药物或镇痛方法,由于每种药物的剂量减小,不良反应相应降低,镇痛作用相加或协同,从而达到最大的效应。NCCN认为没有任何一种阿片类药物适合所有患者。特殊的难以用单一阿片类药物控制的癌痛,需增加辅助用药,多学科综合治疗。如神经病理性疼痛以阿片类药物为主,合用抗抑郁药或抗惊厥类;无创给药方法不能解决的顽固性、难治性癌痛采用神经阻滞、神经毁损等创伤性疗法。联合用药可以减少强阿片药物的增量;可以减少强阿片药物的剂量;可以减少出现过量给药的风险;增加治疗方案的灵活性。当然,大约有10%的晚期癌症患者无法通过“三阶梯治疗方案”缓解疼痛,或不能忍受长期大剂量镇痛药带来的不良反应[21]。鞘内给药镇痛是全新有效的治疗手段,已为大家所共识,在治疗癌痛尤其是顽固性、难治性癌痛有巨大的潜力,增加了疗效,减少了不良反应。与口服与静脉其他途径相比,具有选择性高和使用剂量小的优点[22]。吗啡目前仍然是鞘内使用镇痛药物的金标准,而且也是目前唯一通过FDA认证的鞘内给药治疗慢性疼痛的药物[23]。而且近年来提倡吗啡滴定的快速镇痛理念。加强对患者和家属的健康宣教,同样至关重要,让患者和家属减少对疾病本身及使用阿片类药物成瘾依赖的担忧和心理负担,提高患者的生活质量。尽管阿片类药物癌痛的治疗已经在临床广泛应用与推广,但仍然存在一些政策法规和医疗机构对阿片类药物的使用存在严格的限制,对癌痛患者的治疗造成了障碍,应逐步放开阿片类药物的使用“禁区”,由过去的“限量供应”改为“按需供应”[24]。患者的一些合理治疗需要更多的临床试验来验证支持,我们鼓励肿瘤患者尽可能的参加临床试验研究,为完善癌痛的规范化治疗做出自己的贡献。
[1] 张 帆,闵 苏.阿片类药物滴定及转换在癌痛治疗中的研究进展[J].国际麻醉学与复苏杂志,2015,36(8):737-740.
[2] 孟 勇,陆文汉,段满林.瑞芬太尼用于心脏手术麻醉的进展[J].医学研究生学报,2010,23(7):779-782.
[3] 王 玲,姜荣荣,刘 云.癌性疼痛的评估与护理[J].医学研究生学报,2011,24(2):221-224.
[4] Mcgivney WT.NCCN:your best resource in the fight against cancer[J].J Natl compr Canc Netw,2015,13(2):125-126.
[5] Klepstad P,Kaasa S,Jystad A,et al.Immediat-orsustained-release,morphine for dose finding during start of morphine to cancer patients:arandomized,double-blindtrial[J].Pain,2003,101(1-2):193-198.
[6] 刘红军,朱红梅,程祝强,等.吗啡和曲马多对MADB乳腺癌细胞增殖和凋亡的影响[J].东南国防医药,2014,16(5):449-452.
[7] 吴庆欢,邱海峰,梁 丹,等.2007年我院癌痛者使用吗啡制剂调查分析 [J].中国医药导报,2008,5(12):105-112.
[8] Salzman RT,Roberts MS,Wild J,et al.Can a controlled-re-lease oral dose form of oxycodone be used as readily as an immediate-release form for the purpose of titrating to stable pain control[J].Pain Symptom Manaye,1999,18(4):271-279.
[9] Therry C,Boeynaems M,Paolom M.Action of tilidine and nortilidine on cloned opiooid receptors[J].Eur J Phamacol,2005,506(3):205-208.
[10]孙 莉,李潇潇,梁军成,等.盐酸替利定口服液用于镇痛的随机双盲对照临床试验[J].中国临床药理学杂志,2013,29(1):6-8.
[11]NCB Trends in the licitmovement of narcotic drugs Narcotic Drugs Estimated world requipments for 2001 [R].United Nations New York 2001.
[12]梁晓华.癌痛镇痛药物的规范应用[J].医药综述,2011,32(12):585-588.
[13]Caraceni A, Hanks G,Kaasa S, et al.Use of opioid analgesics in the treatment of cancer pain:evidence-based recommendations from the EAPC[J].Lancet Oncol,2012,13(2):58-68.
[14]Ackerman SJ,Knight T,Schein J,et al.Risk of constipation in patients presctibed fentanyl transdermal system or oxycodone hydrochloride controlled-release in a California Medicaid population[J].Consult Pharm,2004,19(2):118-132.
[15]Anderson R,Saiers JH,Abram S,et al.Accuracy in equianalgesic dosing.nversion dilemmas[J].J Pain Symptom Manage,2001,21(5):397-406.
[16]Heiskanen T,Kalso E.Controlled-release oxycodone and morphine in cancer related pain[J].Pain,1997,73(1):37-45.
[17]Portenoy RK,Ahmed E.Principles of opioin use in cancer pain[J].J Clin Oncol,2014,32(16):1662-1670.
[18]Ripamonti CI,Bandieri E,Roila F.ESMO Guidelines Working Group.Management of cancer pain: ESMO Clinical Practice Guidelines[J].Ann Oncol,2011,22(6):69-77.
[19]Sato C,Okabe T,Nakanishi K,et al.A case of cancer pain management by long-term intrathecai PCA[J].Nihon Med Sch,2010,77(6):333-337.
[20]Yi-Feng Z,Li-Ming J,Wei-Min M,et al. Percutaneous computed tomography-guided lung biopsy of solitary nodular ground-glass opacity[J].Cancer Res Ther,2015, 11(11):231-233.
[21]何敏琪,吴曙粤.晚期癌症病人镇痛治疗进展 [J]. 广西医学,2011,33(1):95-98.
[22]杨冯睿,倪家骧.鞘内给药治疗疼痛进展 [J]. 疑难病杂志,2012,3(11):232-234.
[23]王 昆.鞘内输注系统治疗顽固性癌痛 [J]. 中国肿瘤临床,2013,40(18):1141-1144.
[24]程 乐,钟进才.阿片类药物应用于中、重度癌痛治疗的研究进展[J]. 广西药学杂志,2009,31(5):742-745.
(本文编辑:黄攸生)
210002江苏南京,南京大学医学院附属金陵医院(南京军区南京总医院)疼痛科
李伟彦,E-mail:weiyanlee@sian.cn
王术江,李伟彦.阿片类药物在癌痛治疗的剂量滴定与转换[J].东南国防医药,2016,18(5):522-526.
R971.2
A
10.3969/j.issn.1672-271X.2016.05.022
2016-02-21;
2016-05-13)

