人尿中6种利尿剂的液相色谱-串联质谱联用检测方法研究
赵君 董颖 张丽娟 闫宽 马艳华
1北京化工大学理学院(北京 100029)2国家体育总局反兴奋剂中心(北京 100029)
人尿中6种利尿剂的液相色谱-串联质谱联用检测方法研究
赵君1董颖2张丽娟1闫宽2马艳华2
1北京化工大学理学院(北京 100029)2国家体育总局反兴奋剂中心(北京 100029)
目的:使用液相色谱-串联质谱联用(LC-MS/MS)技术,为氯拉扎尼(chlorazanil,I)、氯索隆(cicletanine,II)、西氯他宁(chlorxolone,III)、苄氢氯噻嗪(benzylhydrochlorothiazide,IV)、芬喹唑(fenquizone,V)和美替克仑(meticrane,VI)等6种利尿剂建立在人尿中的检测方法并进行方法验证。方法:将尿样用同等体积的5%乙酸铅水溶液沉淀蛋白质并离心后,使用电喷雾电离源的正、负离子切换模式,以多反应监测(MRM)模式进行定性和定量分析。结果:上述利尿剂I-VI的最低检测限(LOD)分别为1、0.1、0.01、1、2和10 ng/mL;线性范围(R2>0.99)分别为3~300 ng/mL、0.3~500 ng/mL、0.03~4000 ng/mL、3~1500 ng/mL、6~600 ng/mL和30~1600 ng/mL;6种药物在低、中和高三个浓度水平的日内变异系数均小于8%,日间变异系数均小于12%,检测的准确度在80%至120%之间;基质效应均在83%~115%范围内。结论:新建方法具有前处理简单、分析速度快、灵敏度高和重现性好等特点,已应用于我们实验室的兴奋剂常规检测中。
液相色谱-串联质谱;利尿剂;方法验证;兴奋剂控制
利尿剂在临床上是一类用于治疗水肿和高血压的药物,其作用是增加尿的排泄量,促使积聚在皮下和腹腔中多余的水分在短时间内大量排出,因此,在竞技体育中利尿剂经常被运动员滥用。一方面,利尿剂的促排尿作用可以迅速减轻运动员体重,使之可以参加低体重级别的比赛;另一方面,利尿剂可以加速排泄或稀释其它禁用物质在尿中的浓度,具有掩蔽剂的作用。利尿剂在1988年汉城奥运会上才正式被列为禁用物质并纳入检测项目。长期或过量使用利尿剂会导致血量下降,引发低血压、休克、肾衰、猝死等,其副作用不容忽视。
张韶虹等[1]对利尿剂的检测方法进行了综述。利尿剂通常使用色谱分析法、化学发光法、荧光分析法、电化学法、分光光度法、胶束色谱分析[2]、液相色谱[3-5]和气相色谱-质谱联用技术进行检测[6]。由于利尿剂种类繁多,化学结构和理化性质差别较大,使用上述的检测方法具有很大的局限性。随着液相色谱-质谱联用技术的不断发展和完善,已有大量文献报道用液相色谱-串联质谱联用(LC-MS/MS)技术检测利尿剂[7-14]。秦旸等[15]建立的液相色谱-单四级质谱联用法可同时筛选人尿中26种利尿剂。马艳华等[16]用LC-MS/MS技术可同时检测120种利尿剂和刺激剂等禁用物质。闫宽等[17]使用液相色谱-串联质谱技术对人尿中3种普坦类兴奋剂进行了检测。
Guddat等[18]报道将尿样稀释后直接进样的方法可快速筛查多种兴奋剂,其中包含氯拉扎尼和美替克仑,检测限分别为5和20 ng/mL,灵敏度明显低于本研究的检测方法。通过查阅文献得知,到目前为止,本研究包含的其它四个利尿剂还没有建立LC-MS/MS检测方法(图1)。

图1 6种利尿剂的化学结构式
1 实验部分
1.1 主要仪器与装置
1290/6460C Triple Quad LC-MS/MS:美国安捷伦公司;氮吹仪:英国Bibby Scientific公司;低速离心机:北京雷勃尔离心机有限公司;感量0.0001 g的电子天平:瑞士Mettler Toledo公司;超纯水机:美国Millipore公司;GENIE VORTEX-2涡旋混合器:美国Scientific Industries公司。
1.2 主要材料与试剂
标准品:氯拉扎尼(Chlorazanil):哥伦比亚Matrix Scientific公司;盐酸西氯他宁(Cicletanine Hydrochloride)、氯索隆(Chlorexolone)、苄氢氯噻嗪(Benzylhydrochlorothiazide)和芬喹唑(Fenquizone):加拿大Toronto Research Chemicals公司;美替克仑(Meticrane)和内标倍可降(Mefruside):美国Sigma-Aldrich公司;色谱纯乙腈和甲醇:美国DIKMA公司;色谱纯甲酸铵:Fluka公司;分析纯乙酸铅:国药集团化学试剂有限公司。
1.3 储备溶液、标准溶液和质控样品溶液的制备
储备溶液:准确称量一定量(1 mg左右)的标准品,用色谱纯甲醇溶液溶解制备成浓度为1 mg/mL的溶液。
标准溶液:将储备液用甲醇倍比稀释至100 μg/ mL、10 μg/mL;1 μg/mL的标准溶液用液相色谱的初始流动相(V水∶V乙腈=85∶15)稀释制备。
质控样品溶液:在空白尿中用标准溶液倍比稀释制备低、中和高3个浓度的质控样品溶液。
1.4 液相色谱条件
Agilent Zorbax XDB-C18色谱柱(100 mm×2.1 mm,3.5 μm);柱温40℃,流动相采用pH 3.5的10 mM甲酸铵缓冲液(A)和乙腈(B);梯度洗脱程序:1~5 min:90%A;5~10 min:50%A;10~15 min:10%A;15~16 min:10%A;柱平衡时间:4 min;流速0.4 mL/min;进样量10
μL。
1.5 质谱条件
电喷雾离子源(ESI),采用正、负离子切换检测模式,多反应监测(MRM)扫描,电喷雾毛细管电压4000 V,离子源温度330℃,干燥器流速10 L/min,雾化气压力35 psi。
1.6 样品前处理
用移液枪量取1 ml尿液,加入1 ml浓度为5%的乙酸铅水溶液(其中含有内标倍可降,浓度为200 ng/ ml),涡旋震荡30秒,离心10分钟(4000 rpm),倒出上清液,取10 μL进样分析。
2 结果与分析
2.1 样品的前处理
兴奋剂控制样品的前处理通常采取液液萃取或固相萃取的方式纯化和富集尿中的待测组分,但这些方法耗时较长,成本较高,如果回收率低,还会影响有效成分的检出。为简化样品的前处理程序,实现高通量、快速的检测目标,本研究采取直接进样的方式简化样品的前处理程序,将尿样中的蛋白质用等体积的5%乙酸铅水溶液沉淀后直接上机进行检测[19]。
2.2 质谱分析
因有些利尿剂的酸性较强,不易质子化,因此本方法使用电喷雾离子源并采取正、负离子切换模式进行数据采集。首先通过全扫描方式优化加速电压,得到每个利尿剂的子离子,再通过优化碰撞能量得到丰度较高的诊断离子,表1中包含了质谱参数和每个利尿剂的3对诊断离子。

表1 6种利尿剂的质谱参数和诊断离子对
2.3 方法验证
根据WADA实验室国际标准和有关技术文件的要求,我们对所建立的方法进行了全面考察和验证,包括每种利尿剂的检测限、定量限、线性范围、日间和日内精密度、准确度、基质效应和方法特异性等。
2.3.1 检测限(LOD)和定量限(LOQ)
检测限和定量限分别显示信噪比为3和10时所对应的药物浓度。在6份不同的空白尿中添加一定浓度的标准品,按照上述1.6描述的方法进行前处理,并上机检测,得到6种药物的检测限(LOD)和定量限(LOQ)(表2)。与WADA技术文件[20]中规定的利尿剂检测能力最低要求(200 ng/mL)相比,本方法的灵敏度远远超出对兴奋剂样品的检测要求。

表2 6种利尿剂色谱保留时间、检测限、定量限和线性范围
2.3.2 线性范围
取10份空白尿,自LOQ开始向上配制系列浓度
的样品,根据上述1.6的描述进行前处理并上机检测,用最小二乘法进行线性回归,测量直至曲线出现弯曲时的浓度,此时相关系数r2应大于0.99(表2)。
2.3.3 方法的精密度和准确度
本验证实验是在低、中和高3个浓度下进行的。在6份空白尿中,分别添加上述3个浓度的标准品,依据1.6的描述进行前处理并上机检测,得出日内精密度。按照日内精密度的操作方法,每天操作一次,共做至少3次,计算得出日间精密度(表3)。
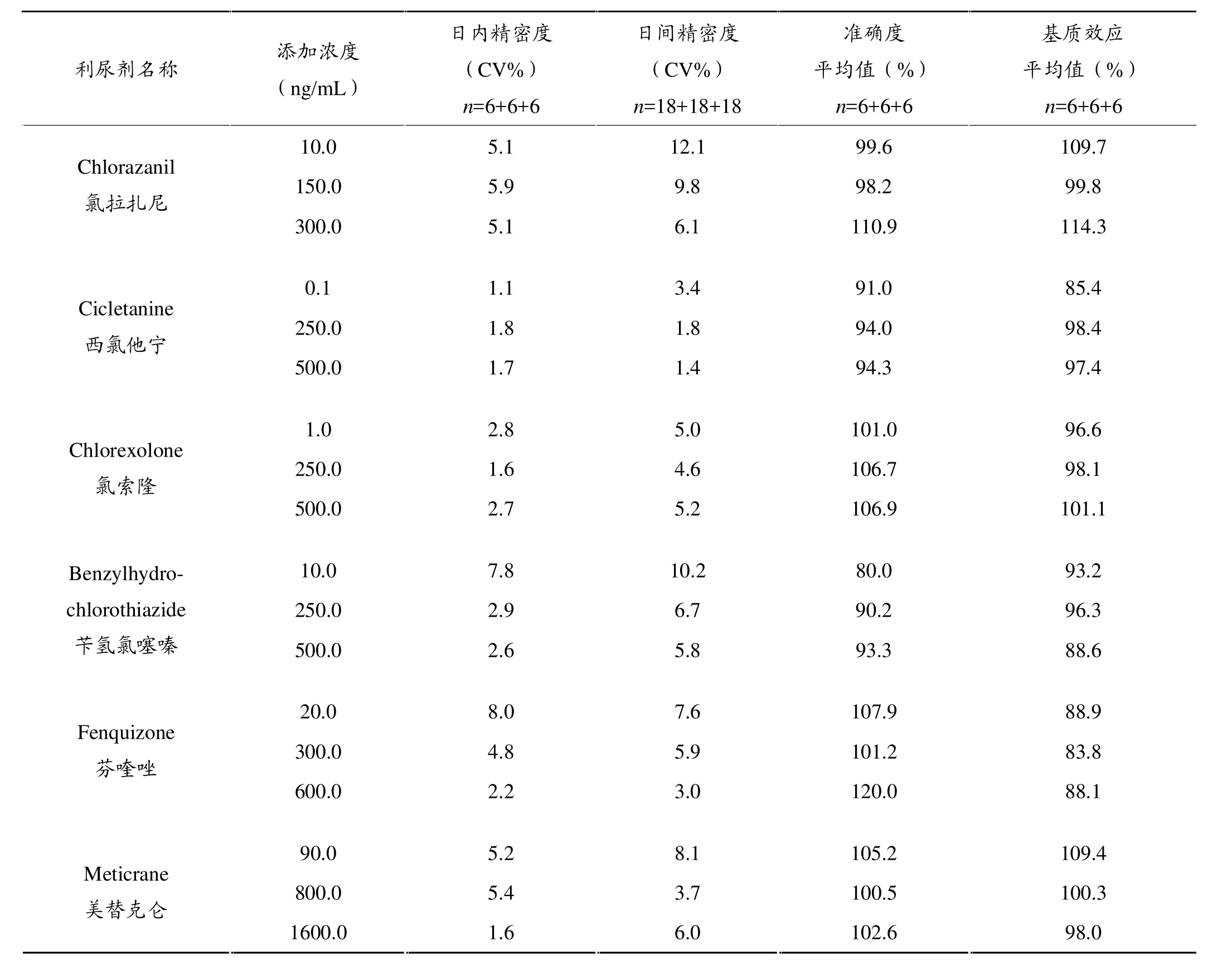
表36 种利尿剂的方法学验证结果
在6份空白尿中,分别添加低、中和高3个浓度级别的标准品,依据1.6的描述进行前处理并上机检测,通过工作曲线计算测量值,与真实值进行比较再乘以百分比,即为准确度(表3)。
实验结果显示6种利尿剂在3个浓度水平下日内变异系数均小于8.0%,日间变异系数均小于12.1%,检测的准确度在80%~120%之间,符合兴奋剂检测实验室常规检测的要求。
2.3.4 基质效应
在6份不同的空白尿中分别添加低、中和高3个浓度的标准品进行基质效应研究。将1 mL空白尿按照上述1.6的描述进行前处理后,在上清液中加入一定浓度的待测物质和内标,上机检测得到峰面积B。同时,将1 mL纯水经过前处理后,在上清液中加入相同浓度的待测物质和内标,上机检测得到峰面积A。基质效应可用下述公式计算:
基质效应=待测物峰面积B/内标峰面积B÷待测物峰面积A/内标峰面积A×100%
实验结果表明6种利尿剂在低、中和高3个浓度下的基质效应均在84%~115%之间(表3),说明该检测方法的基质效应在可接受范围内。
2.3.5 方法特异性
特异性是指在样品介质中有其它组分共存时,检测方法对待测物准确而专属的测定能力。当样品中含
有被分析物时呈阳性反应,不含被分析物时呈阴性反应。必要时,要证明与被分析物结构相似或相近的物质不呈阳性反应。本研究选择50份空白尿样,经前处理并上机检测后,发现尿样中基质对待测离子窗口无影响。
3 总结
本研究建立了高效液相色谱-串联质谱法检测6种利尿剂的方法。该方法具有前处理简单、灵敏度高、线性范围宽、精密度好、特异性强和基质干扰小等特点,能够满足兴奋剂常规样品的检测要求。该方法已经应用于我们实验室的日常检测中。
[1]张韶虹.兴奋剂中利尿剂的检测研究进展.襄樊职业技术学院学报,2005,4(5):99-100.
[2]秦旸,朱绍棠,王超,等.利尿剂的胶束色谱分析.分析测试学报,2002,21(5):85-87.
[3]Woo H,Kim JW,Han KM,et al.Simultaneous analysis of 17 diuretics in dietary supplements by HPLC and LC-MS/MS. Food Addit Contam Part A Chem Anal Control Expo Risk Assess,2013,30(2):209-217.
[4]Ram VR,Dave PN,Joshi HS.Development and validation of a stability-indicatingHPLC assay method for simultaneous determination of spironolactone and furosemide in tablet formulation.J Chromatogr Sci,2012,50(8):721-6.
[5]Belal F,Brashy AM,Enany N,et al.Liquid chromatographic method for the simultaneous determination of eprosartan and hydrochlorothiazide in tablets and human plasma.J AOAC Int,2011,94(3):823-832.
[6]Van Thuyne W,Van Eenoo P,Delbeke FT.Implementation of gas chromatography combined with simultaneously selected ion monitoring and full scan mass spectrometry in doping analysis.J Chromatogr A,2008,12(10):193-202.
[7]HsuKF,ChienKY,Chang-ChienGP,etal.Liquid chromatography-tandem mass spectrometry screening method for the simultaneous detection of stimulants and diuretics in urine.J Anal Toxicol,2011,35(9):665-674.
[8]Mazzarino M,de la Torre X,Botrè F,et al.A rapid screening LC-MS/MS method based on conventional HPLC pumps for the analysis of low molecular weight xenobiotics application to doping control analysis.Drug Test Anal,2010,2(7):311-322.
[9]DeventerK,PozoOJ,VanEenooP,etal.Qualitative detection of diuretics and acidic metabolites of other doping agentsinhumanurinebyhigh-performanceliquid chromatography-tandemmassspectrometry:comparison between liquid-liquid extraction and direct injection.J Chromatogr A,2009,1216(31):5819-5827.
[10]Marchi IRudaz S,Veuthey JL.Sample preparation development and matrix effects evaluation for multianalyte determination in urine.J Pharm Biomed Anal,2009,49(2):459-467.
[11]Mazzarino M,de la Torre X,Botrè F.A screening method for thesimultaneousdetectionofglucocorticoids,diuretics,stimulants,anti-oestrogens,beta-adrenergicdrugsand anabolic steroids in human urine by LC-ESI-MS/MS.Anal Bioanal Chem,2008,392(4):681-698.
[12]Tsai TF,Lee MR.Liquid-phase microextration combined with liquid chromatography-electrospray tandem mass spectrometry for detecting diuretics in urine.Talanta,2008,75(3):658-665.
[13]Thevis M,Schanzer W.Examples of doping control analysis byliquidchromatography-tandemmassspectrometry:ephedrines,beta-receptor blocking agents,diuretics,sympathomimetics,and cross-linked hemoglobins.J Chromatogr Sci,2005,43(1):22-31.
[14]Deventer K,Delbeke FT,Roels K,et al.Screening for 18 diuretics and probenecid in doping analysis by liquid chromatography-tandem mass spectrometry.Biomed Chromatogr,2002,16(8):529-535.
[15]秦旸,徐友宣,吴侔天.液相色谱-质谱法快速筛选人尿中26种利尿剂.质谱学报,2007,28(4):229-232.
[16]马艳华,闫宽,董颖.液相色谱-动态串联质谱技术同时检测人尿中120种刺激剂和利尿剂等禁用物质.中国运动医学杂志,2016,35(5):461-467,472.
[17]闫宽,马艳华,董颖,等.用液相色谱-串联质谱法检测人尿中三种普坦类兴奋剂控制药物.中国运动医学杂志,2015,33(10):989-992.
[18]Guddat S,Solymos E,Orlovius A,et al.High-throughput screening for various classes of doping agents using a new‘dilute-and-shoot’liquid chromatography-tandem massspectrometry multi-target approach.Drug Test Anal,2011,3:836-850.
[19]Dong Y,Yan K,Ma Y,et al.A sensitive dilute-and-shoot approach for the simultaneous screening of 71 stimulantsand 7 metabolites in human urine by LC–MS-MS with dynamic MRM.J Chromatogr Sci,2015,53(9):1528-1535.
[20]World Anti-Doping Agency:WADA Technical Document. http://www.wada-ama.org.
Development and Validation of a LC-MS/MS Method for the Detection of Six Diuretics in Human Urine
Zhao Jun1,Dong Ying2,Zhang Lijuan1,Yan Kuan2,Ma Yanhua2
1 Faculty of Sciences,Beijing University of Chemical Technology,Beijing 100029,China 2 National Anti-Doping Laboratory,China Anti-Doping Agency,Beijing 100029,China Corresponding Author:Dong Ying,Email:dongying@chinada.cn Zhang Lijuan,Email:dazlj@mail.buct.edu.cn
ObjectiveTo develop and validate a LC-MS/MS method for the detection of 6 diuretics including chlorazanil(I),cicletanine(II),chlorxolone(III),benzylhydrochlorothiazide(IV),fenquizone(V)and meticrane(VI).Method An equivalent volume of 5%PbAc2aqueous solution was applied to precipitate the proteins in urine samples.The supernatant was directly introduced into the LC-MS/MS system using electrospray ionization in negative-to-positive switch mode.Results The limit of detections(LODs)for the above described diuretics I-VI were 1,0.1,0.01,1,2 and 10 ng/mL respectively.The assays were linear over the concentration ranges of 3-300 ng/mL(I),0.03-4000 ng/mL(II),0.03-500 ng/mL(III),3-1500 ng/mL(V),6-600 ng/mL(V)and 30-1600 ng/mL(VI)in human urine respectively.The intra-and inter-day variation coefficients of the method at three concentration levels(low,medium and high)were less than 12%. The method also afforded satisfactory results in terms of specificity,accuracy(80-120%)and matrix effect(83-115%).ConclusionsThe established method is precise,sensitive and accurate with minimum sample preparation.It is a fit-for-purpose approach and has been applied in our laboratory for doping-control sample analysis.
LC-MS/MS,diuretics,method validation,doping-control
2016.04.17
董颖,Email:dongying@chinada.cn;张丽娟,Email:dazlj@mail.buct.edu.cn

