克唑替尼治疗ALK重排阳性非小细胞肺癌效果及安全性的Meta分析
崔海忠 曹德东 戈伟▲
1.武汉大学人民医院肿瘤科,湖北武汉430060;2.湖北省枣阳市第一人民医院肿瘤科,湖北枣阳441000
克唑替尼治疗ALK重排阳性非小细胞肺癌效果及安全性的Meta分析
崔海忠1,2曹德东1戈伟1▲
1.武汉大学人民医院肿瘤科,湖北武汉430060;2.湖北省枣阳市第一人民医院肿瘤科,湖北枣阳441000
目的系统评估克唑替尼治疗ALK重排阳性非小细胞肺癌(NSCLC)患者的效果和安全性。方法通过系统检索PubMed、EMbase、Cochrane library、CNKI、CBM、VIP、万方等数据库,日期截至2015年12月。筛选应用克唑替尼治疗ALK重排阳性晚期NSCLC的临床研究,收集治疗效果及不良反应方面的临床数据,运用Meta分析系统评估克唑替尼的疗效及安全性。结果最终共纳入5篇临床研究,包括812例晚期NSCLC患者。Meta分析结果表明:克唑替尼组的疗效明显优于对照组,克唑替尼治疗后的总体客观反应率为67.9%,完全缓解OR值为3.89(95%CI:1.09~13.85;P=0.04),部分缓解OR值为3.62(95%CI:1.97~6.65;P<0.0001)。克唑替尼组与对照组相比,在骨髓抑制(OR=0.55;95%CI:0.37~0.80;P=0.002)、视觉障碍(OR=7.84;95%CI:1.90~32.30;P=0.004)、脱发(OR=0.10;95%CI:0.02~0.59;P=0.01)等不良反应方面差异有统计学意义。结论与化疗相比,克唑替尼用于治疗ALK重排阳性NSCLC具有良好的效果。
克唑替尼;EML4-ALK;非小细胞肺癌;Meta分析
肺癌是全世界所有癌症中最常见的恶性肿瘤之一,近几十年其发生率呈不断上升趋势,其中85%以上为非小细胞肺癌(NSCLC)[1-2]。近年来,遗传异常可能导致癌症发生和进展的认识已经彻底改变肿瘤研究。2007年,在NSCLC患者中首先发现酪氨酸激酶间变性淋巴瘤激酶(ALK)基因的易位,导致ALK融合蛋白的表达[3]。活化的ALK融合蛋白通过作用于多个分子信号传导通路,如PI3K/AKT/mTOR通路、JAK/ STAT通路和RAS/MEK/ERK通路[4-5],从而导致异常的ALK信号传导和致癌性转化。ALK信号通路可强化细胞增殖、细胞存活和细胞代谢。在非特定的NSCLC患者中有2%~7%存在ALK基因重组[6]。正因为ALK及其通路在肿瘤发生发展中的重要作用,已有研究通过抑制ALK通路治疗NSCLC[7-8]。克唑替尼可抑制ALK和间充质上皮生长因子(c-Met)/肝细胞生长因子受体(HGFR)激酶[9],并显著改善ALK阳性NSCLC患者的生存期、反应率和有效期,同时具有较好的安全性[10-11]。本研究遵循系统评价和荟萃分析推荐报道项目(PRISMA)指南[12],以期评估克唑替尼在中国ALK阳性NSCLC患者中的疗效和安全性。
1 资料与方法
1.1检索策略
选取PubMed、Embase、Cochrane Library、中国生物医学文献数据库、中国生物医学期刊文献数据库、中国学术期刊全文数据库、中文科技期刊全文数据库等数据库进行系统筛选。中文关键词为“克唑替尼”“非小细胞肺癌”“肺癌”“间变性淋巴瘤激酶”“ALK”“临床研究”,英文关键词为“crizotinib”“non-small cell lung cancer”“carcinoma”“anaplastic lymphoma kinase”“ALK”“clinical trial”。会议摘要未纳入。对无法获得原文的相关文献,通过与通讯作者联系以获得进一步的信息。
1.2纳入标准
①克唑替尼治疗ALK阳性NSCLC的疗效和/或安全性的临床试验;②可计算或搜集1年总生存期(OS)、无进展生存期(PFS)、总反应率(ORR)、部分缓解(PR)、完全缓解(CR)、稳定疾病(SD),和/或克唑替尼的毒性报道;③英文或中文文献;④可获取全文。
1.3数据提取
首先通过阅读拟纳入研究的文章标题进行初筛。随后,由2名评审员独立阅读初筛后的文章摘要。对符合纳入标准的文献,重点搜集一般资料和结局指标。一般资料包括患者人数、年龄、性别、ALK检测方法、药物剂量等。结局指标包括ORR、PR、CR及不良反应等。当存在意见不一致时,通过讨论达成共识。
1.4统计学方法
采用系统评价软件RevMan 5.3进行数据统计分析。在评估克唑替尼治疗ALK阳性NSCLC的效果和安全性时,根据纳入研究的异质性,选择随机效应模型或固定效应模型进行系统分析。使用Cochran's Q试验计算I2值,评估纳入研究的异质性。I2值>50%时异质性显著。使用Egger's检验评估发表偏倚。以P<0.05为差异有统计学意义。
2 结果
2.1检索结果及质量评价
通过数据库检索,共有96篇文献进入初始筛选,其中80篇由于不符合纳入标准被排除。通过对剩余的研究进行进一步筛选,再次排除8篇文献,排除原因如下:终点数据无法获得;个案报道;综述;会议摘要。研究筛选过程见图1。最终共纳入5篇文献[11,13-16],具体见表1。研究的质量评估具体见表2。
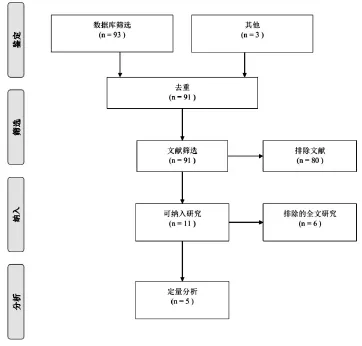
图1 文献筛选线路图
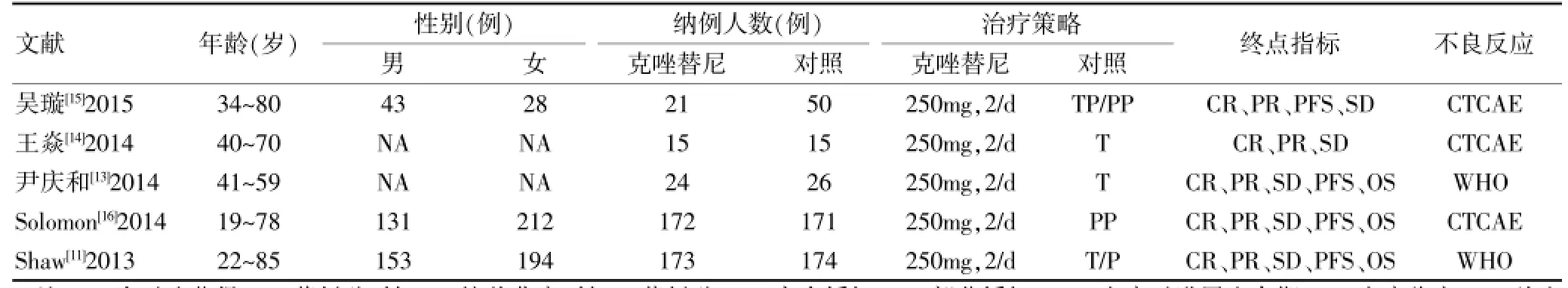
表1 纳入研究的一般资料
2.2Meta分析结果
2.2.1克唑替尼疗效最终纳入5个研究[11,13-16]对克唑替尼治疗ALK阳性NSCLC的疗效进行了报道。如图2所示,ALK阳性NSCLC患者的ORR为67.9%,CR的OR值为3.89(95%CI:1.09~13.85;P=0.04),PR的OR值为3.62(95%CI:1.97~6.65;P<0.0001)。该类患者的CR和PR的比例分别为10%和46.7%。
2.2.2克唑替尼安全性纳入的5个研究[11,13-16]均报道了克唑替尼治疗ALK阳性NSCLC患者的常见不良反应,主要包括视觉障碍、胃肠道反应、骨髓抑制、肝功能损伤及脱发等。如图3所示,综合分析各个研究的临床数据,发现克唑替尼治疗组在骨髓抑制(OR= 0.55;95%CI:0.37~0.80;P=0.002)、视觉障碍(OR=7.84;95%CI:1.90~32.30;P=0.004)、脱发(OR=0.10;95%CI: 0.02~0.59;P=0.01)方面,与对照组比较,差异有统计学意义;而在恶心呕吐(OR=1.18;95%CI:0.66~2.13;P=0.57)、肝功能异常(OR=3.32;95%CI:0.94~11.70;P=0.06)方面,两组差异无统计学意义。
2.2.3发表性偏倚以纳入文献做漏斗图分析可见漏斗图不对称,提示可能存在未发表的阴性结果试验,存在发表性偏倚,见图4。
3 讨论
本研究的目的在于评价克唑替尼治疗ALK阳性NSCLC的效果和安全性。通过整合分析多个临床研究的数据,本研究结果表明,克唑替尼可使ALK阳性晚期NSCLC患者在疾病控制方面获益:克唑替尼可提高治疗有效率,改善治疗效果。与给予化疗的对照组类似,克唑替尼的不良反应主要表现为胃肠道反应、视觉障碍及脱发等,且克唑替尼组在骨髓抑制等不良反应方面较对照组具有一定优势。这些结果表明克唑替尼治疗ALK阳性NSCLC患者的有效性及安全性。

表2 纳入研究方法学质量评价
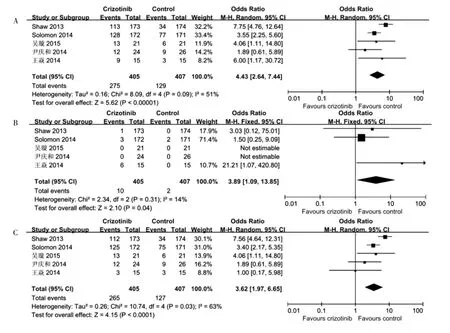
图2 克唑替尼治疗ALK阳性NSCLC患者疗效的Meta分析
2007年,在NSCLC患者中首先发现ALK基因的易位,导致ALK融合蛋白的表达[3]。已有研究表明,在包括NSCLC、炎性肌纤维母细胞瘤、神经母细胞瘤和弥漫性大B细胞淋巴瘤等多种疾病中发现了ALK基因的活化[7,17]。这表明ALK介导的信号通路可能在这些肿瘤的发生、发展中发挥重要作用。由于染色体重组而导致的ALK基因激活常导致多个不同的5'融合伴侣及ALK激酶结构域上游相应的启动子置换。正因为ALK在肿瘤发生发展中的重要作用,已有研究通过抑制酪氨酸激酶作为非小细胞肺癌的一种治疗方法[7-8]。Crizotinib是一种小分子选择性抑制剂,其可抑制ALK和间充质上皮生长因子(c-Met)/肝细胞生长因子受体(HGFR)激酶[9]。克唑替尼的首个人体试验开始于2006年,在实体瘤患者中实施剂量递增试验,随后按照设计原理开始筛选具有ALK或MET激活的特定肿瘤类型,并在该类人群中应用克唑替尼。ALK阳性或MET阳性的肿瘤患者被招募入第二阶段的试验(250 mg,bid, 28 d),并表现出显著疗效。此后的临床研究同样证明克唑替尼可使ALK阳性的晚期NSCLC患者获益。

图3 克唑替尼治疗ALK阳性NSCLC患者后不良反应的Meta分析

图4 纳入研究的发表偏倚分析
已有研究表明[18],克唑替尼可提高ALK阳性NSCLC患者的1年生存率(66.8%)、疾病无进展生存期(8.6个月),并显著改善总体有效率(61.2%)。这与本研究的结果基本一致。值得指出的是,该研究同样通过搜集国外相关文献,经汇总分析后得出上述结论。另一篇针对国人使用克唑替尼的疗效和安全性的Meta分析,通过搜集国内相关临床研究并进行数据汇总分析后得出治疗有效率为59.3%(76/128)[19]。与本研究不同之处在于,上述研究所选取的临床试验大部分为1期单臂临床研究,缺乏有效对照,并未对克唑替尼与化疗的疗效及安全性进行对比。Shaw等[11]进一步对克唑替尼进行了研究,其结果表明一线化疗后复发的ALK阳性晚期NSCLC患者在接受克唑替尼治疗后,其PFS显著延长(7.7比3.3个月,P<0.0001),治疗有效率同样显著改善(65%比20%,P<0.0001)[11]。这与本研究的汇总分析结论一致。因此,对于ALK阳性NSCLC的患者,可推荐使用克唑替尼。但值得注意的是,有约6.5%的患者因克唑替尼的毒性,需要减量或停药。因此,治疗过程中建议定期复查相关指标。
本研究针对ALK阳性NSCLC患者经克唑替尼治疗后的效果及安全性是否优于化疗,通过系统筛选相关文献,经统计学分析后发现,克唑替尼作为一种新批准药物,其在ALK阳性NSCLC中的疗效优于化疗,但安全性方面存在显著差异。这一结论仍需大样本、多中心、随机对照试验等临床证据进行验证。本文所得结果可为临床医生和ALK阳性NSCLC患者制订治疗策略时提供参考,以最大限度地提高肺癌治疗效果。但由于本研究纳入的文献质量不均一,且具有一定异质性,所纳入的文献均不是随机对照研究,纳入人数较少等原因,对其参考价值造成了一定影响。
总之,本研究对克唑替尼治疗ALK阳性NSCLC的效果和安全性进行了系统评价,所得结论与纳入文献的结论一致,克唑替尼可提高治疗效果,并具有良好的安全性。克唑替尼可用于治疗ALK阳性NSCLC,且其疗效优于标准化疗,但这一结论仍需大规模、双盲、随机对照研究予以进一步证实。
[1]Rothschild SI.Targeted Therapies in Non-Small Cell Lung Cancer-Beyond EGFR and ALK[J].Cancers,2015,7(2): 930-949.
[2]方珊珊,戈伟,宋婧,等.Rg3联合化疗对中晚期非小细胞肺癌临床疗效及安全性的系统评价[J].中国医药导报, 2015,12(35):87-92.
[3]Shaw AT,Engelman JA.ALK in lung cancer:past,present,and future[J].Journal of Clinical Oncology:Official Journal of the American Society of Clinical Oncology, 2013,31(8):1105-1111.
[4]Steuer CE,Ramalingam SS.ALK-positive non-small cell lung cancer:mechanisms of resistance and emerging treatment options[J].Cancer,2014,120(16):2392-2402.
[5]Lazzari C,Spitaleri G,Catania C,et al.Targeting ALK in patients with advanced non small cell lung cancer:biology,diagnostic and therapeutic options[J].Critical reviews in Oncology/Hematology,2014,89(3):358-365.
[6]Miyanaga A,Shimizu K,Noro R,et al.Activity of EGFR-tyrosine kinase and ALK inhibitors for EML4-ALK-rearranged non-small-cell lung cancer harbored coexisting EGFR mutation[J].BMC Cancer,2013,13(1):262.
[7]Rossi A,Maione P,Sacco PC,et al.ALK inhibitors and advanced non-small cell lung cancer(review)[J].International Journal of Oncology,2014,45(2):499-508.
[8]Zhang NN,Liu YT,Ma L,et al.The molecular detection and clinical significance of ALK rearrangement in selected advanced non-small cell lung cancer:ALK expression provides insights into ALK targeted therapy[J].PloS One, 2014,9(1):e84501.
[9]Sun Q,Wu JY,Jiao SC.Heterogeneity of epidermal growth factor receptor mutations in lung adenocarcinoma harboring anaplastic lymphoma kinase rearrangements:A case report[J].Oncology Letters,2014,8(5):2093-2095.
[10]Gadgeel SM,Gandhi L,Riely GJ,et al.Safety and activity of alectinib against systemic disease and brain metastases in patients with crizotinib-resistant ALK-rearranged nonsmall-cell lung cancer(AF-002JG):results from the dosefinding portion of a phase 1/2 study[J].The Lancet Oncology,2014,15(10):1119-1128.
[11]Shaw AT,Kim DW,Nakagawa K,et al.Crizotinib versus chemotherapy in advanced ALK-positive lung cancer[J]. The New England Journal of Medicine,2013,368(25): 2385-2394.
[12]Moher D,Liberati A,Tetzlaff J,et al.Preferred reporting items for systematic reviews and meta-analyses:the PRISMA Statement[J].Open Medicine,2009,3(3):e123-130.
[13]尹庆和,肖俏霞,王衍洪,等.多西他赛联合克里唑替尼治疗晚期非小细胞肺癌的临床观察[J].中国药物经济学,2014(6):40-41.
[14]王焱,乔蕾,孟春,等.克唑替尼治疗EML4-ALK阳性晚期非小细胞肺癌的临床疗效观察[J].中国实用医药, 2014(24):157-158.
[15]吴璇,李建雄.克唑替尼治疗EML4-ALK重排阳性患者的临床疗效[J].南方医科大学学报,2015,35(5):753-757.
[16]Solomon BJ,Mok T,Kim DW,et al.First-line crizotinib versus chemotherapy in ALK-positive lung cancer[J]. The New England Journal of Medicine,2014,371(23): 2167-2177.
[17]Murga-Zamalloa C,Lim MS.ALK-driven tumors and targeted therapy:focus on crizotinib[J].Pharmacogenomics and Personalized Medicine,2014,7(7):87-94.
[18]Qian H,Gao F,Wang H,et al.The efficacy and safety of crizotinib in the treatment of anaplastic lymphoma kinasepositive non-small cell lung cancer:a meta-analysis of clinical trials[J].BMC Cancer,2014,14(1):683.
[19]Cui S,Zhao Y,Gu A,et al.Efficacy and tolerability of crizotinib in the treatment of ALK-positive,advanced non-small cell lung cancer in Chinese patients[J].Medical Oncology,2015,32(6):626.
Meta-analysis of clinical efficacy and safety of Crizotinib in the treatment of non-small cell lung cancer patients with positive expression of EML4-ALK
CUI Haizhong1,2CAO Dedong1GE Wei1▲
1.Department of Oncology,Remmin Hospital of Wuhan University,Hubei Province,Wuhan430060,China;2.Department of Oncology,Zaoyang First People's Hospital,Hubei Province,Zaoyang441000,China
Objective To assess the efficacy and safety of Crizotinib in treating ALK positive patients with advanced non-small cell lung cancer(NSCLC).Methods Online databases including PubMed,EMbase,Cochrane library,CNKI, CBM,VIP and WanFang were searched,until December 2015.Data about treatment efficacy and adverse events were extracted to evaluate the efficacy and safety of Crizotinib.Results A total of 5 clinical trials involving 812 cases of patients were included.Meta-analysis results showed that,the efficacy of the Crizotinib group was better than that of the control group,in the Crizotinib group the overall objective response rate was 67.9%,with the OR for CR was 3.89(95% CI:1.09-13.85;P=0.04),OR of PR was 3.62(95%CI:1.97-6.65;P<0.0001),respectively.The results suggested that there were statistically significant differences in myelo-suppression(OR=0.55;95%CI:0.37-0.80;P=0.002),vision disorder(OR=7.84;95%CI:1.90-32.30;P=0.004)and alopecia(OR=0.10;95%CI:0.02-0.59;P=0.01)between the Crizotinib group and the control group.Conclusion Compared with chemotherapy,the efficacy of Crizotinib in the treatment of NSCLC patients with positive expression of EML4-ALK is better.
Crizotinib;EML4-ALK;Non-small cell lung cancer;Meta-analysis
R734.2
A
1673-7210(2016)06(b)-0077-05
国家自然科学基金资助项目(81272500)。
▲
(2016-03-06本文编辑:程铭)

