校园室内环境空气中环状挥发性甲基硅氧烷浓度水平及其健康风险评价
孙梦雪,李清波,,吕晓宁,陈轩,马建民,栾晓新,吴静娴,张猛
1. 大连海事大学 环境科学与工程学院,大连 116026 2. 中国交通运输部科学研究院,北京 100029 3. 兰州大学 资源环境学院 甘肃省环境污染预警与控制重点实验室,兰州 730000
校园室内环境空气中环状挥发性甲基硅氧烷浓度水平及其健康风险评价
孙梦雪1,李清波1,,吕晓宁1,陈轩2,马建民3,栾晓新1,吴静娴1,张猛1
1. 大连海事大学 环境科学与工程学院,大连 116026 2. 中国交通运输部科学研究院,北京 100029 3. 兰州大学 资源环境学院 甘肃省环境污染预警与控制重点实验室,兰州 730000
利用低流量大气采样器采集了大连某高校家庭、男寝、女寝、办公室、实验室中空气样品,分析了样品中4种环状挥发性甲基硅氧烷(cyclic volatile methyl siloxanes,cVMSs):六甲基环三硅氧烷(D3)、八甲基环四硅氧烷(D4)、十甲基环五硅氧烷(D5)、十二甲基环六硅氧烷(D6)的浓度水平、组分特征及其来源,并采用美国国家环境保护局(US-EPA)健康风险评价模型对D5人体健康风险进行了评价。结果表明监测期间室内环境空气中D3、D4、D5与D6检出率均为100%,室内环境总硅氧烷(ΣcVMSs)平均浓度为(12.4±20.7) μg·m-3,范围为0.29~78.4 μg·m-3。办公室与实验室浓度水平最高的为D3,而女寝与家庭为D5,男寝为D6。由于女寝中个人护理品的频繁使用,女寝空气中ΣcVMSs浓度水平分别为男寝、家庭、办公室、实验室的46、80、27、55倍。D5对人体的非致癌危险商值范围为2.14E-04~4.31E-02,对暴露人群尚不存在明显的非致癌风险。
环状挥发性甲基硅氧烷;室内空气;浓度水平;健康风险
Received 6 December 2015 accepted 21 January 2016
挥发性甲基硅氧烷(cyclic volatile methyl siloxanes,以下简称cVMSs),作为有机硅制品的基本原料,被广泛添加于日用品和个人护理品 (personal care products,以下简称PCPs),如洗发水、乳液、化妆品、止汗剂等[1]。cVMSs为高产量化合物,由于其化学性质稳定,cVMSs在进入环境后会表现出持久性与生物富集性[2-4]。近年来,对cVMSs毒理学研究表明,暴露于高十甲基环五硅氧烷(D4)或八甲基环四硅氧烷(D5)浓度下会引起直接或间接的毒性效应,如引雌激素模仿[5-6]、结缔组织病变[7]、不良免疫反应[8]、肝和肺损伤[9]等。加拿大风险评估研究指出,D4和D5会对生态环境造成潜在危害并对生物多样性造成影响[10-12]。因此,cVMSs对人体健康和生态环境的影响受到广泛关注。
目前为止,cVMSs已经在全球范围内多种环境介质中检出,包括大气[13]、水体[14]、土壤与底泥[15]、生物质[16]、污水处理厂进出水及污泥[17]等。近年来,室内环境中cVMSs浓度水平被日益关注。研究表明,cVMSs在室内环境中大量存在,室内环境浓度远高于室外环境cVMSs浓度[18]。人们在一天的活动中>90%的时间是在待在室内[19],室内空气质量是影响人类健康的重要因素。与此同时,由于其高挥发性,在PCPs使用过程中或使用后,约有92%挥发到室内空气中[20],PCPs的使用是室内cVMSs排放的最重要来源[1],除此之外,电子产品排放也是室内环境cVMSs的来源之一[21]。呼吸吸入途径是人类暴露的最主要途径[22],因此研究室内环境cVMSs浓度水平及其对人体健康的风险具有重要意义。
近年来,国外已有大量文献报道了室内环境cVMSs的浓度水平[23-27]。Yucuis等[18]报道了美国芝加哥办公室与实验室空气中D4、D5、十二甲基环六硅氧烷(D6)浓度水平,所有室内样品中D5浓度水平最高占总硅氧烷浓度的97%;Pieri等[28]报道了意大利和英国寝室、办公室和超市室内空气中线状与环状硅氧烷浓度水平;Tran和Kannan[29]报道了纽约奥尔巴尼家庭、办公室、实验室、发廊等室内空气中cVMSs浓度水平,其中D4与D5检出率最高。然而,国内对cVMSs浓度水平研究报道较少。Xu等[30]报道了中国山东省某一有机硅生产工厂车间和附近居民住宅内空气中D4~D6浓度水平;Meng和Wu[31]报道了中国北京装修家庭与普通家庭空气中D4~D6浓度水平。但针对校园寝室、办公室、实验室室内环境中cVMSs浓度水平鲜有报道。本文利用Isolute ENV+主动采样方法[32],调查了家庭、男生寝室、女生寝室、办公室、实验室空气中cVMSs的浓度水平,分析了不同室内环境cVMSs的组分特征与来源,评估了暴露于室内环境浓度下可能的人体健康风险。

图1 低流量采样器示意图Fig. 1 Diagram of low-flow air sampler
1 材料与方法 (Materials and methods)
1.1 样品采集
于2014年6月—2014年7月间采集了大连某高校室内空气样品。随机选择2个男生寝室、2个女生寝室、3个办公室和1个实验室及1个家庭。样品采集从8 am至20 pm,采集12 h。利用低流量大气采样器进行样品采集,采样器如图1所示。采样期间,每个地点均放置一个野外空白,即将采样柱从铝箔袋中拿出,2~3 s后放回铝箔袋中密封,放到采样器旁,待采样结束后带回实验室进行分析,分析处理步骤与空气样品相同。所有样品放入冰箱4 ℃保存,在12 h内进行处理分析。样品采集期间,记录家庭、男寝、女寝中使用的所有个人护理品和化妆品的成分、厂家等信息;记录办公室、实验室中使用的电子产品种类、个数等。采样器平均流速为(2.37±0.14) L·min-1,平均采样体积为(1.86 ±0.53) m3。
1.2 仪器、试剂与材料
仪器:低流量大气采样器(LFAS_100,专利号201410555569.4,赛茨科技(大连)有限公司);气象色谱-质谱联用分析仪(7890A-5975C,Agilent Technologies,USA);四通道色谱分离仪(CHRO_400,赛茨科技(大连)有限公司);DB-VRX毛细管色谱柱(60 m×0.25 mm×1.4 μm;Agilent Technologies,USA)。
试剂:正己烷色谱纯(Fisher Corporation,USA),异辛烷色谱纯(天津科密欧化学试剂有限公司)。
4种有机硅氧烷标准物质:六甲基环三硅氧烷(D3)、D4、D5、D6,内标物M4Q (四-(三甲基硅氧烷)-硅烷),纯度>98%,购自美国Sigma-Aldrich公司。
6 mL SPE固相萃取空柱由聚丙烯制成, 筛板为超高分子量5 μm孔径聚乙烯筛板(厚度2 mm,直径13 mm)。50 mg Isolute ENV+ (羟化聚苯乙烯—二乙烯基苯共聚物)固相萃取柱(Biotage AB)。
1.3 测定方法1.3.1 采样柱净化
将筛板用玻璃棒手动装入SPE空柱底部中并塞紧,每个空柱只装1枚筛板。筛板装好后,使用四通道色谱仪将带有筛板的SPE柱与ENV+柱用6 mL正己烷分3次(一次2 mL)冲洗,一次30s ,并通过75 kpa的负压将溶剂抽净。之后,将带有筛板的SPE柱与ENV+柱装入铝箔袋中密封放入冰箱4 ℃保存,待采样。采样时,将SPE柱与ENV+柱用转接串联为采样柱,放入低流量大气采样器采样。上端SPE柱用筛板来筛分颗粒物大小,下端ENV+柱吸附空气中的气态cVMSs。
1.3.2 固液萃取
采样结束后,将采样柱拆开,ENV+柱用1 mL的正己烷通过重力作用将其洗脱,之后用洗耳球通过负压将其余全部溶剂收集到2 mL进样小瓶中。用微量移液枪准确移取10 μL M4Q内标加入到每个样品瓶中(上机浓度为200 μg·L-1)。冷藏,待上机测定。
1.3.3 仪器条件
载气为高纯氦气(纯度≥99.99%),流速1.4 mL·min-1;进样口温度110 ℃,分流进样,分流比为25:1;色谱升温程序:初始温度45 ℃保持10 min,以12 ℃·min-1升至190 ℃保持2 min,再以6 ℃·min-1升至225 ℃,保持1 min;传输线温度为235 ℃;离子源温度230 ℃;四级杆温度150 ℃。
1.4 质量保证与质量控制
化合物定量采用8点校正曲线和内标法进行分析。实验过程中尽量减少外部带来的干扰,在实验过程中避免使用任何含有硅酮类成分的用品或仪器;在采样、样品分析处理过程中禁止使用含有硅氧烷的个人护理品与化妆品,并且全过程均带白色手套以避免污染。但野外空白样品中仍有D3~D6检出,平均浓度范围为1.83~3.17 ng·m-3。因此,采集样品的浓度应扣除相应的野外空白。D3~D6的方法定量限为野外空白平均浓度加上10倍标准差,范围为4.84~13.1 ng·m-3。

表1 甲基硅氧烷(cVMSs)洗脱回收率、采样效率与穿透率
注:D3、D4、D5、D6 表示六甲基环三硅氧烷,八甲基环四硅氧烷,十甲基环五硅氧烷,十二甲基环六硅氧烷。RSD表示相对标准偏差。
Note: D3, D4, D5, D6 stand for hexamethylcyclotrisiloxane, octamethylcyclotetrasiloxane, decamethylcyclopentasiloxane, dodecamethylcyclohexasiloxane. RSD stand for relative standard deviation.
以洗脱回收率、采样效率、穿透率3项技术指标作为方法评价标准(表1)。ENV+柱头上添加D3~D6混标(2 ppm),待完全吸附后1 mL正己烷对其进行洗脱。目标物D3~D6的洗脱回收率范围为83.1%~126%,>80%的目标物可被1 mL正己烷洗脱。参考Kierkegaard和McLachlan[32]采样效率与穿透率测定方法,本实验将D3~D6混标(2 ppm)添加到SPE柱的筛板上,立即放入采样器进行采样,上端ENV+柱用来计算采样效率,下端ENV+柱用来计算穿透率(图2)。采样效率除D3低于60%外,D4~D6均介于84%~109%之间,RSD小于13%。D3采样效率较低,原因是采样期间为夏季,室外平均温度为21℃,高温下D3的挥发性强,在打入混标或采样过程中的挥发损失使其采样效率明显低于其他物质[13]。目标物在上端ENV+柱中的含量为下端的ENV+柱的400倍,且仅有<2%的目标物被下端ENV+柱吸附,说明下端ENV+柱上目标物含量可以忽略。

图2 采样柱示意图Fig. 2 Diagram of sampling-train
1.5 健康风险评价
健康风险评价是以风险度作为评价指标,把环境污染与人体健康联系起来,定量描述一个人在被污染的环境中暴露时受到危害的风险[33]。空气中cVMSs主要通过呼吸途径进入人体内部器官,因此参照美国环保局专门针对特定场所的吸入途径健康风险评价方法(EPA-540-R-070-002),评估各个室内环境空气中cVMSs吸入途径的健康风险。
(1)非致癌风险
慢性和亚慢性暴露浓度 (EC):
EC = (CA×ET×EF×ED)/AT
(1)
非致癌危险商 (HQ):
HQ = EC/cREL
(2)
危害指数(HI)为多种污染物危害商值之和。
HI =∑ HQi
(3)
(2)致癌风险
致癌风险由风险值(Risk):
Risk = EC×IUR
(4)
式(1)~(4)中CA为环境浓度,μg·m-3;ET为暴露时间,h·d-1;EF为暴露频率,d·y-1;ED为人体终生暴露时间,y;AT为平均时间;cREL为慢性暴露参考浓度[34],μg·m-3;IUR为单位吸入致癌风险浓度,m3·μg-1。
2 结果与分析 (Results and analysis)
2.1 cVMSs浓度水平
室内环境空气ΣcVMSs平均浓度为(12.4±20.7) μg·m-3,范围为0.29~78.4 μg·m-3,D3、D4、D5与D6检出率均为100%,浓度值均高于方法定量限,见表2。
由图3可见,对于化合物单体来说,办公室D3、D4浓度水平最高,而家庭最低,办公室中D3和D4浓度水平分别为家庭的12倍与4倍;女寝中D5浓度水平最高,而实验室最低,女寝为实验室的201倍;女寝中D6浓度水平最高,而家庭最低,女寝为家庭的30倍。
Tran和Kannan[29]报道了美国奥尔巴尼(办公室)空气中ΣcVMSs平均浓度为0.13 μg·m-3,低于本研究办公室ΣcVMSs平均浓度水平1个数量级;Meng和Wu[31]报道了中国北京普通家庭空气中ΣcVMSs(D4~D6)平均浓度为6.28 μg·m-3,高于本研究家庭ΣcVMSs平均浓度1个数量级;Pieri等[28]报道了意大利与英国(男生卧室)空气ΣcVMSs平均浓度分别145、195 μg·m-3,高于本研究男寝ΣcVMSs平均浓度水平3个数量级;意大利与英国(女生卧室)空气ΣcVMSs平均浓度分别为188、178 μg·m-3,高于本研究女寝ΣcVMSs平均浓度水平1个数量级。
2.2 cVMSs组分特征与来源识别
2.2.1 组分特征
由图4可见,室内环境中D5浓度最高,占总cVMSs浓度的89.0%,而D3与D4浓度最低,均为1.46%。
由图5可见,不同室内环境D3~D6比例大小为:家庭为D5>D6>D4>D3,其中D5所占比例为56.3%;男寝为D6>D5>D3>D4,其中D6所占比例为45.2%;女寝为D5>D6>D4>D3,其中D5所占比例为91.8%;办公室为D3>D5>D4>D6,其中D3所占比例为37.9%;实验室为D3>D6>D5>D4,其中D3所占比例为29.3%。

图3 室内环境空气中cVMSs浓度Fig. 3 The cVMSs concentrations in indoor air
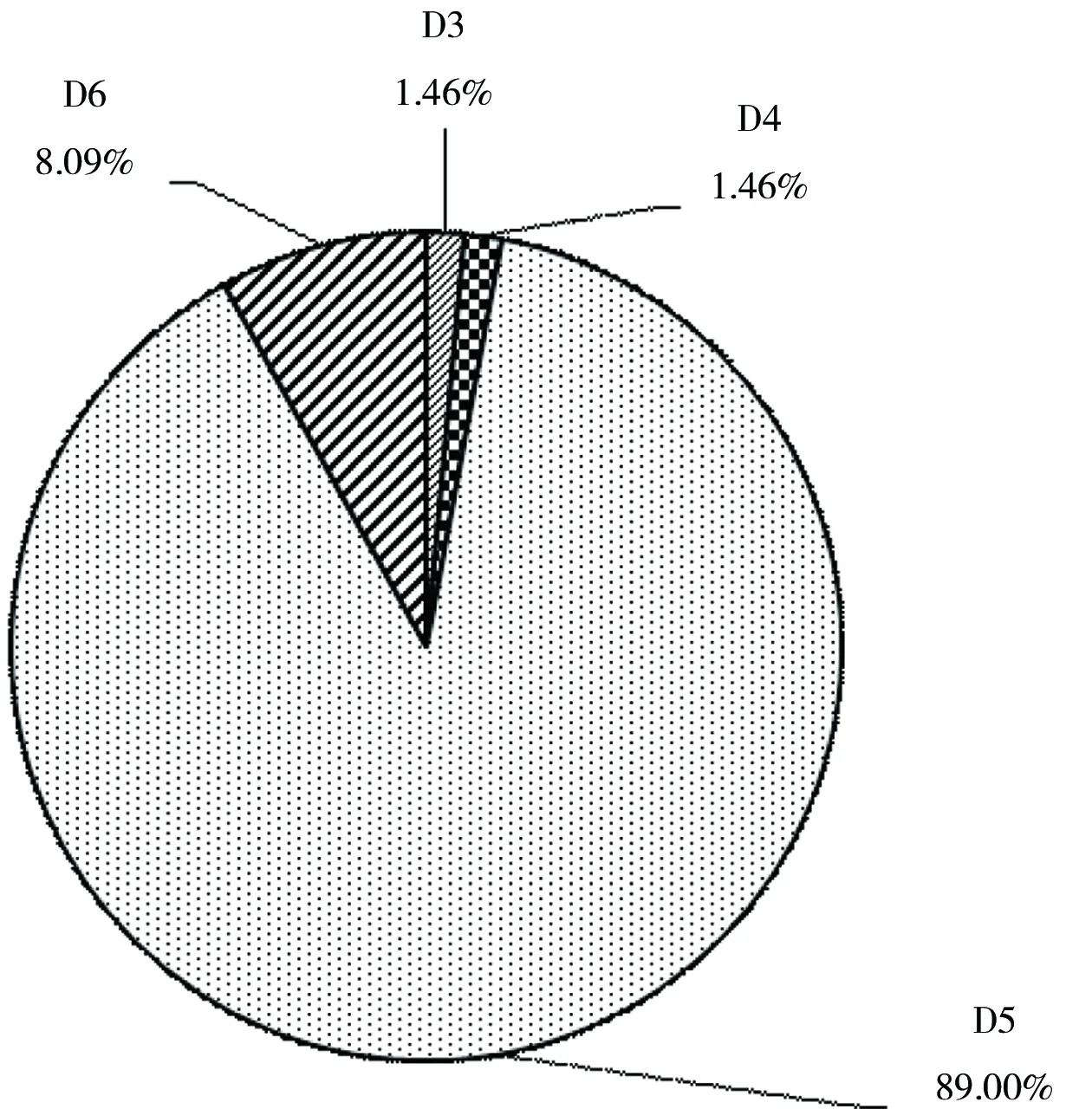
图4 室内环境中的cVMSs组分特征Fig. 4 cVMSs compositions in indoor environments
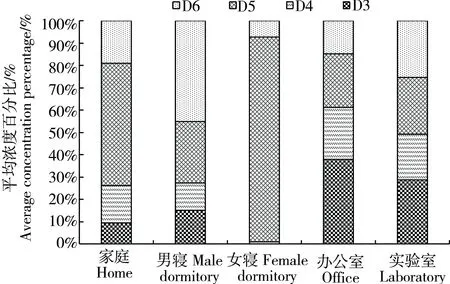
图5 不同室内环境中的cVMSs组分特征Fig. 5 cVMSs compositions in different indoor environments

表2 室内空气中cVMSs的平均浓度(单位:μg·m-3)
2.2.2 来源识别
在所有环状硅氧烷化合物中,D4与D5为最常见的2种物质,因其为PCPs的主要成分,且浓度相对较高,D5/D4比值可说明该室内环境有cVMSs的点源排放存在,而此点源很有可能是PCPs的使用,研究表明,PCPs中D5的浓度远高于D4,分别为2 890 μg·g-1(D5)与141 μg·g-1(D4)[1]。在PCPs使用过程中或使用后,>90%的硅氧烷会挥发到空气中[20],因此可用D5/D4比值来识别室内硅氧烷的来源[18,29]。D5/D4比值会随着不同的室内环境而有所变化,在家庭、男生寝室、女生寝室、办公室和实验室中,D5/D4比值分别为3.29、2.22、144、1.04、1.19,女寝比值为最高(144),而其他室内环境比值基本接近,可以说明PCPs的大量使用是女寝D5/D4比值高的一个重要原因。Tran和Kannan[29]也同样对纽约(奥尔巴尼)室内环境D5/D4比值做了研究,纽约(奥尔巴尼)的家庭、实验室、办公室、学校、发廊与公共环境D5/D4比值分比为7.9、5.7、1.9、6.6、6.4 与 5.7,其中家庭比值为最高,但低于本研究女寝比值。
在对室内环境进行监测时,家庭、男寝、女寝中使用PCPs情况做调查,使用清单见表3。家庭、男寝、女寝PCPs使用差别很大,男寝与家庭所用PCPs较为单一,主要为洗发水、沐浴乳、洗面奶等,所用数量较少,只有洗发水与洗面奶含有硅氧烷类成分;女寝与男寝和家庭相比,PCPs使用数量多,种类杂,尤其是化妆品使用较多,洗发水、乳霜、化妆品均含有硅氧烷类成分。
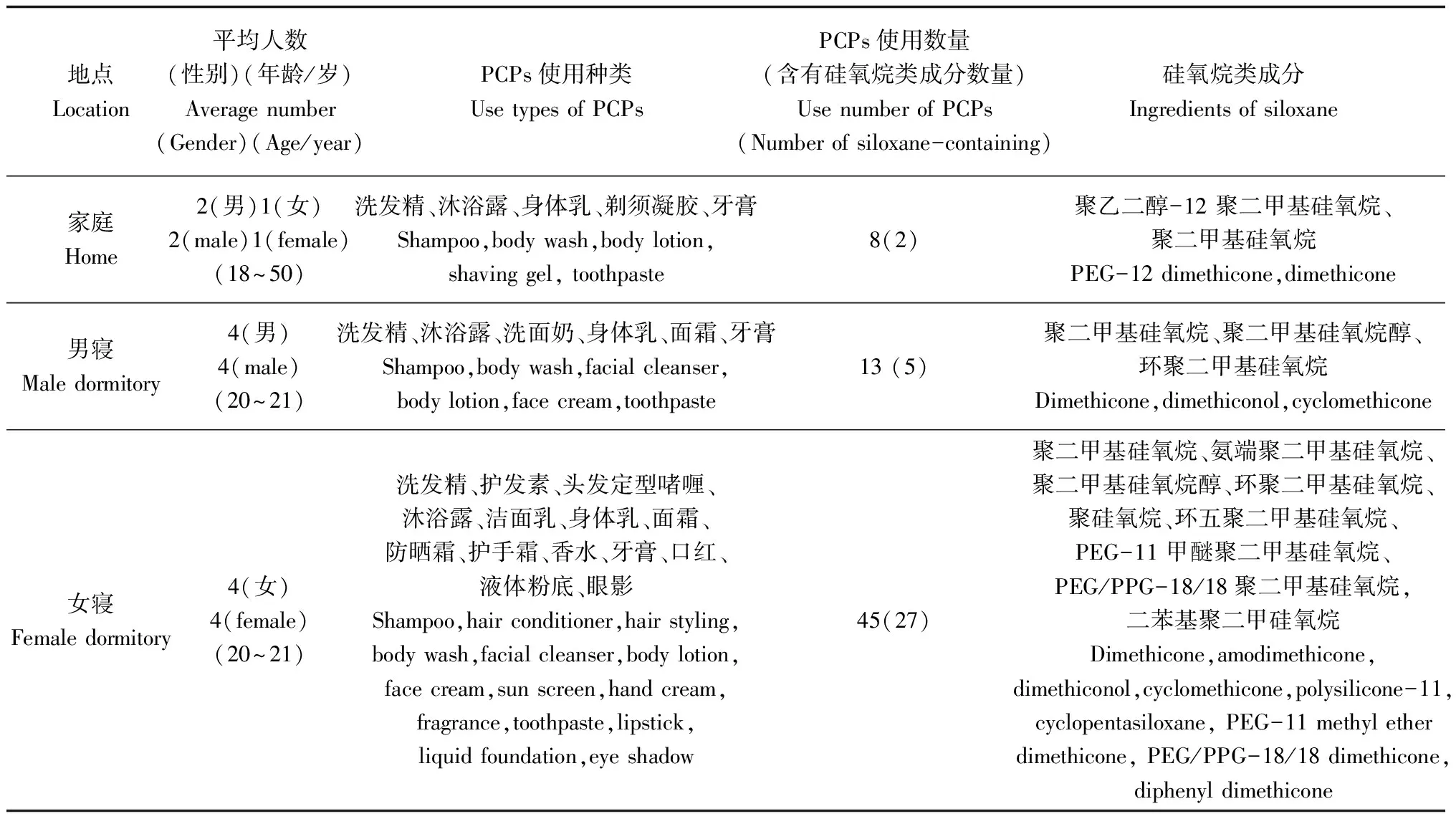
表3 家庭、男寝、女寝个人护理品(PCPs)使用清单

表4 办公室、实验室电子产品使用清单
Wang等[35]检测了加拿大252个PCPs中cVMS的含量,其中D3检出率仅为0.79%,而D4~D6虽未全部检出(检出率分别为4.8%、14%、9.1%),但D4~D6含量高于D3含量1至3个数量级。据报道,D3仅作为PCPs中的D4~D6的杂质被检出,因此国际个人护理品协会命名法委员会已把D3从国际化妆品原料手册中删除[36],因此可以说明D3不是PCPs的主要成分。
但对于办公室、实验室来说,比家庭、男寝、女寝环境要复杂。因为人们会长时间坐在电脑、显示器前,并且打印机、传真机复印机等在工作环境中也被频繁使用,同时现代生活中为了努力提高能源利用率而导致建筑“紧缩”,减少了室内通风率。这2个结果使得即使很低的室内排放可能导致浓度积累而造成高的室内浓度值。监测时,办公室、实验室电子产品使用情况见表4。电脑、空调、打印机在办公室与实验室均被使用。据报道,办公电子设备是室内环境VOCs、臭氧、PM、SVOCs等的重要排放源[37]。有报道指出,手机与电脑键盘,打印机滚轴是由硅酮制成[38],电子元器件涂硅氧烷可增加稳定性防止电击、辐射和振动造成损害并且电子产品有机硅排放为室内灰尘中硅氧烷来源[39],McKone等[21]发现了在打印机或电脑中D3有较高的排放率。由于D3不是PCPs的主要成分,可以推断出室内中电子产品(如电脑、打印机)也可能是室内硅氧烷一个来源。因此本研究中,D3在办公室、实验室浓度较高的原因,很可能是电子产品硅氧烷排放的贡献。
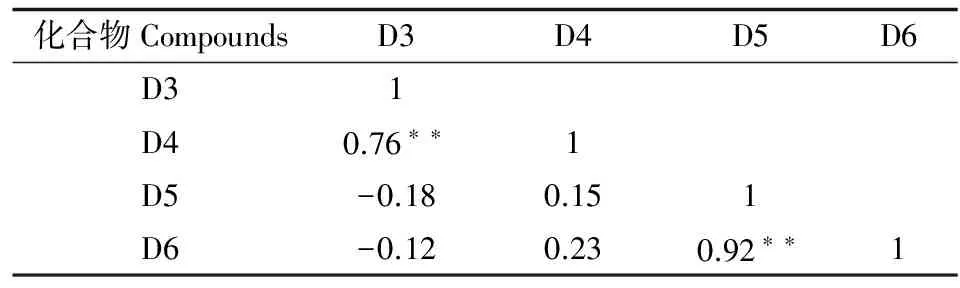
表5 cVMSs各物种间皮尔森相关性
注:**为在0.01 水平(双侧)上显著相关。
Note: **Significant at the 0.01 level (double side).

表6 监测期间室内环境空气中D5的日平均暴露浓度和非致癌危险商
另外,也可以通过对cVMSs不同组分之间的皮尔森相关性(见表5),阐明其可能来源。D3与D4、D5与D6相关性达到1%的显著水平(r=0.70、0.92),说明D3与D4和D5与D6很有可能分别来自同一来源;而D3与D5、D3与D6分别呈负相关性(r=-0.18、-0.12),说明D3与D5、D6来源不同。D5与D6可能来自PCPs,D3可能来自其他源,如电子产品[21,38]。
cVMSs的特征比值、使用清单和相关性分析表明,除PCPs使用外,电子产品使用对室内空气中cVMSs也可能有贡献。因此,对室内cVMSs排放源的监控,除了调查PCPs浓度,还应重点监测电子产品使用时的排放浓度,建立室内cVMSs排放清单,明确电子产品排放比例。
2.3 风险评估
根据国际癌症研究机构(IACR)的分类体系,确定D3~D6为非致癌物。由于目前,仅有美国加州环境健康危害协会办公室(office of environmental health hazard assessment,OEHHA)报道了D5的慢性暴露参考浓度700 μg·m-3[34]。但需要注意的是,D3、D4、D6对人体可能存在非致癌风险,但是目前没有相关非致癌风险评价参数。因此,只评估室内5个地点D5的非致癌性风险。本研究监测时间为8 am至20 pm,暴露时间为12 h·d-1;暴露频率办公室、实验室为按除去法定节假日正常工作时间为250 d·y-1,家庭、女寝、男寝为按节假日时间115 d·y-1[40];人体终生暴露时间为70 y;办公室、实验室平均时间为70 h×250 h×12 h,家庭、女寝、男寝为70 h×115 h×12 h。计算暴露浓度与非致癌危险商见表6。
由表6可见,D5在5个室内地点的EC范围为0.15~30.2 μg·m-3,HQ范围为2.14E-04~4.31E-02,ΣHQ为4.44E-02。其中,女寝非致癌危险商最高,高于其他地点2个数量级。目前中国没有颁布相关健康风险评价标准,参照US-EPA标准,当HI<1时,居民长期暴露在此环境条件下不会出现不良反应。由表6可见,研究区室内空气中HI均小于1,说明cVMSs对研究区人群尚不存在非致癌风险。风险评估模型可以看出,非致癌风险评估可简化为HQ = CA/cREL,一般认为污染物环境浓度低于参考浓度,就不会产生非致癌风险。表2中,所有室内环境D5浓度范围为0.11~70.7 μg·m-3,均小于D5的cREL 700 μg·m-3,说明这些研究区域室内空气中D5的非致癌危险商值尚处于安全范围内,不会对研究区居民产生非致癌损害。
气溶胶和可吸入颗粒物对空气质量具有重要影响,而相对于室外,室内可吸入颗粒物污染对人的影响更为显著,据报道,室内细颗粒物(PM2.5)吸入量为室外的4倍[41]。Tran和Kannan[29]指出,cVMSs也会分布于室内空气颗粒态中,D3~D6在其所监测的室内环境(家庭、办公室、实验室、校园、发廊等)所有颗粒态样品中平均浓度水平分别为3.08、11.2、179、23.2 ng·m-3,气态样品中平均浓度水平分别为16.9、105、543、89.5 ng·m-3,其中D5浓度不论在颗粒态还是在气态均远远<700 μg·m-3,说明对所监测环境的暴露人群不存在非致癌风险,但颗粒态D3~D6在呼吸途径贡献的大小分别为15.4%、9.66%、24.8%、20.5%,说明颗粒态对呼吸途径的贡献不可忽略。因此,今后对室内空气的监测不仅要监测气态浓度,还应加强对颗粒态浓度的监测,明确颗粒态cVMSs对所监测环境的健康影响。
比较近年来国内外研究结果,发现目前环境空气中cVMSs对人体健康尚不存在潜在致癌风险,但是浓度水平较高,因此应当适当降低室内环境空气中cVMSs的浓度(尤其是D5)。主要措施有,一增大室内室外空气交换率,保持室内环境通风良好;二通过与羟基自由基发生均相反应或与气溶胶发生非均相反应[42-43],从而使其降解。鉴于室内空气中cVMSs高浓度水平,为减少居民罹患癌症等风险,我国应加大对室内环境cVMSs的监测,加快研究和完善cVMSs相关毒理学参数与评价标准,开发新型材料替代有机硅工业原料,大力推广居民使用零硅油洗发产品。
综上可知,居住环境(家庭、男寝、女寝)空气D5平均浓度水平最高,工作环境(办公室、实验室)空气中D3浓度水平最高。居住环境D5与D6浓度水平分别是工作环境的63倍与8倍,而工作环境D3与D4浓度分别是居住环境的5倍与2倍,个人护理品使用对室内空气中cVMSs具有重要贡献,电子产品使用对室内空气中cVMSs也有贡献。室内环境中D5对人体的非致癌危险商值范围为2.14E-04~4.31E-02,对暴露人群尚不存在明显的非致癌风险。
致谢:感谢澳大利亚昆士兰大学环境毒理学研究中心王宪钰博士在文章修改中给予的帮助。
[1] Horii Y, Kannan K. Survey of organosilicone compounds, including cyclic and linear siloxanes, in personal-care and household products [J]. Archives of Environmental Contamination & Toxicology, 2008, 55(4): 701-710
[2] Brooke D N, Crookes M J, Gray D, et al. Environmental Risk Assessment Report: Decamethylcyclopentasiloxane [R]. Bristol: Environment Agency of England and Wales, 2009
[3] Brooke D N, Crookes M J, Gray D, et al. Environmental Risk Assessment Report:Dodecamethylcyclohexasiloxane [R]. Bristol: Environment Agency of England and Wales, 2009
[4] Brooke D N, Crookes M J, Gray D, et al. Environmental Risk Assessment Report: Octamethylcyclotetrasiloxane [R]. Bristol: Environment Agency of England and Wales, 2009
[5] Hayden J F, Barlow S A. Structure-activity relationships of organosiloxanes and the female reproductive system [J]. Toxicology & Applied Pharmacology, 1972, 21(1): 68-79
[6] He B, Rhodes-Brower S, Miller M R, et al. Octamethylcyclotetrasiloxane exhibits estrogenic activity in mice via ERα [J]. Toxicology & Applied Pharmacology, 2003, 192(3): 254-261
[7] Quinn A, Regan J J, Marinik B, et al. In vitro and in vivo evaluation of the estrogenic, androgenic, and progestagenic potential of two cyclic siloxanes [J]. Toxicological Sciences, 2007, 96(1):145-153
[8] Granchi D, Cavedagna D, Ciapetti G, et al. Silicone breast implants: The role of immune system on capsular contracture formation [J]. Journal of Biomedical Materials Research, 1995, 29(2): 197-202
[9] Lieberman M W, Lykissa E D, Barrios R, et al. Cyclosiloxanes produce fatal liver and lung damage in mice [J]. Environmental Health Perspectives, 1999, 107 (2): 161-165
[10] Environment Canada and Health Canada. Screening Assessment for the Challenge Octamethylcyclotetrasiloxane (D4) [R]. Ottawa: Environment Canada and Health Canada, 2008
[11] Environment Canada and Health Canada. Screening Assessment for the Challenge:Decamethylcyclopentasiloxane (D5) [R]. Ottawa: Environment Canada and Health Canada, 2008
[12] Environment Canada and Health Canada. Screening Assessment for the Challenge: Dodecamethylcyclohexasiloxane (D6) [R]. Ottawa: Environment Canada and Health Canada, 2008
[13] Krogseth I S, Amelie K, Mclachlan M S, et al. Occurrence and seasonality of cyclic volatile methyl siloxanes in Arctic air [J]. Environmental Science & Technology, 2013, 47(1): 502-509
[14] Xu L, Shi Y L,Cai Y Q. Occurrence and fate of volatile siloxanes in a municipal wastewater treatment plant of Beijing, China [J]. Water Research, 2013, 47(2): 715-724
[15] Zhang Z, Qi H, Ren N, et al. Survey of cyclic and linear siloxanes in sediment from the Songhua River and in sewage sludge from wastewater treatment plants, Northeastern China [J]. Archives of Environmental Contamination & Toxicology, 2011, 60(2): 204-211
[16] Warner N A, Anita E, Guttorm C, et al. Volatile siloxanes in the European Arctic: Assessment of sources and spatial distribution [J]. Environmental Science & Technology, 2010, 44(19): 7705-7710
[17] Wang D G, Steer H, Tait T, et al. Concentrations of cyclic volatilemethylsiloxanes in biosolid amended soil, influent, effluent, receiving water, and sediment of wastewater treatment plants in Canada [J]. Chemosphere, 2012, 93(5): 766-773
[18] Yucuis R A, Stanier C O, Hornbuckle K C. Cyclic siloxanes in air, including identification of high levels in Chicago and distinct diurnal variation [J]. Chemosphere, 2013, 92(8): 905-910
[19] Sarigiannis D A, Karakitsios S P, Gotti A. Exposure to major volatile organic compounds and carbonyls in European indoor environments and associated health risk [J]. Environment International, 2011, 37(4): 743-765
[20] Alleni R B, Kochs P, Chandra G. Industrial Organosilicon Materials, Their Environmental Entry and Predicted Fate. Organosilicon Materials [M]. Heidelberg: Springer Berlin, 1997: 1-25
[21] McKone T, Maddalena R, Destaillats H, et al. Indoor pollutant emissions from electronic office equipment [EB/OL]. [2015-12-06]. http://www.arb.ca.gov/research/seminars/mckone/mckone.pdf
[22] Biesterbos J W H, Beckmann G, Wel L V, et al. Aggregate dermal exposure to cyclic siloxanes in personal care products: Implications for risk assessment [J]. Environment International, 2015, 74(74): 231-239
[23] Shields H C, Fleischer D M,Weschler C J. Comparisons among VOCs measured in three types of U.S. commercial buildings with different occupant densities [J]. Indoor Air, 1996, 6(1): 2-17
[24] Hodgson A T, Faulkner D, Sullivan D P, et al. Effect of outside air ventilation rate on volatile organic compound concentrations in a call center [J]. Atmospheric Environment, 2003, 37(39): 5517-5527
[25] Kaj L, Andersson J, Palm Cousins A, et al. Results from the Swedish National Screening Programme 2004. Subreport 4: Siloxanes [R]. Stockholm: Swedish Environmental Research Institute, 2005
[26] May W, Apte M G, Randy M, et al. Volatile organic compounds in small- and medium-sized commercial buildings in California [J]. Environmental Science & Technology, 2011, 45(20): 9075-9583
[27] Companioni-Damas E Y, Santos F J, Galceran M T. Linear and cyclic methylsiloxanes in air by concurrent solvent recondensation-large volume injection-gas chromatography-mass spectrometry [J]. Talanta, 2014, 118: 245-252
[28] Pieri F, Katsoyiannis A, Martellini T, et al. Occurrence of linear and cyclic volatile methyl siloxanes in indoor air samples (UK and Italy) and their isotopic characterization [J]. Environment International, 2013, 59(3): 363-371
[29] Tran T M, Kannan K. Occurrence of cyclic and linear siloxanes in indoor air from Albany, New York, USA, and its implications for inhalation exposure [J]. Science of the Total Environment, 2015, 511: 138-144
[30] Xu L, Shi Y L, Wang T, et al. Methyl siloxanes in environmental matrices around a siloxane production facility, and their distribution and elimination in plasma of exposed population [J]. Environmental Science & Technology, 2012, 46(21): 11718-11726
[31] Meng F, Wu H. Indoor air pollution by methylsiloxane in household and automobile settings [J]. Plos One, 2015, 10(8): e0135509
[32] Amelie K, Mclachlan M S. Determination of decamethylcyclopentasiloxane in air using commercial solid phase extraction cartridges [J]. Journal of Chromatography A, 2010, 1217(21): 3557-3560
[33] 夏芬美, 李红, 李金娟, 等. 北京市东北城区夏季环境空气中苯系物的污染特征与健康风险评价[J]. 生态毒理学报, 2014, 9(6): 1041-1052
Xia F M, Li H, Li J J, et al. Characteristics and health risk assessment of atmospheric benzene homologues in summer in the northeastern urban area of Beijing, China [J]. Asian Journal of Ecotoxicology, 2014, 9(6): 1041-1052 (in Chinese)
[34] Office of Environmental Health Hazard Assessment (OEHHA). Toxicity Data Review: Decamethylcyclopentasiloxane (D5) [OL]. [2015-12-06]. http://www.arb.ca.gov/toxics/dryclean/oehhad5review.pdf
[35] Wang R, Moody R P, Koniecki D, et al. Low molecular weight cyclic volatile methylsiloxanes in cosmetic products sold in Canada: Implication for dermal exposure [J].Environment International, 2009, 35(6): 900-904
[36] Wilbur J, Bergfeld W F, Belsito D V, et al. Safety assessment of cyclomethicone, cyclotetrasiloxane, cyclopentasiloxane, cyclohexasiloxane, and cycloheptasiloxane [J]. International Journal of Toxicology, 2011, 30(6): 149S-227S
[37] Destaillats H, Maddalena R L, Singer B C, et al. Indoor pollutants emitted by office equipment: A review of reported data and information needs [J]. Atmospheric Environment, 2007, 42(7): 1371-1388
[38] Environmental, Health and Safety Council of North America (SEHSC). Silicone Uses [OL]. [2015-12-06]. http://sehsc.americanchemistry.com/Silicone-Uses
[39] Lu Y, Yuan T, Yun H S, et al. Occurrence of cyclic and linear siloxanes in indoor dust from China, and implications for human exposures [J]. Environmental Science & Technology, 2010, 44(16): 6081-6087
[40] 周静博, 李亚卿, 洪纲, 等. 石家庄市制药行业VOCs排放特征分析及健康风险评价[J]. 生态毒理学报, 2015, 10(4): 177-186
Zhou J B, Li Y Q, Hong G, et al. Characteristics and health risk assessment of VOCs emitted from pharmaceutical industry of Shijiazhuang City[J]. Asian Journal of Ecotoxicology, 2015, 10(4): 177-186 (in Chinese)
[41] 室内PM2.5污染调研报告: 室内PM2.5吸入量占八成[R]. 中国环境科学, 2015, 5: 1569
[42] Atkinson R. Kinetics of the gas phase reactions of a series of organosilicon compounds with hydroxyl and nitrate (NO3) radicals and ozone at 297 ± 2K [J]. Environmental Science & Technology, 1991, 25(5): 863-866
[43] Navea J G, Xu S, Stanier C O, et al. Heterogeneous uptake of octamethylcyclotetrasiloxane (D4) and decamethylcyclopentasiloxane (D5) onto mineral dust aerosol under variable RH conditions [J]. Atmospheric Environment, 2009, 43(26): 4060-4069
Levels and Health Risk Assessment of Cyclic Volatile Methyl Siloxanes in Indoor Air of a University Campus
Sun Mengxue1, Li Qingbo1,*, Lv Xiaoning1, Chen Xuan2, Ma Jianmin3, Luan Xiaoxin1, Wu Jingxian1, Zhang Meng1
1. College of Environmental Sciences and Engineering, Dalian Maritime University, Dalian 116026, China 2. China Academy of Transportation Sciences, Beijing 100029, China 3. Key Laboratory for Environmental Pollution Prediction and Control, Gansu Province, College of Earth and Environmental Sciences, Lanzhou University, Lanzhou 730000, China
Four cyclic volatile methyl siloxanes (cVMSs), including D3 (hexamethylcyclotrisiloxane), D4 (octamethylcyclotetrasiloxane), D5 (decamethylcyclopentasiloxane) and D6 (dodecamethylcyclohexasiloxane), were determined in indoor air samples collected from a university in Dalian City using a novel low-volume air sampler. A range of different microenvironments, including an apartment, a male dormitory, a female dormitory, a laboratory and an office, were investigated. The levels, profiles and sources of these compounds were measured and estimated. In addition, health risk of human exposure to D5 was assessed by US Environmental Protection Agency (US-EPA) health risk assessment model. Results showed that D3, D4, D5 and D6 were found in all the samples and the concentration (mean ± SD) of Σ4cVMSs was measured as (12.4 ± 20.7) μg·m-3, ranging from 0.29 to 78.4 μg·m-3. D3, D5 and D6 was measured with the highest concentration in the office and the lab, the female dormitory and the apartment, and the male dormitory respectively. The concentration of Σ4cVMSs in the female dormitory was measured as 46, 80, 27 and 55 times higher than that in the male dormitory, the apartment, the office and the lab, respectively. Possible explanations include the relatively frequent uses of pharmaceuticals and personal care products (PCPs) by female students. Non-cancer hazard quotient (HQ) for D5 was estimated as from 2.14E-04 to 4.31E-02, indicating that no non-cancer health risks exist for the exposed population.
cVMSs; indoor air; ambient level; human health risk
国家自然科学基金(41371448);中央高校基本科研业务费专项资金资助(3132016326)
孙梦雪(1989-),女,硕士,研究方向为室内环境监测,E-mail: sunmengxue8899@163.com;
*通讯作者(Corresponding author), E-mail: drliqb@163.com
10.7524/AJE.1673-5897.20151206003
2015-12-06 录用日期:2016-01-21
1673-5897(2016)4-194-10
X171.5
A
简介:李清波(1967—),男,教授,研究生导师,主要从事有机污染物生物地球化学循环过程的研究。
孙梦雪, 李清波, 吕晓宁, 等. 校园室内环境空气中环状挥发性甲基硅氧烷浓度水平及其健康风险评价[J]. 生态毒理学报,2016, 11(4): 194-203
Sun M X, Li Q B, Lv X N, et al. Levels and health risk assessment of cyclic volatile methyl siloxanes in indoor air of a university campus [J]. Asian Journal of Ecotoxicology, 2016, 11(4): 194-203 (in Chinese)

