鱼油精制过程中邻苯二甲酸酯类化合物分析及变化规律
张建友,费骁文,刘建华,丁玉庭
(浙江工业大学海洋学院,浙江 杭州,310014)
鱼油精制过程中邻苯二甲酸酯类化合物分析及变化规律
张建友,费骁文,刘建华,丁玉庭*
(浙江工业大学海洋学院,浙江 杭州,310014)
建立了气相色谱-质谱法检测鱼油样品中的邻苯二甲酸酯类化合物(phthalate acid esters,PAEs)的方法,并研究PAEs在鱼油精炼过程中的变化规律。研究表明,16种PAEs标准物质在20min内实现有效分离,在0.05~1.0 μg/mL浓度范围内呈现出良好的线性关系 (R2>0.998 3),加标实验回收率为82.1%~107.4%,相对标准偏差(RSD)为0.8%~12.9%,检出限为0.08~0.30 mg/kg。同时,毛油中3种塑化剂( DIBP,DBP和DEHP )含量分别为0.06、0.05和0.04 mg/kg,且随着精炼工艺的进行呈上升趋势,成品油中的含量分别为0.19、0.24和0.06 mg/kg。精炼工艺中所使用的化学助剂是造成鱼油中3种塑化剂含量增加的主要因素。
鱼油;邻苯二甲酸酯;气相色谱-质谱法
邻苯二甲酸酯类化合物[1](phthalate acid esters,PAEs),俗名塑化剂,广泛应用于工业生产中用来改善塑料制品的柔韧性,耐久性和延展性。这类物质挥发性低,难溶于水,易溶于有机溶剂并且不易降解,会造成内分泌失调,阻碍生物体生殖机能,还会引发恶性肿瘤。
PAEs进入人体的途径[2]多种多样,比如环境污染,食品包装材料,食物等,其中食物是PAEs危害人体的主要途径,特别是水产品,如鱼类、贝类。世界各国都极其重视塑化剂的污染问题,并立法限制其使用。欧洲食品安全局已明确制定了几种PAEs的每天可摄入量,分别为DBP(0.01 μg/kg,以体重计,下同)、BBP(0.5 μg/kg)、DEHP(0.01 μg/kg)、DIDP(0.15 μg/kg)、DOP(0.15 μg/kg)[3]。此外,我国也制定了一系列的政策、法规以限制邻苯二甲酸酯的使用[4]。
由于实际样品中PAEs含量较低,加之检测样品基质的复杂性,因此在检测前往往需要进行前处理工作以富集目标物质和排除不必要的干扰。前处理的方法有很多,如固相萃取[5](SPE),固相微萃取[6](SPME),液相萃取[7](LPE)等。而PAEs分析检测技术[8]从早期的滴定法,比色法和分光光度法发展到后来的气相色谱、高效液相色谱(HPLC)[9]、气相-质谱联用(GC-MS)[10]和液相-质谱联用(HPLC-MS)法,GC-MS是目前测定PAEs广泛使用的一种方法。
鱼油是鱼类脂肪酸的总称,不同鱼种的脂肪酸种类和含量不尽相同,其中最具代表性的是二十碳五烯酸(eicosapentaenoic acid,EPA)和二十二碳六烯酸(docosahexaenoic acid,DHA)。
随着PAEs的大量使用,人类活动排入环境的PAEs的量远超过环境的承载能力,使得在各种环境介质中都存在该类物质,包括水体。鱼油作为一种重要的海洋资源,其安全问题不容忽视。本实验利用气相色谱-质谱法(GC-MS)测定鱼油中的PAEs,研究其在精炼过程中的变化规律,借此为提升鱼油精炼工艺的安全性提供理论参考。
1 材料与方法
1.1 材料与仪器
气相色谱质谱联用仪(7890A-5975C),美国Agilent公司;BS-223S型精密电子天平,北京赛多利斯仪器系统有限公司;旋转蒸发仪,上海亚荣生化仪器厂;CR21GII高速冷冻离心机,Hitachi Kokico,日本;LNG-NF-101实验室膜分离设备,上海朗极膜分离设备工程有限公司;纳滤膜(LNGTM NS036 截留分子量360)。
二氯甲烷(色谱纯),Aladdin;正己烷(色谱纯),Sigma;弗罗里硅土(100~200目),使用前在马弗炉600 ℃加热4 h;无水Na2SO4,优级纯,依次用正己烷和二氯甲烷淋洗2次,每次使用的溶剂体积约为无水Na2SO4体积的2倍。淋洗后转移至烧瓶,在50 ℃烘干,然后在225 ℃烘烤4 h,冷却后干燥器中保存。
邻苯二甲酸酯标准品:邻苯二甲酸二甲酯(DMP),99.0%;邻苯二甲酸二乙酯(DEP),99.0%;邻苯二甲酸二异丁酯 (DIBP), 99.0%;邻苯二甲酸二丁酯 (DBP), 99.0%;邻苯二甲酸二( 2-甲氧基) 乙酯 (DMEP), 98.0%;邻苯二甲酸二(4-甲基-2戊基)酯(BMPP),99.3%;邻苯二甲酸二( 2-乙氧基)乙酯(DEEP),99.5%;邻苯二甲酸二戊酯(DPP), 99.0%;邻苯二甲酸二己酯(DHXP), 99.5%;邻苯二甲酸丁基苄基酯(BBP), 99.5%;邻苯二甲酸二( 2-丁氧基)乙酯(DBEP), 96.0%;邻苯二甲酸二环己酯(DCHP), 99.5%;邻苯二甲酸二( 2-乙基)己酯(DEHP), 98.5%;邻苯二甲酸二正辛酯(DNOP), 99.5%;邻苯二甲酸二壬酯(DNP), 99.0%;邻苯二甲酸二苯酯(DPhP), 99.5%,均购自Dr. Ehrenstorfer GmbH,德国。
1.2 鱼油制备
毛油(金枪鱼鱼油,-4 ℃下保存)由舟山兴业有限公司提供,成品油由实验室自制,在精炼过程中,分别对各个阶段的油脂进行取样(在-4 ℃下保存),供分析测试。
脱胶:在毛油中加入0.1%油重的磷酸(85%),50 ℃作用20 min,离心去胶质,得到脱胶油。
脱酸:在脱胶油中加入7%油重的NaOH(3.11 mol/L),60 ℃作用30 min,离心去皂脚,然后水洗,再离心去水得到脱酸油。
脱色:在脱酸油中加入5%油重的活性白土,60 ℃作用30 min,离心后得到脱色油。
脱臭:将脱酸油溶解于正己烷(V(油)∶V(正己烷)=1∶4),然后于膜分离设备中进行1 h左右(进膜压力20 bar,40 ℃)脱臭处理,随后60 ℃真空旋蒸除正己烷,得到脱臭油[11]。
1.3 标准溶液的配制
16种混合标准储备液的浓度为100 mg/L,用正己烷将其逐级稀释至浓度为0.05,0.10,0.25,0.50,1.0 μg/mL的混合标准工作液,-4 ℃保存,备用。
1.4 样品前处理
样品净化装置如图1所示,临用前用10 mL正己烷进行淋洗处理。配制60 mL正己烷-二氯甲烷溶液(V(正己烷)∶V(二氯甲烷)=95∶5),其中20 mL用于溶解0.2 g鱼油样品,缓慢加入层析柱中,之后用剩余的正己烷-二氯甲烷混合溶液分3次冲洗瓶中残留物质和层析柱。底部用圆底烧瓶收集洗脱液,收集完毕后,于50 ℃下旋蒸至近干,正己烷定容,待测,同时做好空白对照。
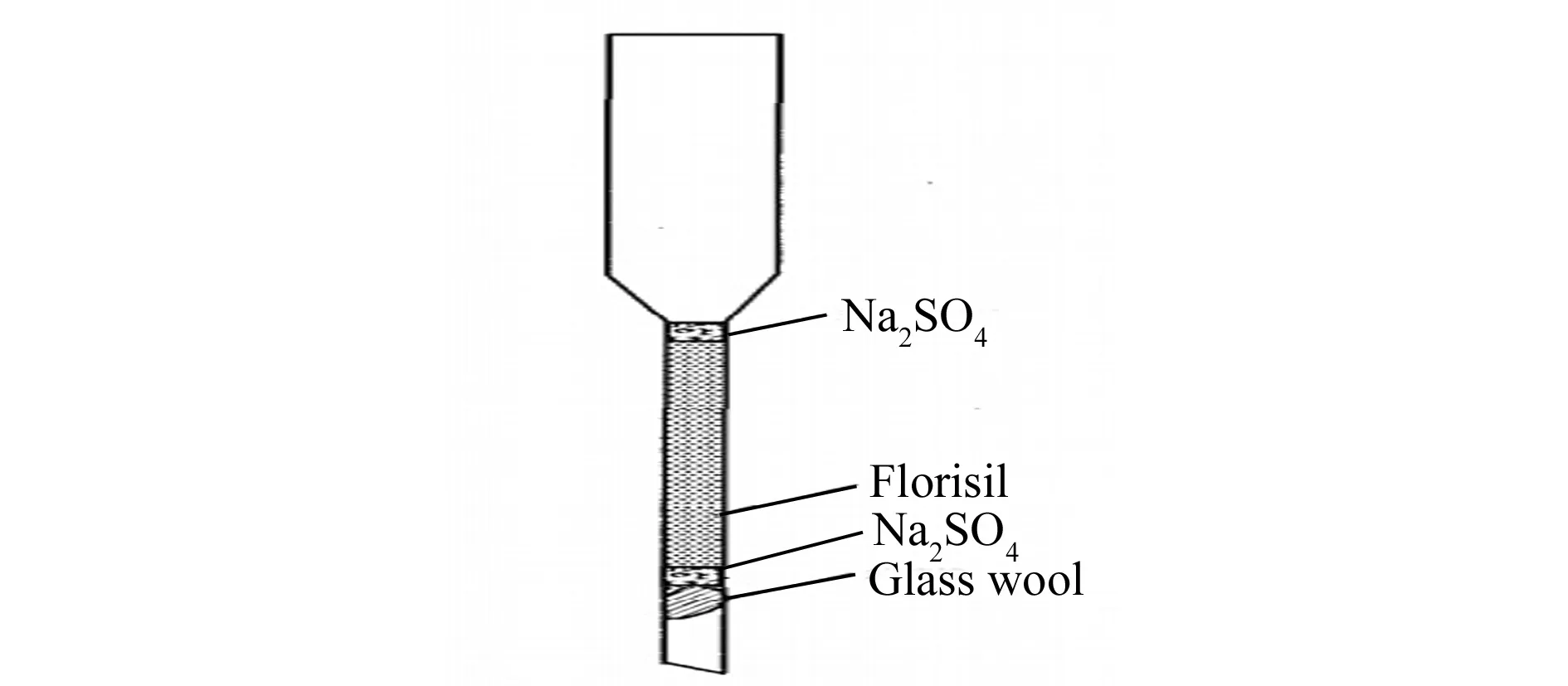
图1 玻璃层析柱结构图Fig.1 The structure of the glass chromatographic column
1.5 色谱条件
1.5.1 气相条件
色谱柱:HP-5MS毛细管柱 (30 m × 0.25 mm × 0.25 μm,Agilent,美国);载气为氦气(纯度>99.99%),流速1.0 mL/min,恒流模式;进样量1 μL,进样口温度250 ℃,柱升温程序:初始60 ℃,保持0.5 min,以20 ℃/min升至280 ℃,保持8 min,不分流进样。
1.5.2 质谱条件
传输线温度280 ℃,EI离子源,电离能量70 eV,离子源温度230 ℃,质量扫描范围40~600 m/z,四级杆温度150 ℃,选择离子检测模式:SIM,定性定量离子见表1。
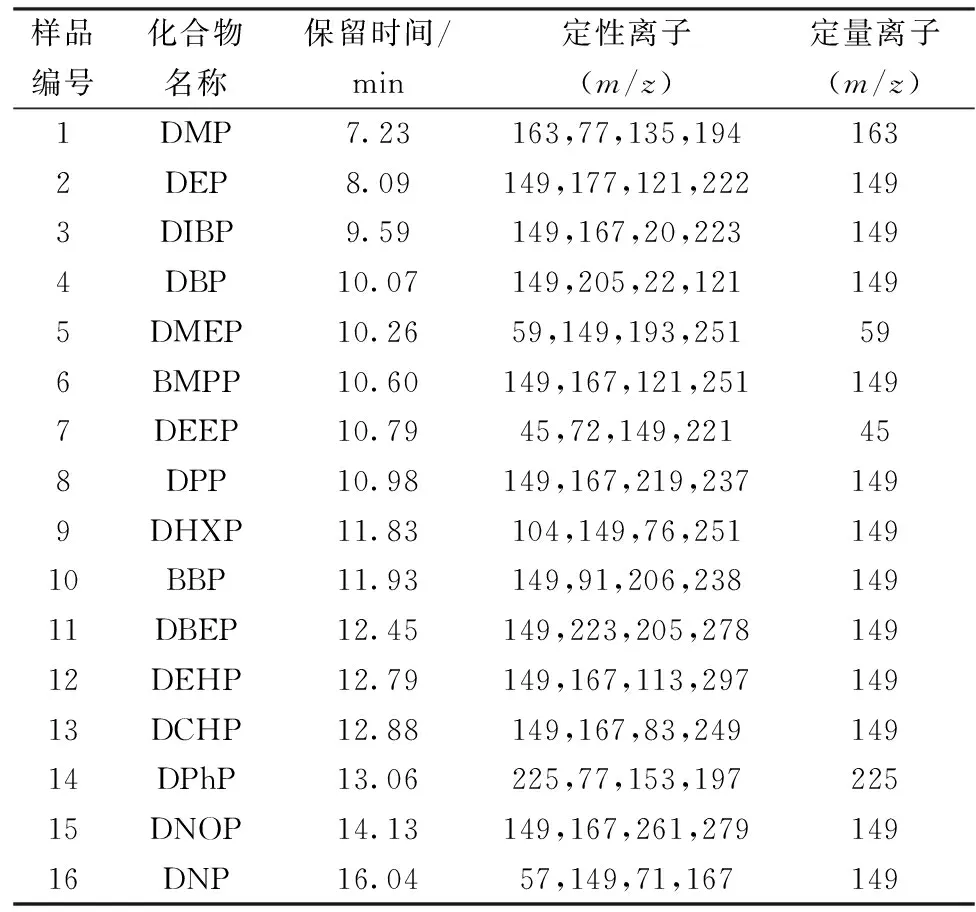
表1 16种PAEs的保留时间和特征离子
2 结果与分析
2.1 定性测定
根据1.5的色谱条件对16种PAEs标准溶液进行测定,分析结果的色谱图见图2。从图2可以看出,16种目标化合物在20 min内有效分开,峰形对称,表明本实验的色谱条件能满足实验要求。
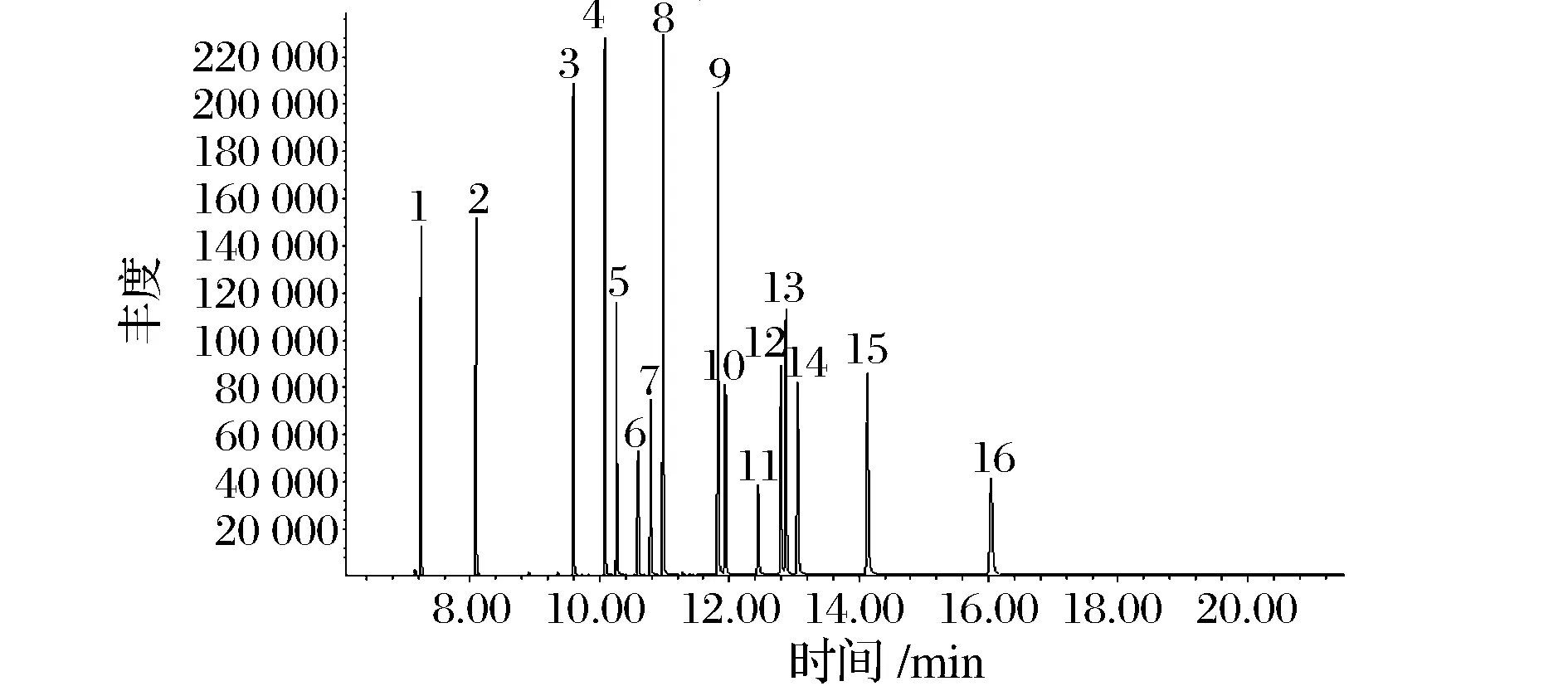
1-DMP; 2-DEP; 3-DIBP; 4-DBP; 5-DMEP; 6-BMPP; 7-DEEP; 8-DPP; 9-DHXP; 10-BBP; 11-DBEP; 12-DEHP; 13-DCHP; 14-DPHP; 15-DNOP; 16-DNP图2 16种PAEs标准品的选择离子色谱图Fig.2 Selected ion monitoring chromatograph of 16 PAEs
2.2 方法的线性范围及检出限
根据1.5的色谱条件对16种PAEs五个浓度梯度的混合标准工作液进行测定,测定的结果以峰面积Y对浓度X作线性回归,其线性范围、回归方程、相关系数(R2)、方法检出限如表2所示。结果表明,16种PAEs线性回归方程的相关系数R2均>0.998 3,表明16种PAEs在0.05~1.0 μg/mL有良好的线性关系。以信噪比(S/N)=3来确定方法的检出限(LOD),LOD值为0.08~0.30 mg/kg,表明方法具有较高的灵敏度,可以满足实验检测的要求。
2.3 方法的精密度和准确度测定
选取本底值较小的毛油样品按1.4的步骤进行加标回收实验,对方法的精密度和准确度进行验证。加标水平分别为0.1、0.25和0.5 μg/mL,每个加标水平重复3次,扣除本底值后计算加标回收率,如表3所示。结果显示,加标样品的3个水平样品的平均加标回收率为82.1%~107.4%,相对标准偏差(RSD)为0.8%~12.9%,其精密度和准确度能够满足分析需求。
2.4 鱼油精制过程中PAEs的变化规律
通过对5个阶段油样取样进行GC-MS分析,与标准品的保留时间,特征碎片离子和碎片离子的相对强度作比较发现,在5个阶段的鱼油样品均检测到了3种塑化剂,结果如图3所示。
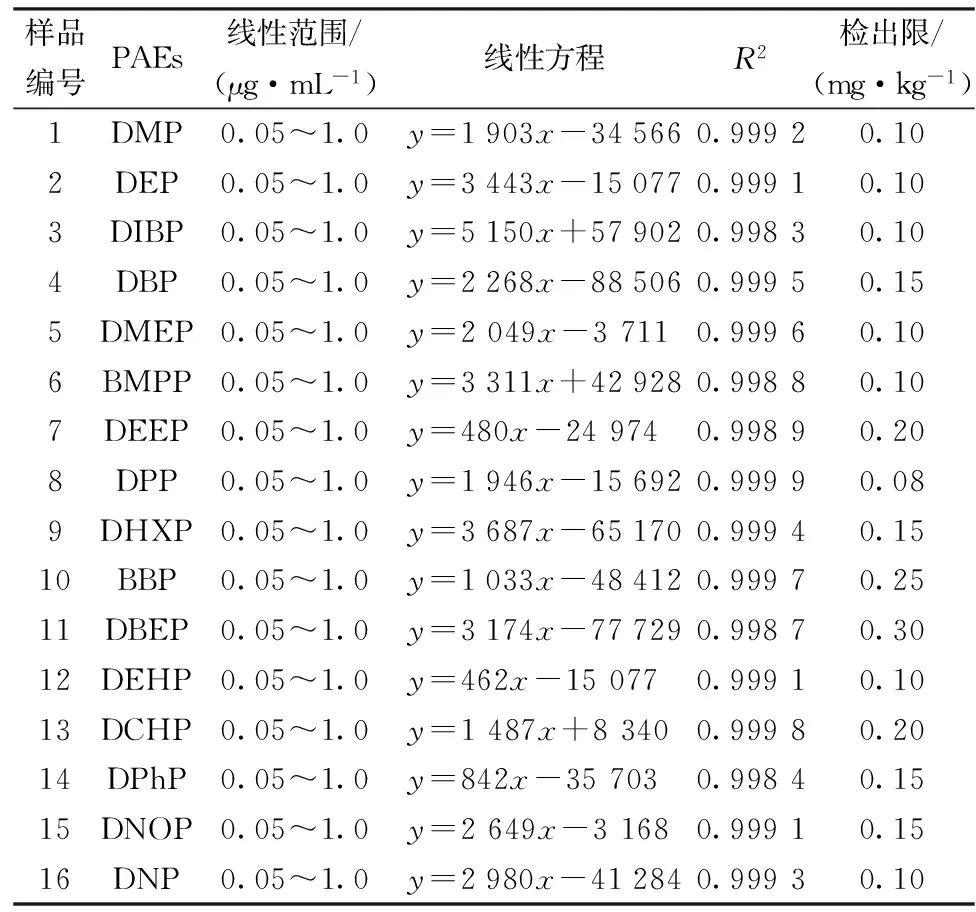
表2 16种PAEs的线性方程、相关系数及检出限
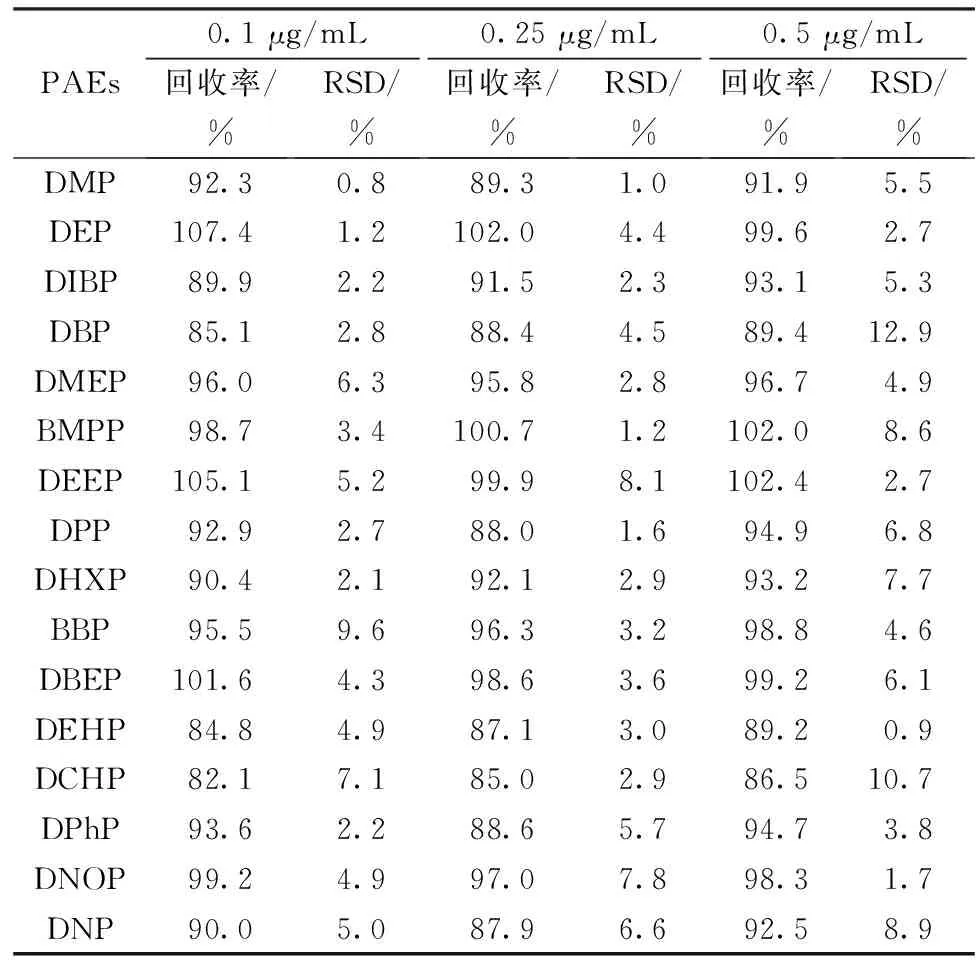
表3 不同加标浓度的加标回收率和相对标准偏差
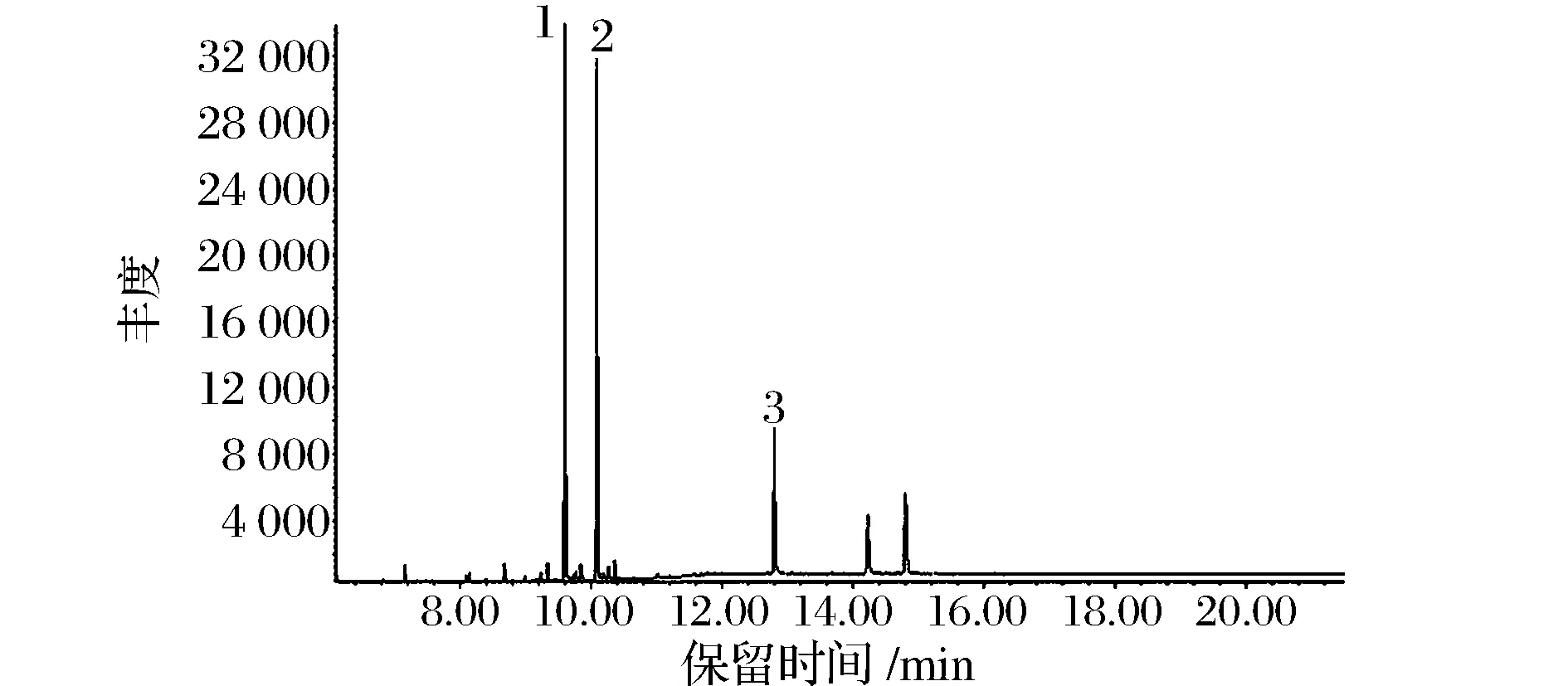
图3 毛油的选择离子色谱图Fig.3 Selected ion monitoring chromatograph of crude oil
3种塑化剂分别是工业上应用最为广泛的的DIBP,DBP和DEHP,毛油中的含量分别为0.06、0.05和0.04 mg/kg,表明其已受到了塑化剂的污染,且随着工艺的进行,3种塑化剂含量呈上升趋势,脱胶油中3种塑化剂的含量分别为0.07、0.08和0.04 mg/kg,脱酸油中含量分别为0.08、0.09和0.04 mg/kg,脱色油中含量分别为0.10、0.11和0.05 mg/kg,脱臭油中的含量分别为0.19、0.24和0.06 mg/kg,脱臭阶段上升幅度较大,可能原因是鱼油长时间、在较高温度下与正己烷(作为浸出油溶剂提取剂)接触,正己烷中部分塑化剂向鱼油发生了迁移有关。同时,DBP,DIBP和DEHP的分子质量在280~300,与膜截留分子质量接近,因此不容易透过,从而有利于塑化剂在鱼油中累积。
由上述数据可以看到,DBP在整个精炼过程中迁移量略高于DIBP,但两者均比DEHP高的多,主要是因为在相同条件下,PAEs分子质量愈小,愈容易发生迁移[12],DBP和DIBP分子质量相同,但小于DEHP,分子阻力小,因此DBP和DIBP迁移量大。同时,检测精制所使用正己烷中的PAEs含量,结果表明正己烷中同样含有DIBP,DBP和DEHP,且含量较高,分别为1.15、1.66和0.08 mg/kg。有研究表明[13],外源污染物PAEs含量越高,溶出塑化剂的含量越大,这就是DBP和DIBP分子质量相同,但是在脱臭阶段,鱼油中DBP增长量要高于DIBP的原因,也表明鱼油在脱臭阶段,受到了正己烷的污染。精炼过程中鱼油中塑化剂含量的变化规律如图4所示。
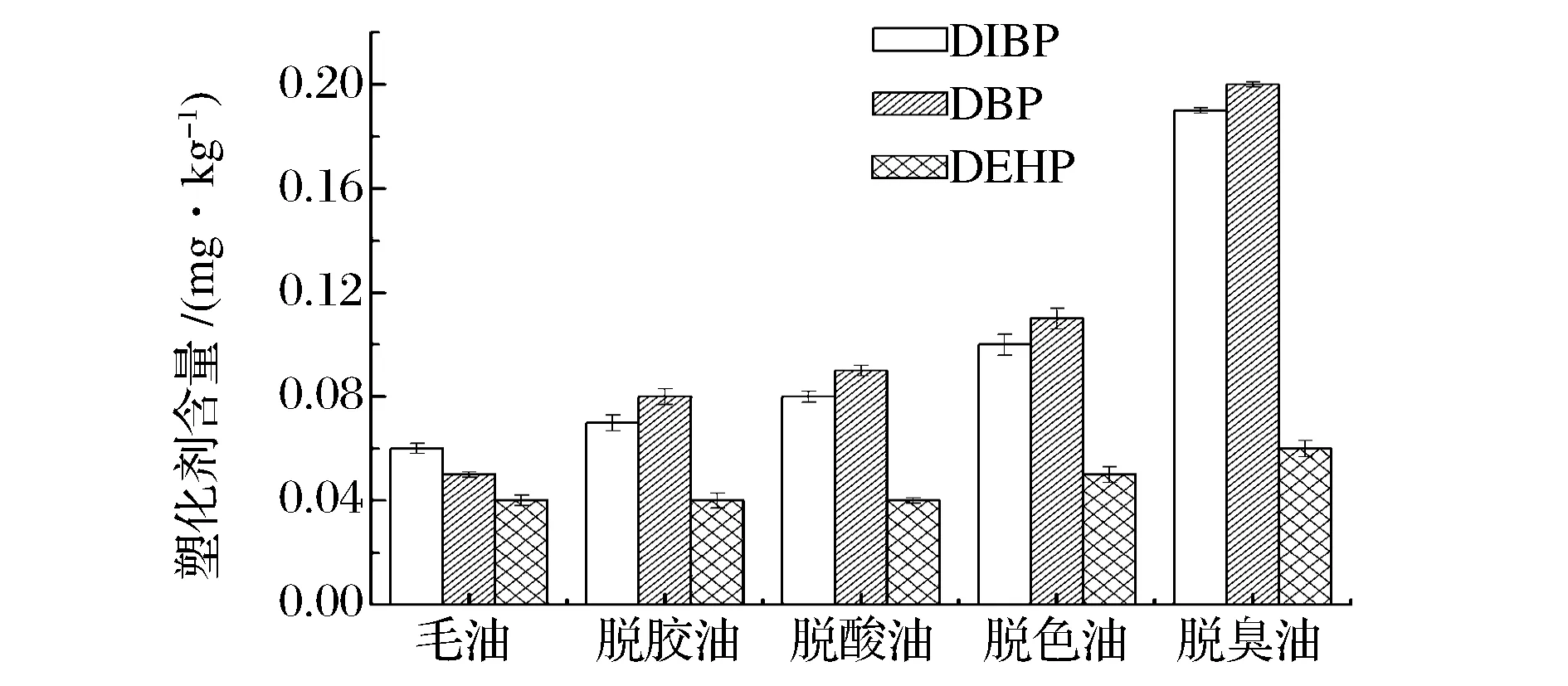
图4 3种塑化剂在鱼油精炼过程中的变化规律Fig.4 The variation of 3 PAEs during fish oil refining process
FARHOODI[14]等进行了DEHP从PET瓶迁移至酸奶的研究,结果表明,DEHP的迁移量与多种因素有关,包括化合物的分子质量,在溶液中的溶解度,温度等,其中温度对迁移的影响较大。曹九超[15]等发表的关于塑化剂的污染途径的综述也提到食用油在加工过程中不可避免地会接触到一些塑料设备,接触过程中塑料中的塑化剂会溶入食用油中,使食用油被塑化剂污染。在食用油制取和精炼过程中用到的化学助剂也有可能使食用油被塑化剂污染,如油脂浸出时所用溶剂正己烷,生产正己烷时接触塑料,然后再用其来提取油脂,从而将塑化剂引入食用油中。因此,要确保精炼过程中鱼油品质的安全性,必不可少的前提就是必须确保所使用的化学助剂的安全性。
3 结论
本文建立了气相色谱-质谱法测定鱼油中的邻苯二甲酸酯类化合物的方法,研究了其在鱼油精炼过程中的变化规律。结果表明,采用气相色谱-质谱法来测定鱼油中的PAEs,方法简便、快速、有效。与此同时,3种塑化剂在鱼油精炼过程中被检测到,且随着精炼工艺的进行,3种塑化剂的含量呈上升趋势,表明鱼油在精炼过程中受到了塑化剂的污染,而工艺中所使用的化学助剂是造成塑化剂污染的主要因素。因此,在实际的工业生产中,为保证鱼油产品的安全性,就必须保证所使用的化学助剂的安全性,这样才能生产满足人们需求的鱼油。
[1] HE J, LYU R, ZHAN H, et al. Preparation and evaluation of molecularly imprinted solid-phase micro-extraction fibers for selective extraction of phthalates in an aqueous sample[J]. Analytica Chimica Acta, 2010, 674 (1): 53-58.
[2] 王瑞元, 金青哲, 安骏. 塑化剂与粮油制品的安全[J]. 中国油脂, 2013, 38(4):1-4.
[3] CAO X L. Phthalate esters in foods:sources, occurrence, and analytical methods[J]. Comprehensive Reviews in Food Science and Food Safety, 2010, 9(1): 21-43.
[4] WANG S, ZHU H, GE Y, et al. Current status and management of chemical residues in food and ingredients in China[J]. Trends in Food Science & Technology, 2009, 20(9): 425-434.
[5] CINELLI G, AVINO P, NOTARDONATO I, et al. Study of XAD-2 adsorbent for the enrichment of trace levels of phthalate esters in hydroalcoholic food beverages and analysis by gas chromatography coupled with flame ionization and ion-trap mass spectrometry detectors[J]. Food Chemistry, 2014, 146(3): 181-187.
[6] LI J, SU Q, LI K Y, et al. Rapid analysis of phthalates in beverage and alcoholic samples by multi-walled carbon nanotubes/silica reinforced hollow fibre-solid phase microextraction[J]. Food Chemistry, 2013, 141(4): 3 714-3 720.
[7] RASMUSSEN K E, PEDERSEN-BJERGAARD S. Developments in hollow fibre-based, liquid-phase microextraction[J]. TrAC Trends in Analytical Chemistry, 2004, 23(1): 1-10.
[8] 李俊儒, 胡继红, 段琼, 等. 我国邻苯二甲酸酯类检测方法研究进展[J]. 食品与发酵工业, 2014, 40(2): 180-183.
[9] RASMUSSEN K E, PEDERSEN-BJERGAARD Y.Optimization of ultrasound-assisted emulsification microextraction with solidification of floating or ganic droplet followed by high performance liquid chromatography for the analysis of phthalate esters in cosmetic and environmental water samples[J]. Microchemical Journal, 2011, 99(1): 26-33.
[10] 王鹏功, 高明星, 程刚, 等. 气相色谱-质谱法对食用油中 17 种邻苯二甲酸酯的测定[J]. 食品科学, 2012, 33(18): 246-249.
[11] CREXI V T, GRUNENNVALDT F L, DE SOUZA SOARES L A, et al. Deodorisation process variables for croaker (M.furnieri) oil[J]. Food Chemistry, 2009, 114(2): 396-401.
[12] 曹九超. 食用油中邻苯二甲酸酯的测定及其迁移动力学的研究[D]. 无锡:江南大学, 2014.
[13] 柴丽月. 食品及包装材料中邻苯二甲酸酯的检测与迁移规律的初步研究[D]. 南京:南京农业大学, 2008.
[14] FARHOODI M, EMAM-DJOMEH Z, EHSANI M R, et al. Migration of model contaminants (ethylene glycol, DEHA and DEHP) from PET bottles into Iranian yogurt drink[J]. e-Polymers, 2008, 8(1): 418-426.
[15] 曹九超, 金青哲. 食用油中塑化剂的污染途径及分析方法的研究进展[J]. 中国油脂, 2013, 38(5): 1-5.
Studies on the analysis and variation of phthalic acid esters in fish oil refining process
ZHANG Jian-you, FEI Xiao-wen, LIU Jian-hua, DING Yu-ting*
(College of Ocean, Zhejiang University of Technology, Hangzhou 310014, China)
A gas chromatography - mass spectrometric method was developed for simultaneous determination of sixteen phthalic acid esters (phthalate acid esters, PAEs) in fish oil. The variation of PAEs in fish oil refining process was stuided. The results indicated that 16 PAEs were separated completely within 20 mins, the calibration curves of 16 PAEs were linear within the range from 0.05 to 1.0 μg/mL (R2>0.998 3). The recovery experiments indicated that recovery rate was from 82.1% to 107.4%, the relative standard deviation was between 0.8% to 12.9%. The limits of detection in GC-MS were between 0.08 to 0.30 mg/kg. At the same time, 3 PAEs (DIBP, DBP and DEHP) were detected in crude oil with content of 0.06 mg/kg, 0.05 mg/kg and 0.04 mg/kg, and increased with the refining process. The content in refined oil were 0.19 mg/kg, 0.24 mg/kg and 0.06 mg/kg. Industrial additives used in the refining process were the main pollution sources of PAEs.
fish oil; phthalate acid esters; PAEs; GC-MS
10.13995/j.cnki.11-1802/ts.201610028
博士,副教授(丁玉庭教授为通讯作者)。
2016-03-02,改回日期:2016-03-29

