阿拉伯树胶修饰的纳米Ru-Zn催化剂上苯选择加氢制环己烯
孙海杰 陈建军 黄振旭 刘仲毅*, 刘寿长
(1郑州师范学院化学化工学院,环境与催化工程研究所,郑州450044) (2郑州大学化学与分子工程学院,郑州450001)
阿拉伯树胶修饰的纳米Ru-Zn催化剂上苯选择加氢制环己烯
孙海杰*,1陈建军2黄振旭1刘仲毅*,2刘寿长2
(1郑州师范学院化学化工学院,环境与催化工程研究所,郑州450044) (2郑州大学化学与分子工程学院,郑州450001)
用共沉淀法制备了纳米Ru-Zn催化剂,考察了阿拉伯树胶修饰对苯选择加氢制环己烯催化剂性能的影响,并用X射线衍射(XRD)、透射电镜(TEM)、N2-物理吸附、X射线光电能谱(XPS)和X射线荧光光谱(XRF)等手段对催化剂进行了表征。结果表明,阿拉伯树胶的用量可以调变Ru-Zn催化剂的粒径。最高环己烯收率随粒径的增大呈火山型变化趋势。当阿拉伯树胶与RuCl3·xH2O的质量比为0.033时,Ru-Zn催化剂的最佳粒径为4.0 nm,最高环己烯收率达59.6%。且该催化剂具有良好的重复使用性能。
苯;选择加氢;环己烯;阿拉伯树胶;钌;锌
化学工业的可持续发展要以绿色化学为基础,目标是“从源头上根除污染”。由苯出发经环己烯制备尼龙6、尼龙66、聚酰胺和聚酯具有安全、节能、碳原子经济和三废近零排放等特点[1-5]。然而苯选择加氢制环己烯是热力学上不利的反应。因此,研发高环己烯选择性催化剂从动力学上克服这一难题是该技术的核心[6-10]。
向反应体系中添加有机反应修饰剂是提高Ru基催化剂环己烯选择性的主要途径之一。Struijk等[11]发现甲醇作反应修饰剂可以提高Ru催化剂的环己烯收率,环己烯最高收率可达8%左右。Spinacé等[12]发现乙二醇作反应修饰剂可以显著提高Ru/ SiO2催化剂的环己烯收率,环己烯最高收率可达19%。Fan等[13]发现乙二胺和ZnSO4作反应修饰剂可以显著提高Ru-Co-B/γ-Al2O3催化剂的环己烯收率,环己烯最高收率可达34.8%。Sun等[14]发现二乙醇胺和ZnSO4作反应修饰剂可以显著提高Ru-Zn催化剂的环己烯收率,环己烯最高收率可达63.6%。他们还发现聚乙二醇-10000和ZnSO4作反应修饰剂可以显著提高Ru-Zn催化剂的环己烯收率,环己烯最高收率可达64.5%[15]。以上有机反应修饰剂都含有N和O等元素,原因是:一方面,这些元素都含有孤电子对,可以与环己烯的双键上的氢形成氢键,稳定中间产物环己烯,提高环己烯收率;另一方面,它们还可以与水分子形成氢键,增加催化剂的表面的亲水性,使生成的环己烯从催化剂表面加速脱附,并抑制脱附的环己烯再吸附到催化剂表面进而加氢生成环己烷,提高环己烯的收率。
Scheme 1
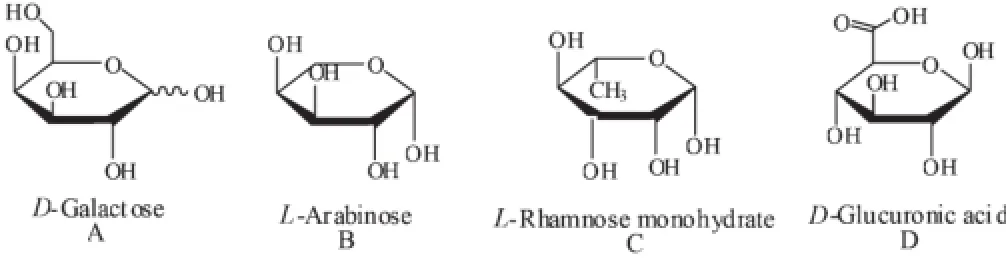
水溶性聚合物修饰纳米颗粒是优化制备纳米颗粒最有效的手段,可以制备出小尺寸、近单层分散、形貌可控的纳米颗粒[16]。阿拉伯胶(Scheme 1)是由D-半乳糖(式A)、L-阿拉伯糖(式B)、L-鼠李糖(式C)和D-葡萄糖醛酸(式D)等单体组成的一种弱酸性大分子多糖,含有大量的羟基。因此,阿拉伯树胶是修饰苯选择加氢制环己烯Ru基催化剂理想的天然水溶性聚合物大分子材料。本文首次将阿拉伯树胶用于修饰Ru基催化剂,并考察了阿拉伯树胶修饰对苯选择制环己烯Ru基催化剂结构和性能的影响。
1 实验部分
1.1实验试剂
水合三氯化钌(AR)购自昆明贵研铂业股份有限公司;七水合硫酸锌(AR)购自天津市福晨化学试剂厂;阿拉伯树胶粉(AR)购自国药集团化学试剂有限公司;氢氧化钠(GR)、苯(AR)均购自天津市科密欧化学试剂有限公司;二氧化锆自制,具体方法见文献[17]。
1.2催化剂制备
将20.0 g RuCl3·3H2O、4.5 g ZnSO4·3H2O和一定量的阿拉伯树胶溶于200 mL蒸馏水中,搅拌下快速加入质量分数为5%的NaOH溶液200 mL,于80℃下搅拌30 min以沉淀完全。将所得混合液转移至GS-1型哈氏合金反应釜中,在5.0 MPa H2和800 r·min-1搅拌下升温至140℃,还原3 h后取出,用蒸馏水洗涤至中性,即得Ru-Zn催化剂。不同量阿拉伯树胶修饰的Ru-Zn催化剂记作Ru-Zn-x,x为阿拉伯树胶的用量(g)。
1.3催化剂表征
催化剂物相分析在荷兰PAN Nalytical公司的XPert PRO型X射线衍射(XRD)仪上进行.Ni滤光片,滤除Kβ线,Cu Kα射线(λ=0.154 18 nm),管电压40 kV,管电流40 mA,扫描范围5°~90°,扫描步长0.03°。催化剂形貌在日本电子公司的JEOL JEM 2100型透射电子显微镜(TEM)上观察。催化剂中各元素含量分析在德国Bruker公司的S4 Pioneer型X射线荧光仪(XRF)上进行。催化剂织构性质在美国Quantachrome公司的Nova 1000e型物理吸附仪上测试,样品在150℃下真空预处理2 h,于-196℃下N2静态吸附,采用BET(Brunauer-Emmett-Teller)法计算样品的SBET。DFT理论计算采用Gaussian 09程序包中的M06-2X方法,6-31G(d,p)基组。
1.4催化剂评价
催化剂性能评价在山东威海化工机械有限公司生产的GS-1型哈氏合金釜中进行。将2.0 g Ru催化剂,10.0 g分散剂ZrO2、49.2 g反应修饰剂ZnSO4· 7H2O和280 mL水加入反应釜中。在H2压力为5.0 MPa和搅拌速率为800 r·min-1的条件下,升温至150℃后加入140 mL苯,调节转速至1400 r·min-1(以消除外扩散),每隔5 min取样。采用杭州科晓GC-1690型气相色谱仪分析产物(苯、环己烷和环己烯)组成,FID检测器,面积校正归一法计算产物浓度,进而计算苯转化率和环己烯选择性。色谱柱为AT·SE-30(30 m×0.32 mm×0.25 μm),柱箱温度为70℃,进样温度和检测器温度均为210℃,柱前压为0.1 MPa。催化剂循环使用按如下步骤进行:反应后冷却至室温,利用分液漏斗将有机相(包括反应物苯、产物环己烯和环己烷)和反应浆液(包括ZnSO4·7H2O水溶液、催化剂和ZrO2)分离,将反应浆液重新加入高压釜中,其它步骤同上,中间不补加任何物质。n次加氢后的催化剂记作Ru-Zn-x-n。
2 结果与讨论
2.1阿拉伯树胶的修饰作用
图1(a)给出了不同量阿拉伯树胶修饰Ru-Zn催化剂XRD图。所有样品都只出现了六方相金属Ru的特征衍射峰(PDF No.01-070-0274),说明Ru主要以金属态存在。随阿拉伯树胶用量的增加,Ru-Zn催化剂的衍射峰的强度逐渐减弱,根据Scherrer公式计算出粒径分别为5.0、4.1、3.6和3.0 nm,说明阿拉伯树胶调变了催化剂的粒径。所有样品都未出现Zn物种的衍射峰,说明它们的粒径很小或以无定形存在。Sun等[18-19]认为Ru-Zn催化剂中Zn以无定形态的ZnO形式存在。图1(b)给出了加氢后催化剂的XRD图。所有样品都只在2θ=43.9°处出现了微弱的金属Ru特征峰,其它衍射峰都归属于分散剂单斜相ZrO2的特征峰(PDF No.00-024-1165)。这说明加氢后金属Ru被ZrO2分散。Sun等[18-19]认为加氢过程中Ru-Zn催化剂中的ZnO可以与反应修饰剂ZnSO4反应生成(Zn(OH)2)3(ZnSO4)(H2O)5盐,该盐可以自发分散在Ru和ZrO2上。因此,加氢后催化剂的XRD图上也未出现Zn物种特征峰。

图1 不同量阿拉伯树胶修饰Ru-Zn催化剂加氢前后的XRD图Fig.1XRD patterns of Ru-Zn catalysts modified by the different dosages of arabic gum before(a)and after(b)hydrogenation
图2给出了不同阿拉伯树胶修饰Ru-Zn催化剂的TEM照片及粒径分布图。可以看出,所有的样品都为圆形或椭圆形。0、0.25、0.5和0.75 g阿拉伯树胶修饰的Ru-Zn催化剂的粒径主要集中在4.8、4.0、3.5和3.2 nm,与XRD计算结果一致。
表1给出了不同量阿拉伯树胶修饰Ru-Zn催化剂的织构性质、粒径和加氢前后的组成。可以看出,随阿拉伯树胶用量的增加,Ru-Zn催化剂的比表面积和孔容略有增加,孔径呈减小的趋势,Ru-Zn催化剂的粒径逐渐减小。加氢前Ru-Zn催化剂的组成接近,说明阿拉伯树胶修饰不改变催化剂的组成。加氢后Ru-Zn催化剂的组成也近似。然而,加氢后Ru-Zn催化剂的组成比加氢前的略高,说明在加氢过程中反应修饰剂中的部分Zn2+吸附在了催化剂表面上。
图3给出了0.25 g阿拉伯树胶修饰Ru-Zn催化剂表面Ru3p3/2(a)和Zn2p(b)的电子结合能。由图3 (a)可以看出,位于461.2 eV处的谱峰可以归属于Ru3p3/2,说明催化剂表面Ru主要以金属态存在,与XRD结果一致。该值小于文献[20]报道的单金属Ru催化剂的462.2 eV,说明Ru得到了部分电子。由图3(b)可以看出,位于1022.3 eV处的谱峰可以归属于Zn2p3/2,说明催化剂表面Zn主要以+2价存在。该值高于文献[21]报道的+2价Zn的1021.7 eV,说明Zn失去了部分电子。综上所述,Ru-Zn催化剂表面+2价Zn将部分电子转移给了Ru,与文献[18,20]报道一致。
图4给出了不同量阿拉伯树胶修饰Ru-Zn催化剂的苯选择加氢制环己烯性能。可以看出,随阿拉伯树胶用量的增加,催化剂的活性逐渐增加,环己烯选择性和收率先升高而后降低。根据以上表征可知,阿拉伯树胶修饰主要改变了Ru-Zn催化剂的粒径,而粒径是影响Ru-Zn催化剂性能的主要因素。图5给出了Ru-Zn催化剂粒径与环己烯最高收率之间的关系。可以看出,随粒径的增加,最高环己烯收率呈火山型变化趋势。当阿拉伯树胶用量为0.25 g时,Ru-Zn催化剂环己烯最高收率达到了59.6%,这是目前文献[22]报道的最高环己烯收率之一。Bu等[23]也发现Ru-Ba/SBA-15催化剂的粒径与最高环己烯收率存在类似的关系。
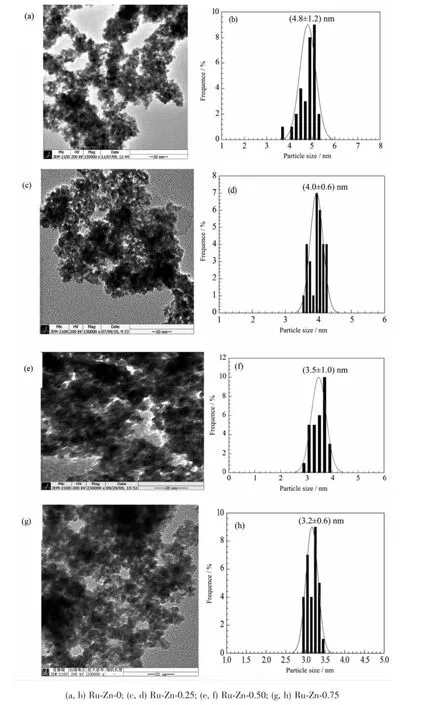
图2 不同量阿拉伯树胶修饰Ru-Zn催化剂的TEM照片及粒径分布图Fig.2TEM images and particle size distribution of Ru-Zn catalysts modified by the different dosages of arabic gum
随阿拉伯树胶用量的增加,Ru-Zn催化剂的粒径逐渐减小,催化剂比表面积逐渐增大,这是Ru-Zn催化剂活性增加的主要原因。巴兰金的多位理论几何适应性可以用来解释Ru-Zn催化剂粒径与环己烯最高收率之间的关系。多位理论几何适应性的主要内容为:对于不同结构的反应基团,就要求与不同活性中心结构的催化剂相适应。目前普遍认可的苯加氢机理为Prasad等[24]提出的两历程反应模型:(1)分步加氢,即苯经由环己二烯、环己烯到环己烷;(2)苯一步加氢生成环己烷。根据多位理论几何适应规则,要发生苯一步加氢生成环己烷,至少需要4个吸附活性位,即1个苯吸附活性位和3个H2分子吸附活性位。4个吸附活性位、1个苯分子和3个H2分子形成活化配合物,进而分解形成环己烷,如图6(a),其中K代表对反应有活性的催化剂原子。而苯选择加氢制环己烯需要3个活性位,即1个苯吸附活性位和2个H2分子吸附活性位。3个吸附活性位、1个苯分子和2个H2分子形成活化配合物,进而分解形成环己烯,如图6(b)。苯分步加氢只需要2个活性位,苯、H2分子和2个活性位先形成活化配合物,分解为环己二烯;环己二烯、H2分子和2个活性位再形成活化配合物,分解为环己烯;环己烯、H2分子和2个活性位又形成活化配合物,分解为环己烷,如图6(c)。较大纳米Ru粒子,含有较多的Ru活性位,可提供较多的四位体,发生苯一步加氢生成环己烷几率大,因此环己烯收率较低。较小的单个纳米Ru粒子,含有较少的活性位,易发生分步加氢。但较小的纳米粒子含有总数最多的表面活性位,环己烯与Ru粒子碰撞、吸附、加氢生成环己烷的几率就大。因此,Ru纳米粒子越小,环己烯的选择性就越低。而只有在粒径合适的纳米Ru粒子上,含有最多的三位体,苯一步加氢生成环己烯几率最大,环己烯收率最高。
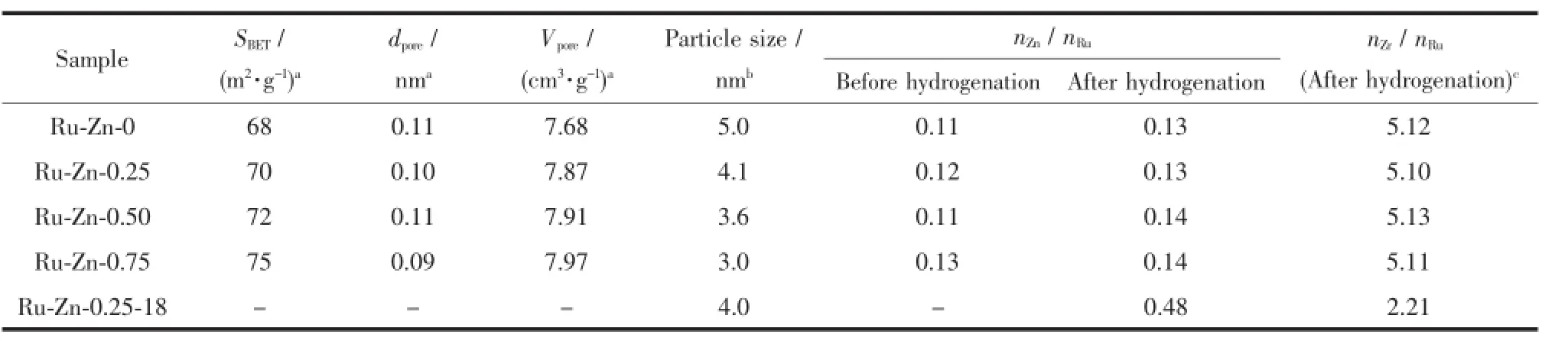
表1 不同样品催化剂的织构性质、粒径和nZn/nRuTable 1Texture properties,particle sizes and nZn/nRuof the different samples
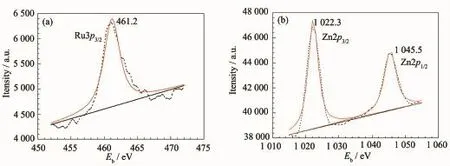
图3 0.25 g阿拉伯树胶修饰Ru-Zn催化剂加氢后的Ru3p3/2(a)和Zn2p(b)的XPS谱图Fig.3XPS spectra of Ru3p3/2(a)and Zn2p(b)of the Ru-Zn catalyst modified by 0.25 g of arabic gum

图4 不同量阿拉伯树胶修饰Ru-Zn催化剂的苯选择加氢制环己烯性能Fig.4Performance of Ru-Zn catalysts modified by the different dosages of arabic gum for the selective hydrogenation of benzene to cyclohexene

图5 Ru-Zn催化剂粒径与环己烯最高收率之间的关系Fig.5Correlation of particle size with the maximum cyclohexene yield
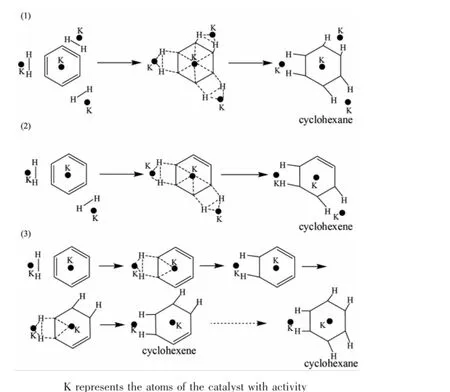
图6 不同多位体活性中心上苯加氢反应机理Fig.6Reaction mechanism of benzene hydrogenation over the active sites of the different multiplet
表面金属Ru与+2价Zn之间的电子作用也是Ru-Zn催化剂表现出高环己烯选择性的重要原因之一。XPS结果表明+2价Zn可以将部分电子转移给金属Ru。富电子Ru有利于苯选择加氢制环己烯,主要归结于以下两方面的原因:(1)Sun等[18]通过DFT方法计算发现苯环碳原子的电子密度低于环己烯上的碳原子。Ru与环己烯之间的静电斥力高于Ru与苯之间的。富电子的Ru有利于环己烯从催化剂表面脱附,并抑制脱附的环己烯再吸附;(2)富电子的Ru不利于环己烯的π电子与Ru空d轨道之间的重叠,不利于环己烯加氢生成环己烷[25]。
此外,吸附在Ru纳米粒子的阿拉伯树胶还可与环己烯分子形成分子间氢键,稳定环己烯分子,提高环己烯收率。图7给出了阿拉伯树胶单体L-阿拉伯糖与环己烯形成的分子间氢键及键长。可以看出,L-阿拉伯糖可以与环己烯形成五元环氢键(如图7(a)),2个氢键的键长分别为0.254 4和0.261 8 nm;它们还可以形成8元环氢键(如图7(b)),2个氢键的键长分别为0.295 7和0.276 9 nm。键长为0.22~0.32 nm的氢键为弱氢键。因此,阿拉伯树胶与环己烯分子之间氢键对环己烯的稳定作用是非常弱的。Struijk等[11]也认为甲醇与环己烯之间的分子间氢键对环己烯稳定作用很弱,键能只有3.7 kJ·mol-1左右。
2.2催化剂循环使用性能
图8给出了0.25 g阿拉伯树胶修饰的Ru-Zn催化剂的循环使用性能。可以看出,前10次循环使用中苯转化率稳定在88%以上,环己烯选择性和收率分别稳定在64%和58%以上。这说明该催化剂具有良好的循环使用性能和稳定性,具有良好的应用前景。从第11次开始,苯转化率和环己烯收率逐渐降低,而环己烯选择性逐渐升高。
为研究催化剂失活的原因,我们对第18次循环使用后的催化剂进行了表征。图9给出了使用18次后0.25 g阿拉伯树胶修饰的Ru-Zn催化剂的TEM图。可以看出,浅灰色的圆形或椭圆形颗粒为ZrO2,粒径为10.0 nm左右。Ru纳米粒子的粒径为3.9 nm,与Ru-Zn催化剂的粒径接近。且Ru纳米颗粒被ZrO2分隔开了,说明ZrO2对Ru纳米粒子起到了分散作用,抑制了在反应过程中催化剂颗粒之间相互碰撞而导致的聚结。这说明了催化剂粒径在反应过程中并未长大。
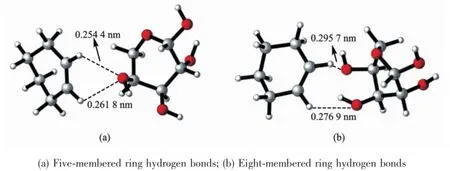
图7 L-阿拉伯糖与环己烯形成的氢键Fig.7Hydrogen bonds formed between L-Arabinose and cyclohexene
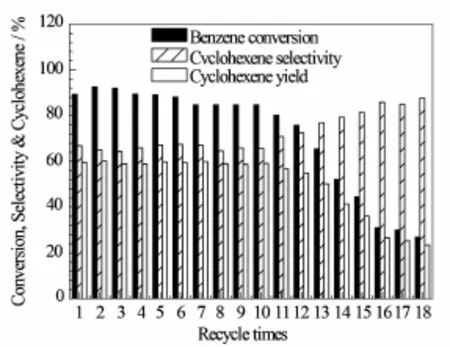
图8 Ru-Zn-0.25催化剂的循环使用性能Fig.8Reusability of the Ru-Zn-0.25 catalyst
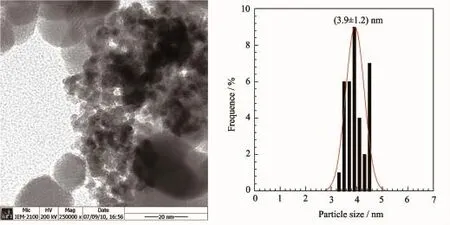
图9 Ru-Zn-0.25-18催化剂的TEM照片(a)和粒径分布图(b)Fig.9TEM image(a)and particle size distribution(b)of the Ru-Zn-0.25-18 catalyst
图10给出了0.25 g阿拉伯树胶修饰Ru-Zn催化剂、分散剂ZrO2、第1次加氢后和第18次加氢后Ru-Zn催化剂的XRD图。第1次加氢后催化剂样品只在2θ=43.9°处出现了微弱的金属Ru的特征峰,同样说明了分散剂ZrO2将金属Ru分散成了很小的颗粒。第18次加氢后催化剂样品上出现了金属Ru特征峰,利用Scherrer公式计算出粒径为4.0 nm,与TEM结果一致。ZrO2特征衍射峰减弱。XRF元素分析结果(表1)表明第18次加氢后催化剂的Zr与Ru原子比为2.21,比第1次加氢后的5.10小,说明在加氢过程中分散剂ZrO2流失较多。第18次加氢后催化剂上还出现了(Zn(OH)2)3(ZnSO4)(H2O)5(PDF No. 01-078-0246)和(Zn(OH)2)3(ZnSO4)(H2O)0.5(PDF No.00-044-0674)的特征峰,说明在加氢过程中Zn2+水解生成了(Zn(OH)2)3(ZnSO4)(H2O)x(x=5或0.5)并吸附在了催化剂表面上。表1中XRF元素分析结果也显示第18次加氢后催化剂的Zn与Ru原子比(0.48)比第1次加氢后的(0.13)明显高,也说明有大量的Zn2+吸附在了催化剂表面上。Sun等[26]也认为Zn2+水解可以生成(Zn(OH)2)3(ZnSO4)(H2O)x盐。他们还认为化学吸附在催化剂表面的(Zn(OH)2)3(ZnSO4)(H2O)x盐可以降低催化剂的活性,提高环己烯的选择性[18,26-28]。因此,化学吸附在催化剂表面大量的(Zn(OH)2)3(ZnSO4)(H2O)x盐是导致催化剂活性降低,环己烯选择性升高的主要原因。图11给出了补加0.5 g催化剂、6.0 g ZrO2和0.8 g浓H2SO4(以溶解吸附的(Zn(OH)2)3(ZnSO4) (H2O)x盐)后第19次催化剂加氢性能。可以看出,催化剂活性和环己烯选择性几乎与催化剂第1次循环的接近,环己烯收率达到了58.9%,说明催化剂性能恢复。

图10 不同样品加氢前后的XRD图Fig.10XRD patterns of the different samples before and after hydrogenation

图11 第1次和第19次循环使用中Ru-Zn-0.25催化剂性能Fig.11Performance of the Ru-Zn-0.15 catalyst in the 1st recycle and the 19th recycle
3 结论
利用阿拉伯树胶制备了不同粒径的Ru-Zn催化剂。随粒径减小,催化剂活性增加,最高环己烯收率呈火山型变化趋势。当阿拉伯树胶用量为0.25 g时,Ru-Zn催化剂最佳粒径为4.0 nm,环己烯最高收率达到了59.6%。因为该粒径的催化剂上可能含有较多适宜苯直接加氢生成环己烯的三位体。该催化剂重复使用10次,催化剂活性和环己烯选择性没有明显衰减。10次后,由于不可避免的催化剂损失和化学吸附在催化剂表面大量的(Zn(OH)2)3(ZnSO4)(H2O)x盐,催化剂活性逐渐降低,环己烯选择性逐渐升高。但通过补加催化剂和添加H2SO4的方法可以使催化剂活性和环己烯选择性恢复。
[1]Liao H G,Ouyang D H,Zhang J,et al.Chem.Eng.J.,2014, 243:207-216
[2]WANG Zheng-Bao(王正宝),ZHANG Qi(张琪),LU Xiao-Fei (路晓飞),et al.Chinese J.Catal.(催化学报),2015,36(3): 400-407
[3]SUN Hai-Jie(孙海杰),ZHOU Xiao-Li(周小莉),ZHAO Ai-Juan(赵爱娟),et al.Chinese J.Inorg.Chem.(无机化学学报),2015,31(7):1287-1295
[4]Zhang P,Wu T B,Jiang T,et al.Green Chem.,2013,15: 152-159
[5]ZHANG Ye(张晔),FU Hai-Yan(付海燕),LI Rui-Xiang (李瑞祥),et al.Chinese J.Inorg.Chem.(无机化学学报), 2013,29(3):577-582
[6]WEI Jun-Fang(魏珺芳),WANG Yan-Ji(王延吉),LI Juan (励娟),et al.Chinese J.Inorg.Chem.(无机化学学报), 2011,27(5):850-854
[7]Ning J B,Xu J,Liu J,et al.Catal.Lett.,2006,109:175-180
[8]SUN Hai-Jie(孙海杰),LI Shuai-Hui(李帅辉),TIAN Xiang-Yu(田翔宇),et al.J.Mol.Catal.(China)(分子催化), 2013,27(4):362-370
[9]SUN Hai-Jie(孙海杰),JIANG Hou-bin(江厚兵),LI Shuai-Hui(李帅辉),et al.Chinese J.Catal.(催化学报),2013,34(4): 684-694
[10]SUN Hai-Jie(孙海杰),LI Shuai-Hui(李帅辉),ZHANG Yuan-Xin(张元馨),et al.Chinese J.Catal.(催化学报), 2013,34(8):1482-1488
[11]Struijk J,Scholten J J F.Appl.Catal.A:Gen.,1992,82:277-287
[12]Spinacé E V,Vaz J M.Catal.Commun.,2003,4:91-96
[13]Fan G Y,Li R X,Li X J,et al.Catal.Commun.2008,9: 1394-1397
[14]SUN Hai-Jie(孙海杰),PAN Ya-Jie(潘雅洁),WANG Hong-Xia(王红霞),et al.Chinese J.Catal.(催化学报),2012,33(4): 610-620
[15]Sun H J,Jiang H B,Li S H,et al.Chem.Eng.J.,2013,218: 415-424
[16]HUANG Xin(黄鑫),ZHANG Hui(张慧),LIANG Li-Yun (梁丽芸).Prog.Chem.(化学进展),2010,22(5):953-961
[17]LIU Zhong-Yi(刘仲毅),SUN Hai-Jie(孙海杰),WANG Dong-Bin(王栋斌),et al.Chinese J.Catal.(催化学报),2010,31 (2):150-152
[18]Sun H J,Wang H X,Jiang H B,et al.Appl.Catal.A:Gen., 2013,450:160-168
[19]SUN Hai-Jie(孙海杰),ZHANG Xu-Dong(张旭东),CHEN Zhi-Hao(陈志浩),et al.Chinese J.Catal.(催化学报),2011, 32(2):224-230
[20]SUN Hai-Jie(孙海杰),LI Yong-Yu(李永宇),LI Shuai-hui (李帅辉),et al.Acta Phys.-Chim.Sin.(物理化学学报), 2014,30(7):1332-1340
[21]CHEN Xi(陈熙),LI Li(李莉),ZHANG Wen-Zhi(张文治), et al.Chinese J.Inorg.Chem.(无机化学学报),2015,31(10): 1971-1980
[22]Liu J L,Zhu Y,Liu J,et al.J.Catal.,2009,268:100-105
[23]Bu J,Liu J L,Chen X Y,et al.Catal.Commun.,2008,9: 2612-2615
[24]Prasad K H V,Prasad K B S,Mallikarjunan M M,et al.J. Catal.,32:1-16
[25]Liu J L,Zhu L J,Pei Y,et al.Appl.Catal.A:Gen.,2009, 353:383-287
[26]Sun H J,Pan Y J,Jiang H B,et al.Appl.Catal.A:Gen., 2013,464-465:1-9
[27]Sun H J,Pan Y J,Li S H,et al.J.Energy Chem.,2013,22: 710-716
[28]Su H J,Chen L X,Li S H,et al.J.Rare Earths,2013,31: 1023-1028
Selective Hydrogenation of Benzene to Cyclohexene over the Nano-Sized Ru-Zn Catalyst Modified by Arabic Gum
SUN Hai-Jie*,1CHEN Jian-Jun1HUANG Zhen-Xu1LIU Zhong-Yi*,2LIU Shou-Chang2
(1Institute of Environmental and Catalytic Engineering,Department of Chemistry,Zhengzhou Normal University, Zhengzhou 450044,China) (2College of Chemistry and Molecular Engineering,Zhengzhou University,Zhengzhou 450001,China)
A nano-sized Ru-Zn catalyst was prepared by a co-precipitation method and the effect of arabic gum modification on the performance of Ru-Zn catalysts was investigated.The catalysts were characterized by X-ray diffraction(XRD),transimission electron microscopy(TEM),N2physisorption,X-ray photoelectron spectroscopy (XPS),and X-ray fluorescence(XRF).It was found that the dosage of arabic gum could tune the particle size of the Ru-Zn catalysts.The maximum cyclohexene yield showed a volcanic-type variation tendency with the particle size of Ru-Zn catalysts increasing.When the mass ratio of arabic gum to RuCl3·xH2O was 0.033,a Ru-Zn catalyst with a optimum particle size of 4.0 nm was obtained,and a maximum cyclohexene yield of 59.6%was achieved. Moreover,the catalyst exhibited the excellent reusability.
benzene;selective hydrogenation;cyclohexene;arabic gum;Ru;Zn
O614.24+1;O614.82+1
A
1001-4861(2016)02-0202-09
10.11862/CJIC.2016.019
2015-08-08。收修改稿日期:2015-11-10。
国家自然科学基金(No.21273205,U1304204)、河南省高等学校重点科研项目(No.16A150025)和河南省博士后科研项目(No.2013006)资助。
*通信联系人。E-mail:sunhaijie406@163.com;liuzhongyi@zzu.edu.cn;会员登记号:S06N9580M1403(孙海杰),S06N7911M1205(刘仲毅)。
——树胶印法(gum print)与其在水彩画中的部分应用

