水溶液中痕量Cu2+离子的EDI富集
管 山,雷 航,刘 玥
(天津工业大学环境与化学工程学院,天津 300387)
水溶液中痕量Cu2+离子的EDI富集
管 山,雷 航,刘 玥
(天津工业大学环境与化学工程学院,天津 300387)
为了快速、连续地测定水溶液中的痕量重金属离子,研究了原水连续、浓水循环的EDI过程,对原水质量浓度为0.01~1 mg/L Cu2+溶液进行了富集.以离子平衡为依据,对进料流量、进料浓度和操作电流等因素对富集倍数的影响和稳定时间进行了考察.结果表明:EDI在工作电流为190 mA、原水流量为60 mL/min的条件下运行,可将Cu2+富集189倍,稳定时间为105 min.通过对实验数据的拟合,得到了原水浓度和浓缩液浓度的对应关系,相关系数为0.993 5.
电去离子(EDL);富集;Cu离子
在环境和生产中,由于废水中重金属离子浓度含量较低,需要对痕量重金属离子进行快速、连续的富集.传统的水处理方法有很多,如离子交换法(IX)、固相萃取(SPE)、吸附等.这些技术已被广泛应用于溶液中重金属离子的分析[1-4],但这些方法都不同程度地存在着成本高、能耗高、易产生二次污染等缺点[5].电去离子(EDI)作为一种新型富集分离技术具有很多优点,如操作方便、降低设备成本和减少运行时间.EDI有相对高的富集因子,可以富集水中的痕量重金属离子.此外,该技术具有较高的处理容量且无需化学再生,从而避免了化学试剂二次污染[6-12].近年来,已有研究者尝试将EDI用于低浓度重金属废水的处理,并取得了一定的效果[13-15].此前的研究采用了较大的膜面积(37.8 cm2),平衡时间较长约为150min,并考察了原水质量浓度为0.1mg/L的Cu2+离子溶液中膜堆电流、淡水流量、浓水流量、电极水流量等因素对EDI膜堆富集倍数的影响[16].为了缩短平衡时间,本文减小膜堆有效膜面积,并以0.01~1 mg/L Cu2+离子溶液作为原水,采用EDI富集水溶液中的Cu2+离子,考察进料流量、操作电流和进料浓度对Cu2+富集倍数的影响,为开发痕量离子连续富集的EDI过程提供理论和实验支持.
1 实验部分
1.1 材料与设备
所用材料包括:低渗透异相阴阳离子交换膜,上海上化水处理材料有限公司产品;强酸强碱性凝胶型离子交换树脂,南开大学化工厂产品;Cu2+原液,100 mg/L,由CuSO4·5H2O溶解在适量去离子水中配制而成;实验中所使用的水均为自制的去离子水.
所用仪器包括:EDI膜堆,自制;数字电导率仪,石家庄科达仪表研究所产品;数字电阻率仪,上海诚磁电子有限公司产品;T6型紫外分光光度计,北京普析通用仪器有限公司产品.
1.2 实验装置与流程
实验装置与流程如图1所示.实验采用的膜堆内部构造如图2所示.

图1 实验装置示意图Fig.1 Schematic diagram of experiments

图2 膜堆内部构造图Fig.2 Inner cell configuration of EDI module
膜堆主要由阳极室、阴极室、淡化室及2个浓缩室构成.这些隔室由隔板隔开,有效膜面积为21cm2.阳极和阴极室分别填充了100%的阳离子交换树脂和阴离子交换树脂,以增强传质性和导电性.淡化室内填充了按3∶2均匀混合的阳离子与阴离子交换树脂,进行离子的传递作用和交换作用.在浓缩室内各加入2层丝网,改善浓室内部的流体流动状况以强化传质.原水为Cu2+溶液,由Cu2+原液稀释而成,质量浓度为0.01~1.00 mg/L,流量为20~60 mL/min;浓水采用闭路循环,初始循环液为pH=2的硫酸溶液,循环流量为20 mL/min;电极水为pH=2的硫酸溶液,流量为15 mL/min,从负极流向正极.实验通过变化原水流量、工作电流和原水浓度3个参数来观察Cu2+富集倍数的变化.
1.3 水质分析
淡水进出水分别采用电导率仪与电阻率仪进行在线监测.Cu2+离子浓度的测定采用2,9-二甲基-1,10-菲啰啉分光光度法,采用紫外分光光度计在波长为457 nm下进行测定.为了评价铜离子的富集程度,将富集倍数(电子)定义为:

式中:Cc,out为浓水中出水的Cu2+浓度;Cd,in为淡水中进水的Cu2+浓度.
2 结果与讨论
2.1 膜堆的稳定状态
为了分析膜堆的稳定状态,确定实验的稳定时间,Cu2+的质量浓度表示膜堆在某一条件下Cu2+的富集程度,被定义为:

式中:Qin为原水进水流量;Nc为浓水获得的Cu2+含量;Nr为原水中的Cu2+含量.Nc和Nr被定义如下:

式中:Cc和Qc分别为浓溶液中Cu2+的质量浓度(mg/L)和流量(mL/min);Cd、Qd分别为原水中Cu2+的质量浓度(mg/L)和流量(mL/min);in和out分别代表水流输入口和输出口;C代表膜堆对Cu2+的富集程度.在电流190 mA、原水流量60 mL/min时不同原水浓度条件下C随时间的变化如图3所示.

图3 不同原水浓度下Cu2+的浓度Fig.3 Cu2+concentration at different feed concentrations
由图3可以看出,实验开始时,C急剧增加;随着运行时间变长,C减缓增长,并在105 min左右达到一个相对稳定的值.初始阶段,Cu2+在电场作用下定向迁移至浓缩室,浓水中Cu2+浓度不断上升.膜堆平衡后,树脂为盐型,没有额外的Cu2+进入浓水.因此,在平衡时间后,进入浓缩室的Cu2+离子与淡水中脱除的Cu2+保持平衡.在平衡时间取样不会影响富集倍数的准确性.
2.2 原水与浓缩液浓度关系
图4所示为在105 min时,电流190 mA,原水流量60 mL/min条件下原水浓度和浓水浓度的关系.

图4 原水浓度与浓水浓度的关系Fig.4 Relationship of feed concentration and concentrated concentration
由图4可以看出,原水浓度和浓水浓度呈良好的线性关系,线性回归方程为Y=68.258X+8.163 8(X为原水中Cu2+质量浓度,Y为浓水中Cu2+质量浓度),线性相关系数为0.993 5.利用此关系可以准确地由富集后的溶液推算原始溶液浓度.
2.3 原水流量的影响
实验原水使用0.05 mg/L的铜离子溶液,分别选取60、140、200 mA作为工作电流,对原水流量范围为20~60 mL/min下的铜离子富集因子进行考察,结果如图5所示.
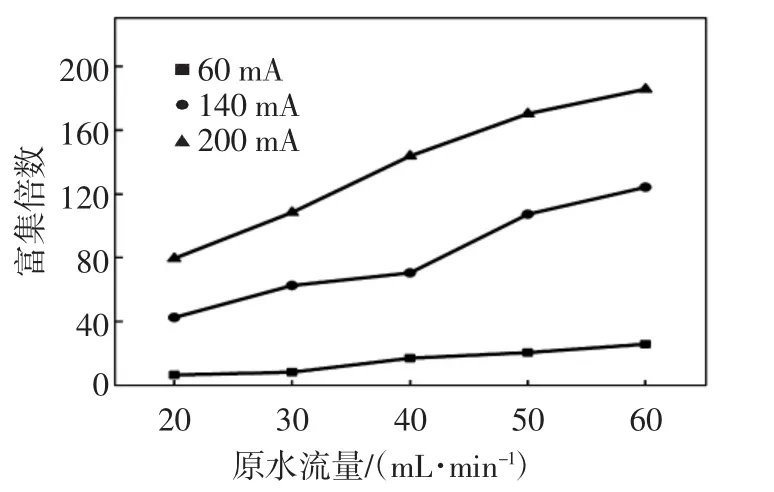
图5 不同工作电流下富集倍数与原水流量的关系Fig.5 Relationship of Cu2+enrichment factor and feed flow rate at different operating currents
由图5可以看出,随着流量增大,在低电流下电流富集倍数仅略有增加,高电流时富集因子急剧增加.当硫酸铜溶液进入淡化室,溶液中Cu2+被树脂吸附,在直流电场作用下进行定向迁移,进入浓缩室.当流量提高时,大量的铜离子会进入浓缩室,导致富集因子的增加.根据实验结果,适当的提高原水流量有利于Cu2+富集.但是当原水流量继续增大时,膜堆内部的压强也变大、扩散加快、透水量增多.因此,实验中选取60 mL/min作为原水流量.
2.4 操作电流的影响
当含有0.05 mg/L的Cu2+原液流速为60 mL/min时,富集倍数和工作电流之间的关系如图6所示.
由图6可以看出,当操作电流从65 mA上升至190 mA时,富集倍数随之增大;当高于190 mA时,Cu2+富集倍数保持在一个相对稳定的值.当电流低于190 mA时,离子传递的驱动力不足,部分离子仍留在淡化室,因此,富集倍数低.随着电流的增大,Cu2+的迁移率和树脂再生增强,导致更多Cu2+进入浓缩室[17-19].在190 mA时,富集因子达到189,吸附在离子交换树脂上的离子的量与从树脂再生的离子的量保持平衡,淡化室中的离子几乎都被传递,浓溶液的浓度趋于稳定.然而,如果电流超过限值,膜堆中的水解程度加剧,从电极反应中产生过多的氢离子迁移到浓缩室,导致电流效率降低[20].因此,190 mA是进出离子达到平衡的最低电流.

图6 富集倍数随工作电流的变化Fig.6 Changes of Cu2+enrichment factor with operating currents
2.5 原水浓度的影响
图7所示为在电流恒定在190 mA、原水流量为60 mL/min时,不同原水浓度条件下Cu2+的富集倍数随原水浓度的变化曲线.

图7 富集倍数随原水浓度的变化Fig.7 Enrichment factor of Cu2+ions at different feed concentrations
由图7可知,随着原水中Cu2+浓度增大,Cu2+的富集倍数减小.当原水中Cu2+浓度较低时,膜堆负荷较小,树脂电再生和水解离作用明显,加强了对Cu2+的富集.随着原水中Cu2+离子增加,树脂电再生和水解离作用减弱,Cu2+脱除率降低,因此富集倍数减小.当原水中离子浓度过高时,由于其电导率与树脂电导率差别不大,有部分离子不经过离子交换树脂相,直接通过树脂缝隙间的溶液相进行传递,没有经过膜堆的富集导致富集倍数降低.因此,原水中所含的Cu2+浓度不宜过高.
3 结论
本实验考察了工作电流、原水流量及原水浓度对EDI过程中Cu2+富集倍数的影响.实验结果表明,适当的提高原水流量,适宜的电流及较低的原水离子浓度有利于膜堆对Cu2+的富集.通过优化操作条件,在工作电流为190 mA,原水流量为60 mL/min的条件下,运行105 min后,利用EDI可以将质量浓度0.05 mg/L Cu2+溶液富集到189倍,浓水中Cu2+浓度达到9.45 mg/L.浓缩液浓度与原水浓度可呈良好的线性关系由此可以准确的确定原水中的Cu2+浓度.证实了EDI对水溶液中痕量Cu2+离子富集效果显著,可实现高效、连续的测定痕量Cu2+.虽然EDI过程中存在着不够稳定等问题,但从本文实验结果可以看出,EDI有望成为一种有良好前景的重金属离子富集方法.
[1]PYRZYNSKA K,TROJANOWIC Z M.Functionalized cellulose sorbents for preconcentration of trace metals in environmental analysis[J].Critical Reviews in Analytical Chemistry,1999,29(4):313-321.
[2]ANTHEMIDIS A N,ZACHARIADIS G A,STRATIS J A.On
line solid phase extraction system using PTFE packed column for the flame atomic absorption spectrometric determination of copper in water samples[J].Talanta,2001,54(5):935-942.
[3]DABROWSKI A,HUBICKI Z,PODKOSCIELNY P.Selective removal of the heavy metal ions from waters and industrial wastewaters by ion-exchange method[J].Chemosphere,2004,56(2):91-106.
[4]GHASE M I,JAHAN B,ZOLFONOUN E.Simultaneous spectrophotometric determination of trace amounts of uranium,thorium,and zirconium using the partial least squares method after their preconcentration by alpha-benzoin oxime modified Amberlite XAD-2000 resin[J].Talanta,2010,80(3):1191-1197.
[5]董建.EDI技术处理重金属废水的研究进展[J].化工时刊,2008,22(3):58-61.DONG J.Research progress of heavy metal wast water treatment by electrodeionization technology [J].Chemical Industry Times,2008,22(3):58-61(in Chinese).
[6]SOUILAH O,AKRETCHE D E,AMARA M.Water reuse of an industrial effluent by means of electrodeionisation[J]. Desalnation,2004,167(1/2/3):49-54.
[7]SPOOR P B,GRABOVSKA L,KOENE L,et al.Pilot scale deionisationof a galvanic nickel solution using a hybrid ionexchange/electrodialysis system[J].Chemical Engineering Journal,2002,89(1/2/3):193-202.
[8]SPOOR P B,KOENE L,TERVEEN W R,et al.Continuous deionization of a dilute nickel solution[J].Chemical Engineering Journal,2002,85(2/3):127-135.
[9]SPOOR P B,KOENE L,TERVEEN W R,et al.Electrodeionisation 3:The removal of nickel ions from dilute solutions[J]. Journal of Applied Electrochemistry,2002,32(1):1-10.
[10]GUAN S,WANG S C.Experimental studies on electrodeionization for the removal of copper ions from dilute solutions[J]. Separation Science and Technology,2007,42:949-961.
[11]TAGHDIRIAN H R,MOHEB A,MEHDIPOURGHAZI M. Selective separation of Ni(II)/Co(II)ions from dilute aqueous solutions using continuous electrodeionization in the presence of EDTA[J].Membrane Science and Technology,2010,362(1/2):68-75.
[12]MAHMOUD A,MUHR L,GREVILLOT G,et al.Experimental tests and modelling of an electrodeionization cell for the treatment of dilute copper solutions[J].CanadianJournalofChemical Engineering,2007,85(2):171-179.
[13]SUNG S.Recycling of copper from metal finishing wastewaters using electrodialysis ion exchange[D].Connecticut:University of Connecticut,1997.
[14]SPOOR P B,KOENE L,JANSSEN L J J.Potential and concentration gradients in a hybrid ion-exchange/electrodialysis cell[J].Journal of Applied Electrochemistry,2002,32:369-377.
[15]DZYAZKO Y S,BELYAKOV V N.Purification of a diluted nickel solution containing nickel by a process combining ion exchange ion and electrodialysis[J].Desalination,2004,162:179-189.
[16]杨一超,管山,郭玉高.EDI过程用于低浓度Cu(II)溶液的富集[J].天津工业大学学报,2014,33(5):53-56. YANG Y C,GUAN S,GUO Y G.Enrichment of Cu(II)ions from dilute aqueous solutions using continuous electrodeionization [J].Journal ofTianjin Polytechnic University,2014,33(5):53-56(in Chinese).
[17]FENG X,WU Z,CHEN X.Removal of metal ions from electroplating effluent by EDI process and recycle of purified water[J].Separation and Purification Technology,2007,57:257-263.
[18]DERMENTZIS K.Removal of nickel from electroplating rinse waters using electrostatic shielding electrodialysis/electrodeionization[J].Journal of Hazardous Materials,2010,173(1/2/ 3):647-652.
[19]SONG J H,YEON K H,MOON S H.Transport characteristics of Co2+through an ion exchange textile in a continuous electrodeionization(CEDI)system under electroregeneration[J].Separation Science and Technology,2004,39(15):3601-3619.
[20]MAHMOUD A,MUHR L,VASILUK S,et al.Investigation of transport phenomena in a hybrid ion exchange-electrodialysis system for the removal of copper ions[J].Journal of Applied Electrochemistry,2003,33(10):875-884.
Preconcentration of trace Cu2+in aqueous solution by electrodeionization process
GUAN Shan,LEI Hang,LIU Yue
(School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China)
In order to preconcentrate the trace heavy metal ions in aqueous solution rapidly and continuously,the elec
electrodeionization(EDI);preconcentration;copper ions
X703.1
A
1671-024X(2016)05-0042-04
10.3969/j.issn.1671-024x.2016.05.008
2016-05-23 基金项目:国家自然科学基金资助项目(21416172)
管 山(1969—),男,博士,副教授,硕士生导师,主要研究方向为膜法水处理技术.E-mail:guanshan69@163.com
trodeionization(EDI)processes of continuous feed solutions and cycled concentrated solution were studied,and the concentrations of feed solutions were in the range of 0.01-1 mg/L.Based on the ion balance,the effects of feed flow rate,feed concentration and operating current on enrichment factor and steady time were investigated. The results show that an enrichment factor of 189 was obtained at a constant stack current of 190 mA and a flow rate of 60 mL/min and the steady time is 105 min.Through fitting the experimental data,the relationship between the concentrations of feed and concentrated solutions was constructed with a correlation coefficient of 0.993 5.

