HPLC法同时测定小儿感冒颗粒中4种成分的含量Δ
陈国宝,郑艳萍,严国俊,宋桂萍,柳 佳,蔡 廷(.江阴市中医院,江苏江阴 4400;.南京海昌中药集团有限公司,南京 006;.南京中医药大学药学院,南京 009;4.中国药科大学药学院,南京0009)
HPLC法同时测定小儿感冒颗粒中4种成分的含量Δ
陈国宝1*,郑艳萍2,严国俊3,宋桂萍1,柳佳1,蔡廷4#(1.江阴市中医院,江苏江阴214400;2.南京海昌中药集团有限公司,南京210061;3.南京中医药大学药学院,南京210029;4.中国药科大学药学院,南京210009)
目的:建立同时测定小儿感冒颗粒中(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A含量的方法。方法:采用高效液相色谱法。色谱柱为Hedera C18,流动相为乙腈-0.1%甲酸(梯度洗脱),流速为1.0 ml/min,检测波长为254、330、370 nm,柱温为40℃,进样量为5 μl。结果:(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A的检测质量浓度线性范围分别为6.6~105 μg/ml(r= 0.999 9)、9~140 μg/ml(r=0.999 9)、9~144 μg/ml(r=0.999 8)、9~138 μg/ml(r=0.999 6);定量限分别为330、450、450、450 ng,检测限分别为66、90、90、90 ng;精密度、稳定性、重复性试验的RSD<3%;加样回收率分别为95.01%~98.77%(RSD=1.48%,n=6)、95.14%~98.91%(RSD=1.52%,n=6)、95.11%~97.54%(RSD=0.93%,n=6)、95.58%~99.63%(RSD=1.73%,n= 6)。结论:该方法操作简便、结果准确,适用于测定小儿感冒颗粒中(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A的含量。
小儿感冒颗粒;(R,S)-告依春;绿原酸;木犀草苷;异绿原酸A;高效液相色谱法
小儿感冒颗粒收载于2015年版《中国药典》(一部)中,由广藿香、菊花、板蓝根、大青叶、石膏等10味药物组成[1],具有疏风解毒、清热解毒之功效,可用于治疗小儿风热感冒,发热重、头胀痛,咳嗽痰黏、咽喉肿痛,流感等。木犀草苷、绿原酸和异绿原酸A是菊花中的指标性成分,具有散风清热、平肝明目、清热解毒等药理作用,可用于风热感冒、头痛眩晕、目赤肿痛、眼目昏花、疮痈肿毒等证,有明显的抗炎、解热及肉毒素中和作用[2-3]。(R,S)-告依春是板蓝根抗病毒的有效成分之一,是衡量板蓝根质量的一个重要指标,同时也是反映感冒颗粒质量的重要指标,具有清热解毒、凉血利咽等药理作用,可用于温疫时毒、发热咽痛、温毒发斑、痄腮、烂喉丹痧、大头瘟疫、丹毒、痈肿[4-5]。目前,小儿感冒颗粒的质量标准中载有用薄层色谱法来鉴定大青叶和板蓝根中均含有的靛玉蓝,却并没有控制板蓝根质量的专属标准[6-8]。因此,本课题组采用高效液相色谱法(HPLC)同时测定小儿感冒颗粒中的木犀草苷、绿原酸、异绿原酸A以及(R,S)-告依春的含量,以期为该药的质量控制提供参考。
1 材料
1.1仪器
LC-20AB型HPLC仪,包括二极管阵列检测器(日本Shimadzu公司);FA1104型电子分析天平(上海精密科学仪器有限公司);KQ3200DB型数控超声波清洗器(昆山市超声仪器有限公司,功率:350 W,频率:40 kHz);TGL-16C型离心机(上海安亭科学仪器厂)。
1.2药品与试剂
小儿感冒颗粒(江阴市中医院,编号:S1、S2、S3,规格:6 g/袋);(R,S)-告依春对照品(批号:111753-201103,纯度:100.0%)、异绿原酸A对照品(批号:111782-200801,纯度≥98%)、绿原酸对照品(批号:110753-200413,纯度:96.2%)和木犀草苷对照品(批号:111720-200905,纯度:96.5%)均购自中国食品药品检定研究院;甲醇、乙腈为色谱纯,其余试剂均为分析纯,水为去离子水。
2 方法与结果
2.1色谱条件
色谱柱:Hedera C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%甲酸(B),梯度洗脱(洗脱程序见表1);流速:1.0 ml/min;检测波长:254、330、370 nm;柱温:40℃;进样量:5 μl。
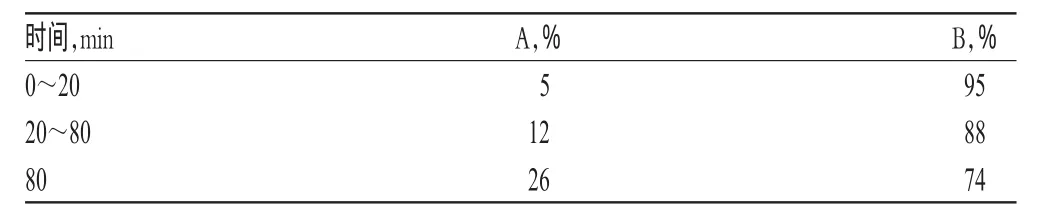
表1 梯度洗脱程序Tab 1 Conditions of gradient elution
2.2溶液的制备
2.2.1混合对照品溶液分别精密称取(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A对照品21.00、7.19、7.46、14.29 mg,分别置于10 ml量瓶中,用甲醇定容,摇匀,即得(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A的质量浓度分别为2.100、0.692、0.720、1.400 mg/ml的单一对照品溶液。分别取上述单一对照品溶液各0.5、1、1、0.5 ml,置于同一5 ml量瓶中,加甲醇定容,即得。
2.2.2供试品溶液精密称取样品5 g,置于50 ml具塞三角瓶中,加甲醇10 ml,称定质量,超声处理30 min,放冷,再次称定质量,用甲醇补足减失的质量,摇匀,置于1.5 ml离心管中,以半径为0.5 cm、12 000 r/min离心10 min,取上清液,经0.45µm微孔滤膜滤过,取续滤液,即得[7]。
2.2.3阴性对照溶液按样品的制备工艺和配方比例,制备不含菊花和板蓝根的阴性样品,再按“2.2.2”项下方法制备阴性对照溶液。
2.3系统适用性和专属性试验
精密量取“2.2”项下混合对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>1.5;理论板数以(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A峰计算均>5 000;保留时间分别为13.90、21.15、47.31、53.59 min。结果表明,其他成分对测定无干扰。
2.4线性关系考察
取“2.2.1”项下混合对照品溶液适量,精密量取4、2、1、0.5、0.25、0.125 ml,分别置于8 ml量瓶中,用甲醇定容,得系列线性溶液。分别取上述系列线性溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以质量浓度(x,μg/ml)为横坐标、峰面积(y)为纵坐标进行线性回归,回归方程与线性范围详见表2。
2.5定量限与检测限考察
取“2.2.1”项下混合对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD),结果详见表3。
2.6精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,计算日内精密度;连续进样测定3 d,计算日间精密度。结果,(R,S)告依春、绿原酸、木犀草苷和异绿原酸A峰面积的日内精密度的RSD分别为0.96%、0.92%、0.60%、0.43%(n=6),日间精密度的RSD分别为0.85%、0.86%、0.45%、0.34%(n=6),表明仪器精密度良好。
2.7稳定性试验
取“2.2.2”项下供试品溶液适量,分别于室温下放置0、2、4、8、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,(R,S)告依春、绿原酸、木犀草苷和异绿原酸A峰面积的RSD分别为2.11%、1.77%、0.85%、1.52%(n=5),表明供试品溶液在室温下12 h内基本稳定。
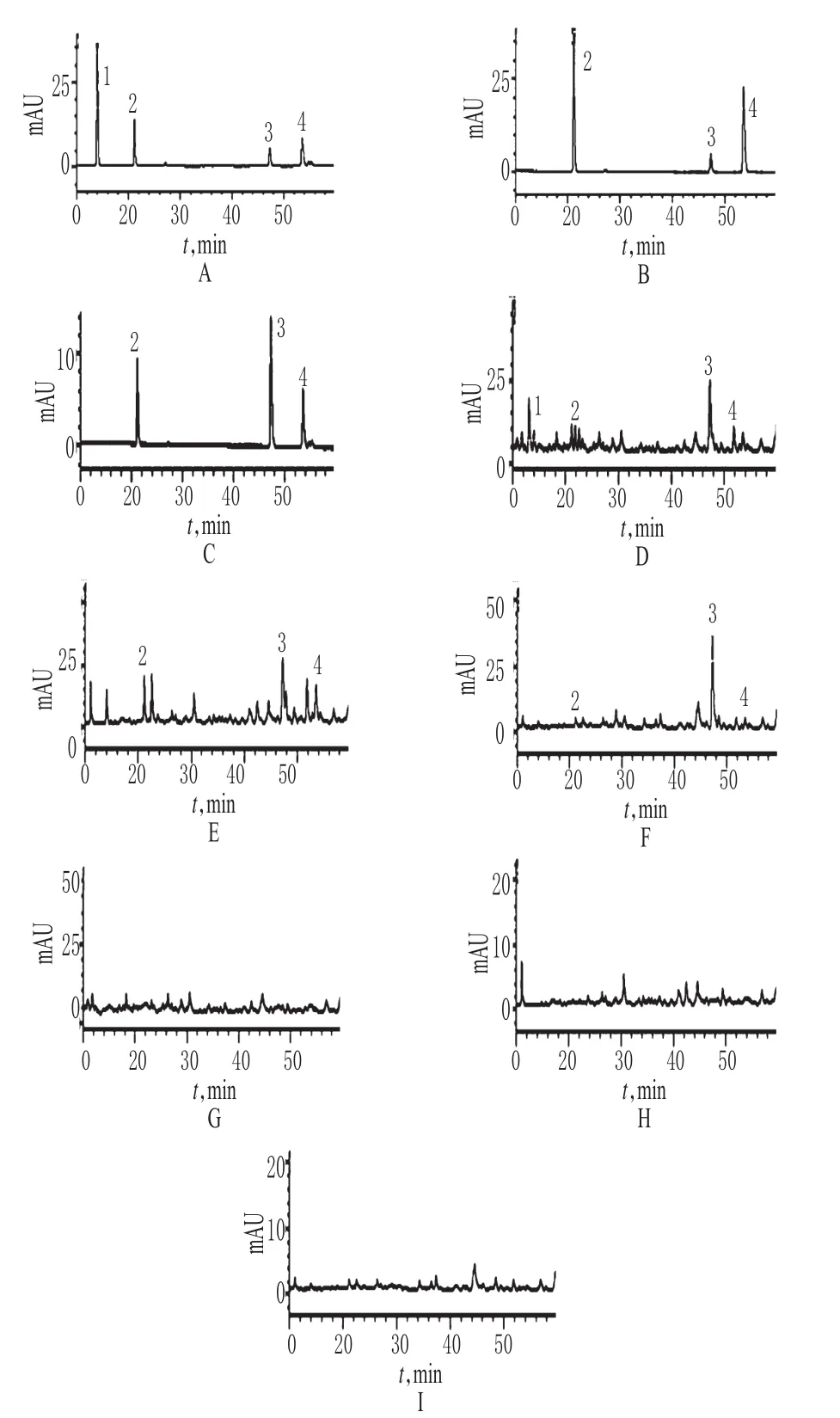
图1 高效液相色谱图A.混合对照品(254 nm);B.混合对照品(330 nm);C.混合对照品(370 nm);D.供试品(254 nm);E.供试品(330 nm);F.供试品(370 nm);G.阴性对照(254 nm);H.阴性对照(330 nm);I.阴性对照(370 nm);1(.R,S)-告依春;2.绿原酸;3.木犀草苷;4.异绿原酸AFig 1 HPLC chromatogramsA.mixed reference substance(254 nm);B.mixed reference substance(330 nm);C.mixed reference substance(370 nm);D.test sample(254 nm);E.test sample(330 nm);F.test sample(370 nm);G.negative control(254 nm);H.negative control(330 nm);I.negative control(370 nm);1.R,S-goitrin;2.chlorogenic acid;3.luteoloside;4.isochlorogenic acidA

表2 回归方程与线性范围Tab 2 Regression equations and linear ranges
2.8重复性试验
取同一批样品(编号:S1)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算含量,结果详见表4。由表4可知,本方法重复性良好。
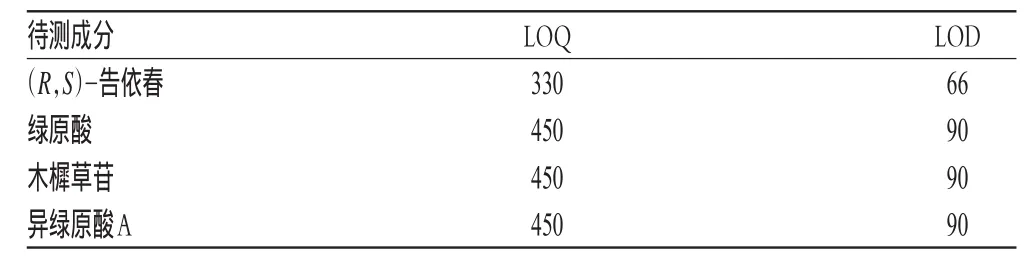
表3 定量限与检测限测定结果(ng)Tab 3 Determination results of quantitation limit and detection limit(ng)
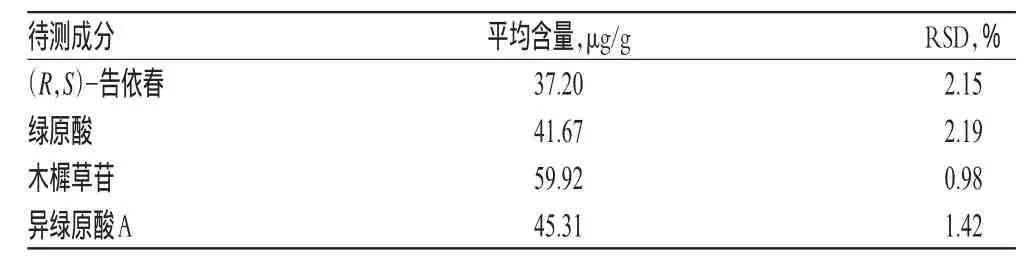
表4 重复性试验结果(n=6)Tab 4 Results of reproducibility tests(n=6)
2.9加样回收率试验
精密称取样品(编号:S1)5 g,置于50 ml具塞三角瓶,再精密加入一定量(R,S)-依春绿原酸、木犀草苷和异绿原酸A对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果详见表5。
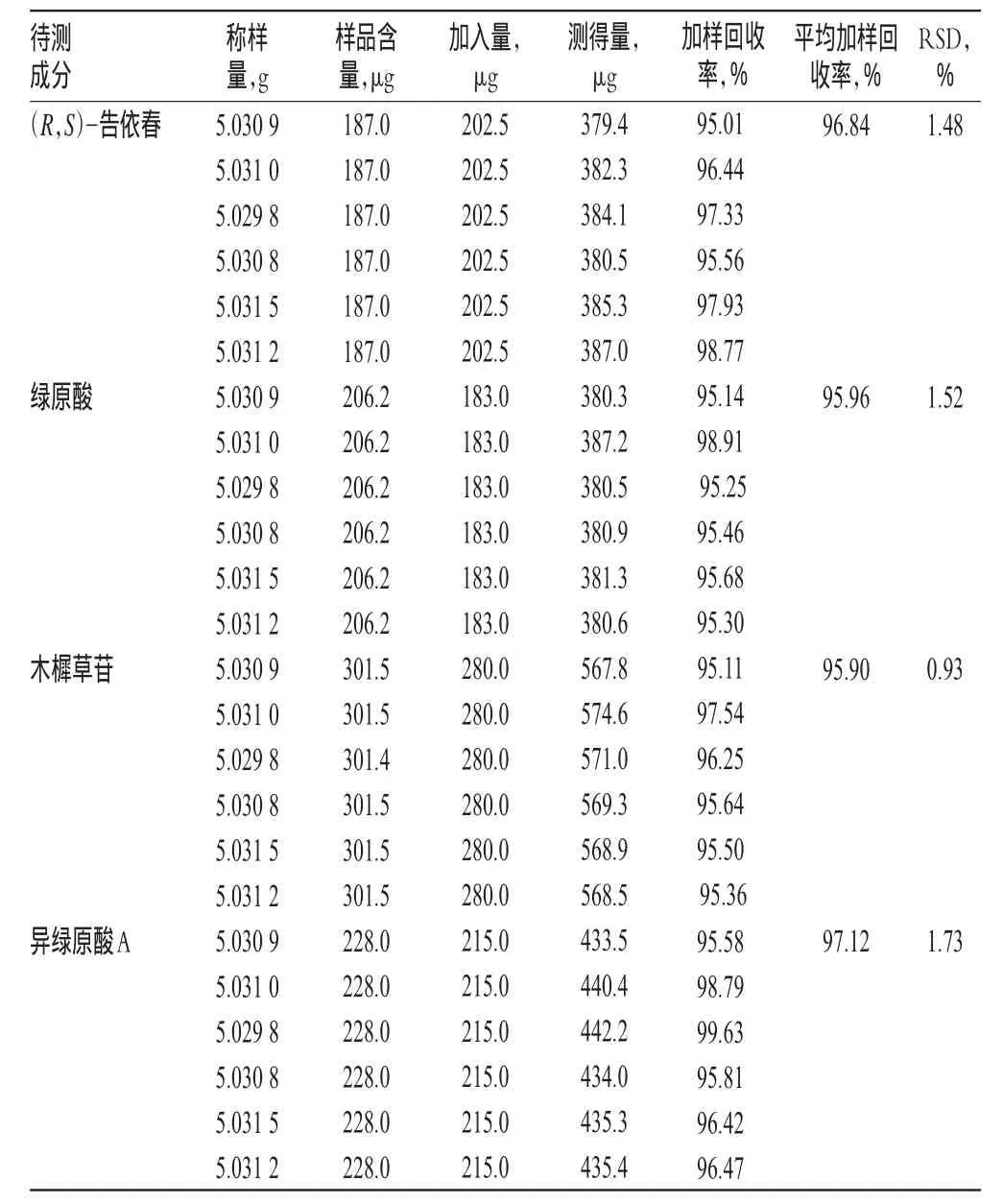
表5 加样回收率试验结果(n=6)Tab 5 Result of recovery tests(n=6)
2.10样品含量测定
取3个编号样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算各成分含量,结果详见表6。
3 讨论
本试验参考了相关文献中(R,S)-告依春、绿原酸和异绿原酸A、木犀草苷含量测定时的检测波长[9-12],同时采用190~800 nm全波长进行扫面验证。结果,在200~265 nm波长范围内(R,S)-告依春具有紫外吸收,木犀草苷、绿原酸和异绿原酸A分离度不好;在330 nm波长处绿原酸和异绿原酸A有很好的分离,但是(R,S)-告依春却没有吸收峰;在370 nm波长处木犀草苷的分离效果最好,而(R,S)-告依春、绿原酸、异绿原酸A吸收峰却很低。为得到更好的各成分峰,综合考虑,本试验中(R,S)-告依春、绿原酸和异绿原酸A、木犀草苷的检测波长分别选用254、330、330、370 nm。
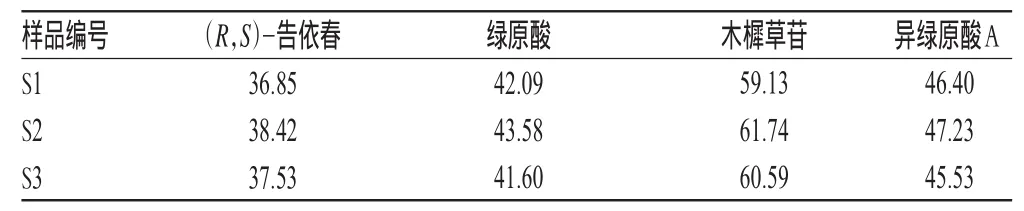
表6 样品含量测定结果(n=3,μg/g)Tab 6 Results of content determination of samples(n=3,μg/g)
综上所述,本方法操作简便、结果准确,适用于测定小儿感冒颗粒中(R,S)-告依春、绿原酸、木犀草苷和异绿原酸A的含量[13-14]。
[1]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:560.
[2]李其固,李振化,赵振宇,等.HPLC法测定抗病毒栓中的鸟苷,(R,S)告依春,百秋里和广藿香酮[J].中成药,2014,36(6):1 208.
[3]茅纯,郑娟,邹耀华.高效液相色谱法同时测定桑菊感冒片中绿原酸、木犀草苷和3,5-O-二咖啡酰基奎宁酸含量[J].中华中医药学刊,2014,32(1):193.
[4]安益强.HPLC法测定不同产地板蓝根中表告依春[J].中草药,2008,39(11):1 739.
[5]王瑞,杨海英,杨琪伟,等.板蓝根质量标准研究[J].中草药,2010,41(3):478.
[6]姚文冰.HPLC法同时测定痰热清注射液中木犀草苷和黄芩苷的含量[J].中国药房,2011,22(35):3 311.
[7]孙汝明,李翔,曹红,等.感冒清热颗粒HPLC特征图谱研究[J].药物分析杂志,2013,33(2):335.
[8]李丹,闫静.HPLC法测定感冒退热颗粒中表告依春和连翘苷[J].哈尔滨商业大学学报:自然科学版,2014,30(2):164.
[9]韩桂茹,张淑萍,安丽娜,等.HPLC法测定金银花及小儿咽扁颗粒中4种绿原酸[J].中成药,2013,35(3):517.
[10]李向阳,屠万青.HPLC法测定同时测定双金连合剂中的11种成分含量[J].药物分析杂志,2015,35(3):222.
[11]吕海鸿,王雪芹,刘乃强,等.HPLC-MS法测定双黄连口服液中木犀草苷和绿原酸的含量并评价二者对成品质量的影响[J].中国药房,2011,22(44):4 204.
[12]宁科贤,黄燕萍.HPLC法同时测定双黄连颗粒中绿原酸、木犀草苷、连翘苷和黄芩苷的含量[J].中国药房,2014,25(40):3 819.
[13]范磊.小儿感冒颗粒的质量控制方法研究[J].中国医药指南,2013,35(11):355.
[14]朱粉霞,张亚丽,汪晶,等.一测多评法测定金银花复方制剂中新绿原酸、绿原酸和隐绿原酸[J].中成药,2013,35(12):2 666.
(编辑:刘柳)
Simultaneous Determination of 4Components in Xiaoer Ganmao Granule by HPLC
CHEN Guobao1,ZHENG Yanping2,YAN Guojun3,SONG Guiping1,LIU Jia1,CAI Ting4(1.Jiangyin TCM Hospital,Jiangsu Jiangyin 214400,China;2.Nanjing Haichang Chinese Medicine Group Co.,Ltd.,Nanjing 210061,China;3.School of Pharmacy,Nanjing University of Chinese Medicine,Nanjing 210029,China;4.School of Pharmacy,China Pharmaceutical University,Nanjing 210009,China)
OBJECTIVE:To establish a method for the simultaneous determination of(R,S)-goitrin,chlorogenic acid,luteoloside and isochlorogenic acid A in Xiaoer ganmao granule.METHODS:HPLC was performed on the column of Hedera C18with mobile phase of acetonitrile-0.1%formic acid aqueous at a flow rate of 1.0 ml/min,the detection wavelength was 254 nm,330 nm and 370 nm,column temperature was 40℃,and the injection volume was 5 μl,RESULTS:The linear range was 6.6-105 μg/ml for(R,S)-goitrin(r=0.999 9),9-140 μg/ml for chlorogenic acid(r=0.999 9),9-144 μg/ml for luteoloside(r=0.999 8)and 9-138 μg/ml for isochlorogenic acid A(r=0.999 6);the limits of quantitation were 330 ng,450 ng,450 ng and 450 ng,limits of detection were 66 ng,90 ng,90 ng and 90 ng,respectively;RSDs of precision,stability and reproducibility tests were lower than 3%;recoveries were 95.01%-98.77%(RSD=1.48%,n=6),95.14%-98.91%(RSD=1.52%,n=6),95.11%-97.54%(RSD= 0.93%,n=6)and 95.58%-99.63%(RSD=1.73%,n=6).CONCLUSIONS:The method is simple and accurate,and suitable for the simultaneous determination of(R,S)-goitrin,chlorogenic acid,luteoloside and isochlorogenic acid A in Xiaoer ganmao granule. KEYWORDSXiaoer ganmao granules;(R,S)-goitrin;Chlorogenic acid;Luteoloside;Isochlorogenic acid A;HPLC
R917
A
1001-0408(2016)27-3836-03
10.6039/j.issn.1001-0408.2016.27.30
江苏省自然科学基金-青年基金项目(No.BK2012089)
*副教授,硕士。研究方向:中药制剂。E-mail:cgbjy@sina.com
教授,博士。研究方向:药物制剂。电话:025-83271123。E-mail:tcai@cpu.edu.cn
(2015-10-03
2016-07-03)

