西罗莫司对比他克莫司用于肾移植后抗排异疗效和安全性的Meta分析
陈小娟,黄晓宁,李 勇(中国药科大学国际医药商学院,南京 211198)
西罗莫司对比他克莫司用于肾移植后抗排异疗效和安全性的Meta分析
陈小娟*,黄晓宁,李勇#(中国药科大学国际医药商学院,南京211198)
目的:系统评价西罗莫司(SRL)对比他克莫司(Tac)在肾移植后抗排异的临床疗效和安全性,为临床提供循证参考。方法:计算机检索PubMed、EMBase、Medline、Science Direct、Cochrane图书馆、中国期刊全文数据库、中文科技期刊数据库、万方数据库,收集SRL(试验组)对比Tac(对照组)用于肾移植后抗排异的随机对照试验(RCT),提取资料并对纳入文献进行质量评估后,采用Rev Man 5.2统计软件进行Meta分析。结果:共纳入5项RCT,合计594例患者。Meta分析结果显示,两组患者急性排异反应发生率[RR=1.26,95%CI(0.82,1.93),P=0.30]、移植物丢失率[RR=0.91,95%CI(0.32,2.55),P=0.85]和死亡率[RR=0.87,95%CI(0.34,2.22),P=0.77]比较差异无统计学意义;而试验组患者感染率显著低于对照组,差异有统计学意义[RR=0.13,95%CI(0.04,0.40),P<0.001]。结论:相比Tac,肾移植后抗排异治疗中使用SRL具有相同的抗排异效果,且不改变移植物丢失率和患者死亡率,还能降低患者用药后的感染风险,安全性较高。
他克莫司;西罗莫司;肾移植;抗排异;Meta分析
截至2015年,终末期肾病(End-stage renal disease,ESRD)的发病率、患病率及死亡率在美国及许多欧洲国家相比2000年已经翻倍[1]。作为ESRD患者的最佳治疗选择,肾移植在全球范围内的需求不断增加。移植术后的免疫抑制和急性排异反应的预防和治疗通常采用他克莫司(Tac)一类的钙调磷酸酶抑制剂(Calcineurin inhibitor,CNI),但长期使用CNI容易引起不良反应。西罗莫司(SRL)是一种雷帕霉素靶位抑制剂(Target of rapamycin inhibitors,TOR-I),其与胞浆蛋白结合后不会抑制钙调磷酸酶,由此避免了CNI引起的肾毒性[2]。因此,部分学者指出,临床上可以将SRL作为肾移植后免疫抑制方案的基础用药,从而替代Tac一类的CNI药物。多项随机对照试验(RCT)比较了TOR-I与CNI在肾移植后的抗排异效果,而多数以此为基础进行的系统评价只注重TOR-I与CNI的比较[3],或者SRL与CNI的比较[4],单纯比较SRL与Tac的Meta分析很少[5],且不同研究的结果缺乏一致性。因此,本研究采用Meta分析的方法系统评价了SRL对比Tac用于肾移植后抗排异的临床疗效和安全性,以期为临床提供循证参考。
1 资料与方法
1.1纳入与排除标准
1.1.1研究类型国内外公开发表的RCT,不限制地区或人群,语种限定为中文和英文。
1.1.2研究对象肾移植术后即刻采用SRL或Tac进行抗排异的患者,排除接受除肾移植外其他器官移植的患者。纳入患者年龄、性别不限。
1.1.3干预措施试验组患者肾移植术后即刻采用SRL进行抗排异治疗;对照组患者肾移植术后即刻采用Tac进行抗排异治疗。两组其余干预措施相同,均使用吗替麦考酚酯(MMF)、强的松(Pred)和兔抗人胸腺细胞球蛋白(Thy)。两组疗程不限。
1.1.4结局指标疗效指标包括:①急性排异反应发生率;②移植物丢失率。安全性指标包括:③死亡率;④感染发生率。其中,①为主要指标,②③④为次要指标。
1.1.5排除标准治疗方案或数据报道不完整;缺乏结局指标,统计方法不恰当;研究设计不合理;重复发表的文献;动物实验及综述类文章。
1.2检索策略
计算机检索各数据库建库起至2015年6月1日之前发表的相关中英文文献,数据库包括 Medline、PubMed、ScienceDirect、EMBase、Cochrane图书馆、中国期刊全文数据库、中文科技期刊数据库、万方数据库。英文检索词包括“Sirolimus”“TOR_I”“Tacrolimus”“Prograf”“FK506”“CNI”“Kiney transplantation”“Renal transplantation”“RCT”;中文检索词包括“他克莫司”“普乐可复”“赛氏”“钙调磷酸酶抑制剂”“西罗莫司”“雷帕霉素”“雷帕鸣”“雷帕霉素靶位抑制剂”“肾移植”。
1.3资料提取和质量评价
对所有可能相关的文献进行标题、摘要和全文查找,两位研究员独立完成查找工作,有争议的部分由第三人共同协商并达成一致。同时,利用统一的标准提取如下信息:(1)研究设计类型:是否RCT以及随机化方案的隐藏情况;(2)文献的一般情况:第一作者、发表时间、试验实施地点、是否多中心试验、文献语言类别;(3)患者的一般情况:年龄、性别、样本量、是否首次肾移植;(4)治疗方案:相关诱导免疫抑制剂及维持免疫抑制方案;(5)患者的随访情况;(6)结果测量,主要观察4个指标:急性排异反应发生率、移植物丢失率、死亡率、感染发生率。
采用Jadad评分系统对纳入的RCT进行质量评价,具体内容包括随机化方法、盲法、失访/退出3个方面。采用0~5分计分法:<3分为低质量研究;3~4分为较高质量研究;5分为高质量研究[6]。同时,以是否使用分配隐藏(AC)和意向性分析(ITT)来辅助评估纳入研究的方法学质量。
1.4统计学方法
采用Cochrane协作网提供的Rev Man 5.2统计软件进行数据分析。首先,对于各个研究结果之间异质性的检验采用χ2检验,如果各研究间无统计学异质性(P>0.1,I2<50%),选择固定效应模型进行Meta分析;反之,则选择随机效应模型进行Meta分析。合并效应量之后,对于两组结果的比较,采用95%置信区间(CI)下的相对危险度(RR)进行分析,同时绘制森林图。P<0.05为差异有统计学意义。最后,采用倒漏斗图联合Egger’s法共同检验文献发表偏倚。
2 结果
2.1文献检索流程
初步检索得到215篇文献,排除综述类、重复发表的文献47篇;阅读题目和摘要后,排除非RCT、非首次器官移植、维持免疫抑制方案或免疫诱导抑制剂不符要求、非肾移植后即刻用药的文献132篇;阅读全文后,排除缺乏结局指标、有明显错误、原始数据缺失、观察期内改变用药剂量或用药方案的文献31篇,最终纳入5篇(项)研究[7-11]。
2.2纳入研究基本信息与质量评价结果
纳入的5项研究共计594例患者,其中试验组302例,对照组292例。纳入研究基本信息与质量评价结果见表1。
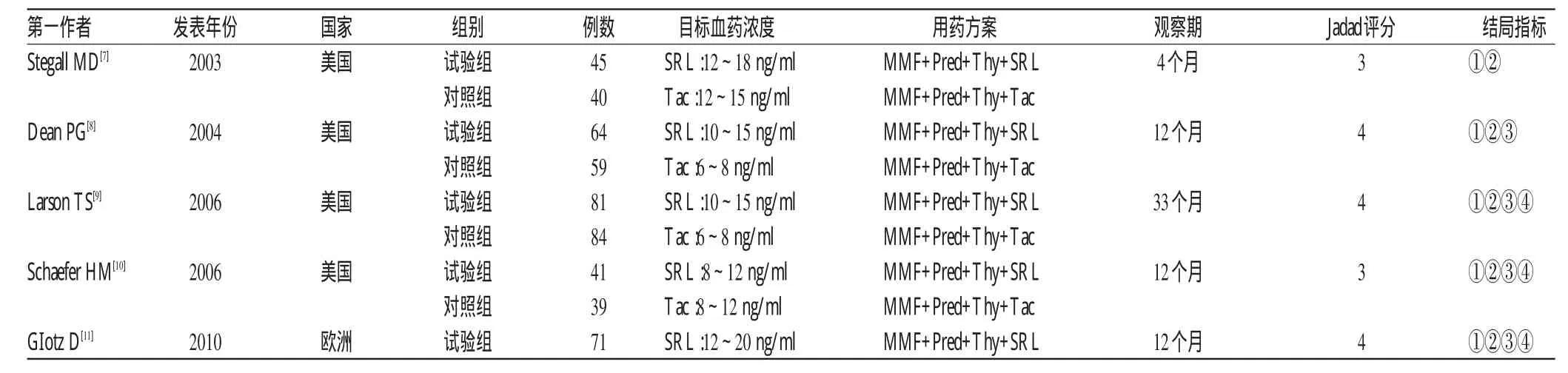
表1 纳入研究基本信息与质量评价结果Tab 1 General information of included litetatures and quality evaluation results
2.3Meta分析结果
2.3.1急性排异反应发生率5项研究报道了急性排异反应发生率,试验组急性排异反应发生率为13.58%(41/302),对照组急性排异反应发生率为10.96%(32/292)[7-11]。各研究结果间无异质性(P=0.64,I2=0),采用固定效应模型进行分析,详见图1。Meta分析结果显示,两组患者急性排异反应发生率比较差异无统计学意义[RR=1.26,95%CI(0.82,1.93),P=0.30]。
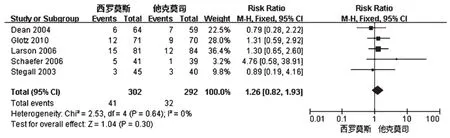
图1 两组患者急性排异反应发生率的Meta分析森林图Fig 1 Forest plot of Meta-analysis of the incidence of acute rejection in 2groups
2.3.2移植物丢失率5项研究报道了移植物丢失率,试验组移植物丢失率为6.95%(21/302),对照组移植物丢失率为7.19%(21/292)[7-11]。各研究间有异质性(P=0.07,I2=54%),采用随机效应模型进行分析,详见图2。Meta分析结果显示,两组患者移植物丢失率比较差异无统计学意义[RR=0.91,95%CI(0.32,2.55),P=0.85]。
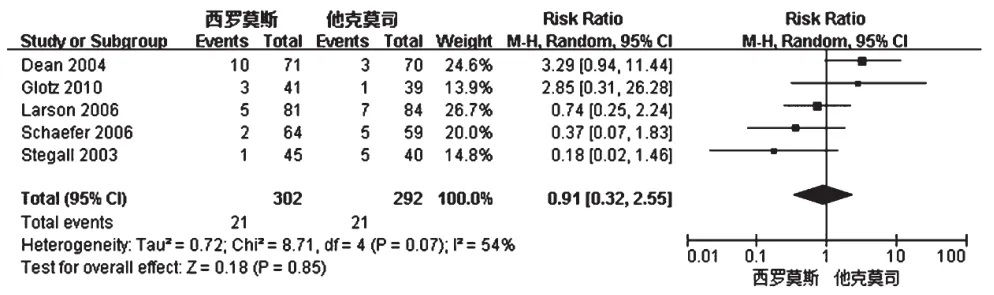
图2 两组患者移植物丢失率的Meta分析森林图Fig 2 Forest plot of Meta-analysis of gaft loss rate in 2 groups
2.3.3死亡率4项研究报道了死亡率,试验组死亡率为2.72%(7/257),对照组死亡率为3.17%(8/252)[8-11]。各研究间无异质性(P=0.36,I2=7%),采用固定效应模型进行分析,详见图3。Meta分析结果显示,两组患者死亡率比较差异无统计学意义[RR=0.87,95%CI(0.34,2.22),P=0.77]。
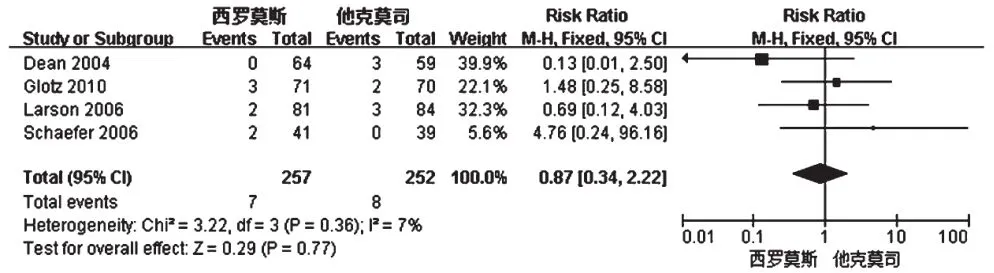
图3 两组患者死亡率的Meta分析森林图Fig 3 Forest plot of Meta-analysis of mortality rate in 2 groups
2.3.4感染率3项研究报道了感染率,试验组感染率为1.55%(3/193),对照组感染率为13.47%(26/193)[9-11]。各研究间无异质性(P=0.67,I2=0),采用固定效应模型进行分析,详见图4。Meta分析结果显示,试验组感染率显著低于对照组,差异有统计学意义[RR=0.13,95%CI(0.04,0.40),P<0.001]。
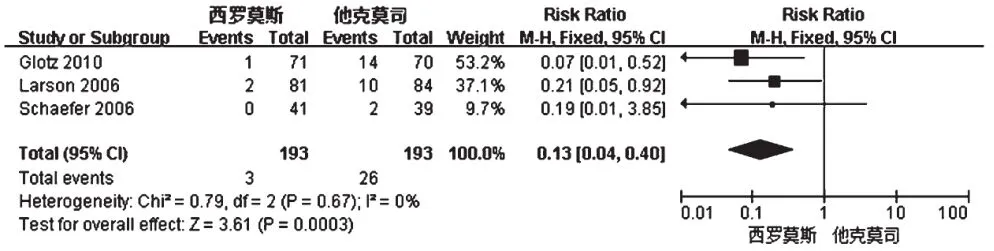
图4 两组患者感染率的Meta分析森林图Fig 4 Forest plot of Meta-analysis of infection rate in 2 groups
2.4发表偏倚
以急性排异反应发生率为指标,分别采用倒漏斗图(图5)和Egger’s法进行定性分析和定量分析。由图5可知,左右散点分布不完全对称,提示可能存在发表偏倚;采用Egger’s法进行定量分析,结果显示文献不存在发表偏倚[RR=0.638,95%CI(-2.628,3.903),P=0.578]。
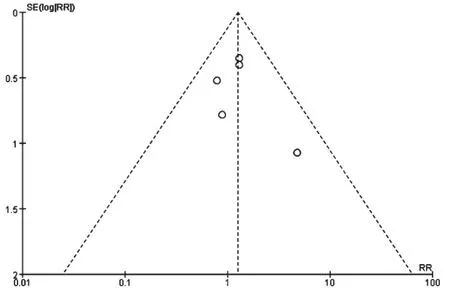
图5 急性排异反应发生率的倒漏斗图Fig 5 Inverted funnel plot of the incidence of acute rejection
3 讨论
自1954年首次成功完成人肾移植术以来,人类与移植术后排异反应的斗争就从未停止。免疫抑制剂已成为肾移植后抗排异治疗中不可缺少的一部分,然而其临床用药选择面临的争议也很多,包括TOR-I或CNI的选择、CNI中Tac与环胞素A的选择、用药剂量高低的选择、即刻应用或转换应用的选择、二联用药或三联用药的选择、免疫诱导抑制剂的选择等。选择不同的药物治疗对用药后的疗效与安全性均会产生一定程度的影响。比如,采用不同的免疫抑制剂维持治疗方案其临床疗效不同。姜丽萍等[12]的研究表明,MMF类免疫抑制方案比硫唑嘌呤方案具有更低的急性排异反应发生率;另外,不同免疫诱导药物对肾移植后疗效也会有一定影响。基于此,本文将研究角度设定在SRL与Tac的对比上,纳入研究对各组病例的性别、年龄等因素进行控制,确保各项研究的纳入与排除标准基本一致,使得各研究基线可比。与以往研究不同的是,本研究还对其他相关因素进行了控制,包括纳入研究均为相同的三联免疫抑制方案,使用相同的免疫诱导抑制剂,且SRL或Tac的使用均为肾移植术后即刻用药、剂量正常。由于本研究对文献纳入条件进行了严格限制,因此排除了多项2011年以后发表的RCT,而仅纳入5篇质量较高的早期临床试验。
Tac通过对钙调磷酸酶的抑制作用来达到抗排异效果,但该药会增强入球小动脉收缩、引起肾小管间质发生纤维化或萎缩、缩小血管腔,最终对患者产生肾毒性。SRL则是通过抑制细胞由Gi期向S期转化,阻断与白细胞介素-2的结合,使得Tc、Td细胞无法成为具有致敏性的T淋巴细胞,从而发挥免疫抑制的作用。由于SRL不具有肾毒性,因此被许多人用作CNI类药物的替代疗法。
本次Meta分析结果显示,在联合用药(MMF+Pred+Thy)相同的情况下,两组患者急性排异反应发生率、移植物丢失率和死亡率比较,差异均无统计学意义。但是,相比Tac,肾移植后使用SRL可以显著降低患者感染率,提示肾移植术后使用SRL安全性较好。SRL降低术后感染发生率的原因可能与SRL抵抗巨细胞病毒有关。肾移植后感染主要由巨细胞病毒引起,关于SRL抗病毒感染的作用机制有两种观点:一种观点认为SRL可以通过抑制病毒mRNA翻译蛋白质,从而抑制病毒复制[13];另一种观点认为,SRL对机体自身固有免疫会产生一定程度的刺激,通过促进炎症因子的表达,从而发挥抗病毒感染的作用[14]。另外,有研究表明,相比使用Tac或环孢霉素者,使用SRL治疗的患者发生新的鳞状细胞癌的风险明显降低,推测其可能存在某种特殊的抗肿瘤活性[15]。
本研究存在以下不足:首先,由于此次系统评价纳入的研究都是来自亚洲地区之外的临床试验,缺乏亚洲尤其是我国肾移植患者的临床资料,而王叶新等[15]提出,肾移植患者Tac血药浓度与亚洲人群MDR1 C3435T基因多态性相关,故在临床应用中免疫抑制方案的确定应结合国内患者实际体质进行相应的调整,尤其要注意Tac血药浓度的监测。其次,由于纳入研究报道的均为肾移植后早期发生的不良反应,由此得出的结论也只是对肾移植后早期疗效和安全性的分析,长期临床效果的对比还有待进一步观察。另外,越来越多的研究证实,足量MMF联合低剂量Tac的免疫抑制方案在避免发生急性排异反应的同时,还能减少由于使用Tac导致的新发糖尿病、高血脂、肾毒性等不良反应[16-17],而本研究得出的结论是基于正常剂量的临床试验数据,缺乏不同剂量下SRL与Tac的疗效对比。最后,需要特别注意的一点是,Meta分析是基于文献的二次研究,不可避免会受到纳入文献方法学质量的影响。本研究纳入的文献数量较少,倒漏斗图提示可能存在发表偏倚。基于上述不足,在参考此次Meta分析的结果时,需要结合临床实际情况,谨慎对待。未来关于肾移植后SRL与Tac临床效果的比较研究,应注重提高设计合理性与质量、加大研究样本量、延长观察周期、扩大试验对象来源范围,从而提高临床数据的准确性和可靠性。
综上所述,在联合用药相同的情况下,相比Tac,肾移植术后抗排异治疗中使用SRL具有相同的抗排异效果,且不改变移植物丢失率和患者死亡率,还能降低患者用药后的感染风险,安全性较高。
[1]Ekberg H,Bernasconi C,Nöldeke J,et al.Cyclosporine,tacrolimus and sirolimus retain their distinct toxicity profiles despite low doses in the Symphony study[J].Nephrology Dialysis Transplantation,2010,25(6):2004.
[2]Sehgal SN.Rapamune®(RAPA,rapamycin,sirolimus):mechanism of action immunosuppressive effect results from blockade of signal transduction and inhibition of cell cycle progression[J].Clinical Biochemistry,1998,31(5):335.
[3] 吴斌,吴逢波,卢静,等.肾移植术后TOR-I替代CNI免疫抑制治疗的Meta分析[J].中国药房,2011,22(34):3229.
[4]王沫.肾移植术后初期使用西罗莫司同钙调磷酸酶抑制剂相对比的Meta分析[D].广州:南方医科大学,2014.
[5] 周静怡,沈毅,程军,等.肾移植后应用西罗莫司和他克莫司的有效性与安全性的荟萃分析[J].中华器官移植杂志,2014,35(10):584.
[6]Jadad AR,Moore RA,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary?[J].Controlled Clinical Trials,1996,17(1):1.
[7]Stegall MD,Larson TS,Prieto M,et al.Kidney transplantation without calcineurin inhibitors using sirolimus [C]//Transplantation Proceedings.Elsevier,2003,35(3):S125.
[8]Dean PG,Lund WJ,Larson TS,et al.Wound-healing complications after kidney transplantation:a prospective,randomized comparison of sirolimus and tacrolimus1[J]. Transplantation,2004,77(10):1555.
[9]Larson TS,Dean PG,Stegall MD,et al.Complete avoidance of calcineurin inhibitors in renal transplantation:a randomized trial comparing sirolimus and tacrolimus[J]. Am J Transplant,2006,6(3):514.
[10]Schaefer H M,Kizilisik AT,Feurer I,et al.Short-term results under three different immunosuppressive regimens at one center[J].Transplant Proc,2006,38(10):3466.
[11]Glotz D,Charpentier B,Abramovicz D,et al.Thymoglobulin induction and sirolimus versus tacrolimus in kidney transplant recipients receiving mycophenolate mofetil and steroids[J].Transplantation,2010,89(12):1511.
[12]姜丽萍,胡善联,陈文.肾移植免疫抑制治疗方案的决策树分析[J].中国药房,2007,18(2):89.
[13]Pengel LH,Liu LQ,Morris PJ.Do wound complications or lymphoceles occur more often in solid organ transplant recipients on mTOR inhibitors?A systematic review of randomized controlled trials[J].Transpl Int,2011,24(12):1216.
[14]Säemann MD,Haidinger M,Hecking M,et al.The multifunctional role of mTOR in innate immunity:implications for transplant immunity[J].Am J Transplant,2009,9(12):2655.
[15] 王叶新,崔萌,吴玉波.亚洲人群MDR1 C3435T基因多态性与肾移植患者他克莫司血药浓度关系的Meta分析[J].中国药房,2015,26(3):359.
[16] 季曙明,陈江华,谭建明,等.肾移植后吗替麦考酚酯联合低剂量他克莫司加皮质激素的应用[J].中国组织工程研究,2013,17(5):777.
[17]Ekberg H,Bernasconi C,Nöldeke J,et al.Cyclosporine,tacrolimus and sirolimus retain their distinct toxicity profiles despite low doses in the symphony study[J].Nephrol Dial Transplantat,2010,25(6):2004.
(编辑:申琳琳)
Efficacy and Safety of Sirolimus versus Tacrolimus for Anti-rejection after Renal Transplantation:A Metaanalysis
CHEN Xiaojuan,HUANG Xiaoning,LI Yong(School of International Pharmaceutical Business,China Pharmaceutical University,Nanjing 211198,China)
OBJECTIVE:To systematically review the clinical efficacy and safety of sirolimus(SRL)versus tacrolimus(Tac)for anti-rejection after renal transplantation,and provide evidence-based reference for clinical treatment.METHODS:Retrieved from PubMed,EMBase,Medline,Science Direct,Cochrane library,CJFD,VIP and Wanfang Database,randomized controlled trials(RCT)about SRL(test group)versus Tac(control group)for anti-rejection after renal transplantation were collected.Meta-analysis was performed by using RevMan 5.2 software after data extraction and quality evaluation.RESULTS:Totally 5 RCTs were included,involving 594 patients.Results of Meta-analysis showed,there was no significant difference in the incidence of acute rejections[RR=1.26,95%CI(0.82,1.93),P=0.30],graft loss rate[RR=0.91,95%CI(0.32,2.55),P=0.85]and mortality rate[RR=0.87,95%CI(0.34,2.22),P=0.77]in 2 groups;while the infection rate in test group was significantly lower than control group,the difference was statistically significant[RR=0.13,95%CI(0.04,0.40),P<0.001].CONCLUSIONS:Compared with Tac,SRL has the same anti-rejection effect after renal transplantation,not changed graft loss rate and mortality rate,but reduced the infection rate with higher safety.
Tacrolimus;Sirolimus;Renal transplantation;Anti-rejection;Meta-analysis
R692
A
1001-0408(2016)27-3821-04
10.6039/j.issn.1001-0408.2016.27.26
*硕士研究生。研究方向:药物经济学。E-mail:471943117@qq. com
副教授,硕士生导师。研究方向:药物经济学、技术经济学。E-mail:32899784@qq.com
(2015-10-07
2016-07-22)

