甲钴胺片清洁验证分析方法研究
徐鹏鹤,张婷,余永华,华洁,雷锦璟
1.杭州康恩贝制药有限公司,浙江杭州310052;2.杭州新博思生物医药有限公司,浙江杭州310052;3.杭州新诺华医药有限公司,浙江杭州310052
甲钴胺片清洁验证分析方法研究
徐鹏鹤1,张婷2,余永华3,华洁1,雷锦璟1
1.杭州康恩贝制药有限公司,浙江杭州310052;2.杭州新博思生物医药有限公司,浙江杭州310052;3.杭州新诺华医药有限公司,浙江杭州310052
目的建立甲钴胺片清洁验证分析方法及取样方法。方法采用高效液相法,以Hypersil ODS2-C18(5 μm, 4.6×150 mm)为色谱柱,以0.05 mol/L乙酸铵溶液-乙腈(83∶17)为流动相,流速为1.0 mL/min,检测波长为266 nm,进样量为20 L,柱温30℃。结果甲钴胺对照品溶液在检测浓度0.03~1.60 μg/mL范围内线性关系良好(r=0.999),且回收率符合要求(回收率为99%)。结论该方法简便、准确、重复性好,灵敏度高,可用于甲钴胺片清洁验证药品残留量的检测。
甲钴胺片;清洁验证;方法学
甲钴胺是一种内源性的辅酶B12,临床用于治疗周围神经病。本品最早有卫材研发上市,国内上市剂型常见有片剂、胶囊和注射液,其中以片剂市场占有率最高。杭州康恩贝制药有限公司生产的甲钴胺片规格为0.5 mg。目前尚未有文献表明相关的清洁验证方法报道,工艺生产的清洁验证其含量及浓度均较低,而甲钴胺见光易分解,因此在检测过程中易引起多种偏差。中国药典2015版及现有文献中甲钴胺均采用高效液相色谱法进行含量测定,但色谱条件如流动相及检测波长[1]等均存在多样化。该文采用高效液相色谱法对甲钴胺片进行生产清洁验证分析方法开发及验证,并对样品进行分析测定。
1 仪器与试药
1.1仪器
高效液相色谱仪(Waters,e2695/2498);电子分析天平(Mettler-Toledo,XS105Dualrange);pH计(Mettler-Toledo,DELTA320),除湿机(杭州弘泰电器有限公司)。
1.2试药
乙腈(TEDIA,批号16030553,HPLC级);乙酸铵(国药集团化学试剂有限公司,批号20151207,分析纯);磷酸(上海凌峰化学试剂有限公司,批号20141218,分析纯);纯化水(Milli-Q integral 10)。甲钴胺(20160115,浙江省食品药品检定研究院标化)。棉签(稳健医疗集团有限公司);水系滤头(Φ2.5 cm,0.45 μm,上海昊清科技有限公司)。
2 方法及结果
2.1色谱条件
色谱柱为Hypersil ODS2-C18(5 μm,4.6×150 mm),流动相为0.05 mol/L乙酸铵溶液-乙腈(83∶17)为流动相,流速为1.0 mL/min,检测波长为266 nm,进样量为20 L,柱温30℃[2]。
2.2溶液的配制
2.2.1对照品溶液制备取甲钴胺对照品28~200 mL量瓶中,精密称定,加水振摇使溶解并至刻度;精密量取1 mL,置50 mL量瓶中,用水稀释至刻度,摇匀,即得甲钴胺对照品储备液(浓度约2.8 μg/mL)。精密量取5~ 20 mL量瓶中,用水稀释至刻度,摇匀,即得对照品溶液(浓度约0.7 μg/mL)。
2.2.2供试品溶液制备取两个用水湿润的棉签,轻轻压住,在100 cm2的不锈钢设备表面按图1擦拭,擦拭结束后旋转90°,按图2擦拭,再取一个用水润湿的取样棉签按相同方法擦拭1次。
图1 擦拭方向(横向)
图2 擦拭方向(纵向)
将擦拭后的2个棉签置烧杯中,精密量取10 mL水,超声10 min;棉球挤干后取出,以0.45 μm水系滤膜过滤,取续滤液作为供试品溶液。
2.3方法学验证
2.3.1系统适用性取对照品溶液照上述色谱条件连续进样5针,以峰面积计,应符合标准要求:五针峰面积RSD≤2.0%,理论板数>200 0,分离度R>1.5。结果:五针峰面积RSD为0.7%,理论踏板数均>2000,分离度均>1.5。
2.3.2专属性分别进空白溶液(即棉签浸出液:取两个棉签置100 mL烧杯中,加水10 mL,超声溶解10 min)、空白辅料溶液(取空白辅料同供试品溶液配制)和使用前用0.45 μm纤维素滤膜滤过)、对照品溶液,照上述色谱条件进样检测,记录色谱图。要求:主峰分离度>1.5,纯度角小于纯度阈值,空白辅料及棉签浸出液对主峰无干扰。结果,供试品主峰分离度符合要求(无杂质峰),峰纯度符合要求(纯度角0.917<纯度阈值1.264),溶剂、空白辅料及棉签浸出液对主峰无干扰。见图3。
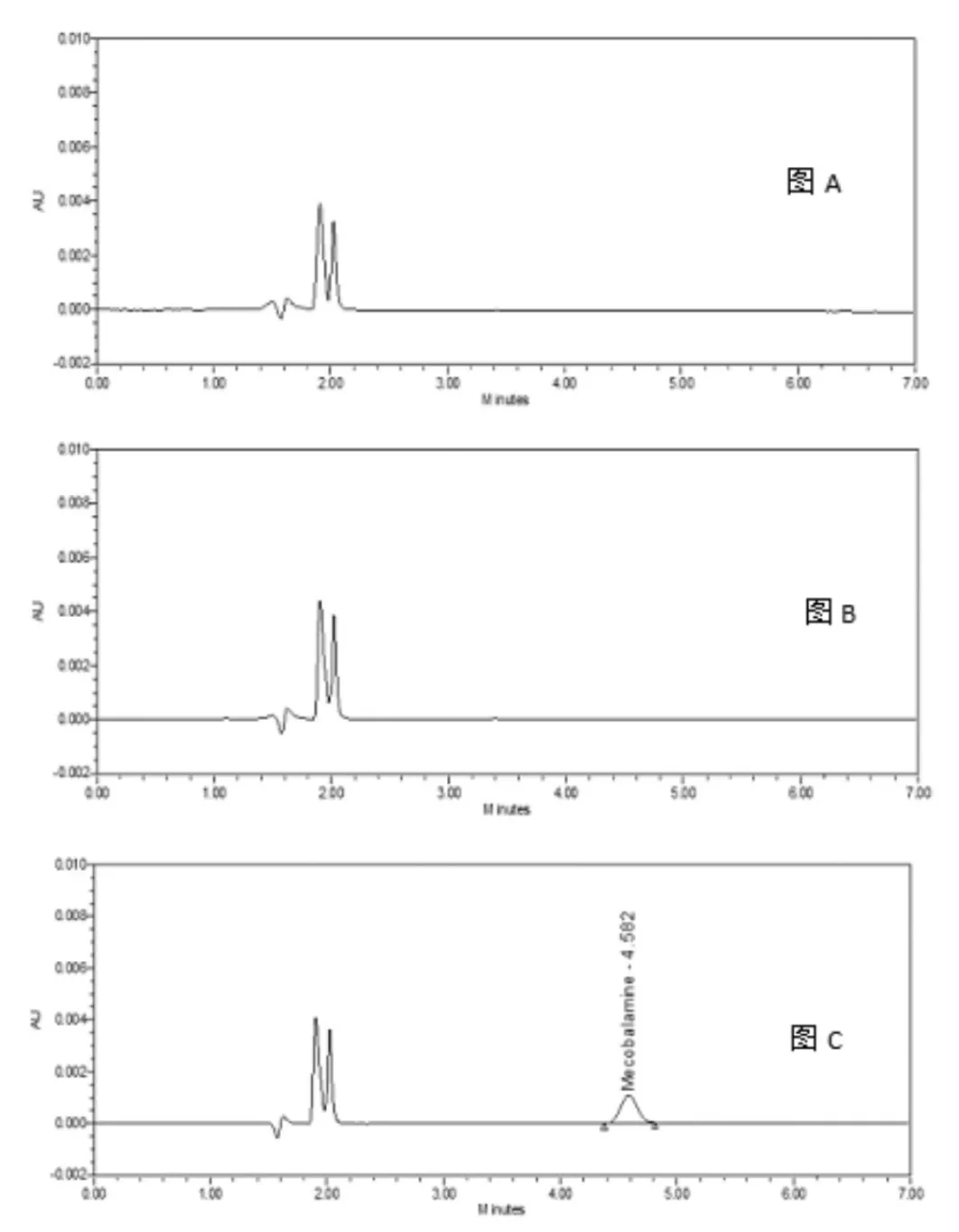
图3 空白溶液(A)、空白辅料(B)、甲钴胺对照品溶液(C)色谱图
2.3.3检测限与定量限取甲钴胺对照品储备液,逐级稀释,使甲钴胺主峰信噪比约为3∶1和10∶1,记录对应的对照品溶液浓度,即为对应的检测限与定量限,照上述色谱条件进样检测,平行进样2次。标准要求:检测限信噪比约3∶1;定量限信噪比约10∶1。结果,检测限为0.01 g/mL,定量限为0.03 g/mL。
2.3.4线性取对照品储备液,用水逐步稀释成定量限及限度范围内制备不同浓度的溶液,浓度分别为定量限、0.4 μg/mL、0.7 μg/mL、1.0 μg/mL、1.4 μg/mL、1.6 μg/mL,照上述色谱条件进样检测分别进样;并以峰面积(Y)对浓度(X)进行线性回归,得线性方程。标准要求:r≥0.999。结果表明,甲钴胺浓度在0.03 μg/mL~1.6 g/mL,范围内与峰面积呈良好线性关系,r=0.999。
2.3.5准确度
2.3.5.1方法回收率取对照品储备液,分别用水稀释成限度的50%、100%、120%溶液,即为0.4 μg/mL、0.7 μg/mL和1.0 μg/mL,照上述色谱条件进样检测,每个浓度进样两针,平行实验3次。标准要求:回收率应在95%~105%。结果:该法回收率良好,平均回收率99%。
2.3.5.2擦拭回收率取对照品储备液,用水稀释成4 μg/mL、7μg/mL和10 μg/mL的溶液。精密量取1 mL至3个10 cm×10 cm的不锈钢板上,晾干,照供试品溶液制备方法进行制备并照上述色谱条件进样检测,平行实验3次。标准要求:回收率≥50%。结果擦拭回收率良好,平均回收率75%。
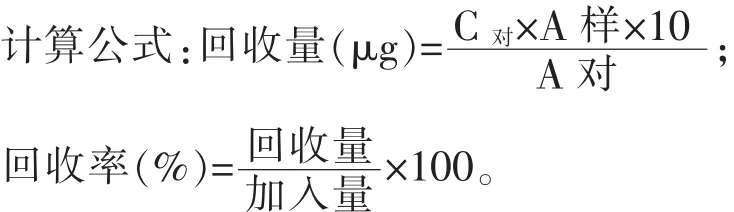
2.3.6精密度取对照品储备液用水稀释成0.7 μg/mL的溶液,照上述色谱条件重复进样6次,记录峰面积,计算其相对标准偏差(RSD),作为重复性。另以不同人员同法操作,以两位操作者12针样品的峰面积,计算12次的相对标准偏差,作为中间精密度。标准要求6份供试品溶液含量RSD≤2.0%;两个QC之间所测得含量的结果偏差≤2.0%。结果,该法精密度良好,重复性RSD为0.3%,中间精密度,RSD为1.4%。
2.3.7溶液稳定性取对照品溶液和供试品溶液,分别在0、4、8、12、24、48 h照上述色谱条件进样,进行含量测定。标准要求:对照品溶液回收率在95%~105%之间,样品溶液峰面积与0 h样品溶液峰面积偏差≤2.0%,则认为对照品溶液和供试品溶液是稳定的。结果,该法稳定性良好,在48 h内对照品溶液及供试品溶液偏差< 2.0%[3-4]。
3 讨论
甲钴胺溶液对光不稳定,本实验在综合摸索不同的实验条件是,最终采用全程照度低于5 lx的红色LED灯,因此该法检测限可达0.01 g/mL,并保证最低量至限度范围内(0.03~1.6 g/mL)良好的线性和准确度,因此对产品生产的清洁具有重大意义。
甲钴胺在266 nm处有强烈的紫外吸收,用该波长进行测定,大大提高了甲钴胺的检测灵敏度,对生产更加个有指导意义。
该方法验证是基于ICH和GMP的指导原则进行,由于不同人员的擦拭效果不一致,因此对清洁擦拭人员进行全面的培训和考核。结果该法简便、灵敏、专属性强。
[1](美)L.R.森德尔,J.J.柯克兰,J.L.柯克兰.实用高效液相色谱法的建立[M].张玉奎,王杰,张维冰,译.2版.北京:华文出版社,2001:62-68.
[2]国家食品药品监督管理总局.YBH12632004,甲钴胺[S].北京:国家食品药品监督管理总局,2014.
[3]桑国卫,陈竺,邵明立,等.药品质量标准分析方法验证指导原则·中国药典四部[S].北京:国家药典委员会,2015.
[4]International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use.Validation of analytical procedures:text and methodology ICH Q2(R1):November 2005.
Research on Validated Analytical Method of Mecobalamin Tablets Cleaning
XU Peng-he1,ZHANG Ting2,YU Yong-hua3,HUA Jie1,LEI Jin-jing1
1.Hangzhou Conba Pharmaceutical Co.,Ltd,Hangzhou,Zhejiang Province,310052 China;2.Hangzhou New Allen Biotechnology Co.Ltd,Hangzhou,Zhejiang Province,310052 China;3.Hangzhou new Novartis Pharmaceutical Co.,Ltd.Hangzhou, Zhejiang Province,310052 China
Objective To establish a validated analytical method of mecobalamin tablets cleaning and sampling method. Methods The high performance liquid chromatography was adopted with Hypersil ODS2-C18(5 μm,4.6×150 mm)column, with 0.05 mol/L ammonium acetate solution-acetonitrile(83∶17)as the mobile phase at a flow rate of 1.0 mL/min.The absorbance was monitored at 266 nm.The injection volume was 20 μl and the column temperature was 30℃.Results The liner correlation of mecobalamin contrast solution was good from the 0.03 μg/mL to 1.60 μg/mL detection concentration R= 0.999,and the recycle rate met the requirement(the recycle rate was 99%).Conclusion The method is simple and accurate with good repeatability and high sensitivity,which can be used in the detection of mecobalamin tablets in the cleaning validation of drug residue.
Mecobalamin tablets;Cleaning validation;Methodology
R96
A
1672-5654(2016)11(a)-0050-03
10.16659/j.cnki.1672-5654.2016.31.050
徐鹏鹤(1982.4-),男,浙江淳安人,本科,工程师,研究方向:药物质量标准及分析方法学研究。
(2016-08-05)

