拟南芥WRKY基因家族应答非生物胁迫基因的鉴定1)
魏晓爱 姚文静 姜廷波 周博如
(林木遗传育种国家重点实验室(东北林业大学),哈尔滨,150040)
拟南芥WRKY基因家族应答非生物胁迫基因的鉴定1)
魏晓爱 姚文静 姜廷波 周博如
(林木遗传育种国家重点实验室(东北林业大学),哈尔滨,150040)
WRKY转录因子家族是植物特有的一类转录因子家族,在植物生长发育和应答各种胁迫反应过程中起重要作用。为筛选和鉴定植物抗逆关键基因,以拟南芥(Arabidopsisthaliana)WRKY家族基因为研究对象,从数据库中搜索到72个拟南芥WRKY基因,通过生物信息学分析,根据其结构特点,可将其分为3大类:GroupI、GroupII和GroupIII。其中,GroupII又可分为5个亚类:IIa、IIb、IIc、IId和IIe。用实时定量RT-PCR筛选出30个应答盐胁迫的基因,其中上调表达的23个,下调表达的7个。
拟南芥;WRKY转录因子;非生物胁迫
WRKY转录因子是植物所特有的一类转录因子[1],1994年Ishiguro et al[2]从甘薯中克隆得到第一个WRKY转录因子SPF1,随后相继在野燕麦、拟南芥、烟草(NicotianatabacumL.)和水稻(OryzasativaL.)中克隆得到WRKY。最新研究表明:在原生生物、粘菌及绿藻中也有WRKY转录因子的存在,高等植物的WRKY基因源于早期的真核生物,并在进化过程中经历的多次加倍和扩张[3]。WRKY转录因子具有1~2个包含标志性WRKYGQK肽段的WRKY结构域,该结构域由大约60个高度保守的氨基酸残基组成,能够与DNA序列中W-box结合,在WRKY结构域C末端还具有一个锌指结构(CX4-5CX22-23HX1H型或CX7CX23HX1C型),是决定WRKY蛋白是否能够和相关基因顺式作用元件W-box(TTGACT/C)结合的关键因素[4-5]。数量庞大的WRKY基因家族在调控植物生长发育、物质代谢和响应各种逆境胁迫的应答中具有重要作用[6],目前在拟南芥中发现72个,水稻中105个,玉米(ZeamaysL.)119个,杨树(Populus)104个,油菜(BrassicacampestrisL.)46个,胡萝卜(DaucuscarotaL.)中有95个WRKY基因[7-11]。目前,人们主要基于转录组分析、实时荧光定量PCR、Northern杂交等技术分析WRKY基因在非生物胁迫下的表达模式,并初步预测WRKY基因的相关功能,有的WRKY基因通过进一步的遗传转化验证了其在调控植物免疫反应应答中的具体功能[12],现在普遍认为植物耐盐性是多种抗盐生理性状的综合表现,由位于不同染色体上多个基因控制的数量性状[13]。本研究以72个拟南芥WRKY基因为研究对象,分析其在NaCl胁迫24 h下的表达情况,为进一步研究WRKY转录因子的功能提供参考。
1 试验材料
本研究所用拟南芥(Arabidopsisthaliana)为Col-0(Columbia-0)。首先4 ℃春化2~3 d,播种于人工混合土中(V(黑土)∶V(蛭石)∶V(珍珠岩)=5∶3∶2,并121 ℃高温灭菌40 min),补足水分并盖上保鲜膜,置于正常植物光照培养室培养,设置光照16 h,黑暗8 h,光照强度2 500~5 000 lx,温度22~24 ℃,湿度为70%,3~4 d后揭下保鲜膜,确保水分供应充足。将4周左右的拟南芥幼苗用150 mmol/L的NaCl处理24 h,用水处理作对照,采集叶片,用于RNA提取或于冰箱中-80 ℃保存备用。
2 试验方法
2.1 RNA的提取
用柱式植物RNAout(TIANDZ Corp,Beijing,China)试剂盒法提取拟南芥总RNA,具体步骤参照附带的说明书,用琼脂糖凝胶电泳和NanoDrop 2000c的分光光度计(NanoDrop Technologies,WilmingtonDE,USA)检测总RNA的质量与浓度,用RNA反转录试剂盒(TaKaRa Corp.,Dalian,China)合成cDNA,稀释5倍作为RT-qPCR的模板,用于检测基因的表达水平。
2.2 应答盐胁迫基因的筛选
从PlantTFDB数据库中获得72个拟南芥WRKY转录因子基因信息,用RT-qPCR分析其在150 mmol/L NaCl处理24 h的表达情况。实时定量PCR在7500 real-time PCR system(Applied Biosystems)上进行,以ACT作为内参[14]。RT-qPCR的20 μL体系包含10 μL的SYBR Premix Ex Taq II(TaKaRa),0.4 μL的ROX ReferenceDye II(TaKaRa),正向引物(10 μmol/L)和反向引物(10 μmol/L)各0.8 μL(引物终浓度为0.4 μmol/L),2 μL的cDNA模板(100 ng以下)和6 μL的无菌水。RT-qPCR的反应程序如下:预变性(95 ℃ 30 s),变性(95 ℃ 5 s),退火(60 ℃ 34 s),25个循环,然后进行熔解曲线分析[15]。用-ΔΔCt值来计算基因相对表达水平[14],用F值(2-ΔΔCt)来计算基因相对表达量。
2.3 生物信息学分析
利用NCBI在线搜索程序确定拟南芥转录因子家族基因的开放阅读框(ORF)[16],预测编码的氨基酸序列及蛋白质的分子量和等电点;用MEGA6.0来绘制邻接(Neighbor-joining,N-J)系统进化树[17];用NCBI的Conserved Domains(http://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi)程序预测蛋白质结构域。
3 结果与分析
3.1 拟南芥WRKY转录因子家族系统进化分析
利用MEGA6.0构建拟南芥72个WRKY转录因子家族蛋白的系统进化树,可将其分成3大类:12个属于GroupI,45个属于GroupII,14个属于GroupIII,还有一个独立的基因AtWRKY59。其中,GroupII又可分为5个亚类:IIa、IIb、IIc、IId和IIe,分别包含8、8、14、7、8个基因(图1,表1)。WRKY家族蛋白最重要的特征是具有高度保守的WRKY结构域。用Conserved Domains程序分析拟南芥WRKY转录因子蛋白的氨基酸序列,表明WRKY结构域在WRKY家族蛋白中高度保守,但其结构域数量在不同类型中有所不同,有些WRKY蛋白还有不同的锌指结构,有的是C2H2(CX4-5CX22-23HXH)型,有的是C2HC(CX7CX23HXC)型。结构域的数量及类型和锌指结构类型是WRKY家族蛋白分类的重要依据。GroupI中的转录因子含有两个WRKY结构域和C2H2型锌指结构,GroupII中的转录因子含有一个WRKY结构域和C2H2型锌指结构,GroupIII中的转录因子含有一个WRKY结构域和C2HC型锌指结构。
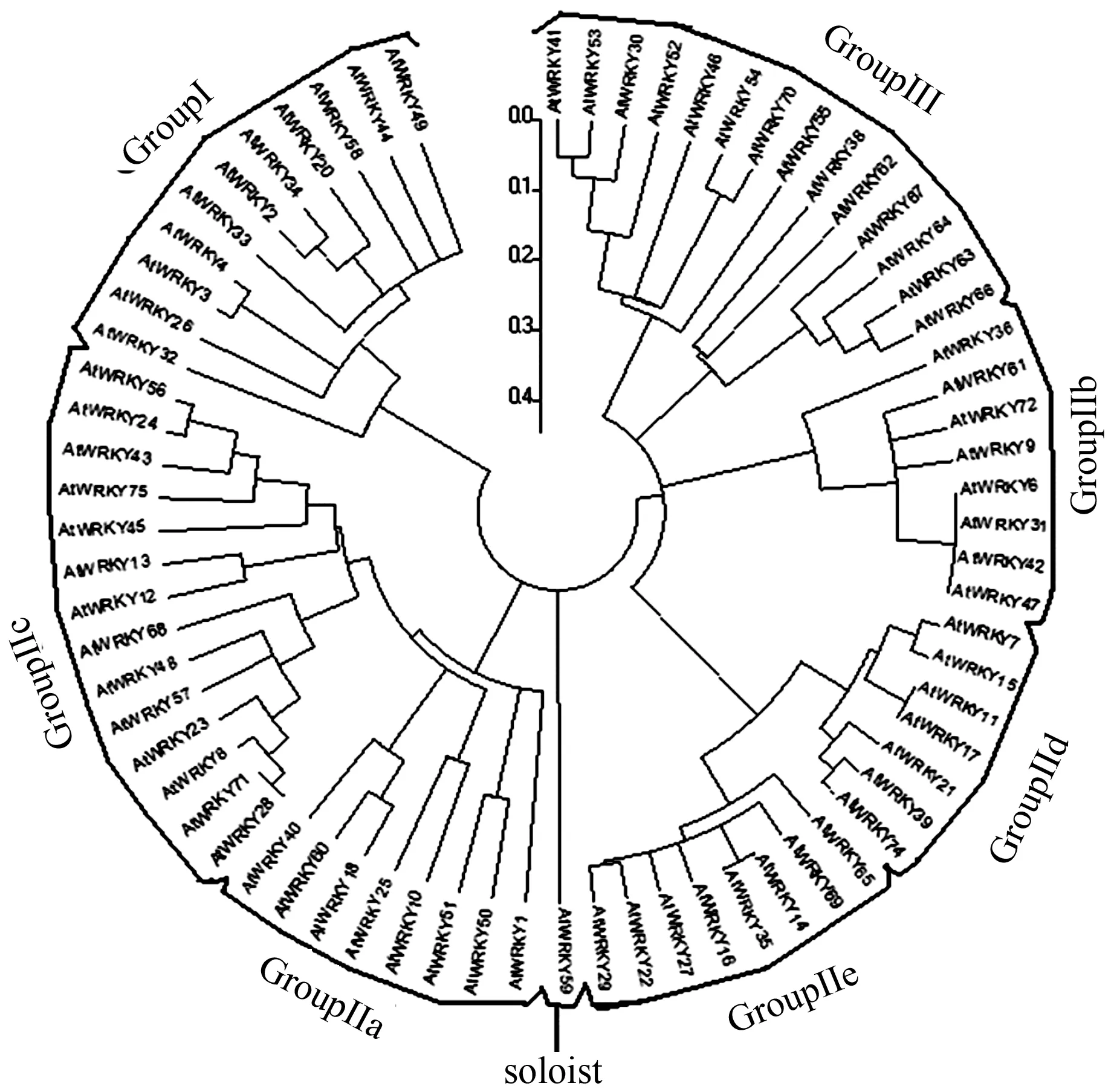
图1 拟南芥WRKY转录因子家族蛋白的进化树
3.2 拟南芥WRKY转录因子家族蛋白质理化性质
不同WRKY蛋白的氨基酸数目变化明显,理化性质不同,分子质量范围在12.95~200.00 ku,理论等电点的范围在4.01~10.41,并且不同酸碱性蛋白在不同类别中的分布差异较大。在GroupI的12个蛋白中有7个属于碱性,3个酸性,2个中性。在GroupIIa的8个蛋白中有5个属于碱性,3个酸性。在GroupIIb的8个蛋白中有1个属于碱性,3个酸性,4个中性。在GroupIIc的14个蛋白中有11个属于碱性,2个酸性,1个中性。GroupIId的7个蛋白均属碱性。在GroupIIe的8个蛋白中有1个属于碱性,6个酸性,1个中性。在GroupIII的14个蛋白中有2个属于碱性,12个酸性。不同类型WRKY蛋白间的差异可能与其具有不同的生物功能和参与的不同生理过程密切相关(表1)。
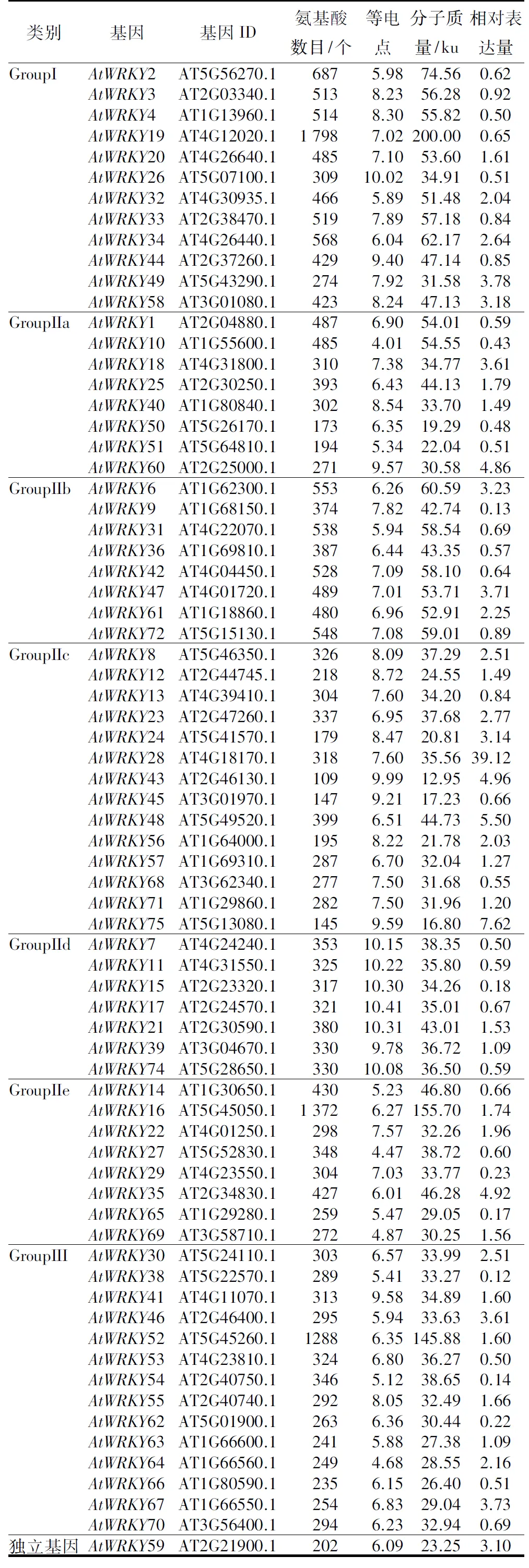
表1 拟南芥WRKY家族蛋白理化性质和相对表达量
3.3 拟南芥应答盐胁迫WRKY基因的筛选
用实时定量RT-qPCR检测NaCl胁迫24 h拟南芥WRKY转录因子基因的表达模式,将基因相对表达量大于2倍定义为上调表达,小于0.5倍定义为下调表达,介于上述两者之间的定义为没发生明显变化。结果表明:在72个基因中有30个(40.5%)盐胁迫应答基因,23个为上调表达基因,7个为基因下调表达。结合系统进化树分析发现,上调表达基因有4个分布在GroupI,14个分布在GroupII(GroupIIa中2个,GroupIIb中3个,GroupIIc中8个,GroupIIe中1个),4个分布在GroupIII,1个单独存在。而7个下调表达的基因中有1个分布在GroupIIb,1个分布GroupIId,2个分布在GroupIIe,3个分布在GroupIII(表1)。可见,上调表达的基因在GroupIIc中比例最高,占57.1%;其次是GroupIIb,占37.5%。下调表达的基因在GroupIIe和GroupIII中比例较高,分别占25%和21.4%(表2)。
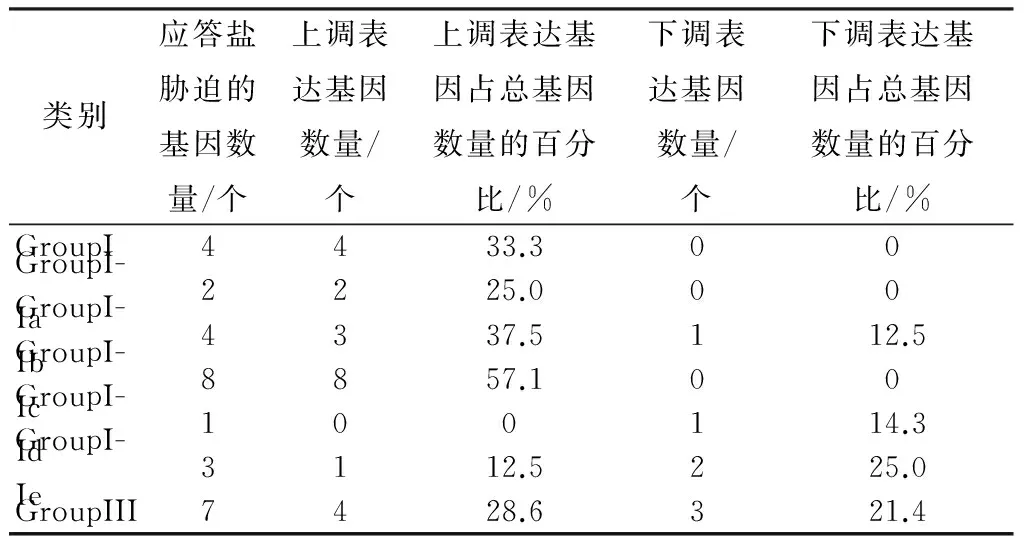
表2 应答盐胁迫WRKY基因在不同组中的分布
3.4 应答盐胁迫基因与其编码蛋白酸碱性的关系
拟南芥72个WRKY转录因子等电点范围在4.01~10.41,而30个应答盐胁迫的转录因子等电点范围在4.68~10.30(表3)。在23上调表达的转录因子中有19个等电点的范围在5.89~8.47,占总数的82.6%。在7个下调表达的转录因子中有3个等电点在5.12~5.47,有2个等电点分别为6.36和7.03。可见,在盐胁迫条件下,上调表达的WRKY转录因子基因编码蛋白的pH值多在5.89~8.47,多数属中性蛋白;上调表达基因编码蛋白的pH值多在5.12~7.03,多数属酸性蛋白。
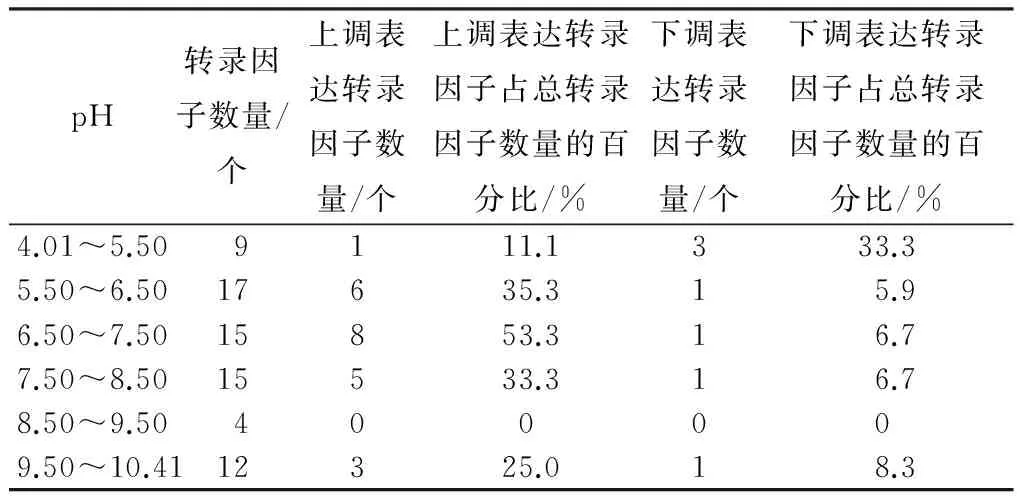
表3 应答盐胁迫WRKY蛋白的酸碱性及分布
4 结论与讨论
植物在逆境条件下,其体内会发生一系列的生理生化变化以适应逆境,一些抗逆相关基因也会大量表达,以感应传导逆境胁迫的信号和适应胁迫环境,如蛋白激酶、转录因子蛋白和抗逆相关蛋白等[18-20],WRKY转录因子基因在植物响应逆境胁迫和信号转导过程中起着非常重要的调控作用[21]。本研究为了解拟南芥WRKY转录因子的结构及其与应答盐胁迫的关系,对72个WRKY转录因子蛋白进行生物信息学分析,根据其WRKY结构域数量和锌指结构特点分为3大类GroupI、GroupII和GroupIII,其中GroupII又可分为IIa、IIb、IIc、IId和IIe 5个亚类;WRKY转录因子在植物中广泛参与抗病反应、信号转导、生长发育、形态建成等过程[22-26]。不同拟南芥WRKY转录因子蛋白的理化性质差异很大,其氨基酸数目在109~1 798,分子质量在12.95~200.00 ku,理论等电点介于4.01~10.41。这是不同拟南芥WRKY转录因子具有不同生物功能的分子基础,预示着WRKY基因可能参与不同的生理过程。在72个拟南芥WRKY转录因子基因中,有42个基因对盐胁迫反应不明显,在30个应答盐胁迫的基因中有23个上调表达基因,7个基因下调表达。
目前,有关WRKY转录因子基因提高植物抗逆能力的研究较多,但主要集中在抗病反应上。Dong et al[27]研究72个拟南芥的WRKY转录因子与抗病的关系,发现有49个受病原菌Pseudomonas syringae pvtomato(Pst)和SA诱导,进而调节相关抗病基因的表达。如拟南芥过量表AtWRKY70基因会增加其对Pst的抗性,反之,如果抑制AtWRKY70的表达,就会增加拟南芥对E.c.carotovora的敏感性[28]。拟南芥中的AtWRKY38、AtWRKY62、AtWRKY11、AtWRKY17对病原菌抗性具有负调控作用,插入突变沉默这些基因的拟南芥对病原菌的抗性增强,而过量表达AtWRKY38、AtWRKY62拟南芥对病原菌的抗性减弱[29]。欧美杂交杨Pnd-WRKY3基因在锈菌侵染后表现出抗病反应[30]。
植物WRKY基因广泛参与植物的盐胁迫。用150 mM NaCl处理拟南芥根系,有18个AtWRKY基因被诱导表达[31]。干旱和NaCl处理使拟南芥AtWRKY25和AtWRKY33的表达量提高,并且AtWRKY33缺失突变体和AtWRKY25、AtWRKY33双缺失突变体会增加植株对NaCl胁迫的敏感性,而超表达其中任何一个基因则会提高对NaCl胁迫的抗性[32]。NaCl胁迫可强烈诱导TcWRKY53的表达[33]。小麦TaWRKY10通过调节渗透平衡,活性氧清除和逆境相关基因的转录在盐胁迫的过程中起作用[34]。过表达GmWRKY5的转基因拟南芥可通过转录因子STZ/Zat10的调控增强耐盐性,但过表达GmWRKY13的转基因拟南芥对盐胁迫的敏感性提高[21]。在烟草中过表达棉花GhWRKY39-1可提高转基因植物对盐胁迫的耐性[35]。胡萝卜DcWRKY27和DcWRKY30基因可响应盐胁迫[11]。本研究对拟南芥WRKY转录因子进行生物信息学分析,并利用RT-qPCR筛选出30个应答盐胁迫的基因,可为进一步分析这些基因的功能提供参考依据。
[1] ULKER B, SOMSSICH I E. WRKY transcription factor: from DNA binding towards biological function[J]. Current Opinion in Plant Biology,2004,7(5):491-498.
[2] ISHIGURO S, NAKAMURA K. Characterization of a cDNA encoding anovel DNA-binding protein, SPF1, that recognizes SP8 sequencesin the 5′ upstream regions of genes coding for sporamin and beta-amylase from sweet potato[J]. Molecular and General Genetics,1994,244(6):563-571.
[3] ZHANG Y J, WANG L J. The WRKY transcription factor superfamily: its origin in eukaryotes and expansion in plants[J]. BMC Evolutionary Biology,2005,5(1):1-12.
[4] CAI M, QIU D Y, YUAN T, et al. Identification of novel pathogen-responsive cis-elements and their binding proteins in the promoter of OsWRKY13, a gene regulating rice disease resistance[J]. Plant, Cell & Environment,2008,31(1):86-96.
[5] CIOLKOWSKI I, WANKE D, BIRKENBIHL R P, et al. Studies on DNA-binding selectivity of WRKY transcription factors lend structural clues into WRKY-domain function[J]. Plant Molecular Biology,2008,68(1):81-92.
[6] 冉昆,王少敏,魏树伟,等.植物非生物胁迫相关的WRKY转录因子研究进展[J].青岛农业大学学报(自然科学版),2014,31(3):217-224.
[7] EULGEM T, RUSHTON P J, ROBATZEK S, et al. The WRKY superfamily of plant transcription factors[J]. Trends in Plant Science,2000,5(5):199-206.
[8] WEI K F, CHEN J, CHEN Y F, et al. Molecular phylogenetic and expression analysis of the complete WRKY transcription factor family in maize[J]. DNA Research An International Journal for Rapid Publication of Reports on Genes Genomes,2012,19(2):153-164.
[9] HE H S, DONG Q, SHAO Y H, et al. Genome-wide survey and characterization of the WRKY gene family in Populus trichocarpa[J] . Plant Cell Reports,2012,31(7):1199-1217.
[10] YANG B O, JIANG Y Q, RAHMAN M H, et al. Identification and expression analysis of WRKY transcription factor genes in canola (BrassicanapusL.) in response to fungal pathogens and hormone treatments[J]. BMC Plant Biology,2009,9(1):68-87.
[11] LI M Y, XU Z S, TIAN C, et al. Genomic identification of WRKY transcription factors in carrot (Daucus carota) and analysis of evolution and homologous groups for plants[J]. Scientific Reports,2016,6(10):1-17.
[12] 王娜,张振葆,黄凤珠,等.WRKY转录因子参与植物非生物胁迫应答的研究进展[J].核农学报,2014,28(10):1819-1827.
[13] FOOLAD M R, JONES R A. Mapping salt-tolerance genes in tomato using trait-based marker analysis[J]. Theor Appl Genet,1993,87(1):184-192.
[14] NICOLE R, BEAT F. Experimental comparison of relative RTqPCR quantification approaches for gene expression studies inpoplar[J]. BMC Molecular Biology,2010,11:1471-2199.[15] 张贺,李波,周虚,等.实时荧光定量PCR技术研究进展及应用[J].动物医学进展,2006,27(S1):5-12.
[16] HANCOCK J M, BISHOP M J. ORF find (open reading frame finder)[M]. Hoboken: John Wiley Sons Inc,2013.
[17] TAMURA K, PETERSON D, PETERSON N, et al. MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods[J]. Molecular Biology and Evolution,2011,28(10):2731-2739.
[18] 李晓星,张大兵,陈亮,等.水稻bHLH基因家族成员表达模式分析[J].厦门大学学报(自然科学版),2006,45(增刊):73-77.
[19] 李洁.植物转录因子与基因调控[J].生物学通报,2004,39(3):9-11.
[20] 雷娟.对拟南芥转录因子TCP家族的生物信息学分析[M].北京:科学出版社,2010.
[21] ZHOU Q Y, TIAN A G, ZOU H F, et al. SoybeanWRKY-type transcription factor genes,GmWRKY13,GmWRKY21, andGmWRKY54, confer differential tolerance to abiotic stresses in transgenic Arabidopsis plants[J]. Plant Biotechnol,2008,6(5):486-503.
[22] YU D Q, CHEN C H, CHEN Z X. Evidence for an important role of WRKY DNA binding proteins in the regulation of NPR1 gene expression[J]. Plant Cell,2001,13(7):1527-1540.
[23] ASAI T, TENA G, PLOTNIKOVA J, et al. MAP kinase signaling cascade in Arabidopsis innate immunity[J]. Nature,2002,415:977-983.
[24] JOHNSON C S, KOLEVSKI B, SMYTH D R. Transparent testa glabra2, a trichome and seed coat development gene of Arabidopsis, encodes a WRKY transcription factor[J]. Plant Cell,2002,14(6):1359-1375.
[25] LUO M, DENNIS E S, BERGER F, et al. MINISEED3 (MINI3), a WRKY family gene, and HAIKU2(IKU2), a leucine-rich repeat (LRR) KINASE gene, are regulators of seed size in Arabidopsis[J]. Proc Natl Acad Sci USA,2005,102(48):17531-17536.
[26] ROBATZEK S, SOMSSICH I E. Targets of AtWRKY6 regulation during plant senescence and pathogen defense[J]. Genes Dev,2002,16(9):1139-1149.
[27] DONG J X, CHEN C H, CHEN Z X. Expression profiles of the Arabidopsis WRKY gene superfamily during plant defense response[J]. Plant Molecular Biology,2003,51(1):21-37.
[28] LI J, BRADER G, PALVA E T. The WRKY70 transcription factor: a node of convergence for jasmonate-mediated and salicylate-mediated signals in plant defense[J]. The Plant Cell,2004,16(2):319-331.
[29] KIM K C, LAI Z B, FAN B F, et al. Arabidopsis WRKY38 and WRKY62 Transcription Factors Interact with Histone Deacetylase 19 in Basal Defense[J]. Plant Cell,2008,20(9):2357-2371.
[30] 牛春阳,李丹蕾,王峰,等.基于转录组的欧美杨Pnd-WRKY3基因克隆及其抗锈菌表达[J]. 东北林业大学学报, 2015, 43(9):1-5.
[31] JIANG Y Q, DEVHOLOS M K. Comprehensive transcriptional profiling of NaCl stressedArabidopsisroots reveals novel classes of responsive genes[J]. BMC Plant Biology,2006,6(25):25-44.
[32] LI S J, FU Q T, CHEN L G, et al.ArabidopsisthalianaWRKY25, WRKY26, and WRKY33 coordinate induction of plant thermo tolerance[J]. Planta,2011,233(6):1237-1252.
[33] WEI W, ZHANG Y X, LU H, et al. A novel WRKY Transcriptional factor fromThlaspicaerulescensnegatively regulates the osmotic stress tolerance of transgenic tobacco[J]. Plant Cell Reports,2008,27(4):795-803.
[34] WANG C, DENG P Y, CHEN L L, et al. A wheat WRKY transcription factor TaWRKY10 confers tolerance to multiple abiotic stresses in transgenic tobacco[J]. PloS ONE,2013,8(6):e65120.
[35] SHI W N, HAO L L, LI J, et al. The Gossypium hirsutum WRKY gene GhWRKY39-1 promotes pathogen infection defense responses and mediates salt stress tolerance in transgenicNicotianabenthamiana[J]. Plant Cell Reports,2014,33(3):483-498.
Identification ofWRKYGene in Response to Abiotic Stress from WRKY Transcription Factor Gene Family ofArabidopsisthaliana//
Wei Xiaoai, Yao Wenjing, Jiang Tingbo, Zhou Boru
(Northeast Forestry University, Harbin 150040, P. R. China)//Journal of Northeast Forestry University,2016,44(10):45-48,55.
For screening and identifying stress-related genes inArabidopsisthaliana, theWRKYgene families were as study object, and 72WRKYgenes were explored from the database ofA.thaliana, and the structure characteristics were analyzed by bioinformatics. WRKY family was further divided into three groups: GroupI, GroupII and GroupIII. The gene members in GroupII were further divided into five sub-groups: IIa, IIb, IIc, IId, IIe. The differential expression of WRKY genes were determined by real-time RT-PCR. There were 30 genes response to salt stress, of which 23 were up-regulated genes, and 7 were down-regulated genes.
Arabidopsisthaliana; WRKY transcription factor; Abiotic stress
魏晓爱,女,1990年2月生,林木遗传育种国家重点实验室(东北林业大学),硕士研究生。E-mail:15244689083@163.com。
周博如,林木遗传育种国家重点实验室(东北林业大学),副教授。E-mail:boruzhou@yahoo.com。
2016年2月19日。
Q78;S332.1
1)卓越农林人才教育培养计划改革试点项目。
责任编辑:潘 华。

