反应结晶制备碳酸锂的粒度及形貌控制*
王彦飞,王磊鑫,邢 红,杨 静,赵艳平,杨立斌,朱 亮,赵晓昱,沙作良,王文海
(1.天津科技大学化工与材料学院,天津市海洋资源与化学重点实验室,天津300457;2.青海盐湖佛照蓝科锂业股份有限公司)
研究与开发
反应结晶制备碳酸锂的粒度及形貌控制*
王彦飞1,王磊鑫1,邢 红2,杨 静1,赵艳平1,杨立斌1,朱 亮1,赵晓昱1,沙作良1,王文海2
(1.天津科技大学化工与材料学院,天津市海洋资源与化学重点实验室,天津300457;2.青海盐湖佛照蓝科锂业股份有限公司)
碳酸锂的粒度及形貌决定其性能和应用。通过考察反应结晶温度、进料速率、晶种用量和搅拌速率对碳酸锂产品平均粒径的影响以及添加剂的用量对产品形貌的影响,提供了一种经过优化的制备碳酸锂的反应结晶工艺。通过正交实验确定了反应结晶制备碳酸锂的最佳实验条件:200 mL质量浓度为90 g/L的氯化锂溶液一次性加入反应结晶器内,质量浓度为260 g/L的碳酸钠溶液的加料速率为0.5 mL/min,晶种用量为2%(占碳酸锂理论产量的分数),搅拌速率为400 r/min,反应温度为80℃,添加剂六偏磷酸钠用量为2%(占碳酸锂理论产量的分数)。在此条件下制得的碳酸锂为平均粒径为132 μm、变异系数为51.53%的密实球形产品。研究表明,反应温度对晶体粒度的影响最大,添加剂对晶体的粒度和形貌起到调控作用。
反应结晶;碳酸锂;粒度分布;形貌;添加剂
碳酸锂用途非常广泛,在玻璃、能源、冶金、电池、医药等重要工业领域都是不可或缺的原料。随着全球新能源开发的升温以及动力和储能用锂离子电池的高速发展,作为核心原材料的碳酸锂,其市场前景十分广阔[1-5]。目前生产碳酸锂的原料主要来自于矿石和盐湖卤水。其中矿石提取工艺主要有石灰石焙烧法、硫酸法和硫酸盐法,虽然其方法较成熟,但是存在能耗高、成本高、污染严重等缺点[6-7]。盐湖卤水提取碳酸锂的工艺较多,常用的包括碳酸盐沉淀法、煅烧浸取法和太阳池浓缩法,并且凭借其耗能低、生产成本低、工艺简单等优势,来自盐湖卤水的锂产品逐渐取代了来自固体矿石的锂产品,成为市场的主流[8-11]。米泽华[9]对碳酸锂微粉的制备方法进行了探讨,他们将其制备方法分为机械粉碎法、固相法、混相法、液相法(沉淀法)和气相法。孙玉柱[10]主要研究了溶析-反应结晶、喷雾干燥、超声、膜分散等碳酸锂结晶技术。王雪梅[11]研究了球形碳酸锂产品的制备工艺和形成机理,并通过沉淀法制备出超细粉碳酸锂产品。张嫦等[12]对球形微细碳酸锂粉体的制备工艺进行了研究,采用的方法是碳酸氢铵复分解法。当前工业级碳酸锂产品平均粒径小,粒度分布不均匀,晶体产品形貌呈针状,难以过滤回收,含湿量高(现有工业生产碳酸锂固液分离后的湿固相含湿质量分数为40%),杂质含量高,导致后续干燥能耗大。解决上述问题的关键是增大产品粒径以及控制产品形貌。现有文献对碳酸锂粒度及形貌调控的研究匮乏。笔者以氯化锂和碳酸钠反应结晶为基础,考察了反应温度、进料速率、晶种用量和搅拌速率对碳酸锂产品粒径的影响,开发出一种能得到较大平均粒径的球形碳酸锂产品的方法,彻底解决了目前困扰企业产品品质的瓶颈问题。
1 实验材料和方法
1.1 主要试剂和仪器
试剂:无水碳酸钠、无水氯化锂、六偏磷酸钠均为分析纯,所有溶液采用去离子水配制,晶种自制。
仪器:Mettler Toledo FBRM D600型聚焦光束反射测量仪(用于测定产品的粒度);日立SU1510型扫描电镜(用于表征样品的形貌);普析XD-3型转靶X射线多晶衍射仪(用于表征样品的物相组成)。
1.2 实验方法
将200 mL质量浓度为90 g/L(25℃)的LiCl2溶液,一次性加入玻璃夹套反应器中恒温,加入一定量晶种和2%六偏磷酸钠(二者加入量都为占碳酸锂理论产量的分数)恒温10 min,然后将40℃恒温的Na2CO3溶液(100 mL,260 g/L,25℃下配制)以一定速率滴加到反应器中,加料完毕后继续搅拌30 min,实验过程全程采用FBRM监测。反应完毕将碳酸锂晶体洗涤、过滤、烘干,对烘干前后的产品进行称量,考察其含湿量。通过单因素实验及正交实验考察反应温度、进料速率、晶种用量和搅拌速率对产品平均粒径的影响。在优化工艺参数基础上,进一步考察了添加剂用量对碳酸锂形貌的影响。
2 实验结果与讨论
2.1 单因素实验
2.1.1 加料速率的影响
固定条件:LiCl2溶液质量浓度为90 g/L,Na2CO3溶液质量浓度为260 g/L,反应温度为90℃,晶种用量为2%,六偏磷酸钠用量为2%,搅拌转速为400 r/min。改变碳酸钠溶液加料速率分别为0.5、1.0、2.0、4.0 mL/min,考察碳酸钠加料速率对碳酸锂产品粒径的影响,结果见图1。由图1得出碳酸钠不同加料速率制得碳酸锂平均粒径分别为114.01、130.17、120.20、86.99 μm,在加料速率为1.0 mL/min时制得产品的粒度最大。随着加料速率增大,反应体系中过饱和度逐渐增大,晶体成核占主导地位,因而产品粒度变小。而加料速率过小时(0.5 mL/min),产品粒度呈双峰分布,并且分布较宽。究其原因有可能是加料速率过慢导致反应结晶时间过长,搅拌导致产品破碎程度较大,使得产品粒径呈现双峰分布。

图1 碳酸钠不同加料速率制得碳酸锂的粒度分布图
图2为碳酸钠加料速率为1.0 mL/min条件下所得碳酸锂在反应过程中的粒度和粒数的变化。由图2看出,从反应开始到16 min左右,由于过饱和度过大导致爆发成核,有大量小粒度晶体生成,因而此时产品的平均粒度突然下降,粒数急剧增加。此后过饱和度变小,晶体开始生长,产品粒度开始变大并伴随着粒数减少,最终到反应结束时稳定。
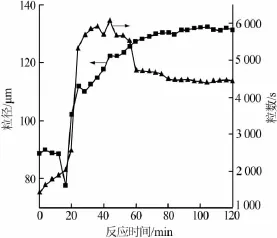
图2 反应结晶过程中碳酸锂粒度和粒数变化
2.1.2 晶种用量的影响
在反应体系中加入晶种(平均粒径为10 μm左右),可以提供有效生长表面,使得产品在晶种晶体表面生长。控制溶液过饱和度在一定范围内,避免出现初级成核现象,这样可以控制晶体的生长,获得较均匀的晶体产品。
选择碳酸钠溶液加料速率为1.0 mL/min,晶种加入量分别为1%、2%、5%、8%,其他工艺条件同2.1.1节,考察晶种加入量对碳酸锂粒度的影响。最终产物的粒度分布图及相应的晶体粒度和变异系数(CV)分别见图3和表1。
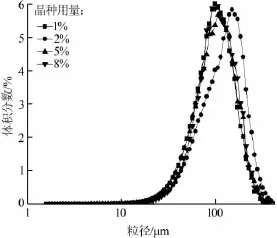
图3 不同晶种用量制得碳酸锂的粒度分布图

表1 不同晶种用量制得碳酸锂的粒度及变异系数
从图3和表1可以明显地看出,晶种用量对结晶过程有一定的影响。从表1可以看出,加入2%晶种时得到的产品平均粒径最大,证明此时晶种的用量最合适。如果加入1%的晶种,由于晶种用量不够,不能够提供更多的表面供晶体生长,从而不能消耗过多的过饱和度,使得小晶体增多,粒度变小;反之晶种过多又会影响产品平均粒径的增长。从表1还可以得知,加入晶种制得产品的变异系数都在50%左右,均一度良好,晶种用量的不同也没有使得变异系数有大的变化。从图3可以明显地看出,各组产品平均粒径分布都很均匀,宽度相差很小。
2.1.3 反应温度的影响
反应温度是结晶工艺中的一个重要参数,碳酸锂的溶解度随温度的升高而下降。选择加料速率为1.0 mL/min,反应温度分别为60、70、80、90℃,其他工艺条件同2.1.1节,考察反应温度对碳酸锂产品粒度及含湿量(质量分数)的影响,结果见图4及表2。

图4 不同反应温度制得碳酸锂的粒度分布图

表2 不同反应温度制得碳酸锂的含湿量
从图4和表2看出,反应温度越高,碳酸锂的粒度越大,含湿量越小。这是由于温度升高,体系黏度减小,利于晶体生长,因而制备的产品粒度越大,晶体的分散性、流动性越好,所以产品的含湿量越小。反应温度为60~90℃时制得产品的含湿量<14%。
2.1.4 搅拌速率的影响
其他工艺条件同2.1.1节,考察搅拌速率对碳酸锂产品粒度的影响,结果见图5。
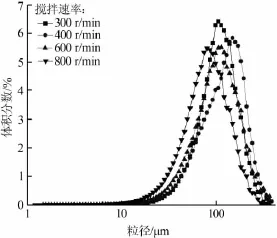
图5 不同搅拌速率制得碳酸锂的粒度分布图
由图5看出,不同搅拌速率所得碳酸锂平均粒经分别为115.53、130.17、115.69、89.74μm。在搅拌速率为400 r/min时所得产品平均粒度最大(130.17 μm),而较小搅拌速率和较大搅拌速率所得产品粒度都偏小。分析原因为,搅拌速率过低,晶体在反应体系中混合不均匀,不利于晶体生长;搅拌速率过高,晶浆内流体剪应力增大,又会增大二次成核的速率和晶体破碎的概率,使得晶体粒度减小。
2.2 正交实验
在单因素实验基础上,对反应温度、加料速率、晶种用量和搅拌速率4个因素采用L9(34)正交表进行正交实验,对碳酸锂反应结晶实验条件做进一步优化。实验结果列于表3。
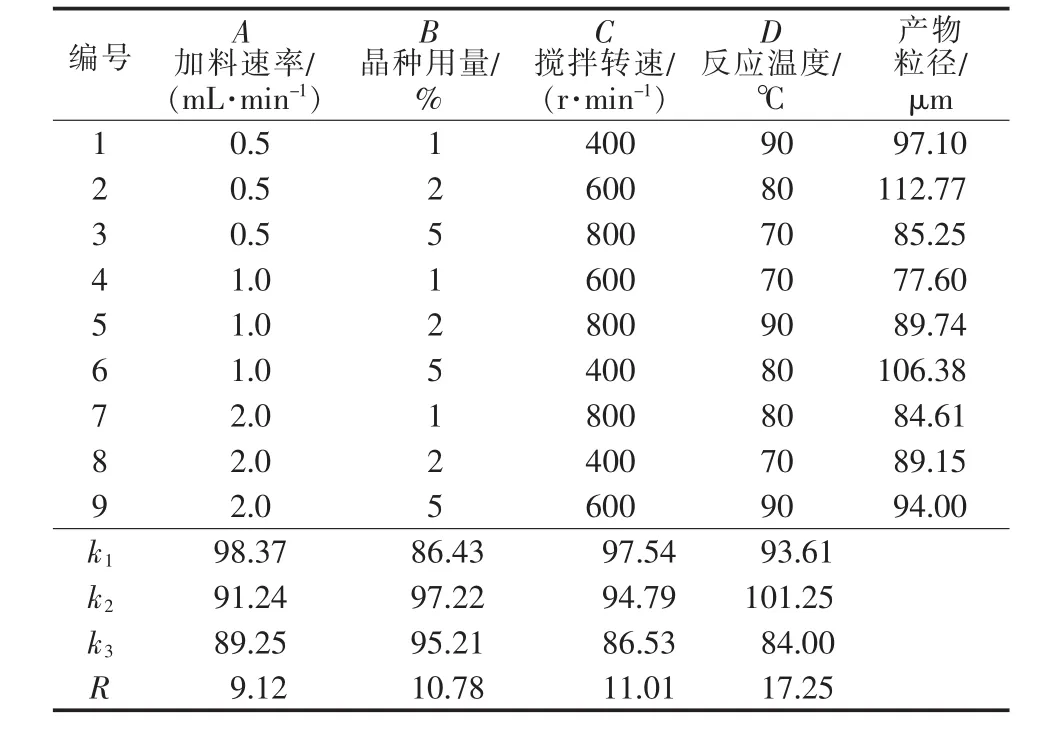
表3 正交实验设计及结果
从表3看出,反应温度(D)对产品粒度的影响最大,故因素D是最主要因素;因素A1为边值(0.5 mL/min),由于进料速率再慢会导致设备产能太低,又因价值影响较低,故不再进一步降低进料速率。从表3得出最佳实验方案为A1B2C1D2,按此因素组合得出相应条件:LiCl2溶液质量浓度为90 g/L,Na2CO3溶液质量浓度为260 g/L,晶种用量为2%,六偏磷酸钠用量为2%,反应温度为80℃,加料速率为0.5 mL/min,搅拌速率为400 r/min。按此条件进行验证实验得到碳酸锂平均粒径为132 μm,固液分离后产品含湿量为8.26%,变异系数为51.53%,实验结果优于单因素实验和正交实验的最佳结果。由于加料速率对考察目标的影响最小,为提高设备产能,在实际生产过程中,可以适当提高碳酸钠加料速率。
优化条件下制备的碳酸锂晶体经洗涤、干燥进行XRD和SEM表征,结果见图6和图7。图6显示,产品物相中只检测出Li2CO3。从图7可以看出,碳酸锂产物为紧密、规则的球形晶体。
2.3 六偏磷酸钠用量对产品形貌和粒度的影响
在最优条件下考察六偏磷酸钠用量对碳酸锂产品形貌和平均粒径的影响,结果见图8。由图8看出,在六偏磷酸钠用量分别为0%、1%、2%、3%条件下,碳酸锂平均粒径依次为130.20、107.65、132.00、 93.33 μm。在没投加六偏磷酸钠情况下,产品为棒状晶体而且有明显的团聚现象,虽然所测平均粒径为130.20 μm,但并不能反应其真实大小;随着六偏磷酸钠用量增加,球体聚结越来越密实,孔隙率越来越小,逐渐从花瓣状变成密实球体;但加入3%六偏磷酸钠时,过量六偏磷酸钠对碳酸锂助溶作用[11]过大,导致小粒度球形产品增多,产品粒度变小,所以合适的六偏磷酸钠用量为2%。
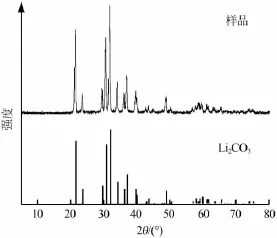
图6 最优条件下制得碳酸锂XRD谱图

图7 最优条件下制得碳酸锂SEM照片
3 结论
1)氯化锂和碳酸钠反应结晶制得形貌规则的球形碳酸锂产品的最优实验条件:LiCl溶液质量浓度为90 g/L,Na2CO3溶液质量浓度为260 g/L,反应温度为80℃,搅拌速率为400 r/min,晶种用量为2%,六偏磷酸钠用量为2%,加料速率为0.5 mL/min。在最优工艺条件下制得碳酸锂产品的平均粒径132 μm,含湿量为8.26%。2)碳酸锂的平均粒径受反应温度的影响最大,受其他因素的影响由高到低分别是搅拌速率、晶种用量和加料速率。3)碳酸锂的晶体形貌取决于六偏磷酸钠的加入量,六偏磷酸钠对产品的形貌有调控作用。4)通过对反应结晶制备碳酸锂工艺参数的优化,实现了对碳酸锂产品粒度和形貌的控制。制得的碳酸锂产品的平均粒径是现有工业化产品粒径的10倍左右(现有工业产品平均粒径为10~20 μm),产品的形貌为规则球形,固液分离后产品的含湿量是现有工业产品含湿量的1/4左右。该方法提高了碳酸锂的纯度,降低了产品的含湿量,解决了目前困扰企业生产的技术瓶颈问题。
[1] 陈婷,闫书一,康自华.我国盐湖卤水提锂的研究进展[J].盐业与化工,2007,36(2):19-21.
[2] 杨兆娟,向兰.从盐湖卤水中提锂的研究进展[J].海湖盐与化工,2005,34(6):27-29.
[3] 刘元会,邓天龙.国内外从盐湖卤水中提锂工艺技术研究进展[J].世界科技研究与发展,2006,28(5):69-75.
[4] 钟辉,周燕芳,殷辉安.卤水锂资源开发技术进展[J].矿产综合利用,2003(1):23-28.
[5] 刘向磊,钟辉,唐中杰.盐湖卤水提锂工艺技术现状及存在的问题[J].无机盐工业,2009,41(6):4-6.
[6] 郑春辉,董殿权,刘亦凡.卤水锂资源及其开发进展[J].盐业与化工,2006,35(6):39-41.
[7]Mehta V C.Process for recovery lithium from salt brines:US,4723962[P].1988-02-29.
[8]Neipert M P,Bon C K.Method of lithium recovery:US,3306700[P]. 1967-02-28.
[9] 米泽华.碳酸锂微粉的制备方法探讨[J].新疆有色金属,2001(4):22-24.
[10] 孙玉柱.碳酸锂结晶过程研究[D].上海:华东理工大学,2010.
[11] 王雪梅.碳酸锂反应结晶过程的研究[D].天津:天津大学,2014.
[12] 张嫦,赵青.球形微细碳酸锂粉体的制备工艺研究[J].西南民族大学学报:自然科学版,2008,34(2):326-329.
Size and morphology controlling of lithium carbonate in reactive crystallization process
Wang Yanfei1,Wang Leixin1,Xing Hong2,Yang Jing1,Zhao Yanping1,Yang Libin1,Zhu Liang1,Zhao Xiaoyu1,Sha Zuoliang1,Wang Wenhai2
(1.Tianjin Key Laboratory of Marine Resources and Chemistry,College of Chemical Engineering and Materials Science,Tianjin University of Science&Technology,Tianjin 300457,China;2.Qinhai Saltlake Fozhao Lake Lithium Co.,Ltd.)
The properties and applications of lithium carbonate depend on its size and morphology.A novel size and morphology controlling technology of lithium carbonate in reactive crystallization process was proposed.The effects of reactive crystallization temperature,feeding rate,seeding dosage,and stirring rate on the average particle size and the effect of additive on the morphology were investigated.By study of orthogonal experiments,the optimal experimental conditions for the reactive crystallization of lithium carbonate were concluded by:put 200 mL lithium chloride solution with mass concentration of 90 g/L into the reaction crystallizer,the sodium carbonate solution with mass concentration of 260 g/L was fed with the rate of 0.5 mL/min,seeding dosage was 2%(relative to the mass fraction of lithium carbonate theoretical yield),stirring rate was 400 r/min,reactive temperature was 80℃and additive was 2%(relative to the mass fraction of lithium carbonate theoretical yield)sodium hexametaphosphate.Under those conditions,the product was a dense spherical product with the average size of 132 μm and with the variation coefficient of 51.53%.The study showed that size of particles was mainly determined by reactive temperature,and the additive,however,played an adjustable effect on both size and morphology.
reactive crystallization;lithium carbonate;particle size distribution;morphology;additive
TQ131.11
A
1006-4990(2016)09-0013-05
2016-03-12
王彦飞(1977— ),男,博士,副教授,研究领域为工业结晶。
青海省科技厅科技支撑计划(2015-GX-109A);教育部科研创新团队培育计划([2013]373);天津市高等学校创新团队培养计划(TD12-5004)。
联系方式:wangyanfei@tust.edu.cn

