慢性炎性脱髓鞘性多发性神经病与腓骨肌萎缩症-I型的临床及神经电生理比较
刘璟洁韩萍高震巩付华马晓灵向莉
慢性炎性脱髓鞘性多发性神经病与腓骨肌萎缩症-I型的临床及神经电生理比较
刘璟洁*韩萍△高震*巩付华*马晓灵*向莉*
目的比较慢性炎性脱髓鞘性多发性神经病(chronic inflammatory demyelinating polyneuropathy,CIDP)与腓骨肌萎缩症-I型(type-I Charcot Marie Tooth disease,CMT-I)的临床及神经电生理特点,以指导两者的鉴别诊断。方法纳入CIDP患者31例、CMT-I患者28例,收集其一般临床资料并对两组患者进行神经电生理检测,比较两组患者的临床特点及电生理指标,并对电生理严重程度与临床症状严重程度进行相关性分析。结果CIDP与CMT-I两组患者起病部位、主观感觉障碍、足部畸形、脑脊液蛋白比较有统计学差异(P<0.05)。运动末梢潜伏期(distal motor latency,DML)、运动传导速度(motor conduction velocity,MCV)、感觉传导速度(sensory conduction velocity,SCV)、传导阻滞/波形离散、下肢神经继发性轴索变性具有统计学差异(P<0.05)。失神经电位、MUAP形态异常、募集减少具有统计学差异(P<0.05)。CIDP临床症状严重程度与电生理严重程度有相关性(r=0.84,P<0.05);而CMT-I临床症状严重程度与电生理严重程度分离,不具有相关性(r=0.27,P>0.05)。结论综合分析临床特点、神经传导、针极肌电图、临床与电生理严重程度的相关性可以对CIDP与CMT-1进行鉴别诊断。
慢性炎性脱髓鞘性多发性神经病 腓骨肌萎缩症-I型 神经电生理
慢性脱髓鞘性周围神经病在多发性周围神经病中很常见,按病因主要分为获得性和遗传性两类。慢性炎性脱髓鞘性多发性神经病(chronic inflammatory demyelinating polyneuropathy,CIDP)是最常见的获得性慢性脱髓鞘性周围神经病类型。而腓骨肌萎缩症-I型(type-I Charcot-Marie-Tooth disease,CMT-I),又称遗传性运动感觉性周围神经病-I型,是最常见的遗传性慢性脱髓鞘性周围神经病类型。这两种疾病均起病隐匿,主要表现为肢体无力,自远端向近端发展,下肢症状重于上肢,伴有肌肉萎缩及感觉障碍,脑脊液蛋白均可升高,临床表现极为相似;同时肌电图上均可表现为周围神经潜伏期延长、传导速度减慢等脱髓鞘病变特点,因此极易发生误诊误治。本文对CIDP及CMT-I患者进行临床及神经电生理比较,以进一步指导二者的鉴别诊断。
1 对象与方法
1.1研究对象 收集于2012年1月至2015年6月在西安交通大学第二附属医院神经内科就诊的CIDP患者31例,其中男16例,女15例,就诊年龄39~63岁,病程6个月~3.5年;CMT-I患者28例,其中男15例,女13例,就诊年龄19~69岁,病程11个月~14年。两组患者在年龄、性别、病程上无统计学差异。入组标准:①CIDP符合2010年中国慢性炎性脱髓鞘性多发性神经根神经病诊疗指南推荐的诊断标准[1],而CMT-I符合1997年陈氏[2]的诊断标准;②均接受肌电图及腰椎穿刺检查;③临床资料完整;④均签署知情同意书。排除标准:①其余原因导致的周围神经病变;②存在神经肌肉接头病变、肌肉病变或前角病变;③既往曾应用糖皮质激素、丙种球蛋白或免疫抑制剂治疗。所有患者均签署知情同意书,并通过西安交通大学第二附属医院伦理委员会审核。
1.2研究方法
1.2.1临床资料收集 所有患者均详细登记临床资料,包括性别、年龄、病史、体征、家族史、脑脊液结果等。
1.2.2神经电生理检查 采用上海海神-NDI094型肌电图诱发电位仪行肌电图检查。采用表面电极进行运动神经传导速度测定,检测神经有双侧正中神经、尺神经、腓总神经、胫神经,观察指标包括:运动末梢潜伏期(distal motor latency,DML)、远端复合肌肉动作电位(distal compound motor action potential,dCMAP)波幅、近段复合肌肉动作电位(proximal compound motor action potential,pCMAP)波幅、运动传导速度(motor conduction velocity,MCV)、传导阻滞(conduction block,CB)及波形离散。DML采用从刺激开始至CMAP起始点之间的时间。CMAP波幅采用峰-峰值波幅。传导阻滞采用1999年美国电诊断医学协会的标准[3],包括了肯定的传导阻滞及可能的传导阻滞。肯定的传导阻滞定义为:近段刺激与远端比较,当CMAP时限增加小于等于30%时,波幅下降大于50%。可能的传导阻滞定义为:近段刺激与远端比较,当CMAP时限增加大于30%时,波幅下降大于50%。波形离散定义为:周围神经常规节段近段刺激与远端比较,CMAP时限增宽30%以上。采用逆向法对以上神经进行感觉神经传导速度测定,观察指标包括:感觉神经动作电位(sensory nerve action potential,SNAP)波幅、感觉传导速度(sensory conduction velocity,SCV)。SNAP波幅采用峰-峰值波幅。所有患者均行针极肌电图检查,检测肌肉为单侧第一骨间背侧肌、三角肌、胫前肌及股直肌,观察指标包括:静息电位、运动单位电位(motor unit action potential,MUAP)以及募集电位。
1.2.3分组根据改良 Rankin量表(modified Rankin scale,MRS)评估患者的运动功能,细则如下:0分:完全无症状;1分:尽管有症状,但无明显功能障碍,能完成日常活动;2分:轻度残疾,不能完成所有活动,但可自理;3分:中度残疾,需要一些照顾,但行走不需要帮助;4分:重度残疾,不能独立行走,无他人帮助不能自理;5分:严重残疾,瘫痪卧床。根据MRS评分结果对CIDP及CMT-I进行临床分组,分为:轻度组:0~1分;中度组:2~3分;重度组:4~5分。所有患者肌电图均符合脱髓鞘病变特点,同时根据下肢周围神经继发性轴索变性程度进行电生理分组,分为:轻度组:CMAP波幅下降小于50%;中度组:CMAP波幅下降大于50%、小于70%;重度组:CMAP波幅下降大于70%或引不出。
1.3统计学方法采用SPSS13.0进行统计分析。计量资料以(x±s)表示,组间比较釆取独立样本t检验;计数资料以例数和构成比表示,两组间比较采用χ2检验或Fisher's检验;Spearman相关分析探讨电生理严重程度与临床症状严重程度的相关性。检验水准α=0.05,双侧检验。
2 结果
2.1临床资料比较 见表1。

表1 CIDP与CMT-I临床资料比较
2.2神经电生理结果比较
2.2.1神经传导检查结果比较 以双侧正中神经、腓总神经为例进行说明,尺神经及胫神经变化规律与之类似(见表2、图1)。

表2 CIDP与CMT-I神经传导结果比较
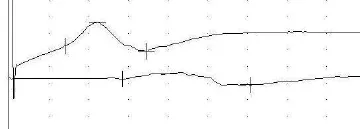
图1 典型CIDP腓总神经的传导阻滞及波形离散 注:扫描速度5m/s,灵敏度1mV/D,刺激电量80mA
2.2.2针极肌电图检查结果比较 所有患者均行针极肌电图检查,CIDP组共检测124块肌肉,CMT-I组共检测112块肌肉。对两组患者失神经电位的出现率进行χ2检验,CIDP组为60.5%(75/124),而CMT-I组为14.3%(16/112),CIDP组失神经电位的出现率显著高于CMT-I组。对两组患者MUAP形态异常的出现率进行χ2检验,CIDP组为64.5%(80/ 124),而CMT-I组为93.8%(105/112),CMT-I组MUAP形态异常的出现率显著高于CIDP组。对两组患者募集减少的出现率进行χ2检验,CIDP组为73.4%(91/124),而CMT-I组98.2%(110/112),CMT-I组显著高于CIDP组。
2.2.3Spearman相关性分析 见表3。

表3 CIDP与CMT-I临床严重程度与电生理严重程度观察
3 讨论
CIDP与CMT-I临床表现类似,极易误诊,而对二者进行鉴别诊断对于进一步的遗传学检查及治疗意义重大。CIDP为后天获得性疾病,很少家族聚集出现,多没有明确的家族史。而CMT-I尽管为遗传性疾病,但由于其遗传方式包括常染色体显性、常染色体隐形或散发[4-5],仅部分患者存在明确家族史,故家族史仅可为部分CMT-I患者的诊断提供线索。对于无家族史的CMT-I需依赖其余方式与CIDP进行鉴别。
CIDP与CMT-I临床表现类似但不完全相同。CIDP主要从下肢起病,少部分从上肢起病或四肢同时起病[6]。而CMT-I神经损伤呈长度依赖性特点,往往从足部开始起病[7],没有从上肢起病者。本研究19%的CIDP患者从上肢起病,而CMT-I主要从下肢起病,与以往结果类似。因此起病部位有助于二者的鉴别。CIDP部分患者存在颅神经麻痹[8],面瘫、球麻痹及眼外肌麻痹并不少见,而颅神经麻痹在CMT-I中极为罕见[9]。本研究CMT-I患者均不存在颅神经受累表现,故颅神经受累有助于CIDP及CMT-I的鉴别。足部畸形的形成与足部固有肌萎缩及受力不均衡有关,且病程越长足部畸形的发生率越高[10]。CMT-I较CIDP病程长,因此其足部畸形出现率高。CMT-I少部分患者存在脑脊液蛋白水平增高,具体机制不详,考虑可能与腰骶神经根肥厚有关,这类患者极易误诊为CIDP,需结合其余临床表现及辅助检查进行鉴别。
神经电生理对于CIDP及CMT-I的鉴别诊断意义重大。CIDP与CMT-I均以脱髓鞘病变为主,神经传导检查都主要表现为DML延长,MCV、SCV减慢[11]。但由于CMT-I病程长,脱髓鞘程度更重,故CMT-I以上指标异常较CIDP更为显著。CIDP常存在传导阻滞及波形离散,而CMT-I由于病程长,周围神经各节段病变程度一致,故传导阻滞、波形离散非常少见。CIDP及CMT-I均主要从下肢起病,下肢周围神经病变程度较上肢重,且随着病情进展可出现继发性轴索变性[11]。本研究发现CMT-I下肢周围神经继发性轴索变性的程度较CIDP重,其CMAP、SNAP波幅更低,且CMAP、SNAP消失更为常见;而两组上肢周围神经继发性轴索变性程度均较轻,无显著性差异。因此对于存在严重脱髓鞘病变但不存在传导阻滞或波形离散的患者,或者下肢神经存在明显轴索变性的患者,应警惕CMT-I可能。
CIDP及CMT-I针极肌电图检查均呈神经源性病变特点[6,9,12],但二者仍存在一定差异。静息时两组均可见失神经电位,但CIDP由于反复脱髓鞘并继发性轴索变性,使得失神经电位的出现率较高;而CMT-I由于是单向病程、病程长,出现肌肉的神经再支配,因此失神经电位的出现率低。本研究发现CIDP组有60.5%肌肉出现失神经电位,而CMT-I组仅为14.3%,与之一致。进一步观察MUAP发现,两组均表现为波幅高、时程宽、多相波增多,大力收缩时募集减少,但由于CMT-I病程长,故以上慢性神经再生特点更为显著。因此对于针极肌电图以失神经电位为主的患者倾向于CIDP的诊断;而对于失神经电位不明显,以慢性神经再生为主的患者更倾向于CMT-I的诊断。
本研究对临床症状的严重程度与电生理的严重程度进行了相关性分析,发现CIDP的临床症状严重程度与电生理的严重程度正相关;而CMT-I电生理较重但临床症状相对较轻,出现电生理与临床症状分离现象。考虑与以下因素有关:①由于CMT-I病程较长,出现肌肉的神经再支配及肌力的代偿;②PMP22基因重复突变是CMT-I最常见的基因突变,该型病情往往较轻,大部分患者终身保持行走能力,部分患者仅存在神经电生理的异常[13,14]。
综上,尽管CIDP与CMT-I临床及电生理表现类似,但二者亦存在一定的差异。详细的临床资料,准确、全面的神经电生理检查,临床及神经电生理严重程度的相关性评估有助于CIDP及CMT-I的鉴别诊断。
[1]中华医学会神经病学分会神经肌肉病学组,中华医学会神经病学分会肌电图及临床神经电生理学组,中华医学会神经病学分会神经免疫学组.中国慢性炎性脱髓鞘性多发性神经根神经病诊疗指南[J].中华神经科杂志,2010,43(8):586-588.
[2]陈嵘,梁秀龄.腓骨肌萎缩症的临床表现和分型及遗传学[J].中山医科大学学报,1997,18(3):213-215.
[3]刘银红,崔丽英.传导阻滞[J].国外医学神经病学神经外科学分册,2004,31(5):484-487.
[4]HOYLE JC,ISFORT MC,ROGGENBUCK J,et al.The genetics of Charcot-Marie-Tooth disease:current trends and future implications for diagnosis and management[J].Appl Clin Genet, 2015,10(8):235-243.
[5]TAZIR M,HAMADOUCHE T,NOUIOUA S,et al.Hereditary motor and sensory neuropathies or Charcot-Marie-Tooth diseases:an update[J].Neurol Sci,2014,347(1-2):14-22.
[6]崔芳,黄旭升,陈朝晖,等.慢性吉兰-巴雷综合征32例临床分析[J].第三军医大学学报,2005,27(8):799-801.
[7]SZIGETI K,LUPSKI JR.Charcot-Marie-Tooth disease[J].Eur J Hum Genet,2009,17(6):703-710.
[8]MCCOMBE PA,POLLARD JD,MCLEOD JG.Chronic inflammatorydemyelinatingpolyradiculoneuropathy:aclinicaland electrophysiological study of 92 cases[J].Brain,1987,110(pt6):1617-1630.
[9]梁银杏,葛辉,廖松洁,等.遗传性运动感觉性周围神经病I型的临床及电生理特点[J].中国神经精神疾病杂志,2010,4(36):217-219.
[10]BURNS J,Ryan MM,OUVRIER RA.Evolution of foot and ankle manifestations in children with CMT1A[J].Muscle Nerve,2009,39(2):158-166.
[11]MANGANELLI F,PISCIOTTA C,REILLY MM,et al.Nerve conduction velocity in CMT1A:what else can we tell?[J].Eur J Neurol,2016,7(1):1-6.
[12]黄献,宋治,郑文,等.腓骨肌萎缩症患者的临床与神经电生理特征分析[J].现代电生理学杂志,2010,3(17):139-142.
[13]ZHAN Y,ZI X,HU Z,et al.PMP22-Related neuropathies and other clinical manifestations in Chinese han patients with charcot-marie-tooth disease type 1[J].Muscle Nerve,2015,52(1):69-75.
[14]HATTORI N,YAMAMOTO M,YOSHIHARA T,et al.Demyelinating and anonal features of Charcot-Marie-Tooth disease with mutations of myelinrelated proteins(PMP22,MPZ and Cx32):a clinicopathological study of 205 Japanese patients[J]. Brain,2003,126(pt):134-151.
(责任编辑:李立)
Comparison of clinical manifestations and electrophysiological features in patients with chronic inflammatory demyelinating polyneuropathy and Type-I Charcot Marie Tooth Disease.
LIU Jingjie,HAN Ping,GAO Zhen,GONG Fuhua,MA Xiaolin,XIANG Li.Department of Neurology,the Second Affiliated Hospital,Xi'an Jiaotong University,Xi'an 710004,China.Tel:029-87679000.
Objectives To compare clinical manifestations and electrophysiological features in patients with chronic inflammatory demyelinating polyneuropathy(CIDP)and Type-I Charcot Marie Tooth Disease(CMT-I)for guiding differential diagnosis.Methods Data including clinical manifestations and electrophysiological indexes was collected from thirty-one CIDP cases and 28 CMT-I cases.Correlation analysis was used to assess the association of the severity of electrophysiology with the severity of clinical symptoms.Results There were statistically significant differences in onset site,sensory dysfunction,foot deformity and cerebrospinal fluid protein between these two groups(P<0.05).There were significant differences in indexes of nerve conduction and needle electromyography between these two groups(P<0.05). The severity of clinical symptoms was not related with the severity of electrophysiology in CMT-I group(r=0.27P,>0.05).Conclusions Differential diagnoses of CIDP and CMT-I can be made based on clinical manifestations and electrophysiological features.
Chronic inflammatory demyelinating polyneuropathy Type-I Charcot-Marie-Tooth Disease(CMT-I)Electrophysiology
R744.5
A
10.3969/j.issn.1002-0152.2016.08.010
*西安交通大学第二附属医院神经内科(西安710004)
△核工业部417医院神经内科(西安,710600)
(E-mail:601146083@qq.com)
(2016-02-22)

