3种酶联免疫吸附试验试剂检测丙型肝炎抗体结果研究
殷剑 王晓明 孙慧 钱希铭
3种酶联免疫吸附试验试剂检测丙型肝炎抗体结果研究
殷剑王晓明孙慧钱希铭
目的探讨3种酶联免疫吸附试验试剂检测丙型肝炎抗体结果情况。方法分析2015年1~9月进行检测丙型肝炎筛查的血液标本3 824例,其中丙型肝炎血液标本作为观察对象,依据酶联免疫吸附试验试剂不同进行分组,Ⅰ组采用A试剂,通过间接法进行检测;Ⅱ组采用B试剂,通过间接法进行检测;Ⅲ组采用C试剂,采用夹心法进行检测,通过聚合酶链反应进行确诊。对质控物进行倍比稀释,分别通过三种检测试剂进行平行检测。结果Ⅲ组检测结果阳性30例,阴性3 794例;Ⅲ组阳性检出率高于Ⅰ组(χ2=21.28,P<0.05),Ⅲ组阳性检出率高于Ⅱ组(χ2=20.64,P<0.05);Ⅲ组真阳性标本准确度高于Ⅰ组(χ2=8.49,P<0.05),Ⅲ组真阳性标本准确度高于Ⅱ组(χ2=8.67,P<0.05);Ⅲ组质控血清灵敏度高于Ⅰ组(χ2=16.37,P<0.05),Ⅲ组质控血清灵敏度高于Ⅱ组(χ2=16.58,P<0.05);Ⅲ组检测阳性标本灵敏度高于Ⅰ组(χ2=21.85,P<0.05),Ⅲ组检测阳性标本灵敏度高于Ⅱ组(χ2=21.47,P<0.05)。结论夹心法酶联合免疫吸附试验(ELISA)检测试剂HCV抗体灵敏度、特异性均高于间接法ELISA检测试剂,值得临床推广应用。
酶联免疫吸附试验;试剂;检测;丙型肝炎抗体
丙型肝炎是由丙型肝炎病毒(hepatitis C virus,HCV)形成的一种传染性疾病,HCV是一种单股正链RNA病毒,在黄病毒科之列。目前全世界有1.85亿已知的HCV感染者,每年有300~400万新发病例[1,2]。感染病例可分为急性感染和慢性感染两类,其中急性感染者有近80%发展成为慢性感染,20年后有1/5的患者可能形成肝脏纤维化、终末期肝癌等,对于丙型感染的诊断、治疗显得尤为重要[3,4]。目前关于HCV检测方法主要以酶联免疫吸附试验为主,采用何种酶联免疫吸附试验成为检测丙型感染抗体结果准确性的重要议题。本研究通过对我院丙型肝炎患者临床资料进行分析,探讨不同联免疫吸附试验丙型肝炎抗体结果情况,报告如下。
1 资料与方法
1.1一般资料选取我院2015年1~9月进行检测丙型肝炎筛查的血液标本3 824例,其中丙型肝炎血液标本作为观察对象,依据酶联免疫吸附试验试剂不同进行分组,Ⅰ组采用A试剂,通过间接法进行检测;Ⅱ组采用B试剂通过间接法进行检测;Ⅱ组采用C试剂,采用夹心法进行检测,通过聚合酶链反应进行确诊,免疫印迹法检测通过美国RIBA试剂进行检测。
1.2仪器与方法(1)首先通过试剂A、试剂B进行抗-HCV抗体酶联免疫吸附试验进行检测,按照操作说明书进行操作,灰区设置范围:血液标本OD值的范围在0.7×cut off~1.0×cut off。任何一种试剂检测标本OD值均在灰区的设置范围之内,准备进行复查。检测过程中注意进行双孔复查,如果双试剂四孔OD值小于cut off,可以判定为阴性,双试剂所有孔的OD值≥cut off可以判定为阳性,除此以外的情况判定为弱阳性。通过试剂A、试剂B检测结果判定为弱阳性和阳性标本通过PCR和RIBA检测,从而确定标本中HCV病毒进行确认,采用3种酶联免疫吸附试验试剂结果进行检测和确证。将1 NCU/ml质控血清进行倍比稀释,获得9份自制标本,联合质控血清共计10份,通过试剂A、试剂B、试剂C对标本进行平行检测。(2)将免疫印迹试验结果阳性标本通过A、B、C试剂进行检测,并且对S/CO值进行对比观察。
1.3观察指标(1)观察Ⅰ组、Ⅱ组和Ⅲ组检测结果比较情况。(2)观察间接法抗HCV阳性和弱阳性标本通过不同组别的检测结果情况。(3)观察Ⅰ组、Ⅱ组和Ⅲ组检测阳性标本准确度情况。(4)观察Ⅰ组、Ⅱ组和Ⅲ组质控血清检测灵敏度情况。(5)观察Ⅰ组、Ⅱ组和Ⅲ组检测阳性标本灵敏度情况。
1.4统计学分析应用SPSS 19.0统计软件,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1Ⅰ组、Ⅱ组和Ⅲ组检测结果比较Ⅲ组检测结果阳性30例,阴性3 794例。见表1。
2.2160份间接法抗HCV阳性和弱阳性标本通过不同组的检测结果Ⅲ组阳性检出率高于Ⅰ组(χ2=21.28,P<0.05),Ⅲ组阳性检出率高于Ⅱ组(χ2=20.64,P<0.05)。见表2。
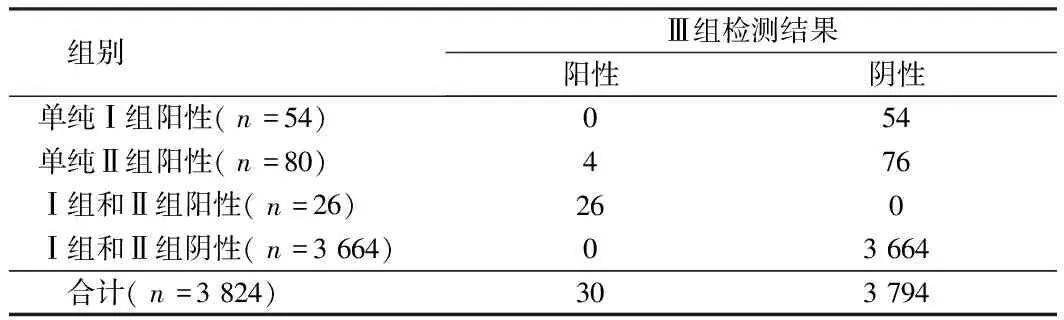
表1 Ⅰ组、Ⅱ组和Ⅲ组检测结果比较 例

表2 160份间接法抗HCV阳性和弱阳性标本通过不同组别检测结果 例(%)
注:与Ⅲ组比较,*P<0.05
2.3Ⅰ组、Ⅱ组和Ⅲ组检测阳性标本准确度情况Ⅲ组真阳性标本准确度高于Ⅰ组,差异有统计学意义(χ2=8.49,P<0.05);Ⅲ组真阳性标本准确度高于Ⅱ组,差异有统计学意义(χ2=8.67,P<0.05)。见表3。

表3 Ⅰ组、Ⅱ组和Ⅲ组检测阳性标本准确度情况
注:与Ⅲ组比较,*P<0.05
2.4Ⅰ组、Ⅱ组和Ⅲ组质控血清检测灵敏度情况Ⅲ组质控血清灵敏度高于Ⅰ组(χ2=16.37,P<0.05),Ⅲ组质控血清灵敏度高于Ⅱ组(χ2=16.58,P<0.05)。见表4。

表4 Ⅰ组、Ⅱ组和Ⅲ组质控血清检测灵敏度情况 %
注:与Ⅲ组比较,*P<0.05
2.5Ⅰ组、Ⅱ组和Ⅲ组检测阳性标本灵敏度情况Ⅲ组检测阳性标本灵敏度高于Ⅰ组(χ2=21.85,P<0.05),Ⅲ组检测阳性标本灵敏度高于Ⅱ组(χ2=21.47,P<0.05)。见表5。
3 讨论
目前国内HCV抗体感染率3%左右,其中大约4 000万例HCV感染患者,已经成为全世界的重大公共卫生问题[5,6]。HCV传播途径主要是通过输血或者血液制品进行传播。本研究通过分析2015年1~9月进行检测丙型肝炎筛查的血液标本3 824例,其中丙型肝炎血液标本为观察对象,依据酶联免疫吸附试验试剂不同进行分组,Ⅰ组采用A试剂,通过间接法进行检测,Ⅱ组采用B试剂,通过间接法进行检测,Ⅲ组采用C试剂,采用夹心法进行检测,通过聚合酶链反应进行确诊。对质控物进行倍比稀释,分别通过三种检测试剂进行平行检测。
试剂C是夹心法检测HCV抗体的ELISA试剂,笔者通过多种不同的方法,对HCV抗体进行平行性检测,通过和间接法ELISA试剂进行比较观察,对夹心法试剂C进行准确的评价[7,8]。有资料显示,通过间接法ELISA检测过程中,采用酶标记抗人IgG作为第二抗体对血清中HCVIgG抗体,但是HCVIgG抗体出现时间比HCVIgM抗体晚,在感染早期其采集血液很容易发生漏检[9,10]。同时为了减少因血清中其他非特异性抗体和类风湿因子形成干扰,试验第一步需要降低检测样本量和稀释样本congress降低反应的板底值,同时也可能降低试剂检测灵敏度[11,12]。另外通过间接法ELISA检测,很容易受到非特异性IgG抗体、类风湿因子等非特异性抗体的影响,从而出现假阳性反应。目前关于HCV抗体诊断试剂逐步从间接法向夹心法逐步过渡。其原因主要是丙肝重组抗原活性和其空间构象有密切关系,抗原结构稳定性和酶标记过程中对于空间构象的影响,为夹心法试剂研究重点和难点问题[13,14]。目前对于HCV抗体检测影响因素主要是包被丙型肝炎病毒抗原。目前国内常用的两种间接法ELISA试剂对HCV抗体进行筛查,为的是降低由于不同厂家包被抗原片段形成的漏检[15,16]。有资料显示,间接法ELISA检测试剂可以增加NS5区作为包被抗原,提高了检测的灵敏度,但本研究结果显示,试剂A和试剂B的间接法ELISA检测假阳性率比较高,可能增加了检查HCV抗体成本和负担[17]。有资料显示,目前HCV感染标志物检测方法主要有两种方式,其中一种通过间接法ELISA试剂检测HCV抗体,另外一种是通过夹心法ELISA试剂对HCV抗体检测,采用某种试剂对HCV核酸进行检测[18]。本结果表明,Ⅲ组检测结果阳性30例,阴性3 794例,Ⅲ组阳性检出率高于Ⅰ组,Ⅲ组阳性检出率高于Ⅱ组,Ⅲ组真阳性标本准确度高于Ⅰ组,Ⅲ组真阳性标本准确度高于Ⅱ组,Ⅲ组质控血清灵敏度高于Ⅰ组,Ⅲ组质控血清灵敏度高于Ⅱ组,Ⅲ组检测阳性标本灵敏度高于Ⅰ组,Ⅲ组检测阳性标本灵敏度高于Ⅱ组,提示通过夹心法和间接法ELISA试剂、HCV核酸试剂进行合理配伍,可以提高丙肝感染标志物阳性筛查准确率,降低假阳性,提高血液准确率,尽可能提高血液检查效率。

表5 Ⅰ组、Ⅱ组和Ⅲ组检测阳性标本灵敏度情况 %
注:与Ⅲ组比较,*P<0.05
综上所述,夹心法ELISA检测试剂HCV抗体灵敏度、特异性均高于间接法ELISA检测试剂,值得临床推广应用。
1武丽娟.3种酶联免疫吸附试验试剂检测丙型肝炎抗体结果分析.国际检验医学杂志,2014,35:3246-3248.
2赵龙友,纪勇平,王德镔,等.两种酶联免疫法检测丙型肝炎病毒抗体结果分析.中华实验和临床病毒学杂志,2013,8:304-306.
3Ghany MG,Strader DB,Thomas DL,et al.Diagnosis, management,and treatment of hepatitis C: an update.Hepatology,2009,49:1335-1374.
4曾艳华,卢香云,张丽,等.酶联免疫吸附试验检测丙型肝炎抗体的可比性研究.中华临床实验室管理电子杂志,2015,3:42-46.
5Thomas DL.Global control of hepatitis C:where challenge meets opportunity.Nat Med,2013,19: 850-858.
6Acar A,Kemahli S,Ntunay H,et al.The significance of repeat testing in Turkish blood donors screened with HBV,HCV and HIV immunoassays and the importance of S/CO ratios in the interpretation of HCV/HIV screening test result and as a determinant for further confirmatory testing.Transfus Med,2010,20:152-159.
7张雪梅,付涌水,黄珂, 等.广州献血人群抗-HCV ELISA检测S/CO值与确证试验结果的相关性.中国输血杂志,2013,26:29-33.
8Stefania C,Martin L.Indeterminate third-generation hepatitis C recombinant immunoblot assay and HCV RNA analysis:isolated reactivity against NS5 associated with HCV viraemia in clinical patients but not bloods.Scand J Infect Dis,2005,37:488-492.
9王红.酶联免疫吸附试验检测丙型肝炎病毒抗体在酶标仪应用中的探讨.检验医学与临床,2012,9:1234-1235.
10Alter MJ,Kuhnert WL,Finelli L,et al.Guidelines for laboratory testing and result reporting of antibody to hepatitis C virus.Centers for Disease Control and Prevention.MMWR Recomm Rep,2003,52:1-13,15.
11汤巧,吴文静,夏永祥.化学发光法和酶联免疫吸附法检测丙型肝炎病毒缸体的比较分析.国际检验医学杂志,2011,32:834-835.
12Ren FR,Lv QS,Zhuang H,et al.Signi cance of the signal-to-cutoff ratios of anti-hepatitis C virus enzyme immunoassays in screening of Chinese blood donors.Transfusion,2005,45:1816-1822.
13薛芳,吴刚.丙型肝炎病毒抗体酶联免疫吸附试剂检测结果可信度的分析.中国国境卫生检疫杂志,2009,32:1-3.
14梁华钦,王敏,黎世杰,等.广州市无偿献血者中抗-HCV阳性人群的比较分析.中国输血杂志,2012,25:449-451.
15赵金仙,李顺祥,蔡英,等.艾滋病病毒感染对酶联免疫吸附试验试剂检测静脉吸毒人员丙型肝炎病毒抗体反应强度影响的探讨.疾病监测,2010,25:49-51.
16Sabin CA,Emery V,Devereux HL,et al.Long-term patterns of hepatitis C virus RNA concentrations in a cohort of HIV seronegative men with bleeding disorders.J Med Virol,2002,68:68-75.
17朱忠政,丛文铭.乙型肝炎病毒和丙型肝炎病毒在肝癌发生中的应用研究进展.中华肝脏病杂志,2011,11:574.
18Islam S,Antonsson L,Westin J,et al.Cirrhosis in hepatitis C virus-infected patients can be excluded using and index of standard biochemical serum markers.Scand J Gastroenterol,2005,40:867-872.
10.3969/j.issn.1002-7386.2016.21.034
214000江苏省无锡市第九人民医院检验科
R 446.11
A
1002-7386(2016)21-3312-03
2016-03-20)

