用印刷电路板蚀刻废液制备氯化亚铜
毛谙章,张银亮,刘小文,周兆安,彭 娟
(深圳市危险废物处理站有限公司,广东 深圳 518049)
用印刷电路板蚀刻废液制备氯化亚铜
毛谙章,张银亮,刘小文,周兆安,彭娟
(深圳市危险废物处理站有限公司,广东 深圳 518049)
以含铜酸性蚀刻废液、碱式氯化铜、亚硫酸钠和氢氧化钠为原料制备氯化亚铜。考察了体系总氯与总铜物质的量比、还原剂亚硫酸钠与总铜物质的量比、pH值、反应时间、反应温度等对氯化亚铜收率的影响,并对氯化亚铜产品质量进行了分析。结果表明,在体系总氯与总铜物质的量比为1.4∶1、还原剂亚硫酸钠与总铜物质的量比为1.4∶1、pH值为3.4、反应时间为1 h、反应温度为30 ℃的最佳条件下,氯化亚铜收率可达94%。制备的氯化亚铜按液固比3∶1(mL∶g)的比例用1%的稀盐酸洗涤2次,再用无水乙醇进行防氧化处理,真空干燥后得到纯度高、晶型完整的氯化亚铜产品,其质量达到精制级氯化亚铜的国家化工行业标准(HG/T 2960-2010)。
氯化亚铜;印刷电路板;蚀刻废液;碱式氯化铜;亚硫酸钠
氯化亚铜是一种重要的化工原料,被广泛应用于有机合成、石油化工、油脂化工、冶金、电镀等领域[1-2]。如,在有机合成中,是应用较广的催化剂,能生产多种有机化工产品,如乙烯基乙炔、一氯丁二烯、丙烯腈等;在石油化工中,用作脱离剂、脱硫剂及脱色剂;在油脂化工中,用作催化剂和还原剂,尤以前者著称;在有机硅工业中,作为合成甲基氯硅烷混合单体(以二甲基二氯硅烷为主导)的催化剂。氯化亚铜催化剂市场需求量大且呈逐年上升趋势[3-4]。
目前生产氯化亚铜的主要方法有废铜盐酸法[5-7]、废铜氯气直接氧化法[8]、铜丝空气氧化法[9-10]、硝酸催化氧化法[9,11-13]、硫酸铜还原法[14],普遍存在产品纯度较低、生产成本较高、操作环境恶劣、废水量大等不足[8,15],制约了其在生产中的推广。
作者以印刷电路板蚀刻废液为原料,通过非水解法制备氯化亚铜,优化制备条件,并对产品进行了质量分析。
1 实验
1.1材料与试剂
某线路板企业的含铜碱性蚀刻废液和含铜酸性蚀刻废液(总Cu 130 g·L-1,总Cl-247.4 g·L-1,H+2.79 g·L-1,Na+40.1 g·L-1)。其中含铜酸性蚀刻废液的主要杂质含量(×10-6)为:As 5.8,Cr 2.4,Fe 4.7,Ni 6.4,Sn 1.1,Zn 43.5,Cd未检出,Pb未检出。
亚硫酸钠(AR)、1%稀盐酸、氢氧化钠(AR)、工业级无水乙醇。
1.2实验原理
用含铜酸性蚀刻废液(含有Cu+和Cu2+)、碱式氯化铜、亚硫酸钠和氢氧化钠为原料制备氯化亚铜的原理如下:
Cu2(OH)3Cl+3H+=2Cu2++3H2O+Cl-
1.3方法
以含铜酸性蚀刻废液为底液,控制反应条件,向反应液中加入碱式氯化铜和亚硫酸钠,用氢氧化钠调节并控制反应pH值,生成的氯化亚铜沉淀先陈化一定时间再过滤、洗涤、防氧化处理,最后真空干燥得到氯化亚铜产品。
按照国家化工行业标准(HG/T 2960-2010)对制备的氯化亚铜及除杂处理后的氯化亚铜产品进行质量分析,采用ICP-AES测定铜含量。
2 结果与讨论
2.1合成条件优化
2.1.1体系总氯与总铜物质的量比对氯化亚铜收率的影响
在还原剂亚硫酸钠与总铜物质的量比为1.4∶1、反应温度为30 ℃、pH值为3.4、反应时间为1 h的条件下,考察体系总氯与总铜物质的量比(简称氯铜物质的量比)对氯化亚铜收率的影响,结果见图1。
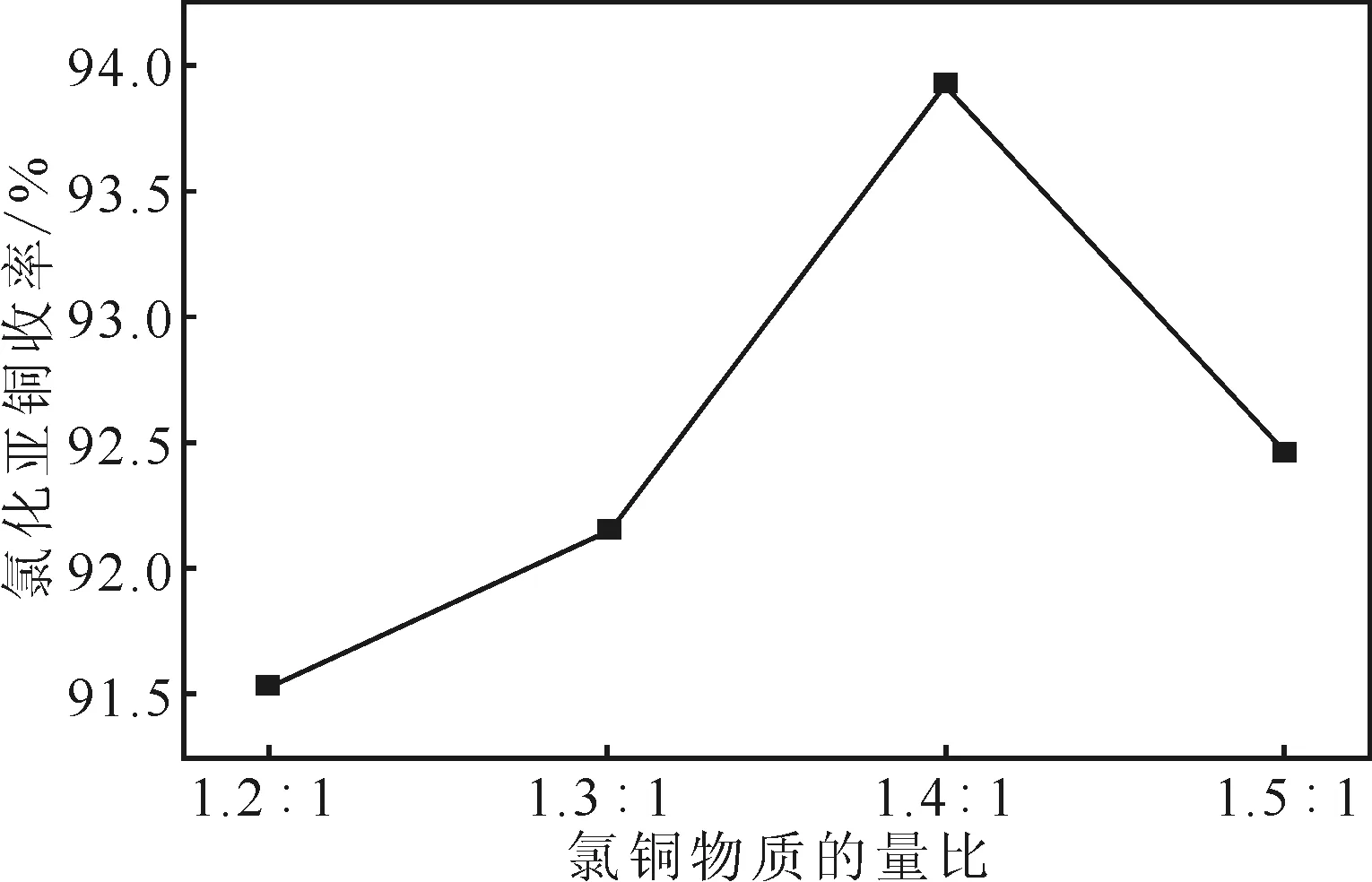
图1 氯铜物质的量比对氯化亚铜收率的影响Fig.1 Effect of molar ratio of total chloride and total copper on yield of cuprous chloride
由图1可知,随着体系中氯铜物质的量比的增大,氯化亚铜收率逐渐升高,在氯铜物质的量比为1.4∶1时收率达到最高,随后氯化亚铜收率开始下降。主要是因为,继续增加氯用量,会使氯化亚铜转化为可溶解的Na(CuCl2),降低氯化亚铜收率。因此,选择氯铜物质的量比为1.4∶1。
2.1.2还原剂亚硫酸钠与总铜物质的量比对氯化亚铜收率的影响
在体系氯铜物质的量比为1.4∶1、反应温度为30 ℃、pH值为3.4、反应时间为1 h的条件下,考察还原剂亚硫酸钠与总铜物质的量比对氯化亚铜收率的影响,结果见图2。
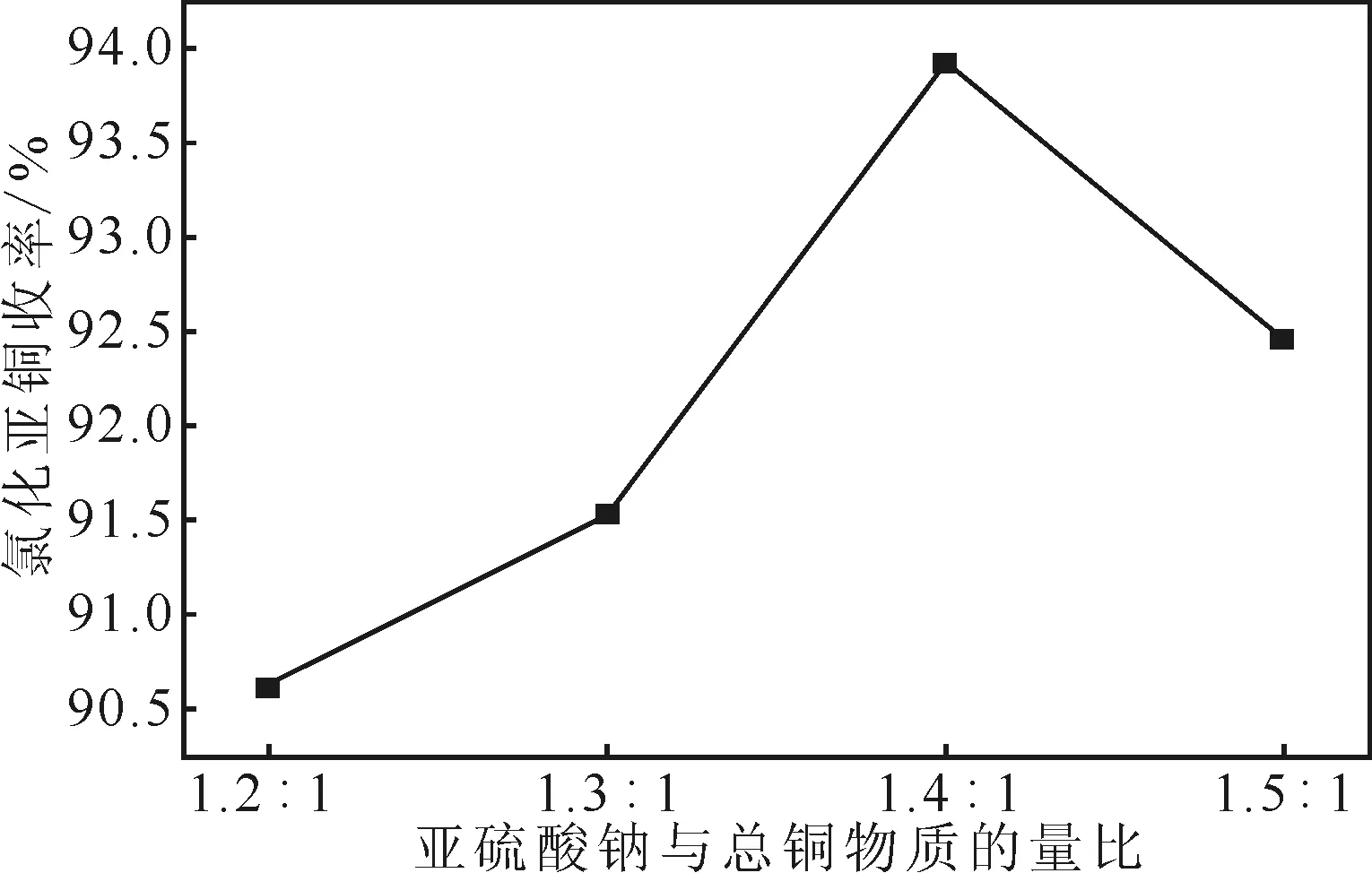
图2 亚硫酸钠与总铜物质的量比对氯化亚铜收率的影响Fig.2 Effect of molar ratio of sodium sulfite and total copper on yield of cuprous chloride
由图2可知,随着体系中还原剂亚硫酸钠与总铜物质的量比的增大,氯化亚铜收率逐渐升高,在还原剂亚硫酸钠与总铜物质的量比为1.4∶1时,收率达到最高,随后开始下降。主要是因为,当还原剂亚硫酸钠与总铜物质的量比大于1.4∶1时,由于体系中亚硫酸根浓度较高,能与亚铜离子络合生成稳定的化合物,从而降低了氯化亚铜收率。因此,选择还原剂亚硫酸钠与总铜物质的量比为1.4∶1。
2.1.3pH值对氯化亚铜收率的影响
在体系氯铜物质的量比为1.4∶1、还原剂亚硫酸钠与总铜物质的量比为1.4∶1、反应温度为30 ℃、反应时间为1 h的条件下,考察pH值对氯化亚铜收率的影响,结果见图3。

图3 pH值对氯化亚铜收率的影响Fig.3 Effect of pH value on yield of cuprous chloride
由图3可知,随着pH值的增大,氯化亚铜收率逐渐升高,在pH值为3.4时收率达到最高93.92%,随后逐渐下降。这是由于,在pH值小于3.4时,随着pH值的增大,H+减少,有利于氯化亚铜的生成;当pH值大于3.4时,氯化亚铜开始水解,生成氢氧化亚铜中间体;当pH值大于4.0后,大部分氯化亚铜转化为氧化亚铜和碱式氯化铜,氯化亚铜收率大幅降低。因此,选择pH值为3.4。
2.1.4反应时间对氯化亚铜收率的影响
在体系氯铜物质的量比为1.4∶1、还原剂亚硫酸钠与总铜物质的量比为1.4∶1、反应温度为30 ℃、pH值为3.4的条件下,考察反应时间对氯化亚铜收率的影响,结果见图4。

图4 反应时间对氯化亚铜收率的影响Fig.4 Effect of reaction time on yield of cuprous chloride
由图4可知,反应时间对氯化亚铜收率的影响不大。反应时间为0.5 h时,氯化亚铜收率即达到93.41%;随着反应时间的延长,氯化亚铜收率升幅不明显。因此,选择反应时间为1 h。
2.1.5反应温度对氯化亚铜收率的影响
在体系氯铜物质的量比为1.4∶1、还原剂亚硫酸钠与总铜物质的量比为1.4∶1、pH值为3.4、反应时间为1 h的条件下,考察反应温度对氯化亚铜收率的影响,结果见图5。
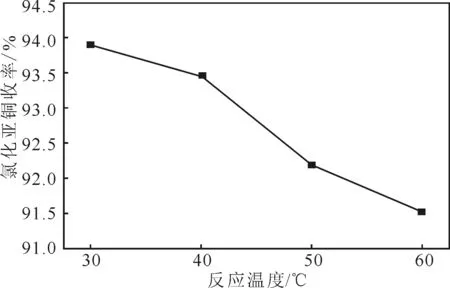
图5 反应温度对氯化亚铜收率的影响Fig.5 Effect of reaction temperature on yield of cuprous chloride
由图5可知,反应温度对氯化亚铜收率的影响较大。随着反应温度的升高,氯化亚铜收率逐渐下降。主要是因为,温度越高,亚硫酸钠分解速度越快,从体系溢出的二氧化硫越多,从而影响铜的还原,导致氯化亚铜收率降低。因此,选择反应温度为30 ℃。
综上可知,制备氯化亚铜的最佳条件为:体系氯铜物质的量比1.4∶1、还原剂亚硫酸钠与总铜物质的量比1.4∶1、pH值3.4、反应时间1 h、反应温度30 ℃,在该条件下,氯化亚铜收率可达94%。
2.2产品质量控制与分析
在最佳条件下制备得到的氯化亚铜含有硫酸钠、氯化铜等杂质,其质量不能达到精制级氯化亚铜的标准,需进行除杂处理。按液固比3∶1(mL∶g)的比例用1%的稀盐酸对制备的氯化亚铜洗涤2次,再用无水乙醇进行防氧化处理,最后真空干燥得到氯化亚铜产品,其质量指标如表1所示,其XRD图谱如图6所示。
由表1可知,经稀盐酸洗涤、无水乙醇防氧化处理、真空干燥后所得氯化亚铜产品符合精制级氯化亚铜国家化工行业标准(HG/T 2960-2010)要求。
由图6可以看出,除杂处理所得氯化亚铜产品的XRD图谱基本不含其它杂质衍射峰,且CuCl特征峰显著。表明,氯化亚铜产品纯度较高、晶型完整。
3 结论
采用含铜酸性蚀刻废液、碱式氯化铜、亚硫酸钠和氢氧化钠为原料制备氯化亚铜。最佳制备条件为:体系总氯与总铜物质的量比1.4∶1、还原剂亚硫酸钠与总铜物质的量比1.4∶1、pH值3.4、反应时间1 h、反应温度30 ℃,在此条件下,氯化亚铜收率可达94%。制备的氯化亚铜按液固比3∶1(mL∶g)的比例用1%的稀盐酸洗涤2次,再用无水乙醇进行防氧化处理,真空干燥后得到纯度高、晶型完整的氯化亚铜产品,其质量符合精制级氯化亚铜的国家化工行业标准(HG/T 2960-2010)要求。
表1 氯化亚铜产品的质量指标

Tab.1 Quality index of cuprous chloride product
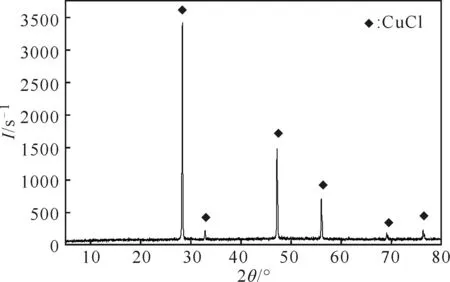
图6 除杂处理所得氯化亚铜产品的XRD图谱Fig.6 XRD pattern of purified cuprous chloride product
[1]胥建芳.氯化亚铜生产工艺及设备研究[J].云南冶金,2001,30(4):26-27.
[2]梁礼渭,曾清全,熊卫江,等.氯化亚铜的制备工艺[J].材料研究与应用,2011,5(4):296-299.
[3]赵伟.氯化亚铜合成及精制[J].氯碱工业,1999(4):32-34.
[4]陈庆根,曾青云.氯化亚铜抗氧化研究[J].江西有色金属,2005,19(2):32-34.
[5]董才华.利用废酸废铜料生产氯化亚铜快速方法[J].矿业快报,2000(4):19.
[6]夏士朋,杨勇.废铜制取氯化铜的新工艺[J].四川化工,1997(4):18-19.
[7]马普利,张析.以铜灰为原料直接生产氯化亚铜工艺研究[J].湿法冶金,2000,19(3):59-62.
[8]王沛喜,刘积灵,张玉坤.氯化亚铜制备技术进展和用途[J].中国氯碱,2002(11):17-19.
[9]李国庭,杨久义,胡庆福,等.催化法制氯化亚铜新工艺[J].河北轻化工学院学报,1993,14(1):69-74.
[10]戴江洪.氯化亚铜微晶的制备及其表征[D].赣州:江西理工大学,2007.
[11]李国庭,卢国军.废紫铜催化制备氯化亚铜新工艺[J].无机盐工业,2002,34(2):40-41,43.
[12]徐旺生,宣爱国.催化转化法由低品位铜矿制备活性氯化亚铜[J].无机盐工业,2000,32(5):34-36.
[13]黄宗明.硝酸催化氧化法制备氯化亚铜的研究[J].化学世界,2002,43(8):404-405.
[14]黄凌涛.从含铜电镀废水制备氯化亚铜及提高其抗氧化性的研究[D].贵阳:贵州大学,2008.
[15]林丞.氯化亚铜的表面修饰及对其磁学特性的影响[D].福州:福建师范大学,2006.
Preparation of Cuprous Chloride with Waste Etching Solution from Printed Circuit Boards
MAO An-zhang,ZHANG Yin-liang,LIU Xiao-wen,ZHOU Zhao-an,PENG Juan
(ShenzhenHazardousWasteTreatmentStationCo.,Ltd.,Shenzhen518049,China)
Cuprouschloridewaspreparedusingacidicwasteetchingsolutioncontainingcopper,tribasiccopperchloride,sodiumsulfiteandsodiumhydroxideasrawmaterials.Effectsofmolarratiooftotalchlorideandtotalcopper,molarratioofreducingagentsodiumsulfiteandtotalcopper,pHvalue,reactiontime,andreactiontemperatureonyieldofcuprouschloridewereinvestigated,whilsttheproductqualitywasalsodetermined.Theyieldofcuprouschloridereached94%attheoptimalconditionsasfollows:molarratiooftotalchlorideandtotalcopperwas1.4∶1,molarratioofreducingagentsodiumsulfiteandtotalcopperwas1.4∶1,pHvaluewas3.4,reactiontimewas1h,andreactiontemperaturewas30 ℃.Preparedcuprouschloridewaswashedtwiceby1%dilutedhydrochloricacidwithliquid-solidratioof3∶1(mL∶g),andthenantioxidedbyanhydrousethanol.Finally,cuprouschloridewithhighpurityandcrystalintegritywasobtainedbyvacuumdrying,anditsqualitymetthenationalchemicalindustrystandardoftherefinedlevelofcuprouschloride(HG/T2960-2010).
cuprouschloride;printedcircuitboards;wasteetchingsolution;tribasiccopperchloride;sodiumsulfite
2016-05-23
10.3969/j.issn.1672-5425.2016.10.010
TQ 131.21
A
1672-5425(2016)10-0045-04
毛谙章,张银亮,刘小文,等.用印刷电路板蚀刻废液制备氯化亚铜[J].化学与生物工程,2016,33(10):45-48.

