贝伐单抗联合肝动脉化疗栓塞术对36例晚期原发性肝癌生存预后的影响分析
曾筱怡+邱金宝+陈林


摘 要 目的:探讨贝伐单抗联合肝动脉化疗栓塞术(TACE)治疗晚期原发性肝癌的临床疗效及对生存预后的影响。方法:72例晚期原发性肝癌患者随机分为对照组和观察组各36例。对照组给予TACE治疗,观察组则给予动脉灌注贝伐单抗联合TACE治疗。比较两组患者的临床疗效、不良反应、卡氏生存质量评分以及6、12个月生存率及治疗前后血清甲胎蛋白(AFP)和癌胚抗原(CEA)的水平。结果:观察组治疗后的总有效率(16.67%)和临床获益率(77.78%)显著高于对照组的5.56%和55.56%(P<0.05);观察组患者治疗后血清AFP (416.52±10.89) mg/L和CEA (254.57±50.72)mg/L水平显著低于对照组的(468.34±11.89) mg/L和(314.56±69.84) mg/L (P<0.05)。观察组治疗后的KPS评分(76.86±6.75)分,显著高于对照组的(72.79±5.83)分(P<0.05);观察组治疗后6个月的生存率为91.67%,高于对照组的86.11% (P>0.05)。 观察组治疗后12个月的生存率为83.33%,显著高于对照组的61.11% (P<0.05);两组患者发热、腹痛、黑便、过敏反应和转氨酶升高等不良反应的发生率均无统计学意义。结论:贝伐单抗联合TACE治疗晚期原发性肝癌可提高患者的生存质量,延长患者的生存时间,降低患者血清AFP和CEA的水平,疗效确切,值得应用于临床。
关键词 贝伐单抗 肝动脉化疗栓塞术 原发性肝癌 生存预后
中图分类号:R979.19; R735.7 文献标识码:B 文章编号:1006-1533(2016)19-0020-04
clinical curative effect and survival prognosis of bevacizumab combined with transcatheter arterial chemoembolization in the treatment of 36 cases of advanced primary liver cancer*
CENG Xiaoyi**, QIU Jinbao, CHEN Li(Department of Oncology, The Second Hospital of Pingxiang City, Pingxiang 337000, China)
ABSTRACT Objective: To discuss the clinical curative effect and survival prognosis of bevacizumab combined with transcatheter arterial chemoembolization (TACE) in the treatment of advanced primary liver cancer. Methods: Seventy-two patients with advanced primary liver cancer were randomly divided into an observation group and a control group with 36 cases each. The control group was given TACE conventional treatment while the observation group was given arterial perfusion of bevacizumab besides TACE. The clinical efficacy, adverse reactions, Karnofsky score of quality of life (KPS), 6 and 12 months survival rate, serum AFP (AFP) and carcinoembryonic antigen (CEA) levels before and after treatment were compared between two groups. Results: The total effective rate and clinical benefit rate were significantly higher in the observation group(16.67% and 16.67%) than in the control group (5.56% and 55.56%) after treatment (P<0.05). The serum AFP and CEA levels were significantly lower in the observation group [(416.52±10.89) mg/L and (254.57±50.72) mg/L] than in the control group[(468.34±11.89) mg/L and (314.56±69.84) mg/L] after treatment (P<0.05). The KPS scores were significantly higher in the observation group than in the control group (76.86±6.75 vs 72.79±5.83) (P<0.05). The survival rates were 91.67% in the observation group and 86.11% in the control group 6 months after treatment, which was higher in the observation but without any statistical significance (P>0.05), however, those were significantly higher in the observation group than in the control group(83.33% vs 61.11%) 12 months after treatment (P<0.05). There was no statistical significance in the incidence of adverse reactions such as fever, abdominal pain, black stool, allergic reactions and the elevated transaminase between two groups. Conclusion: Bevacizumab combined with TACE for the treatment of patients with advanced primary liver cancer can improve the quality of survival, extend the survival time of patients, reduce the serum AFP and CEA levels with definite curative effect and worthy of further clinical promotion.
KEY WORDS bevacizumab; transcatheter arterial chemoembolization; primary liver cancer; survival prognosis
原发性肝癌是临床常见的恶性肿瘤之一,具有恶性程度高、预后差、生存率低等特点[1]。原发性肝癌发病隐匿,早期诊断不易发现,绝大多数患者确诊时已到了中晚期。目前,肝动脉化疗栓塞(TACE)是临床用于治疗不能手术切除原发性肝癌患者的首选方式,亦是治疗晚期原发性肝癌患者的标准手段[2]。贝伐单抗是重组的人源化单克隆抗体,能与血管内皮生长因子(VEGF)特异性结合,从而起到抑制肿瘤血管生成的作用[3]。本研究通过贝伐单抗和TACE的联合应用,旨在探讨其治疗晚期原发性肝癌的临床疗效及对患者生存预后的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2013年1月—2015年1月我院收治的晚期原发性肝癌患者72例,根据随机分组的方法分为对照组和观察组各36例。对照组男24例, 女12例,年龄50~76岁,平均(62.81±3.21)岁,根据国际抗癌联盟(UICC)的肿瘤分期(TNM)标准,Ⅲ期26例,Ⅳ期10例。观察组男21例,女15例,年龄48~74岁,平均(63.08±3.06)岁,Ⅲ期28例,Ⅳ期8例。纳入标准符合《原发性肝癌诊疗规范》的诊断标准[4] :①病理学诊断明确,经细胞学或组织学证实是晚期原发性肝癌,且不能接受外科手术切除的患者;②TNM≥Ⅲ期的患者;③肝功能分级(Child-Pugh分级)为A级或B级,且体力状况ECOG评分≤2分;④白细胞计数>4.0×109/L,血小板计数>100.0×109/L的患者;⑤卡氏(KPS)评分>50分的患者;⑥预计生存时间>3个月的患者。排除标准:①不符合TACE适应证的患者;②排除肝癌脑转移或有严重脑疾病的患者;③排除精神异常或依从性差的患者;④排除合并其他恶性肿瘤的患者;⑤排除哺乳期或妊娠期的患者。两组患者的性别、年龄、病程长短等一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
对照组给予TACE治疗,即采用Seldinger穿刺法,在CT或X线的引导下进行股动脉穿刺,将导管穿刺至靶血管一级分支(肝总动脉、肠系膜上动脉),以明确肿瘤供血动脉和肿瘤病灶的性质、数目、大小等情况。经导管向肿瘤供血动脉注入100~120 mg奥沙利铂(国药准字H20123344,由山东罗欣药业股份有限公司生产)、1.0 g 5-氟尿嘧啶(国药准字H31020593,由上海旭东海普药业有限公司生产)和适量的超液化碘油(由法国加柏公司生产)的混悬液。观察组则在TACE治疗前,经导管动脉灌注贝伐单抗(国药准字B3002B028,由罗氏公司生产)5 mg/kg,疗程为6周。
1.3 统计指标
①统计两组患者的临床疗效和不良反应,并进行生存质量评分;②所有患者治疗前后分别采取清晨静脉血5 ml,不加抗凝剂,室温放置1 h,离心10 min并取上清液。采用ELISA(ELISA试剂盒由武汉博士德生物工程有限公司提供)法测定患者血清中AFP和CEA的水平;③治疗 3、6个月后,对患者进行随访,并计算患者6、12个月生存率。
1.4 疗效评定标准[5]
①完全缓解(CR):肿瘤完全消失;②部分缓解(PR):肿瘤体积缩小50%以上;③病情稳定(SD):肿瘤体积缩小50%以下;④病情进展(PD):肿瘤体积无变化或出现新病灶。总有效率(RR)=(CR+PR)/病例总数×100%;临床获益率(CBR)=(CR+PR+SD)/病例总数×100%。
生存质量评分:治疗后,根据KPS评分标准对两组患者进行评分[6],KPS评分越高,患者的生存质量越高。
1.5 统计学方法
采用SPSS 16.0统计学软件分析数据,两组间定量资料的比较采用t检验,计数资料的比较采用卡方检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的临床疗效比较
观察组治疗后的总有效率和临床获益率分别为16.67%和77.78%,显著高于对照组的5.56%和55.56%,两组间差异有统计学意义(P<0.05,表1)。
2.2 两组患者治疗前后血清AFP和CEA水平的变化及生存质量评分
观察组患者治疗后血清AFP和CEA水平分别为(416.52±10.89) mg/L和(254.57±50.72)mg/L,显著低于对照组的(468.34±11.89)mg/L和(314.56±69.84) mg/L,两组间差异有统计学意义(P<0.05)。观察组治疗后的KPS评分为(76.86±6.75)分,显著高于对照组的(72.79±5.83)分,两组间差异有统计学意义(P<0.05,表2)。
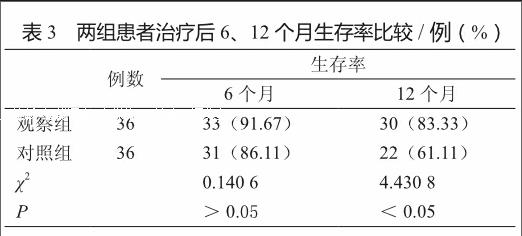
2.3 两组患者治疗6、12个月后生存率比较
观察组治疗后6个月的生存率为91.67%,高于对照组的86.11%,但差异无统计学意义(P>0.05)。观察组治疗后12个月的生存率为83.33%,显著高于对照组的61.11%,两组间差异有统计学意义(P<0.05,表3)。
2.4 两组患者不良反应发生情况的比较
两组患者均未出现严重的不良反应,经对症治疗后,患者均得以痊愈,无病例退出。两组患者发热、腹痛、黑便、过敏反应和转氨酶升高等不良反应的发生率均无统计学意义(P>0.05,表4)。
3 讨论
TACE可明显改善中晚期原发性肝癌患者的生存预后,已广泛应用于临床。研究显示[7],TACE可通过阻断肿瘤供血动脉,减少肿瘤供血,从而抑制肿瘤细胞的生长增值,或是向血管内注射化疗药物,发挥直接杀死肿瘤细胞的作用。有研究亦显示[8-9],TACE可有效抑制肿瘤细胞的生长,明显改善患者的生存预后,使晚期肝癌患者获益。随着TACE的应用,其不足之处也逐渐显露,研究显示[10],TACE的疗效不佳,反复多重治疗后易导致肿瘤复发或转移的情况。近年来研究表明[11-12],贝伐单抗可联合TACE用于中晚期原发性肝癌患者的治疗,且效果确切。贝伐单抗是抑制肿瘤血管生成的药物,可通过与VEGF特异性结合,从而抑制肿瘤内新生血管的形成和使异常血管正常化。研究亦显示[13],贝伐单抗可阻断VEGF对血管内皮细胞的作用,被动截除未成熟或渗漏的脉管,并主动地重塑剩余脉管,从而使异常血管趋于正常,而正常的血管可增加肿瘤化疗药物的敏感性。另外,贝伐单抗还可降低血管的通透性。
本研究结果显示,贝伐单抗联合TACE治疗中晚期原发性肝癌患者的总有效率和临床获益率分别为16.67%和77.78%,均显著高于仅进行TACE治疗者,差异有统计学意义。其中的原因可能是,贝伐单抗的联用可抑制肿瘤供血动脉栓塞后高表达状态的VEGF,抑制肿瘤内新生血管的形成和使异常血管正常化。而正常化的血管可增加肿瘤化疗和放疗的敏感性,从而增强了对肿瘤细胞的杀伤作用[17]。AFP是肝癌特异性肿瘤标志物,80%的肝癌患者血清AFP均具有不同程度的升高[18]。CEA是广谱的肿瘤标志物,研究显示[14],CEA可作为评判肿瘤患者临床疗效和生存预后的一个重要指标。而本研究中观察组患者治疗后血清AFP和CEA的水平显著降低,与对照组比较,差异有统计学意义。结果表明,贝伐单抗联合TACE可通过抑制和杀死肿瘤细胞,从而减少AFP和CEA的表达。同时,结果也间接反映了贝伐单抗联合TACE的临床疗效优于仅进行TACE治疗者。观察组患者治疗后的KPS评分为(76.86±6.75)分,显著高于对照组的(72.79±5.83)分,差异有统计学差异。观察组治疗后6个月的生存率为91.67%,高于对照组的86.11%,但差异无统计学意义,观察组治疗后12个月的生存率为83.33%,显著高于对照组的61.11%,两组间差异有统计学意义。结果表明,贝伐单抗联合TACE可显著提高患者的生存质量,延长患者的生存时间,对晚期原发性肝癌患者的治疗有着重要的临床意义。另外,两组患者治疗后不良反应发生率比较,差异无统计学意义。而对于不良反应,应给予对症支持治疗,降低其对患者机体造成的二次伤害,如治疗后出现过敏反应的患者应及时给予糖皮质类激素治疗。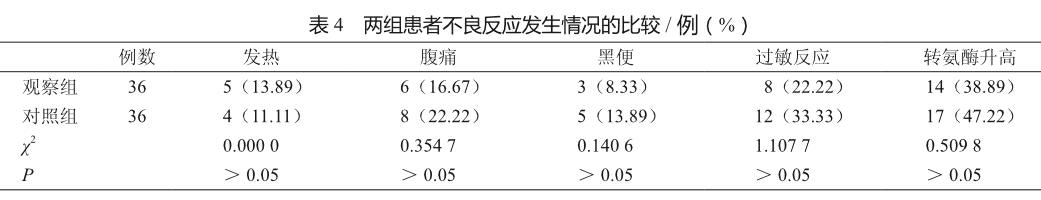
综上所述,贝伐单抗TACE治疗晚期原发性肝癌可提高患者的生存质量,延长患者的生存时间,且还降低患者血清AFP和CEA的水平,疗效确切,值得应用于临床。
参考文献
[1] 肇晖. 樊嘉:用创新播撒大爱[J]. 上海医药, 2015, 36(21): 1-2.
[2] 朱帝文, 张海潇, 顾俊鹏, 等. 贝伐单抗动脉灌注联合化疗栓塞术治疗原发性肝癌的血管造影变化及初步评价[J].中国全科医学, 2015, 18(3): 350-354.
[3] 中华人民共和国卫生部. 原发性肝癌诊疗规范(2011年版)[J]. 临床肿瘤学杂志, 2011, 16(10): 929-946.
[4] 苏小琴, 徐爱兵, 王建红, 等. 沙利度胺联合吉西他滨及奥沙利铂方案治疗中晚期肝癌的临床对照研究[J]. 胃肠病学和肝病学杂志, 2012, 21(7): 604-606.
[5] 郑志范, 徐崇德. 奥沙利铂联合吉西他滨治疗原发性肝癌的近期疗效及不良反应观察[J]. 中国初级卫生保健, 2013, 27(6): 113-114.
[6] 黄芹青, 刘忠华, 沈间凤. 肝动脉化疗栓塞术联合深部热疗治疗晚期原发性肝癌的临床研究[J]. 疑难病杂志, 2015, 14(2): 154-157.
[7] Forner A, Gilabert M, Bruix J, et al. Treatment of intermediate-stage hepatocellular carcinoma[J]. Nat Rev Clin Oncol, 2014, 11(9): 525-535.
[8] 曹耿飞, 纪卫政, 顾俊鹏, 等. 贝伐单抗联合TACE治疗TACE-抵抗性肝癌13例疗效观察[J]. 介入放射学杂志, 2015, 24(1): 69-73.
[9] 黄文, 曾茹雪, 钟辉, 等. 康艾注射液联合介入化疗栓塞对晚期肝癌患者凝血功能及血清VEGF的影响[J]. 海南医学院学报, 2014, 20(10): 1380-1382.
[10] 赵灵华, 曾斌. 贝伐单抗联合肝动脉化疗栓塞术治疗原发性肝癌的临床疗效及安全性评价[J]. 中国临床药理学杂志, 2016, 32(2): 126-128.
[11] 周海平. 表柔比星经导管TACE介入治疗对晚期原发性肝癌患者生存率的影响[J]. 中国现代医生, 2014, 52(34): 61-64, 71.
[12] Sieghart W, Hueke F, Pinter M, et al. The ART of decision making: retreatment with transarterial chemoembolization in patients with hepatoeellular carcinoma[J]. Hepatology, 2013, 57(6): 2261-2273.
[13] 牛武学. 肝动脉栓塞化学治疗联合免疫治疗对晚期肝癌患者免疫功能及生存的影响[J]. 新乡医学院学报, 2015, 32(2): 171-174.
[14] Arjaans M, Oude Munnink TH, Oosting SF, et al. Bevacizumab-induced normalization of blood vessels in tumors hampers antibody uptake [J]. Cancer Res, 2013, 73(11): 3347-3355.

