气相色谱法测定自制山银花露中芳樟醇的含量*
唐富山,覃 飞,吴 庆,周旭美
(遵义医学院 药学院,贵州 遵义 563099)
技术与方法
气相色谱法测定自制山银花露中芳樟醇的含量*
唐富山,覃飞,吴庆,周旭美
(遵义医学院 药学院,贵州 遵义563099)
目的 建立测定山银花露中芳樟醇的气相色谱方法。方法 采用水蒸气蒸馏法制备山银花露; 气相色谱法采用Agilent HP-5MS色谱柱(30 m×0.32 mm×0.25 μm), 柱初始温度为70 ℃, 程序升温到250 ℃; 汽化室温度为260 ℃;载气:高纯N2,流速:1 mL/min;进样量为3 μL。采用樟脑为内标以内标法测定芳樟醇含量。结果 制剂辅料和测定用溶剂不干扰测定,芳樟醇2.16~216 μg/mL范围内线性关系良好,测得标准曲线回归方程为y=66.455x+0.006 6(R2=0.999 4),平均加样回收率为98.4%(RSD=1.4%)。结论 所建立的芳樟醇气相色谱定量方法专属性强、精密、准确, 可用于山银花露的质量控制。
芳樟醇; 气相色谱; 山银花; 露剂; 质量控制
山银花为灰毡毛忍冬、红腺忍冬、华南忍冬或黄褐毛忍冬等的干燥花蕾或带初开的花[1-2], 采收、干燥后为常用中药, 临床应用广泛。山银花的主要化学成分[2-5]有绿原酸类(绿原酸、异绿原酸)、黄酮化合物类(槲皮素、木犀草苷等)、挥发油类(芳樟醇、棕榈酸、亚油酸、香叶醇、松油醇以及辛烯醇等)。灰毡毛忍冬主要生长于湖南、四川、贵州、广西等地且药材质量较好, 产量高, 资源蕴藏丰富。山银花是贵州省重要的经济作物及绿化树种, 具有重要的药用价值和经济效益[6- 7]。山银花中挥发油及挥发油中挥发性成分分析已有报道[8-9], 研究表明芳樟醇是山银花中最重要的挥发性成分, 占挥发油总量的24.51%。目前市面销售的金银花露产品较多, 而山银花露产品则相对较少, 基于山银花与金银花挥发性成分的区别和可能药效的一致性[4,10-11], 为了开发山银花更多的利用价值, 我们参考中国药典和有关文献[1,12]研究制备了山银花露。文献中关于气相色谱法测定金银花露中芳樟醇含量已有报道[13], 但测定山银花露中芳樟醇含量作为其质量控制的研究未见报道。本文建立了气相色谱法测定自制山银花露中芳樟醇含量的方法,旨在为山银花露的质量控制提供试验依据, 促进山银花资源的有效利用。
1 材料与方法
1.1药品与试剂山银花药材(购自贵州省遵义市绥阳县小关乡, 经遵义医学院生药学教研室杨建文主任药师鉴定为灰毡毛忍冬); 芳樟醇对照品(中国药品生物制品检定所, 批号: 00608); 樟脑对照品(中国药品生物制品检定所, 批号: 110747-201008); 其余制备用试剂为分析纯或化学纯, 分析用试剂均为分析纯, 水为超纯水。
1.2实验仪器气质联用仪(美国Agilent, 型号: 5973N); 挥发油测定器; 电子天平(北京赛多利斯天平有限公司); Dura12纯水处理器(泽拉布仪器有限公司)。
1.3方法
1.3.1山银花露的制备参考中国药典金银花露的制备方法[1-2], 按如下流程制备: 取山银花65 g, 水蒸汽蒸馏, 收集蒸馏液1 000 mL, 加入适量的蔗糖(矫味剂)、亚硫酸氢钠(抗氧化剂)和苯甲酸钠(防腐剂), 并以氢氧化钠或盐酸调节其pH为3.6, 过滤, 灌装, 灭菌, 即得。
1.3.2溶液的配制
1.3.2.1内标物溶液的配制精密称取樟脑对照品7.6 mg, 于25 mL的容量瓶中加入无水乙醇制备成含樟脑0.304 mg/mL的内标物溶液。
1.3.2.2对照品溶液储备液的配制精密称量芳樟醇对照品10.8 mg, 放置于25 mL的容量瓶中, 用无水乙醇溶解并稀释至刻度, 摇匀, 即为对照品溶液储备液。
1.3.2.3挥发油的提取与供试品溶液的制备取山银花露100 mL, 置于150 mL的圆底烧瓶中, 加入氯化钠20 g, 连接挥发油测定器,在其上端加水装满刻度部分, 并溢流入圆底烧瓶为止, 再加入乙酸乙酯2 mL, 然后, 加热到沸腾并保持微沸2 h, 放置冷却后再吸取乙酸乙酯层, 加入适量无水硫酸钠脱去多余的水分。取其上层清液置于5 mL容量瓶中, 然后, 精密加入0.5 mL内标物溶液, 用无水乙醇稀释至刻度, 摇匀, 即为供试品溶液。
不含山银花的山银花露阴性样品供试溶液, 除不加入山银花药材和内标物樟脑外, 按山银花露制备及本项下完全相同步骤制备。
1.3.3气相色谱试验法对对照品和供试品溶液中的挥发性成分采用气相色谱分析, 所得结果用内标法计算样品中芳樟醇的相对百分含量。色谱条件: Agilent HP-5MS色谱柱(30 m×0.32 mm×0.25 μm); 程序升温: 初始温度为70 ℃, 保持1 min, 以3 ℃/min的速率升温到130 ℃, 再以50 ℃/min的速率升温到250 ℃, 维持10 min; 汽化室温度: 260 ℃; 载气: 高纯N2, 流速: 1 mL/min; 进样量为3 μL; 分流比20∶1。
1.3.4分析方法的方法学考察
1.3.4.1方法专属性吸取配制好含有内标物樟脑的供试品、对照品及不含山银花的山银花露阴性样品供试溶液各适量, 按1.3.3项下色谱条件分别进行气相色谱测定, 记录色谱图, 对比芳樟醇和樟脑的出峰情况和保留时间。
1.3.4.2线性关系试验精密量取已配好的对照品储备液0.05、0.1、0.3、1.0、2.0、5.0 mL, 分别置于10 mL容量瓶中, 各精密加入内标物溶液0.5 mL, 用无水乙醇稀释至刻度, 制备系列对照品溶液。按照1.3.3节条件进行气相色谱法分析。以芳樟醇与内标物的峰面积比对浓度比进行线性回归, 求取标准曲线回归方程。以芳樟醇对内标物浓度之比为横坐标, 芳樟醇对内标物的峰面积之比为纵坐标, 绘制标准曲线。
1.3.4.3精密度试验精密量取已配好的对照品储备液1.0 mL, 置于10 mL容量瓶中, 精密加入已配好的内标物溶液0.5 mL, 用无水乙醇稀释至刻度, 将配好的溶液按照1.3.3节条件进行气相色谱法分析, 连续进样6次, 记录芳樟醇及内标物的峰面积。
1.3.4.4重复性试验在较短的时间间隔内, 取已配好的供试品溶液按照1.3.3节条件进行气相色谱法分析, 连续进样6次, 记录芳樟醇及内标物的峰面积。
1.3.4.5稳定性试验分别在供试溶液配制后0、1、2、4、8 h, 按照1.3.3节条件进行气相色谱法分析, 记录芳樟醇及内标物的峰面积。
1.3.4.6加样回收率试验精密吸取已知芳樟醇浓度的山银花露约100 mL, 精密加入一定量的芳樟醇对照品溶液, 按1.3.2.3节方法提取挥发油并制备供试品溶液, 按照1.3.3节条件进行气相色谱法分析。计算加样回收率。
1.3.5样品含量测定取3个批次的自制山银花露, 按1.3.2.3节方法提取挥发油并制备供试品溶液, 按照1.3.3节条件进行气相色谱法分析。记录峰面积, 计算样品含量。
2 结果
2.1方法专属性供试品、对照品及阴性样品色谱图(见图1)。色谱图显示, 对照品芳樟醇与内标物樟脑分离良好, 出峰时间适宜; 样品及由样品提取的挥发油中其它成分对芳樟醇测定没有干扰。芳樟醇对照品中加入内标物樟脑, 芳樟醇和樟脑的保留时间分别为8.469、9.807 min, 山银花露供试品溶液中加入内标物樟脑, 测得相应的保留时间分别为8.431、9.794 min, 阴性样品供试溶液色谱图中无相应色谱峰。结果表明, 制剂处方中的辅料及色谱测定溶剂不影响芳樟醇及樟脑的定性和定量, 该分析方法具有较高的专属性。
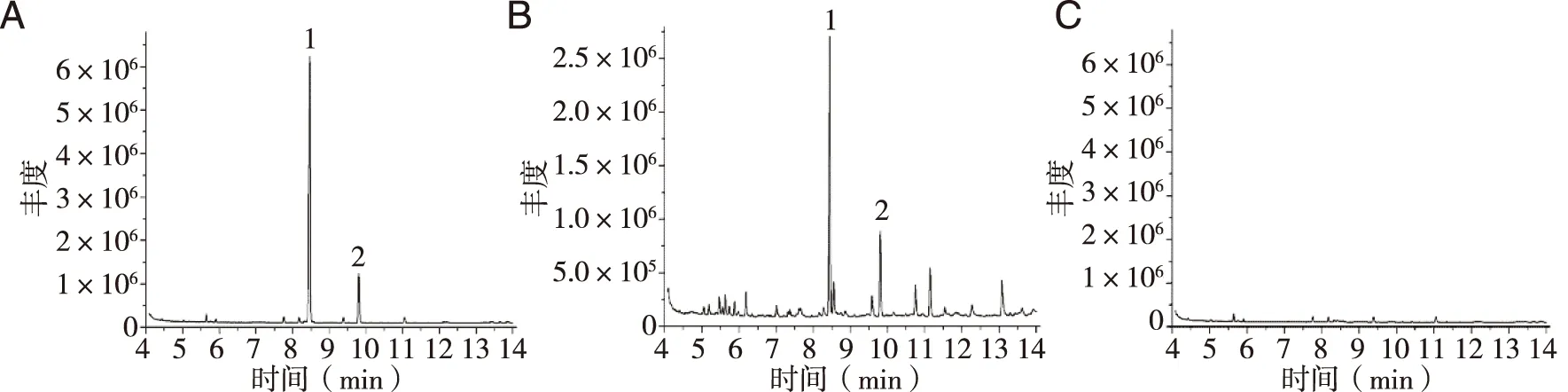
A: 芳樟醇对照品+内标物(樟脑); B: 山银花露挥发油+内标物(樟脑); C: 山银花阴性样品。1: 芳樟醇; 2: 樟脑。图1 气相色谱图
2.2线性关系以芳樟醇对内标物浓度之比为横坐标, 芳樟醇对内标物的峰面积之比为纵坐标, 绘制标准曲线, 得出标准曲线回归方程为y=66.455x+0.006 6(R2= 0.999 4), 表明在芳樟醇2.16~216 μg/mL范围内线性关系良好。
2.3精密度同一浓度对照品供试溶液连续进样6次, 芳樟醇对内标物的峰面积比值的RSD=0.9%, RSD<2.0%, 表明该方法仪器精密度良好。
2.4重复性同批次样品供试品溶液连续进样6次, 芳樟醇对内标物的峰面积比值的RSD=1.2%, RSD<2.0%, 表明该方法重复性良好。
2.5稳定性供试品溶液配制后不同时间进样, 芳樟醇对内标物的峰面积比值RSD=1.9%, RSD<2.0%, 表明样品溶液在8 h内稳定, 方法稳定性良好。
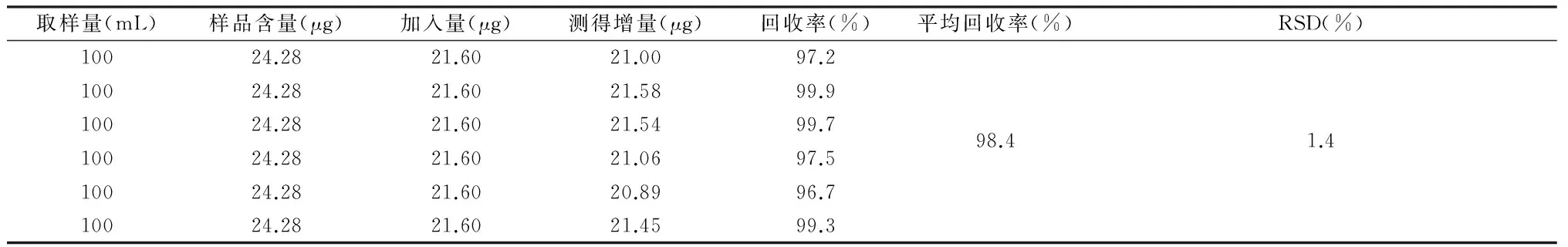
2.6加样回收率加样回收率结果见表1, RSD<2.0%, 表明本试验方法准确可靠。
表1山银花露中芳樟醇加样回收率试验数据
取样量(mL)样品含量(μg)加入量(μg)测得增量(μg)回收率(%)平均回收率(%)RSD(%)10024.2821.6021.0097.210024.2821.6021.5899.910024.2821.6021.5499.798.41.410024.2821.6021.0697.510024.2821.6020.8996.710024.2821.6021.4599.3
2.7样品含量测定结果样品含量结果见表2。
表2山银花露中芳樟醇含量测定结果

样品批号芳樟醇含量(μg/100mL)15102429.3315110724.2815111420.14
3 讨论
芳香水剂为挥发油或其他挥发性芳香药物的饱和或近饱和澄明水溶液, 露剂系指含挥发性成分的饮片用水蒸气蒸馏法制成的芳香水剂[1-2]。本实验中所制得的山银花露为无色至淡黄色透明液体, 味道微甜, 带有芳香气味。因挥发油或挥发性物质在水中的溶解度很小, 故芳香水剂中挥发性成分的浓度都很低, 因此本实验参考有关文献[14-17], 并结合产品和仪器实际情况, 采用气相色谱法测定山银花露中芳樟醇浓度。又由于气相色谱法的进样量一般仅数微升, 尤其当采用手工进样时, 留针时间和室温等对进样量也有影响, 进样误差对结果的影响较大。为减少进样等操作过程的误差, 故采用内标法定量。
已有文献[8,18]研究结果表明, 山银花中芳樟醇含量显著低于金银花, 而本文中自制山银花露中芳樟醇的含量却显著高于文献报道中以类似方法制备的金银花露中芳樟醇的含量[13]。这很可能与测定中挥发油提取环节有关, 本文所建立的方法中, 提取挥发油时, 在露剂中加入一定量的氯化钠, 促进油水分层, 便于除去水分获得挥发油, 使得挥发性成分提取更加完全。然而,当然也提示有必要通过更多研究来探索和确证山银花中挥发性充分等效用成分与金银花的异同。
山银花露的开发研究, 对山银花的综合利用、相关产业的开发和地域经济的发展具有一定的参考价值[19]。质量控制是其中主要的技术环节。本文采用气相色谱法建立了山银花露中芳樟醇含量的测定方法。结果表明该方法简便、可靠、重复性强, 为山银花露的质量控制提供了试验依据。该方法也可为其它制剂中芳樟醇等挥发性成分的检测提供参考。
[1] 国家药典委员会. 中国药典一部[S]. 北京: 中国医药科技出版社, 2015.
[2] 国家药典委员会. 中国药典一部[S]. 北京: 中国医药科技出版社, 2010.
[3] 柴兴云, 李萍, 唐力英. 山银花化学成分研究[J]. 中国中药杂志, 2004, 29(9): 865-867.
[4] 温建辉,倪付勇, 赵祎武, 等. 山银花化学成分研究[J]. 中草药, 2015, 46(13): 1883-1886.
[5] 王振中, 毕宇安, 尚强, 等.金银花与山银花挥发性成分GC-MS的研究[J].中草药, 2008, 39(5): 672-674.
[6] 张倩茹, 周旭美, 荆晶, 等. 遵义小关山银花的质量评价[J]. 光谱实验室, 2012, 29(5): 2707-2712.
[7] 张艳, 周旭美, 姚晓东, 等. HPLC-ELSD测定绥阳山银花中绿原酸和灰毡毛忍冬皂苷乙的含量[J].遵义医学院学报, 2013, 36(6): 575-577.
[8] 刘艳, 熊伟, 李春红, 等. 不同加工方法对泸州山银花挥发油含量的影响[J]. 中国医院药学杂志, 2013, 33(23): 2004-2006.
[9] 何兵, 冯文宇, 田吉, 等. 四川泸州山银花挥发油化学成分的气相色谱-质谱联用分析[J]. 时珍国医国药, 2007, 18(10): 2368-2369.
[10] 杨倩茹, 赵媛媛, 郝江波, 等. 金银花与山银花化学成分及其差异的研究进展[J]. 中国中药杂志, 2016,41(7): 1204-1211.
[11] 贺红, 杨姣, 胡超, 等. 基于谱动学研究金(山)银花的生物等效性[J]. 中国实验方剂学杂志, 2016,22(16): 1-5.
[12] 唐静. 浓缩金银花露的研制[D]. 湖北中医学院, 2008.
[13] 李奇, 田静. GC法测定金银花露中芳樟醇的含量[J]. 临床合理用药杂志, 2014, 7(9B): 89-90.
[14] 张启明, 姜平川, 刘刚. 气相色谱法测定岗松油中芳樟醇和桉油精的含量[J]. 中国药学杂志, 2004, 39(4): 298-300.
[15] 刘艳, 何兵, 熊伟, 等. 不同加工方法对泸州山银花品质影响的研究[J]. 药物分析杂志, 2013, 33(11): 1984-1988.
[16] 刘童斌, 潘明月, 凌雪峰, 等. 毛白杜鹃花挥发油化学成分GC-MS分析[J]. 中药材, 2013, 36(10): 1617-1619.
[17] 吴丽芬, 庞玉新, 杨全, 等. GC法同时测定艾纳香油中5个主要成分的含量[J]. 药物分析杂志, 2015, 35(7): 1179-1184.
[18] 万琴, 萧伟, 王振中, 等. 气相色谱法测定金银花中芳樟醇的含量[J]. 南京中医药大学学报, 2010, 26(4): 317-318.
[19] 童红, 江维克, 周涛, 等. 贵州金银花与山银花的产业现状调查[J]. 贵州农业科学, 2014, 42(1): 238-242.
[收稿2016-06-14;修回2016-07-16]
(编辑:王静)
Determination of linalool in Flos Lonicerae distillate with gas chromatography
TangFushan,QinFei,WuQing,ZhouXumei
(School of Pharmacy, Zunyi Medical University, Zunyi Guizhou 563099, China)
Objective To establish the gas chromatography method for determination of linalool in Flos Lonicerae distillate.Methods Flos Lonicerae distillate was prepared by steam distillation. The volatile constituents represented by linalool in Flos Lonicerae distillate were determinated by gas chromatography with camphor as internal standard. Agilent HP-5MS colummn (30 m×0.32 mm×0.25 μm﹚was used as stationary phase with programmed temperature from 70 ℃ to 250 ℃. The temperature of vaporizing chamber was set as 260 ℃. High purity nitrogen was used as carrier gas with a flow rate of 1 mL/min. The injection volume was set as 3 μL.Results The pharmaceutical adjuncts and the solvents did not disturb the determination. Good linearity could be found between the peak area ratio and the concentration ratio of linalool vs. internal standard at linalool concentration of 2.16~216 μg/mL with regression equation,y= 66.455x+ 0.006 6 (R2= 0.999 4). The average sample recovery rate of linalool was 98.4% with RSD of 1.4%.Conclusion The GC method could be used for quality control of Flos Lonicerae distillate for its specificity, good precision and high accuracy.
linalool; gas chromatography (GC); Flos Lonicerae; distillate; quality control
国家自然科学基金资助项目(NO:31460246);贵州省科学技术基金资助项目(NO:黔科合J字[2013]2323);遵义医学院博士科研启动基金资助项目(NO:F-583)
周旭美,女,教授,硕士生导师,研究方向:药物质量标准建立及新药研发,E-mail:546265853@qq.com。
R917
A
1000-2715(2016)04-0423-04

