高效液相色谱-蒸发光散射检测器法测定健儿宝颗粒中黄芪甲苷含量
谢紫薇,谭天林,王瑷萍,陈玉琼,傅昌吉,廖 芳
(四川省成都市新都区中医医院,四川成都610500)
高效液相色谱-蒸发光散射检测器法测定健儿宝颗粒中黄芪甲苷含量
谢紫薇,谭天林,王瑷萍,陈玉琼,傅昌吉,廖芳
(四川省成都市新都区中医医院,四川成都610500)
目的建立测定健儿宝颗粒中黄芪甲苷含量的高效液相色谱-蒸发光散射检测器(HPLC-ELSD)法。方法色谱柱为Inertsil ODS-2柱(150 mm×4.6 mm,5 μm),流动相为乙腈-水(32∶68),柱温35℃,流速1.0 mL/min;ELSD参数,载气流速2.5 L/min,漂移管温度95℃。结果黄芪甲苷进样量在1.004 8~12.057 6 μg范围内与峰面积呈良好线性关系(r=0.999 8),平均回收率为101.67%,RSD为1.49%(n=6)。结论该方法操作简便、快速、准确,可作为健儿宝颗粒的含量测定方法。
高效液相色谱-蒸发光散射检测器法;健儿宝颗粒;黄芪甲苷;含量测定
健儿宝颗粒由黄芪、桂枝、白芍、白术、大枣、山药、山楂(焦)等15味中药组方,是成都市新都区中医医院在传统经验方基础上研制开发的中药制剂,具有益气合营、健脾开胃等功效,临床使用多年,疗效较好。该制剂质量标准中仅对黄芪甲苷进行定性鉴别,无含量测定项。黄芪功能甘温益气、扶正固表,用量是处方中其他药味的2~4倍,为方中君药,故控制黄芪的含量非常重要。黄芪甲苷是黄芪的主要活性成分[1-2],具有良好的免疫调节[3]、抗炎[4-5]、抗病毒[6]、脏器保护[7-8]、神经细胞保护作用[9-10],并具有一定的氧自由基清除作用[11]。目前,蒸发光散射检测器(ELSD)较多应用于皂苷类成分分析[12],多采用高效液相色谱-蒸发光散射检测(HPLC-ELSD)法检测制剂中黄芪甲苷的含量[13-16]。为更好地控制该制剂的质量提供参考,笔者对此进行了研究,现报道如下。
1 仪器和试药
1.1仪器
Agilent-1200型高效液相色谱仪(美国安捷伦科技有限公司);Alltech ELSD 2000ES型蒸发光检测器(美国奥泰科技有限公司);TGL-16G型离心机(上海安亭科学仪器厂);SY7200-D型超声波清洗仪(上海声源超声仪器设备有限公司);BT125D型电子天平(赛多利斯科学仪器<北京>有限公司);AE 260-S型电子天平(瑞士梅特勒科学仪器有限公司)。
1.2试药
健儿宝颗粒(批号为140901,150501,151101),阴性样品均为我院医院制剂;黄芪甲苷对照品(中国药品生物制品检定所,批号为200613);乙腈(色谱纯,Fisher公司,批号为111760),水为重蒸馏水,其余试剂均为分析纯。
2 方法与结果
2.1色谱条件
色谱柱:Inertsil ODS-2柱(150 mm×4.6 mm,5 μm);柱温:35℃;流动相:乙腈-水(32∶68);流速: 1.0 mL/min;漂移管温度:95℃;载气流速:2.5 L/min。理论板数按黄芪甲苷峰计算不得低于4 000。
2.2溶液制备
称取黄芪甲苷对照品25.12 mg,精密称定,加甲醇溶解并定容至25 mL,即得对照品溶液(质量浓度为1.004 8 g/L)。取供试品(批号151101)约2 g,磨成细粉,精密称定,置锥形瓶中,精密加入甲醇50 mL,称定质量,回流提取40 min,放冷,用甲醇补足质量,摇匀过滤,精密量取续滤液25 mL,水浴蒸干;残渣加水10 mL微热使溶解,用饱和的正丁醇振摇提取3次,每次30 mL,合并正丁醇液,用氨试液洗涤2次,每次30 mL,弃去氨液,正丁醇液蒸干,用甲醇溶解并转移至5 mL容量瓶中,加甲醇至刻度,摇匀,作为供试品溶液。按处方取除黄芪外的其他药材,按供试品溶液制备方法制备阴性对照品溶液。
2.3方法学考察
专属性试验:分别吸取2.2项下3种溶液,按拟订色谱条件进行测定。结果表明,主峰分离度符合要求,且阴性对照品溶液色谱在黄芪甲苷出峰处无干扰。色谱图见图1。

图1 高效液相色谱图
线性关系考察:分别精密量取对照品溶液适量,加甲醇稀释成系列标准溶液(质量浓度分别为0.050 24,0.100 48,0.200 96,0.301 44,0.401 92,0.502 40,0.602 88 g/L),按拟订色谱条件,分别进样20 μL。以黄芪甲苷进样量对数值为横坐标(X)、其峰面积对数值为纵坐标(Y)进行线性回归,得回归方程Y=1.618 9X+ 2.769 6,r=0.999 8(n=7)。结果表明,黄芪甲苷进样量在1.004 8~12.057 6 μg范围内与峰面积呈良好的线性关系。
精密度试验:精密吸取同一对照品溶液20 μL,连续进样6次,测定峰面积,结果见表1。结果的RSD为1.00%(n=6),表明该仪器精密度良好。
重复性试验:取同一批样品,精密称取6份,按2.2项下方法制备供试品溶液6份,按拟订色谱条件依次测定。结果见表1,平均含量为1.221 4 mg/g,RSD为1.66%(n=6),表明方法重复性良好。
稳定性试验:精密吸取同一供试品溶液,分别于0,2,4,6,8,10,12 h时分别进样20 μL,测定峰面积。结果见表2,黄芪甲苷含量的RSD为1.02%(n=7),表明供试品溶液在12 h内稳定。

表1 精密度及重复性试验结果

表2 稳定性试验结果
加样回收试验:精密称取已知含量的供试品(批号为150501,含量为1.091 4 mg/g)细粉6份,每份2 g,分别精密加入质量浓度为1.008 g/L的黄芪甲苷对照品溶液2 mL,再分别精密加入甲醇50 mL,按2.2项下方法制备供试品溶液,依法测定,计算回收率。结果见表3。

表3 黄芪甲苷加样回收试验结果(n=6)
2.4样品含量测定
取供试品(批号为140901,150501,151101)3批,按2.2项下方法制备成供试品溶液,测定并计算黄芪甲苷的含量。结果见表4。
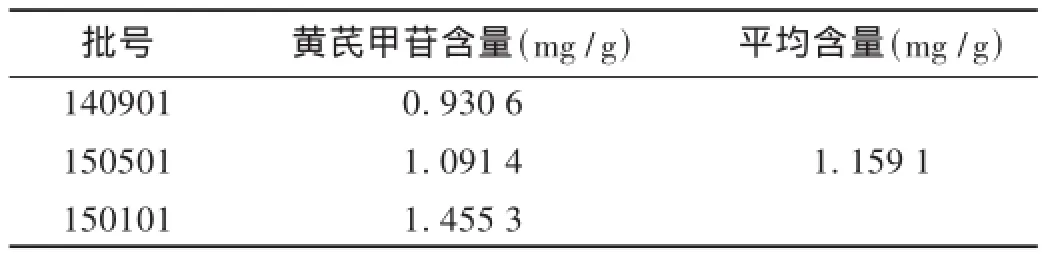
表4 样品含量测定结果
3 讨论
3.1指标成分选择
处方中黄芪属君药,用量大,测定黄芪甲苷的含量对于控制制剂质量有较大意义,故选用黄芪甲苷作指标成分进行含量测定。
3.2检测方法确定
黄芪甲苷为皂苷类成分,在紫外末端有吸收,干扰大,基线不稳定。ELSD为质量通用型检测器,重复性和稳定性均较好,且方法简便,易测定。
提取方式选择:对供试品的提取方式(超声和回流)和提取时间(30,40,60 min)进行考察,采用回流提取比超声提取的黄芪甲苷含量更高,从时间和成本的角度考虑,选择回流提取40 min。
[1]张氵昊.浅谈中药黄芪的化学成分及药理作用[J].当代医药论丛,2015,13(12):45-46.
[2]孙政华,邵晶,郭玫.黄芪化学成分及药理作用研究进展[J].中医临床研究,2015,7(25):22-25.
[3]林琳,沈洪,王立新,等.黄芪甲苷、β-榄香烯对小鼠树突状细胞免疫功能的影响[J].东南大学学报,2011,30(2): 294.
[4]Wang S,Li J,Huang H,et al.Antihipatitis B virusacti vities of astragalosideⅣisolated from radix A stragali[J].Biol-Pharm Bull,2009,32(1):132-135.
[5]Zhang WJ,Hufnaql P,Binder BR,et al.Antiinflammatory activity of astragalosideⅣis mediated by inhibition of NF-kappa B activation and adhesion molecule expression[J].Thromb Haemost,2003,90(5):904-914.
[6]Zhang YY,Zhu HY,Huang CG,et al.AstragalosideⅣexerts antiviral effects against coxsackievirus B3 by upregulating interferon gamma[J].J Cardiovasc Pharmacol,2006,47(2):190.
[7]Liu H,Wei W,Sun WY,et al.Protective effects of astragalosideⅣon porcineserum-induced hepatic fibrosis in rats and in vitro effects on hepatic stellate cells[J].JE thnopharmacol,2009,122(3):502-508.
[8]Qi H,Wei L,Han Y,et al.Proteomic characterization of the cellular response to chemopreventive triterpenoid astragalosideⅣin human hepatocellular carcinoma cell line HepG2[J].Int J Oncol,2010,36(3):725.
[9]Chan WS,Duraira JS,Lu JH,et al.Neuroprotective effects of astragalosideⅣin 6-hydroxydopam intreated primarynigral cell culture[J].Neurochem Int,2009,55(6):414-422.
[10]Zhu SQ,Qi L,Rui YF,et al.AstragalosideⅣinhibits spontaneous synaptic transmission and synchronized Ca2+o scillations on hippocampal neurons[J].Acta Pharmacol Sin,2008,29(1): 57-64.
[11]Qiu LH,Xie XJ,Zhang BQ.AstragalosideⅣimproves homocysteine-induced acute phase endothelial dysfunction via antioxidation[J].Biol Pharm Bull,2010,33(4):641-646.
[12]赵宇新,李曼玲.蒸发光散射检测器在中药成分分析中的应用[J].中国中药杂志,2003,28(10):913-917.
[13]王红,杨慈海,宋军,等.高效液相色谱-蒸发光散射检测法测定抗栓通络丸中黄芪甲苷含量[J].中国药业,2016,25(4):75-77.
[14]吴高芬.高效液相色谱-蒸发光散射器法测定芪芳气血颗粒中黄芪甲苷含量[J].中国药业,2015,24(12):60-62.
[15]葛德洲,邓祖磊.高效液相色谱-蒸发光散射法测定甜梦胶囊中黄芪甲苷含量[J].中国药业,2015,24(5):31-32.
[16]庄妍,朱红,范其坤,等.HPLC-ELSD法测定九味肾清颗粒中黄芪甲苷的含量[J].南昌大学学报(医学版),2015,55(4):18-21.
Content Determination of Astragaloside Ⅳin Jianerbao Granules by HPLC-ELSD
Xie Ziwei,Tan Tianlin,Wang Aiping,Chen Yuqiong,Fu Changji,Liao Fang
(Xindu Hospital of Traditional Chinese Medicine,Chengdu,Sichuan,China610500)
ObjectiveTo establish the content determination method of astragalosideⅣin Jianerbao Granules by HPLC-ELSD. MethodsThe Inertsil ODS-2 column(150 mm×4.6 mm,5 μm)was adopted,the mobile phase was acetonitrile-water(32∶68),the column temperature was 35℃,the flow rate was 1.0 mL/min,the gas flow rate was 2.5 L/min,the drift tube temperature was 95℃. ResultsThe injection volume of astragalosideⅣshowed good linear relationship with the peak area in the range of 1.004 8-12.057 6 μg(r=0.999 8),the average recovery rate was 101.67%,RSD=1.49%(n=6).ConclusionThis method is simple to operate,it is rapid and accurate,and can be used as the quality control method of Jianerbao Granules.
HPLC-ELSD;Jianerbao Granules;astragalosideⅣ;content determination
R284.1;R286.0
A
1006-4931(2016)13-0077-03
谢紫薇(1981-),女,汉族,硕士研究生,高级工程师,主要从事中药制剂质量评价工作,(电子信箱)657064681@qq.com。
2016-02-06;
2016-03-20)

