芳纶原料制备中尾气氯化氢回收制氯清洁工艺
王农跃
(上海方纶新材料科技有限公司,上海 200122)
芳纶原料制备中尾气氯化氢回收制氯清洁工艺
王农跃
(上海方纶新材料科技有限公司,上海200122)
阐述了氯化氢污染现状、以及伴随着有机氯产品的发展而产生更多的副产氯化氢情况。介绍了芳纶制造中副产氯化氢的现有处理方法及特点,重点介绍了最具工业化前景的氯化氢催化氧化制氯气清洁工艺,并通过工艺之间的比较,分析了上海方纶开发的氯化氢氧化工艺的优势与发展前景。
氯化氢;催化氧化;氯气
1 氯化氢污染现状
氯气主要应用于生产PVC、聚氨酯环氧树脂、硅材料、合成橡胶、氟氯烃、TiO2,涂料及一些农用化学品、建筑材料和一些医药制剂[1~2]。1998年,美国和欧洲年消耗氯2 500万t,我国消耗量达到576万t,居世界第二位[3]。2008年我国氯气消费量达到1 700万t,约占世界氯气消费总量的1/3[4]。
然而在有氯气参与的工业生产中,主要进行的是有机物的氯取代反应,氯资源的原子利用率最高不超过50%,另外一半的氯成为大量的副产氯化氢。1986年,日本副产HCl就达47万t之多,全世界副产HCl约达1 650万t之多[5]。2011年,我国工业副产氯化氢总量达到了380万t[6],随着MDI、TDI、甲烷氯化物等涉氯产品的大规模扩产和氯碱行业的发展,预计5年内(2012 ~2016年)副产HCl的总量将达到500万t/年。
2 有机氯产品的发展
有机氯是指结构中含有氯元素的有机化合物。目前,我国主要的有机氯产品的生产能力已经稳居世界第1位[7]。国内规模以上氯产品有数十个品种,根据2011年的产能估算[8],其中聚氯乙烯、甲烷氯化物、环氧氯丙烷、MDI/TDI等产能规模较大,约占国内有机氯产品产能的70%以上。
2.1聚氯乙烯(PVC)
聚氯乙烯是氯碱行业耗氯量最大的有机氯产品,其耗氯量约占行业总耗氯量的35%~40%[9]。2005年,我国聚氯乙烯产量为688万t,2014年增至1 630万t,年均增长率达10.4%。近年中国聚氯乙烯产量情况见图1。并且,未来几年中国聚氯乙烯新建项目较多,据不完全统计,新增产能将达到400万t/年左右[10]。
2.2甲烷氯化物
甲烷氯化物包括一氯甲烷、二氯甲烷、三氯甲烷(氯仿)和四氯化碳,是有机氯产品中仅次于聚氯乙烯的最大宗产品。
2003年,我国甲烷氯化物总生产能力接近40万t[11],2010年产能约为116万t/年,2010~2011年新增产能约30万t,达到146万t/年,2013年产能超过200万t/年。目前,国内尚有部分企业正在或计划扩建甲烷氯化物项目[8]。
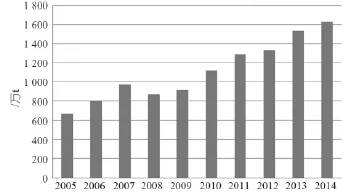
图1 聚氯乙烯产量情况
2.3环氧氯丙烷
环氧氯丙烷是生产环氧树脂、合成甘油和氯醇橡胶的重要原料,近年环氧氯丙烷产能增长情况见下图2。

图2 环氧氯丙烷产能情况
2015年我国环氧氯丙烷产能继续增长,产能有些过剩,市场需求面临考验,但是长期来看,随着经济复苏,需求释放,届时我国环氧氯丙烷的消费也将进入一个新的发展时期[12]。
2.4MDI/ TDI
2.4.1MDI(二苯基甲烷-4,4′-二异氰酸酯)
据不完全统计,2015年我国MDI产能达到261万t/年。且德国拜耳计划在上海新建50.0 万t/年生产装置;巴斯夫公司在重庆新建的40.0 万t/年MDI项目;上海联恒异氰酸酯有限公司在上海启动了新建24.0万t/年MDI生产装置项目。此外,甘肃银光聚银化工有限公司、沧州大化集团有限责任公司、天脊集团等公司也有新建MDI生产装置的初步意向和前期规划。如果这些项目能够按照计划实施,预计到2018年,我国MDI的总生产能力将达到约375.0万t/年,继续领先世界产能潮流[13]。
2.4.2TDI(甲苯二异氰酸酯)
2012年,我国TDI产能为82万t/年[8],2014年产能为88.5万t/年,预计,到2020年国内TDI产能将达到131万t/年[14]。
有机氯产品产能近年来快速增长,从上述列出的几类有机氯产品的产能/产量增长情况可以窥见一斑。伴随着国内氯产品产能的快速增长,氯气的消耗量进一步加大,副产氯化氢量也将随之快速增长。因此,亟待开发一种环保、节能、充分利用副产氯化氢资源的技术。
3 氯化氢制氯气工艺
传统的副产HCl处理方法一是用水吸收制成盐酸被回收利用或低价出售,因其中含有一定量的有机杂质,其用途受到了较大的限制,造成副产盐酸涨库,直接影响主导产品的生产;二是用碱液中和后直接排空,这不仅影响氯产品生产的经济效益,还会造成严重的环境污染。
而许多产生副产氯化氢的工艺同时又是大量消耗氯气的过程,将氯化氢重新转化为氯气,可以实现氯化氢的循环利用。目前,氯化氢制备氯气的方法主要可以分为三类:电解法,直接氧化法和催化氧化法。
3.1电解法
氯化氢电解法分为湿法和干法,而湿法又分为隔膜电解和氧阴极电解。
3.1.1隔膜电解法
隔膜电解法要求氯化氢气体通过吸收使氯化氢变为盐酸,盐酸经过精制除去杂质后在隔膜电解槽中电解,生成氢气和氯气,反应方程式为:2HCl=H2↑+Cl2↑。隔膜电解法工艺是由赫斯特、 拜耳公司和伍德公司合作开发的, 已对世界上一百余家氯碱厂提供该技术。但是该方法能耗大,没有发展潜力。
3.1.2氧阴极电解法
氧阴极电解法也是需要氯化氢气体通过吸收变成盐酸,盐酸经过深度精制除去杂质后,在离子膜电解槽中电解,阴极通入氧气,从而生产出氯气和水,化学方程式为:4HCl+O2=2H2O+2Cl2↑。拜耳公司是世界上利用盐酸电解方法生产氯气的最大生产商,目前在德国有40万t/年生产能力,其中2万t/年采用的是最新的ODC氧阴极盐酸电解工艺。该方法比传统的隔膜法电解节电35%,但是投资大、离子膜电解槽对材质要求高、氧阴极要求高且要求有纯氧供给。
3.1.3干法电解
美国杜邦公司在 20 世纪 90 年代中期发明了干电解氯化氢生产氯的工艺用于乙烯氯化。该方法延长了隔膜的使用寿命,但是对杂质敏感,电解氯化氢前,一般需先将气体用加热的方法进行预处理,脱除有机物和其他杂质,然后加入电解槽阳极一侧,氯化氢转化成氯气,质子通过全氟阳离子交换膜转移到阴极,转化成含水氢气,该工艺能耗高,成本高。
3.2直接氧化法
直接氧化法是利用 NO2、SO3、NOHSO4和混合酸HNO3/H2SO4等无机氧化剂直接氧化HCl制备Cl2的一种方法,典型工艺为杜邦公司20世纪60年代开发的硝酸氧化法Kel-Chlor工艺[15],该工艺使用硝酸和硫酸的混合物氧化氯化氢。反应方程式为:
NO2+2HCl⇋NO+Cl2+H2
NO+ NO2+H2SO4⇋2NOHSO4+H2O
NOHSO4+HCl⇋NOCl+ H2SO4
2NOCl⇋2 NO+Cl2
2 NO+ O2⇋2 NO2
直接氧化法由于存在反应过程中产生腐蚀性物质、产物分离困难、能耗较大、废液处理难等问题,难以实现工业化。
3.3催化氧化法
1868年,英国人Deacon首先采用负载在载体沸石上的铜或锰盐等作为催化剂,氧气或空气作为氧化剂,使氯化氢氧化生成氯气,并发表了一系列专利[16~20],其反应方程式可表述为:4HCl(g)+O2⇋2H2O+Cl2+114.48(kJ),人们习惯上将以上反应称为Deacon反应。在工程应用中存在的问题包括:①受反应平衡的限制,氯化氢转化率只有60%~70%;②反应温度过高(430~475℃之间),活性组分氯化铜在400℃以上容易挥发,导致催化剂流失、活性迅速降;③未反应的氯化氢与可能凝结的水蒸气结合生成盐酸,带来严重的设备腐蚀问题。
1962年,美国Shell Oil Company[21~23]采用SiO2负载铜盐催化剂,并开发了采用该催化剂的固定床工艺[24],于1965年分别在荷兰和印度建成了30 000 t/年的装置,由于催化剂活性组分流失及转化率无法提高等因素,该装置已经关停。
日本住友化学工业株式会社研制公开了以氧化钌为活性组份、氧化钛为载体的催化剂体系[25~27]以及使用氧化钌催化剂的列管式反应器,见图3,在列管中将催化剂分成2~4个串联排列的反应段进行装填,其中至少有一个反应段的温度控制所用的热交换介质为50%~55%硝酸钾、37%~43%亚硝酸钠和5%~10%的硝酸钠所组成的熔盐。其氯气产能为12万t/年规模的固定床反应器已先后在日本三菱公司、拜耳上海公司和万华宁波工业园等地实际应用[28]。该方法中催化剂成本过于昂贵,投资成本高。
Benson小组[29]为了改善固定床反应器氯化氢转化率较低的问题,开发了双流化床二段法工艺。这种工艺流程将反应分为低温氯化(氧化铜和氯化氢在200~280℃下反应)和高温氧化(氯化铜和氧气在340~380℃下反应)两个步骤,催化剂在2个反应器之间通过固体催化剂循环装置进行交互传递。反应方程式为:CuO+2HCl→CuCl2+H2O CuCl2+1/2O2→CuO+Cl2,工艺示意图见图4,该工艺的缺点在于两个反应器中的压力不一样,固体催化剂容易从高压的氧化反应器进入压力低的氯化反应器,而不容易从低压的氯化反应器进入高压的氧化反应器,难以实现催化剂颗粒循环。
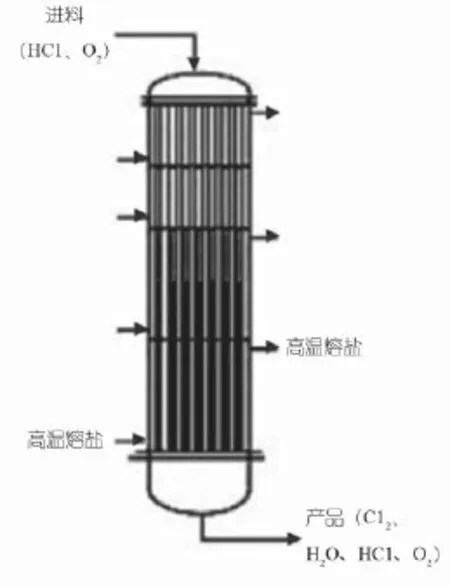
图3 日本住友固定床反应器
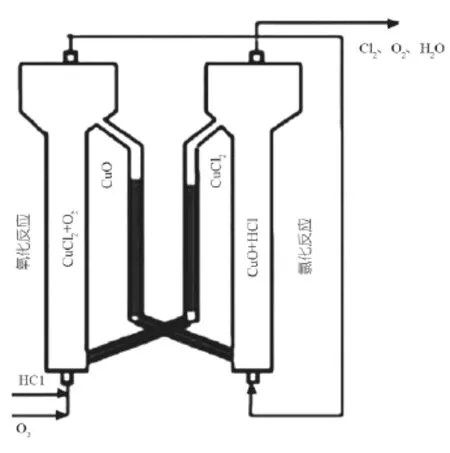
图4 Benson双流化床工艺示意图
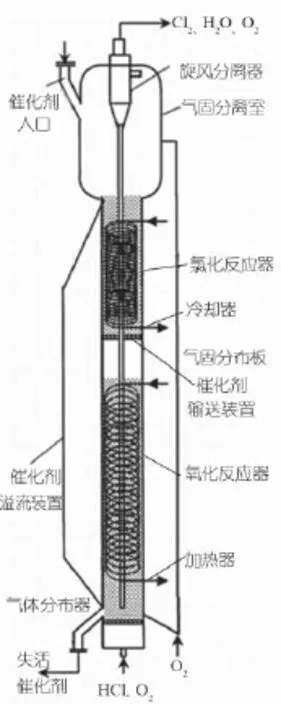
图5 单塔二段流化床
清华大学[30]在Beason工艺的基础上,开发了单塔二段流化床催化氧化工艺,特点是在流化床提升管中设置气固分布板形成二段流化床反应器,上段为进行氯化反应的氯化反应器,下段为发生氧氯化反应的氧化反应器,催化剂的转移靠气流推动和重力完成,见图5,虽然全过程HCl的转化率能接近100%,但在“氧氯化”段氯化氢的转化率未超过60%,且过程操作复杂,控制困难。清华大学和烟台万华共同合作采用该流化床装置在宁波建成了中试装置,但尚未有商业化应用的报道[31]。清华大学在后续对该装置进行了进一步的改进[32],采用气固分布板将流化床反应器主体分为上下两段,上段为氯化段,下段为氧氯化段,氯化氢气体入口设置在氧氯化段的中部,另外通过在氧氯化段设置多层错排气固逆流挡板等措施,进一步提高氯化氢的转化率。
德国巴斯夫公司开发了氯化氢的两阶段固定床催化氧化法[33],第一阶段为氯化,向反应器中通入HCl气体,使HCl与催化剂反应生成水和固定在催化剂上的氯化物,排出水,完成后用惰性气体冲洗反应器;第二阶段为氧化,将气态氧化剂送入反应器,与前面生成的含氯化合物反应,释放出氯气,并排出反应器,随后用惰性气体冲洗反应器。其中,催化剂采用陶瓷材料为载体,用浸渍法将铜、铁、碱金属氯化物等负载于载体上制得。可以用一固定床反应器或多个相连的固定床反应器来实施,图6为5个相连的固定床反应器工艺图。虽然该两阶段固定床反应工艺可以打破氯化氢氧化的化学平衡限制,氯化氢转化率高,但在氧化混合气中仍存在大量的氧气及氮气,难以直接利用。
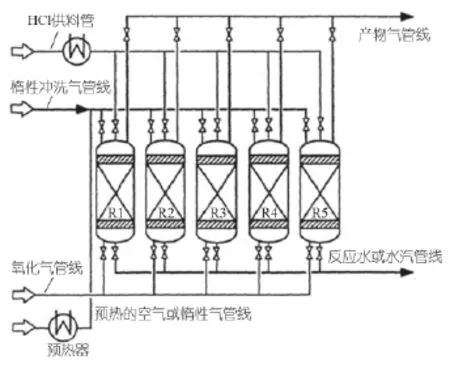
图6 巴斯夫固定床反应器示意图
南京工业大学提出了一种流化床与绝热固定床串联的氯化氢氧化反应工艺[34],可以利用流化床良好的移热性能,避免在列管式固定床反应器中因放热反应产生的飞温现象,图7为流化床反应器与4台绝热反应器串联工艺图。不过,由于固定床与流化床操作气速、催化剂粒度与压降差异均很大,一般很少串联操作使用[35~36],为了满足强放热反应的移热与转化率的要求,可以串联操作,但需要考虑前面的流化床出口夹带的颗粒对后面固定床中催化剂磨损的影响,在0.212~0.424 m/s气速下,固定床中颗粒质量损失可达3%~4%[37];以及后面固定床层对前面流化床催化剂的进一步磨损,并同时关注固定床的允许气速与流化床中细颗粒的机械强度。
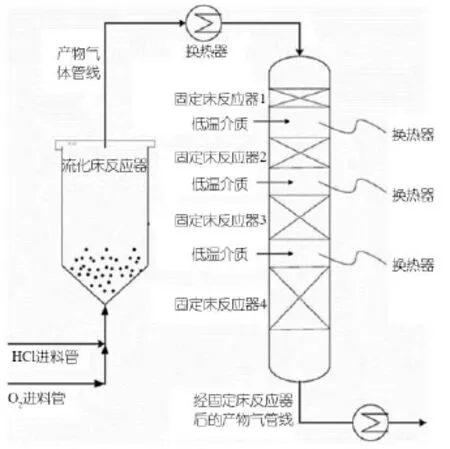
图7 流化床与绝热反应器串联工艺图
万华聚氨酯股份有限公司宁波分公司在生产聚氨酯过程中,每年要产生45万t氯化氢,为此万华也加快了催化氧化制氯技术的研究工作,开发了采用微反应器进行氯化氢氧化制备氯气的工艺[38],微反应器结构示意图见图8。以及一种利用磁稳流化床进行氯化氢氧化制备氯气的工艺[39],磁稳流化床结构示意图见图9。微反应器容易出现微通道堵塞、以及检测与控制难等问题;磁稳流化床的应用需要相应合适的磁性催化剂并确定磁稳流化床的稳定操作区域,磁稳流化床的磁场发生装置在产生磁场的过程中会释放出大量的热量,易对磁性载体和反应过程产生影响。目前来说,这些方法技术都不成熟,工业化困难。
上海氯碱化工股份有限公司,对催化剂进行了改进[40],采用以二氧化硅包覆的氧化铝为载体制备催化剂,并将其应用于固定床工艺,减少了反应过程中催化剂的流失,但是氯化氢转化率低,不到80%。
4 上海方纶新材料开发的氯化氢制氯回收工艺
尽管国内外的企业与科研单位均在加快氯化氢催化氧化制氯技术的开发和改进工作,但是通过前述介绍我们可以看出目前催化氧化工艺仍存在各种问题,其中最大的问题在于:①反应温度较高,催化剂挥发导致活性迅速降低,需要不断更换或者补加催化剂,从而导致生产成本过高;②催化氧化后反应所得气体的分离困难;③成本高,技术不成熟,操作控制难,导致难于实现工业化。

图8 微反应器结构示意图

图9 磁稳流化床结构示意图
针对该情况,上海方纶新材料科技有限公司开发了一种关于氯化氢催化氧化制备氯气的新工艺,该工艺已申请了中国发明专利[41],并提交了PCT国际申请[42]。
上海方纶开发的新工艺可以通过一个或多个串联或并联的装填有催化剂的反应器(优选绝热反应器)来实现。以三个反应器串联、多段进氧为例,工艺流程如图10所示。
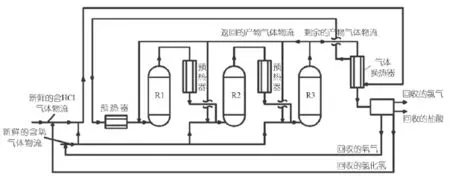
图10 上海方纶材料氯化氢氧化工艺流程
4.1具体工艺步骤
(1)向第一反应器提供含氯化氢气体物流以及用于氧化所述含氯化氢气体物流的含氧气体物流,向第二、第三反应器提供用于氧化所述含氯化氢气体物流的含氧气体物流,以进行催化氧化氯化氢的反应。
(2)将来自第三反应器的经过催化氧化反应的产物气体物流的一部分不经分离直接返回至任意一个或任意多个反应器。
(3)将来自第三反应器的剩余的产物气体物流部分分离以获得氯气,并将分离回收的氯化氢和氧气循环至反应器中继续参与反应。
4.2该工艺具有下列优点
(1)将来自最后一个反应器的经过催化氧化反应的产物气体物流的一部分不经分离返回至反应器,直接利用催化氧化后产物气体物流部分的热能加热含氯化氢气体物流和/或用于氧化含氯化氢气体物流的含氧气体物流,从而使得进入第一反应器的气体物流达到适宜的反应温度,而不必全部使用外部热源对含氯化氢气体物流和/或用于氧化含氯化氢气体物流的含氧气体物流体进行加热到适宜的反应温度。
(2)由于未经分离的产物气体物流再次经过催化剂床层时不再释放反应热,也即这些气体成为只含氯化氢、氧、氯气和水蒸气的不含其他气体成分的相对反应的“惰性”气体,掺混有产物气体物流的气体物流在经过反应器时,反应器中的催化剂床层温度比现有工艺具有更好的可控性。
(3)在返回产物气体物流对反应热的控制作用下,和依次向下游反应器提供含氧气体物流等方式的共同作用下,催化剂寿命得到显著延长。
(4)所返回的产物气体物流与经催化氧化反应得到的产物气体物流成分相同,这大大降低了后续分离操作的难度和对设备的要求;特别地,当选择氧气过量至能够保证氯化氢基本被氧化时,产物气体物流更易于分离。因为氧气过量,使得氯化氢残余量小,甚至可以忽略。因此产物气体物流通过冷凝后,反应形成的水即可以将氯化氢基本吸收,深度脱除水份后,只需要分离氯气和氧气,即可得到氯气,后续分离操作可以进一步简化。
5 氯化氢制备氯气的工艺比较
由于电解法存在着投资大、能耗高、对装置要求高及产品纯度不高等不足之处、而直接氧化法又难以实现工业化,因此,催化氧化法最具工业化潜力,成为氯化氢转化为氯气的主要发展方向。
从工业化能力比较来说:
(1)电解法,能源消耗太大,且离子膜也需要经常更换,成本非常高,每吨氯气回收成本>4 000元。
(2)直接氧化法,回收率低,不可工业化。
(3)催化氧化过程最具工业化潜力,部分工艺已经实现工业化,但是仍然存在氯化氢转化率低,投资成本高等问题。其中固定床催化氧化法,设备投资太大,每吨氯气回收成本>1 200元,万吨氯化氢处理装置投资>10亿,且没有解决系统中由于氯化氢、氧气、水汽、氯气的混合气体,在400℃以上操作温度下的设备腐蚀问题以及反应巨大的放热引起的传热问题;而国内由高校与企业共同研发的流动床工艺一直受到反应温度高、体系材质耐腐蚀等问题的困扰。
(4)上海方纶新材料科技有限公司研发的氯化氢氧化过程,采用多级进氧、反应气循环的绝热反应工艺,既解决了设备腐蚀问题也解决了传热问题,单程转化率达到90%以上,并用吸附与解吸附工艺回收氯气,氯气成本降至400元/t。
氯化氢回收制备氯气的各种工艺的具体比较见表1。

表1 氯化氢制备氯气方法比较
6 上海方纶新材料氯化氢制氯工艺的发展前景
近年来,我国氯碱产能的快速增长带动和刺激了氯产品的发展,与此同时,国内外市场对氯的需求量越来越大,特别是国内外市场对聚氯乙烯和异氰酸酯的强劲需求,使得有机氯产品快速发展,随之而来的是大量的副产氯化氢。除此之外,化肥、轻工、电镀、制药及冶金等行业的生产过程也会产生大量废盐酸,这也是副产氯化氢的重要组成部分,以化肥行业为例,仅仅年产约600万t硫基氮磷钾复合肥,就要副产盐酸约200万t[6]。
大量副产HCl的出路和利用问题已成为制约聚氨酯、氯碱、有机氟、农药、医药化工等众多行业发展的共性难题。因此有效的综合利用副产氯化氢,通过氯化氢的综合利用提供下游有机氯产品赖以发展的原料氯将十分有意义。
但是目前国内仅万华化学在宁波建成了氯化氢催化氧化制氯气工业化装置,虽然其自身也在积极研发氯化氢氧化制氯技术,不过其工业化装置却是引进日本住友的技术。此外,上海氯碱化工股份有限公司自主研发的氯化氢催化氧化制氯气技术已建成千吨级中试装置并平稳运行,但是从上海氯碱公开的技术来看,其氯化氢转化率较低,不到80%。
基于国内的氯化氢催化氧化技术现状并结合副产氯化氢量持续增长的情况来看,上海方纶新材料开发的氯化氢氧化清洁工艺市场前景广阔,其将廉价量大的氯化氢综合利用并高附加值化,实现了氯元素的闭路循环和反应过程的零排放,这将彻底改变整个行业的格局,带来巨大的经济效益和社会效益。参照现有文献[43]估算,如果将我国目前副产的500余万t/年的氯化氢制成氯气或下游产品循环利用,每年可节电约121.3亿kW.h(折标煤425万t/年),间接减排1 000万t各类有机废水,经济效益和社会效益巨大。目前中国产业调整政策已涉及副产氯化氢的综合利用,并列入了国家 2011 年产业结构调整鼓励类名录。因此,上海方纶新材料公司开发的氯化氢催化氧化制氯清洁工艺,也顺应了国家的政策导向,符合循环经济的发展模式,必将得到发展和应用。
[1] 吴玉龙,魏飞,韩明汉,等.回收利用副产氯化氢制氯气的研究进展[J].过程工程学报, 2004,4(3):269~275.
[2]Committee on Medical and Biologic Effects of Environmental Pollutants.Chlorine and Hydrogen Chloride [M]. Washington:National Academy 0f Sciences.1976:282.
[3] 张泗文.世界氯碱产业动向及其对我国市场的影响[J].氯碱工业, 2002,3:1~11.
[4]叶田忠.国内外烧碱市场展望[J].氯碱工业, 2009,45(11):1~7.
[5]万永周.氯化氢催化氧化制氯气工艺研究[D].南京工业大学.2004.
[6]刘建路,何家海,潘玉强,等.我国副产氯化氢的现状和综合利用[J].广州化工, 2011,39(9): 25~28.
[7]何如浩.氯化氢气体在离子液体中溶解性能的研究[D].北京化工大学, 2012.
[8] 刘鹏.氯产品发展建议及主要产业链搭建[J].氯碱工业. 2013.4:1~8.
[9]蔡杰.国内氯产品现状与发展趋势分析(上)[J].观察市场. 2012.1:51~53.
[10]田升江.2014年中国聚氯乙烯市场分析及前景展望[J].中国石油和化工经济分析. 2015.8:55~57.
[11]张鑫.我国甲烷氯化物行业现状及发展趋势[J].中国农药. 2011.7:21~28.
[12]屈叶青.环氧氯丙烷的生产技术及国内外市场分析[J].石油化工技术与经济. 2015.31(4): 26~30.
[13] 李玉芳,伍小明.MDI生产技术进展及国内外市场分析[J].上海化工. 2015.40(10):33~38.
[14] 张悦,张宝辉,宗茂森.甲苯二异氰酸酯产品竞争环境分析[J].化学工业. 2014.32(9):16~18.
[15] Van Kijk C P,Schreiner W C.Hydrogen Chlorine to Chlorine via the Kel.Chlor Process. Chemical Engineering Process. 1973(69)4:57~63.
[16] BP1403(1868).H.Deacon.
[17] Henry Deacon.Manufacture of chlorine:US85370,1 868.
[18] Henry Deacon.Improvement in the manufacture of chlorine:US141333.1873.
[19] Henry Deacon.Improvement in the manufacture of chlorine:US165802.1875.
[20] Henry Deacon.Improvement in apparatus for the manufacture of chlorine:US118209.1871.
[21] W.F.Engel, M.J.Waale, Recent Developments in the Oxidative Recovery of Chlorine from Hydrochloric Acid. Chemistry and Industry. Jan.13.1962:76~83.
[22] WillemF.Engel,FreddyWattimena. Process for the production of chlorine:US3210158.1965.
[23] F.Engel,Freddy Wattimena.Catalyst composition,particularly for catalyzing oxidation of hydrogen chloride to chlorine: US3260678,1996.
[24] Alphonsus M. Alkemade, Johannes H.De Groot. Hydrochloric acid recovery: US3242647.1966.
[25] 西田洋之,阿部川宏明.氯的制造方法:CN1145328.1997.
[26] 阿部川宏明,伊藤祯昭,日比卓男.氯的生产方法:CN1176223.1998.
[27] 铃田哲也,石野胜,岩永清司.制备氯气的方法:CN1201013.1998.
[28] 郭杨龙,孙宇,卢冠忠,等. 用于氯化氢催化氧化制氯气的铜基催化剂及其制备方法和应用:CN104923239.2015.
[29] R.C. Minet, S.W. Benson, and T.T. Tsotsis. Recovery of chlorinr from hydrogen chloride by carrier catalyst process:US4994265.1991.
[30] 韩明汉,魏飞,金涌,等.氯化氢催化氧化生产氯气的工艺方法及装置:CN1417107.2003.
[31] 张钧钧.氯化氢催化氧化制氯气技术进展[J].中国氯碱. 2013,5:6~10.
[32] 魏飞,陈智涛,韩明汉.一种氯化氢催化氧化生产氯气的装置及方法:CN101293637.2008.
[33] O.瓦森伯格,D.阿加尔,C.W.里克,等.氯的制备:CN1156121.1996.
[34] 乔旭,陈献,戴勇,等.一种流化床与绝热固定床串联的HCl氧化反应工艺及系统: CN104030247.2014.
[35] 时钧,汪家鼎,金国综,等.化学工程手册,第2版[M].北京:化学工业出版社, 1996. 25~69.
[36] 金涌,祝京旭,汪展文,等.流态化工程原理[M].北京:清华大学出版社, 2001.334.
[37] 恽松,骞伟中,魏飞.流化床与固定床耦合反应器中的颗粒磨损[J].过程工程学报. 2010.10(1):17~22.
[38] 陈斌,罗务习,孙鲲鹏,等. 一种采用微反应器进行氯化氢氧化制备氯气的方法: CN102101650.2011.
[39] 陈斌,罗务习,张宏科,等.一种利用磁稳流化床进行氯化氢氧化制备氯气的方法: CN103145099.2013.
[40] 孙策,马斌全,缭晖,等.氯化氢催化氧化制氯气的催化剂及其制备方法和应用:CN105289631.2015.
[41] 王农跃,瞿雄伟,李国华,赵全忠,邵建明,闻国强. 一种二(三氯甲基)苯和二(氯甲酰基)苯的制备方法: CN104447188.2013.
[42] 王农跃,瞿雄伟,李国华,赵全忠,邵建明,闻国强.一种三氯甲基取代苯的制备方:WO2015/035937.
[43] 俞志宏,王明亮.氯化氢综合利用现状及展望[J],化工时刊,2012,26(8):56~58.
(R-03)
可吸收纳米复合人工骨材料研究获进展
2016年8月,中国科学院长春应用化学研究所牵头承担的“可吸收纳米复合人工骨材料与器件的产业化关键技术研究”项目顺利通过由省科技厅组织的专家验收。该项目是吉林省“双十工程”重大科技攻关项目,专家组一致认为该项目在可吸收纳米复合人工骨材料方面的研究达到了国内领先水平,并建议进一步加快产品的临床应用和商业化进程,拓宽其应用领域。
该项目通过科研人员的不懈努力,圆满完成了从可降解原材料合成到自主开发可吸收纳米复合人工骨材料的研究任务,获得了系列具有自主知识产权的产业化关键技术,可指导规模化生产。该人工骨材料具有完全人工合成、降解时间可调以及具有骨传导和诱导作用等诸多特点,其物理化学性能和生物学性能等技术指标均达到任务合同要求。
该项目取得的突出进展体现在,从系列生物医用高分子材料PLGA原料的合成和制备出发,实现了LA与GA比例可控,降解时间可调;完成了LA/GA单体的开环聚合和批量制备,PLGA的纯度达到医用级要求;实现了公斤级聚乳酸改性纳米羟基磷灰石(g-HA)原料的合成和制备;聚乳酸接枝率(质量百分比)可控,纯度达到医用级要求;开发了多种骨支架的制备方法和工艺,制备出了系列不同孔结构、孔隙率和孔径的人工骨支架,孔隙率、孔尺寸与降解速度均可根据骨愈合需要进行调整;完成了支架材料和产品的物理/化学性能评价,以及生物学检测和动物实验,获得了人工骨材料的组分、结构、机械性能等重要参数;实现了骨愈合过程中材料的实时成像追踪;制备了与几丁质、胶原等材料具有特异性结合能力的活性生长因子蛋白;创造性地实现了高强度可注射骨支架的制备,可更好地满足临床骨科缺损的微创治疗。
在该项目执行期间,长春应化所与吉林大学骨科成立了联合共建的“骨科生物材料工程研究中心”,进一步为骨科材料基础与临床的合作研究和完善“产学研”开发体系提供了有力保障。
该项目获得了一系列重要成果。其中,获得人工骨支架新产品1个,新建《可吸收人工骨》产品企业标准1项;申请专利6项,授权专利5项,在Biomacromolecules 等学术刊物发表论文9篇;并获得可吸收钉板等配套器件产品注册证2个(国械注准20153461863和国械注准20153461864)。
摘编自“中国聚合物网”
Chlorine cleaning process for recovering hydrogen chloride from tail gas in preparation of aromatic polyamide fi ber
Chlorine cleaning process for recovering hydrogen chloride from tail gas in preparation of aromatic polyamide fi ber
Wang Nongyue
(Shanghai Fanglun New Material Technology Co., LTD., Shanghai200122, China)
This paper expounds the hydrogen chloride pollution situation, and more by-product hydrogen chloride with the development of organic chlorine products. In this paper, the existing treatment methods and characteristics of hydrogen chloride in the production of aramid fi ber are introduced. This paper mainly introduces the clean process of catalytic oxidation of hydrogen chloride to chlorine gas which has the most industrialized foreground. By comparing the process, the advantages and development prospects of hydrogen chloride oxidation process by Shanghai Fanglun are analyzed in this paper.
hydrogen chloride; catalytic oxidation; chlorine gas
TQ124.42
1009-797X(2016)18-0020-09
BDOI:10.13520/j.cnki.rpte.2016.18.005
王农跃(1958-),男,教授级高工,工学博士,管理学博士,荣获多项省部级科技进步一等奖及多项国家发明专利,发表多篇论文及著作。
2016-08-02

