双氧水和pH值对可降解挤压态Mg-0.5Sr合金腐蚀行为的影响*
赵朝勇,潘复生,2,3,张 磊,汤爱涛,2
(1.重庆大学 材料科学与工程学院,重庆 400044; 2.重庆大学 国家镁合金工程材料研究中心,重庆 400044; 3.重庆科学技术研究院,重庆 401123 )
双氧水和pH值对可降解挤压态Mg-0.5Sr合金腐蚀行为的影响*
赵朝勇1,潘复生1,2,3,张磊1,汤爱涛1,2
(1.重庆大学 材料科学与工程学院,重庆 400044; 2.重庆大学 国家镁合金工程材料研究中心,重庆 400044; 3.重庆科学技术研究院,重庆 401123 )
模拟骨科植入材料植入体内时的生理环境,采用浸泡测试、动电极化测试和电化学阻抗测试研究了模拟生理环境中双氧水浓度和pH值变化对可降解挤压态Mg-0.5Sr合金腐蚀行为的影响。结果表明,在不同pH值(7.4和5.2)的Hank 溶液中添加H2O2促进腐蚀反应,增加H2O2浓度进一步加速腐蚀。降低pH值不仅导致镁合金腐蚀速率增加,而且改变了镁合金的腐蚀机理。结果表明模拟植入时的生理环境加速了镁合金植入体的腐蚀,该研究为可降解镁合金骨科植入体的设计、选择和临床应用提供了重要的信息。
镁合金;腐蚀;可降解植入体;双氧水;pH值
0 引 言
由于具有良好的力学性能和生物相容性,特别是在生理环境中的可降解性,镁合金被考虑用作潜在的可降解骨科植入材料[1-6]。现已认为镁合金的降解过程不仅依赖于其元素组成和加工历史,而且依赖于实际的腐蚀环境[7]。因此,在更接近于人体生理环境中研究镁合金的腐蚀行为对其临床使用将具有重要的意义。
人体血液和体液的正常pH值为7.35~7.45。然而,当植入体植入硬组织时,其pH值降低到大约5.2,并在两周内恢复到7.4[8]。同时,植入体植入体内之后将会引起炎性反应,在炎性反应期间,炎性细胞将会释放双氧水(H2O2)[9]。尽管有少量的报道表明模拟体液pH值的变化对镁及其合金的腐蚀行为有明显的影响[10-11]。然而,炎性反应释放的双氧水对镁合金体外腐蚀行为的影响还不清楚。镁合金在模拟植入体内后体液pH值的变化和H2O2浓度对其腐蚀行为的影响还有待研究。
最近,铸态和轧制态Mg-Sr合金被研究用作骨科植入材料,体内外实验表明Mg-Sr合金表现出良好的生物学性能,有潜力用作骨科植入体[12-13]。然而,铸态和轧制态Mg-Sr的力学性能特别是延伸率较差[12-13]。针对这种情况,开发出了1种新的具有良好强度和韧性的挤压态Mg-0.5Sr合金(拉伸屈服强度为205.8 MPa,最大抗拉强度为245.3 MPa,延伸率为16.8%)。本文的目的是研究模拟体液中不同的pH值和H2O2浓度对可降解挤压态Mg-0.5Sr合金体外生物腐蚀性能的影响,并阐明该合金在模拟植入生理环境中的体外降解机理。
1 实 验
1.1实验材料及表征
实验用的材料为含有0.5%(质量分数)Sr的挤压态Mg-0.5Sr合金。所有经过线切割加工的样品用SiC砂纸逐级打磨至1000#,然后放入无水乙醇中用超声波清洗,并用冷风吹干备用。用X射线衍射仪(XRD,Rigaku D/MAX-2500PC)检测挤压态Mg-0.5Sr合金的相组成。样品经苦味酸和冰醋酸混合溶液腐蚀后,用金相显微镜观察合金的金相组织;经硝酸水溶液腐蚀后,用扫描电子显微镜(SEM,TESCAN VEGA II LMU)来观察合金中的第二相。
1.2腐蚀介质的种类及配制
采用浸泡测试和电化学测试来研究挤压态Mg-0.5Sr合金的在模拟体液中的体外腐蚀行为。腐蚀介质采用Hank溶液,它为平衡盐溶液,是模拟体液中的1种,其组成见文献[14]。Hank溶液的pH值保持在人体的生理pH值为7.4。用1 mol/L的稀盐酸将Hank溶液的pH值调整到5.2来模拟植入后体液的pH值。向不同pH值(pH值为7.4和5.2)的Hank溶液中分别加入10和100 mmol/L的H2O2溶液(H2O2的质量分数为30%)来模拟炎性反应期间炎性细胞释放的H2O2。在本文中共使用6种不同的溶液,即pH值为7.4,pH值为7.4+10 mmol/L H2O2,pH值为7.4+100 mmol/L H2O2,pH值为5.2,pH值为5.2+10 mmol/L H2O2,pH值为5.2+100 mmol/L H2O2。
1.3浸泡测试
对于浸泡测试,根据ASTM-G31-72标准,按样品表面积∶溶液体积=1 cm2∶20 mL进行浸泡测试[15]。将10 mm×10 mm×2 mm的样品分别浸泡在上述的6种溶液中,整个浸泡测试在37℃的恒温水浴中进行,浸泡时间为2周。到达设定的浸泡时间后,从浸泡液中取出样品,用蒸馏水冲洗,然后用冷风吹干。用SEM和XRD表征浸泡后样品的表面形貌和化学组成变化。
1.4电化学测试
使用三电极体系在上述的6种溶液中进行电化学测试,其中饱和甘汞电极作为参比电极,铂金片作为对电极,样品作为工作电极。暴露在模拟体液中的工作电极面积为1.13 cm2。使用Gamry Reference 600电化学工作站进行动电极化测试和电化学阻抗测试。在进行动电极化测试之前,将样品分别在上述的6种溶液中浸泡30 min,在相对于开路电压-300 mV作为初始电位开始以1 mV/s的扫描速率进行测试,测试终止于相对于开路电压300 mV。运用Tafel外延法从动电极化曲线中获得腐蚀电流密度(icorr,mA/cm2)[16]。根据下面的公式将腐蚀电流密度换算成平均腐蚀速率(Ri,mm/year)[16-17]
Ri=22.85icorr
电化学阻抗(EIS)测试在开路电压下以10 mV的扰动信号进行,测试的频率范围为10 mHz~100 kHz。
2 结果与讨论
2.1表面形貌和成分表征
图1为挤压态Mg-0.5Sr合金的金相照片。从图1可以看出,挤压态Mg-0.5Sr合金的金相组织为细小的等轴晶,这表明该合金在挤压时发生了完全动态再结晶[18]。

图1 挤压态Mg-0.5Sr合金的光镜图
Fig 1 Optical micrograph of as-extruded Mg-0.5Sr alloy
图2为挤压态Mg-0.5Sr合金的XRD图谱及SEM图。从图2可以看出挤压态Mg-0.5Sr合金由α-Mg 和Mg17Sr2相组成,这是由于锶在镁中的固溶度较低(最大固溶度约0.11%,质量分数)引起的[13]。

图2 挤压态Mg-0.5Sr合金的XRD图谱及SEM图
Fig 2 XRD pattern and SEM micrographs of as-extruded Mg-0.5Sr alloy
图3为挤压态Mg-0.5Sr合金在不同pH值和H2O2浓度的Hank溶液中测试出的动电极化曲线。
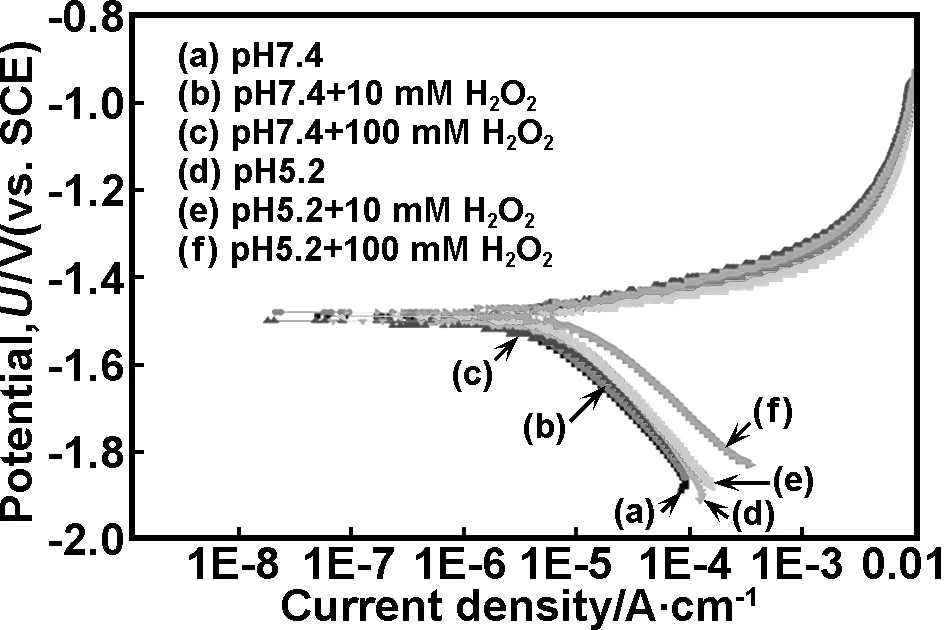
图3挤压态Mg-0.5Sr合金在不同pH值和H2O2浓度的Hank溶液中的动电极化曲线
Fig 3 Potentiodynamic polarization curves of as-extruded Mg-0.5Sr alloy in different solutions
表1列出了从图3获得的各种电化学参数和对应的平均腐蚀速率。从图3和表1可以看出测试的溶液(不同pH值和H2O2浓度的Hank溶液)对合金的耐腐蚀性有很大的影响。随着模拟体液pH值降低,合金的腐蚀电流密度和对应的平均腐蚀速率增加,表明溶液pH值降低使合金的耐腐蚀降低,这与以前文献的报道一致[10-11]。当在不同pH值的溶液中加入H2O2时,合金的腐蚀电流密度和对应的平均腐蚀速率增加,并且随着H2O2加入量的增加而增大,表明溶液中H2O2的加入对合金的的耐腐蚀性是不利的。由图3和表1可以判定挤压态Mg-0.5Sr合金在不同溶液中的耐腐蚀性由高到低为:pH值7.4>pH值7.4+10 mmol/L H2O2>pH值7.4+100 mmol/L H2O2>pH值5.2>pH值5.2+10 mmol/L H2O2>pH值5.2+100 mmol/L H2O2。
表1从动电极化曲线获得的挤压态Mg-0.5Sr合金的电化学参数和平均腐蚀速率
Table 1 Electrochemical parameters and the average corrosion rate of as-extruded Mg-0.5Sr alloy obtained frompotentiodynamic polarization curves
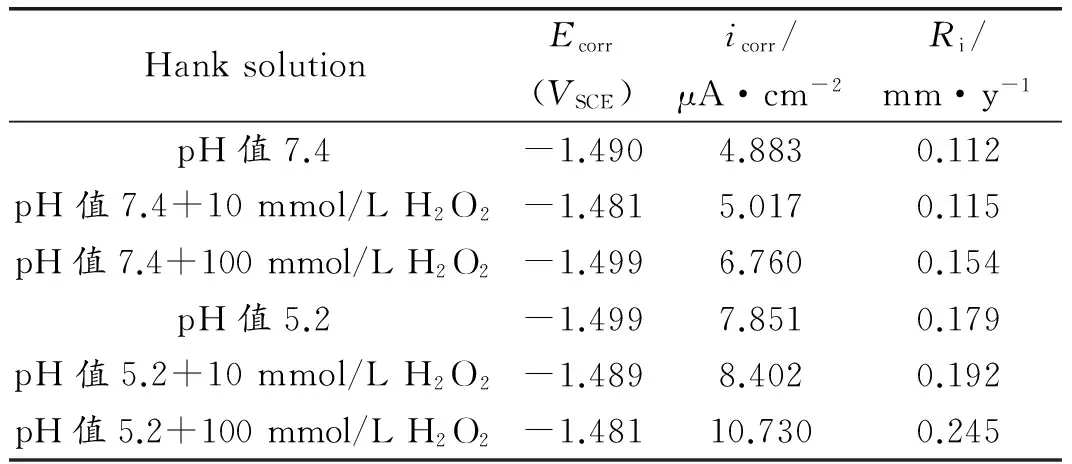
HanksolutionEcorr(VSCE)icorr/μA·cm-2Ri/mm·y-1pH值7.4-1.4904.8830.112pH值7.4+10mmol/LH2O2-1.4815.0170.115pH值7.4+100mmol/LH2O2-1.4996.7600.154pH值5.2-1.4997.8510.179pH值5.2+10mmol/LH2O2-1.4898.4020.192pH值5.2+100mmol/LH2O2-1.48110.7300.245
图4为挤压态Mg-0.5Sr合金在不同pH值和H2O2浓度的Hank溶液中的电化学阻抗图。从奈奎斯特图(Nyquist图)可以看出,合金在同一个pH值(pH值为7.4或5.2)的溶液中测试时,不论含有10或100 mmol/L的H2O2,或者不含有H2O2,它们具有类似的曲线形状,即pH值7.4时,其Nyquist图都由一个高中频的容抗弧和一个低频的诱导弧组成;而pH值5.2时,其Nyquist图都由一个高频的容抗弧,一个中频的容抗弧和一个低频的诱导弧组成。区别在于加入不同浓度的H2O2后弧的直径不同。这表明合金在同一个pH值(pH值为7.4或5.2),且含有不同浓度的H2O2或不含H2O2的溶液中具有相同的腐蚀机理,但是腐蚀速率不同[19]。另一方面,合金在不同pH值(pH值为7.4或5.2)的Nyquist图不仅弧的直径不同,而且曲线的形状不同。这表明合金在不同pH值不仅腐蚀速率不同,而且腐蚀机理不同[20]。据报道高频的容抗弧通常归因于电荷转移阻抗(Rct)和在金属/溶液界面处的双电层容抗,中频的容抗弧归因于合金表面的氧化物薄膜和表面薄膜阻抗(Rf)[21]。在低频区的诱导弧通常认为与亚稳态镁离子的出现或发生点蚀有关[22]。大量的文献表明材料的耐腐蚀性与容抗弧的直径成正比,容抗弧的直径越大,材料的耐腐蚀性越好[22-26]。因此,挤压态Mg-0.5Sr合金在不同pH值和H2O2浓度的溶液中的耐腐蚀性顺序由高到低为:pH值7.4>pH值7.4+10 mmol/L H2O2>pH值7.4+100 mmol/L H2O2>pH值5.2>pH值5.2+10 mmol/L H2O2>pH值5.2+100 mmol/L H2O2。
从波特图(Bode图)中的阻抗模-频率图(Zmod vs.频率图)可见,合金在不同pH值和H2O2浓度的溶液中的阻抗值高低顺序为pH值7.4>pH值7.4+10 mmol/L H2O2>pH值7.4+100 mmol/L H2O2>pH值5.2>pH值5.2+10 mmol/L H2O2>pH值5.2+100 mmol/L H2O2。在Bode图的相位角-频率图(Degree vs频率图)中,合金在pH值7.4并含有不同浓度的H2O2的Hank溶液中测试时具有一个波峰和一个波谷,表明出现了一个容抗弧和一个诱导弧。然而,在pH值为5.2并含有不同浓度的H2O2的Hank溶液中测试时具有两个波峰和一个波谷,表明出现了两个容抗弧和一个诱导弧。
因此,EIS结果表明挤压态Mg-0.5Sr合金在不同的pH值和H2O2浓度的Hank溶液中的耐腐蚀性按照如下的顺序递减:pH值7.4>pH值7.4+10 mmol/L H2O2>pH值7.4+100 mmol/L H2O2>pH值5.2>pH值5.2+10 mmol/L H2O2>pH值5.2+100 mmol/L H2O2,这与极化曲线的结果一致。由此可见,改变溶液的pH值(从pH值7.4降低到5.2)改变了合金的腐蚀机理,而在不同pH值(pH值7.4或5.2)的溶液中添加不同浓度的H2O2(10或100 mmol/L)仅仅改变合金的腐蚀速率,不改变合金的腐蚀机理。模拟体液中H2O2的加入加快了镁合金的腐蚀,并且随着加入的H2O2浓度的增加,合金的腐蚀速率相应增加。
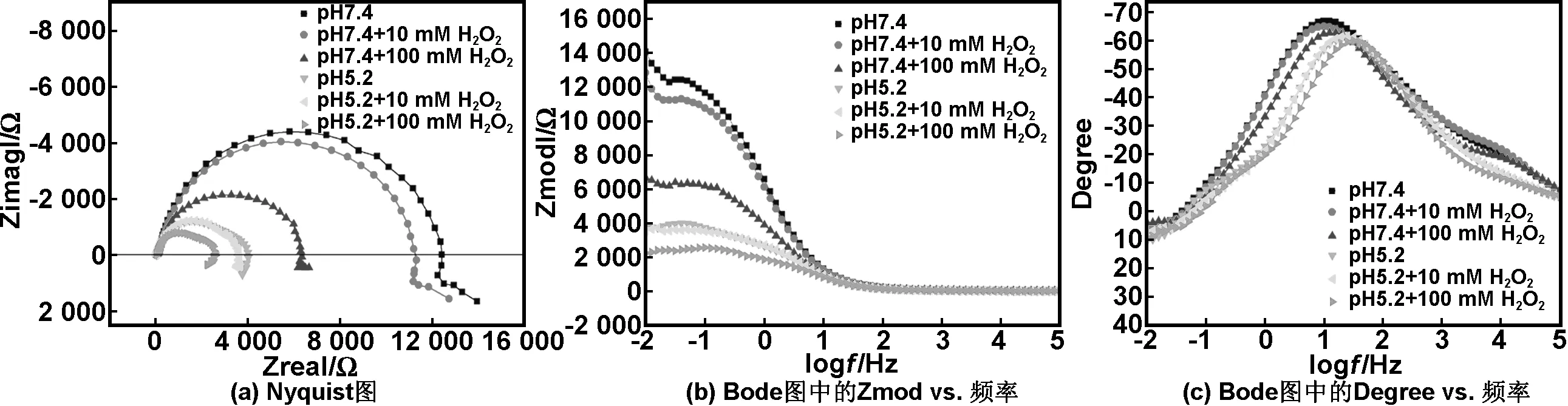
图4挤压态Mg-0.5Sr合金在不同溶液中的电化学阻抗图
Fig 4 EIS spectra of as-extruded Mg-0.5Sr alloy in different solutions
图5为挤压态Mg-0.5Sr合金在不同pH值和H2O2浓度的Hank溶液中浸泡2周后的表面形貌图。从图5可以看出合金在pH值7.4的Hank溶液浸泡2周后,其表面较为致密、光滑,并且有少量的局部腐蚀点。然而,在pH值5.2的Hank溶液浸泡2周后,其表面较为疏松和粗糙,可见大量明显的裂缝和一些脱落的腐蚀产物。当浸泡在pH值5.2的Hank溶液中时,挤压态Mg-0.5Sr合金在低pH值溶液中浸泡的初始阶段具有高的腐蚀速率[11]。高的腐蚀速率使得样品表面具有比溶液中更高的局部pH值[11]。当局部pH值达到一定值时,开始发生Mg(OH)2和一些磷酸盐的沉积,这些沉积物在短期内将延缓合金的腐蚀[11]。图6的XRD图谱证实了Mg(OH)2的存在。图4中挤压态Mg-0.5Sr合金在pH值 5.2的Hank溶液中测试的Nyquist图中的第二个容抗弧可能归因于Mg(OH)2的存在。当浸泡在pH值7.4的Hank溶液中时,合金在相对高的pH值的溶液中具有相对低的腐蚀速率,这表明需要更长的时间使得样品表面的局部pH值才能达到Mg(OH)2的沉积,这就使得点蚀发生[11]。因此,合金在pH值7.4的Hank溶液中浸泡时具有比在pH值5.2的溶液中具有更多的腐蚀点。随着浸泡时间的增加,Hank溶液中的Cl-使Mg(OH)2发生溶解[1]。由于腐蚀产物弱的减缓腐蚀的作用,合金中的第二相Mg17Sr2相作为阴极,α-Mg作为阳极形成微电偶的电偶腐蚀效应加速了α-Mg的腐蚀[12-13,27]。

图5挤压态Mg-0.5Sr合金在不同溶液中浸泡2周后的表面形貌
Fig 5 Surface morphologies of as-extruded Mg-0.5Sr alloy after immersion in different solutions for 2 weeks
图6挤压态Mg-0.5Sr合金在不同溶液中浸泡2周后的XRD图
Fig 6 XRD patterns of as-extruded Mg-0.5Sr alloy after immersion in different solutions for 2 weeks
当在不同pH值的Hank溶液中加入不同浓度的H2O2时,可以看出随着H2O2加入量的增加,合金表面腐蚀越来越严重,并形成了更多的腐蚀产物(图5(c)-(f))。相比较而言,合金在pH值5.2,含有不同浓度的H2O2的Hank溶液中腐蚀更严重。合金在pH值5.2,并含有不同浓度H2O2的Hank溶液中浸泡时,也在样品表面的XRD图谱(图6)中观察到了Mg(OH)2的衍射峰。Nyquist图中的第二个容抗弧可能也归因于Mg(OH)2的存在。当在模拟体液中加入不同浓度的H2O2时,由于H2O2是1种中强氧化剂,它与镁可能发生如下反应
Mg+H2O2=Mg(OH)2
由于Mg(OH)2较弱的防腐能力,它很快被模拟溶液中的氯离子溶解[1],这也可能就是随着溶液中H2O2浓度的增加,镁合金耐腐蚀性降低的原因。浸泡测试的结果与动电极化测试和电化学阻抗测试的结果一致。
3 结 论
(1)挤压态Mg-0.5Sr合金在模拟体液中的耐腐蚀性显著地受到溶液pH值和H2O2浓度的影响。
(2)pH值的降低和H2O2的加入均加快了镁合金的腐蚀,并且在不同pH值时,合金的耐腐蚀性均随着H2O2浓度的增加而增加。pH值的降低改变了镁合金的腐蚀机理,而H2O2的加入仅仅起加快镁合金腐蚀的作用。
[1]Staiger M P,Pietak A M,Huadmai J,et al.Magnesium and its alloys as orthopedic biomaterials:a review [J].Biomaterials,2006,27(9):1728-1734.
[2]Li N,Zheng Y.Novel magnesium alloys developed for biomedical application:a review [J].Journal of Materials Science & Technology,2013,29(6):489-502.
[3]Li Tao,Zhang Hailong,He Yong,et al.Research progress in biomedical magnesium alloys [J].Journal of Functional Materials,2013,44(20):2913-2918.
李涛,张海龙,何勇,等.生物医用镁合金研究进展[J].功能材料,2013;44(20):2913-2918.
[4]Zheng Yufeng,Gu Xuenan,Li Nan,et al.Development and prospects of biodegradable magnesium alloys [J].Materials China,2011,30(4):30-43.
郑玉峰,顾雪楠,李楠,等.生物可降解镁合金的发展现状与展望 [J].中国材料进展,2011;30(4):30-43.
[5]Witte F,Hort N,Vogt C,et al.Degradable biomaterials based on magnesium corrosion [J].Current Opinion in Solid State and Materials Science,2008,12(5):63-72.
[6]Yuan Guangyin,Zhang Jia,Ding Wenjiang.Research progress of Mg-based alloys as degradable biomedical materials [J].Materials China,2011,30(2):44-50.
袁广银,张佳,丁文江.可降解医用镁基生物材料的研究进展 [J].中国材料进展,2011;30(2):44-50.
[7]Witte F,Fischer J,Nellesen J,et al.In vitro and in vivo corrosion measurements of magnesium alloys [J].Biomaterials,2006,27(7):1013-1018.
[8]Liu X,Chu P K,Ding C.Surface modification of titanium,titanium alloys,and related materials for biomedical applications [J].Materials Science and Engineering:R:Reports,2004,47(3):49-121.
[9]Tengvall P,Lundström I,Sjöqvist L,et al.Titanium-hydrogen peroxide interaction:model studies of the influence of the inflammatory response on titanium implants [J].Biomaterials,1989,10(3):166-175.
[10]Ng W,Chiu K,Cheng F.Effect of pH on the in vitro corrosion rate of magnesium degradable implant material [J].Materials Science and Engineering:C,2010,30(6):898-903.
[11]Liu C,Xin Y,Tian X,et al.Degradation susceptibility of surgical magnesium alloy in artificial biological fluid containing albumin [J].Journal of Materials Research,2007,22(7):1806-1814.
[12]Brar H S,Wong J,Manuel M V.Investigation of the mechanical and degradation properties of Mg-Sr and Mg-Zn-Sr alloys for use as potential biodegradable implant materials [J].Journal of the Mechanical Behavior of Biomedical Materials,2012,7:87-95.
[13]Gu X,Xie X,Li N,et al.In vitro and in vivo studies on a Mg-Sr binary alloy system developed as a new kind of biodegradable metal [J].Acta Biomaterialia,2012,8(6):2360-2374.
[14]Zhang E,Yin D,Xu L,et al.Microstructure,mechanical and corrosion properties and biocompatibility of Mg-Zn-Mn alloys for biomedical application [J].Materials Science and Engineering:C,2009,29(3):987-993.
[15]ASTM-G31-72:standard practice for laboratory immersion corrosion testing of metals.Annual book of ASTM standards,philadelphia,pennsylvania[D].USA:American Society for Testing and Materials,2004.
[16]Shi Z,Liu M,Atrens A.Measurement of the corrosion rate of magnesium alloys using Tafel extrapolation [J].Corrosion Science,2010,52:579-588.
[17]Cai S,Lei T,Li N,et al.Effects of Zn on microstructure,mechanical properties and corrosion behavior of Mg-Zn alloys [J].Materials Science and Engineering:C,2012,32(8):2570-2577.
[18]Zhang X,Yuan G,Niu J,et al.Microstructure,mechanical properties,biocorrosion behavior,and cytotoxicity of as-extruded Mg-Nd-Zn-Zr alloy with different extrusion ratios [J].Journal of the Mechanical Behavior of Biomedical Materials,2012,9:153-162.
[19]Zhang X,Yuan G,Mao L,et al.Biocorrosion properties of as-extruded Mg-Nd-Zn-Zr alloy compared with commercial AZ31 and WE43 alloys [J].Materials Letters,2012,66:209-211.
[20]He W,Zhang E,Yang K.Effect of Y on the bio-corrosion behavior of extruded Mg-Zn-Mn alloy in Hank's solution [J].Materials Science and Engineering C,2010,30:167-174.
[21]He M,Liu L,Wu Y,et al.Corrosion properties of surface-modified AZ91D magnesium alloy [J].Corrosion Science,2008,50:3267-3273.
[22]Bobby Kannan M,Singh R.A mechanistic study of in vitro degradation of magnesium alloy using electrochemical techniques [J].Journal of Biomedical Materials Research Part A,2010,93(3):1050-1055.
[23]Pebere N,Riera C,Dabosi F.Investigation of magnesium corrosion in aerated sodium sulfate solution by electrochemical impedance spectroscopy [J].Electrochimica Acta,1990,35(2):555-561.
[24]Zucchi F,Grassi V,Frignani A,et al.Electrochemical behaviour of a magnesium alloy containing rare earth elements [J].Journal of Applied Electrochemistry,2006,36(2):195-204.
[25]Peng Feifei,Kang Feng,Shu Dayu,et al.Research in the application of cryogenic treatment on the stainless steel and aluminum alloy[J].Journal of Chongqing University of Technology(Natural Science),2014,(10):56-59.
彭菲菲,康凤,舒大禹,等.深冷处理技术在不锈钢及铝合金中的应用[J].重庆理工大学学报(自然科学版),2014,(10):56-59.
[26]Baril G,Pebere N.The corrosion of pure magnesium in aerated and deaerated sodium sulphate solutions [J].Corrosion Science,2001,43(3):471-484.
[27]Bornapour M,Muja N,Shum-Tim D,et al.Biocompatibility and biodegradability of Mg-Sr alloys:the formation of Sr-substituted hydroxyapatite [J].Acta Biomaterialia,2013,9(2):5319-5330.
Effects of hydrogen peroxide and pH on corrosion behavior of a biodegradable as-extruded Mg-0.5Sr alloy
ZHAO Chaoyong1,PAN Fusheng1,2,3,ZHANG Lei1,TANG Aitao1,2
(1.College of Materials Science and Engineering,Chongqing University,Chongqing 400044,China; 2.National Engineering Research Center for Magnesium Alloys,Chongqing University, Chongqing 400044,China; 3.Chongqing Academy of Science and Technology,Chongqing 401123,China)
A simulated physiological environment after implantation was used,and the effects of H2O2and pH on the corrosion behavior of a biodegradable as-extruded Mg-0.5Sr alloy in Hank’s solution were investigated by using immersion test,potentiodynamic polarization test and electrochemical impedance spectroscopy test.The results showed that the addition of H2O2in Hank’s solution with different pH(7.4 and 5.2)promoted the corrosion reaction,and a higher H2O2concentration further accelerated the corrosion reaction.The lower pH not only resulted in a higher corrosion rate of magnesium alloy,but also changed its corrosion mechanism.The present investigation indicated that the simulated physiological environment after implantation accelerated the corrosion of magnesium alloy implants,which provided us some important information about design,selection and clinic use of biodegradable magnesium alloy orthopedic implants.
corrosion; magnesium alloy; biodegradable implant; H2O2; pH value
1001-9731(2016)09-09117-05
国家科技支撑计划资助项目(2012BAF09B04)
2015-07-21
2016-04-22 通讯作者:潘复生,E-mail:fspan@cqu.edu.cn
赵朝勇(1982-),男,四川南充人,博士后,合作导师潘复生教授,从事生物医用镁合金研究。
TB34;R318
ADOI:10.3969/j.issn.1001-9731.2016.09.022

