1-苄基-4-羟甲基-1H-1,2,3-三氮唑溶解度的测定及关联
沈 乐, 李惠萍, 高江涛, 李焕新
1-苄基-4-羟甲基-1H-1,2,3-三氮唑溶解度的测定及关联
沈 乐, 李惠萍, 高江涛, 李焕新
(郑州大学 化工与能源学院, 河南 郑州 450001)
设计并组装了用动态法测定固体在液体中溶解度的试验装置,采用激光监视技术常压下测定281.15~315.75 K下1-苄基-4-羟甲基-1H-1,2,3-三氮唑在甲苯、四氢呋喃、丙酮、乙酸乙酯、三氯甲烷、二氯甲烷中的溶解度数据。实验数据表明,1-苄基-4-羟甲基-1H-1,2,3-三氮唑在六种溶剂中的溶解度均随温度的升高而增大,且在。采用van’t Hoff方程、Apelblat方程以及方程关联了溶解度数据,所得平均相对偏差分别为1.23%、1.11%、1.00%,结果表明,van’t Hoff方程、Apelblat方程和方程在所研究的温度范围内都是适用的,且方程要优于van’t Hoff方程和Apelblat方程。上述结果可为1-苄基-4-羟甲基-1H-1,2,3-三氮唑的萃取及结晶过程中溶剂的选择提供基础数据。
溶解度;1-苄基-4-羟甲基-1H-1,2,3-三氮唑;溶解度模型;激光监测技术
1 前 言
1,2,3-三氮唑及其衍生物是一类被广泛应用于工业、农业、制药以及高分子材料等领域的五元氮杂环化合物[1~5]。1-苄基-4-羟甲基-1H-1,2,3-三氮唑(BHMT)为白色针状晶体,结构式为:C10H11N3O,其醇羟基可以被卤素及其它亲核试剂取代生成三氮唑醚、多核唑以及配体等[6~13]。
目前,关于BHMT的合成已有研究[14,15],但还没有关于其纯化方法及溶解度的相关报道。在化工生产及理论研究中涉及到的重结晶过程被认为是获得高纯度产物最有效的方法之一,为了纯化BHMT,以及在生产过程中将产物从反应液中萃取出来,有必要取得BHMT在各类有机溶液中的溶解度数据,为此,本文采用动态法常压下测定了温度范围为281.15~315.75 K下BHMT在甲苯、四氢呋喃、丙酮、乙酸乙酯、三氯甲烷、二氯甲烷中的溶解度数据,并用van’t Hoff方程、Apelblat方程,方程对实验数据进行了关联。本研究为BHMT制备过程中溶剂的选择、萃取剂的选择以及分离纯化过程提供热力学基础数据。
2 实 验
2.1 实验原料
1-苄基-4-羟甲基-1H-1,2,3-三氮唑(BHMT)为实验室自制,经高效液相色谱(Agilent-1100)检测,纯度≥99.0%,甲苯、四氢呋喃、丙酮、乙酸乙酯、三氯甲烷、二氯甲烷均为分析纯试剂,天津科密欧化学试剂有限公司生产。
2.2 溶解度测定方法
溶解度测定的常用方法有平衡法[16,17]与动态法[18~20]。本文采用动态法测定BHMT在溶剂中的溶解度。其核心是一个带夹套的内部容积为100 mL的装有精密温度计、冷凝管和磁力转子的玻璃溶解釜。夹套中通有来自超级恒温槽控温的循环水。测定终点由激光发生器、光电转换器以及光强显示仪组成的激光监视系统来判断,能较好的消除由裸眼观测而带来的偶然误差。
实验开始时,溶剂和溶质经精密分析天平准确称量后加入到溶解釜中,开启磁力搅拌,由超级恒温槽控制体系温度,溶解过程由激光发生器、光电转换器以及光强显示仪组成的激光监视系统来监视。在加热初期,由于大量溶质未溶解,可以较快的升高体系温度,当大部分溶质已溶解时,以0.3 K×h-1的速度缓慢升温到终点,此时所测的体系变为均匀的液相,透过溶解釜的光强达到最大值。记录此时温度计读数即为测量体系的平衡温度。
2.3 实验误差控制及可靠性验证
影响溶解度测定准确性的因素较多,如样品的纯度、称量所用分析天平的精度、温度的测量、溶解终点的判定、测量过程中溶剂的散失以及固-液两相达到相平衡所需的时间,为了准确测量溶解度数据,作者做了如下工作:(1)在实验开始前,对所测样品进行纯化处理,保持样品纯度的一致性,且在真空下干燥24 h;(2)由于所用溶剂为有机溶剂,具有较大的挥发性,因此在每次加料时动作较迅速,同时回流冷凝管中通有冷却水,避免溶剂的挥发;(3)由于固体颗粒较大,如果直接用来测量溶解度,固体颗粒与液体的接触面积较小,固-液两相难以在较短的时间内达到平衡,因此在实验开始前将其充分研磨。为了验证实验方法和测量装置的可靠性,选取氯酸钾-水二元体系作为标准物系[21],测定结果如图1所示。从图1可以看出,实验测定值与文献值符合良好,平均相对偏差小于1%,说明测定溶解度的装置和方法可靠,可用于测定BHMT在相关溶剂中的溶解度。
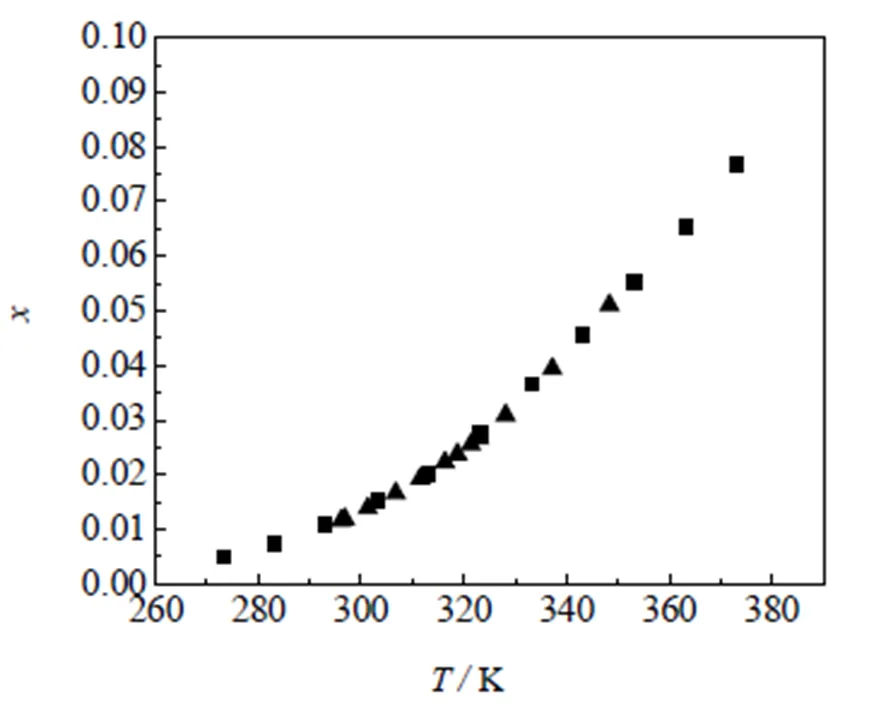
图1 氯酸钾在水中的溶解度
3 结果与讨论
3.1 BHMT溶解度的测定
实验测定了BHMT在甲苯、四氢呋喃、丙酮、乙酸乙酯、三氯甲烷、二氯甲烷中的溶解度数据,实验结果列于表1中。
3.2 溶解度数据的关联
采用van’t Hoff方程(式1)、Apelblat方程(式2)以及方程(式3)对实验数据进行关联。
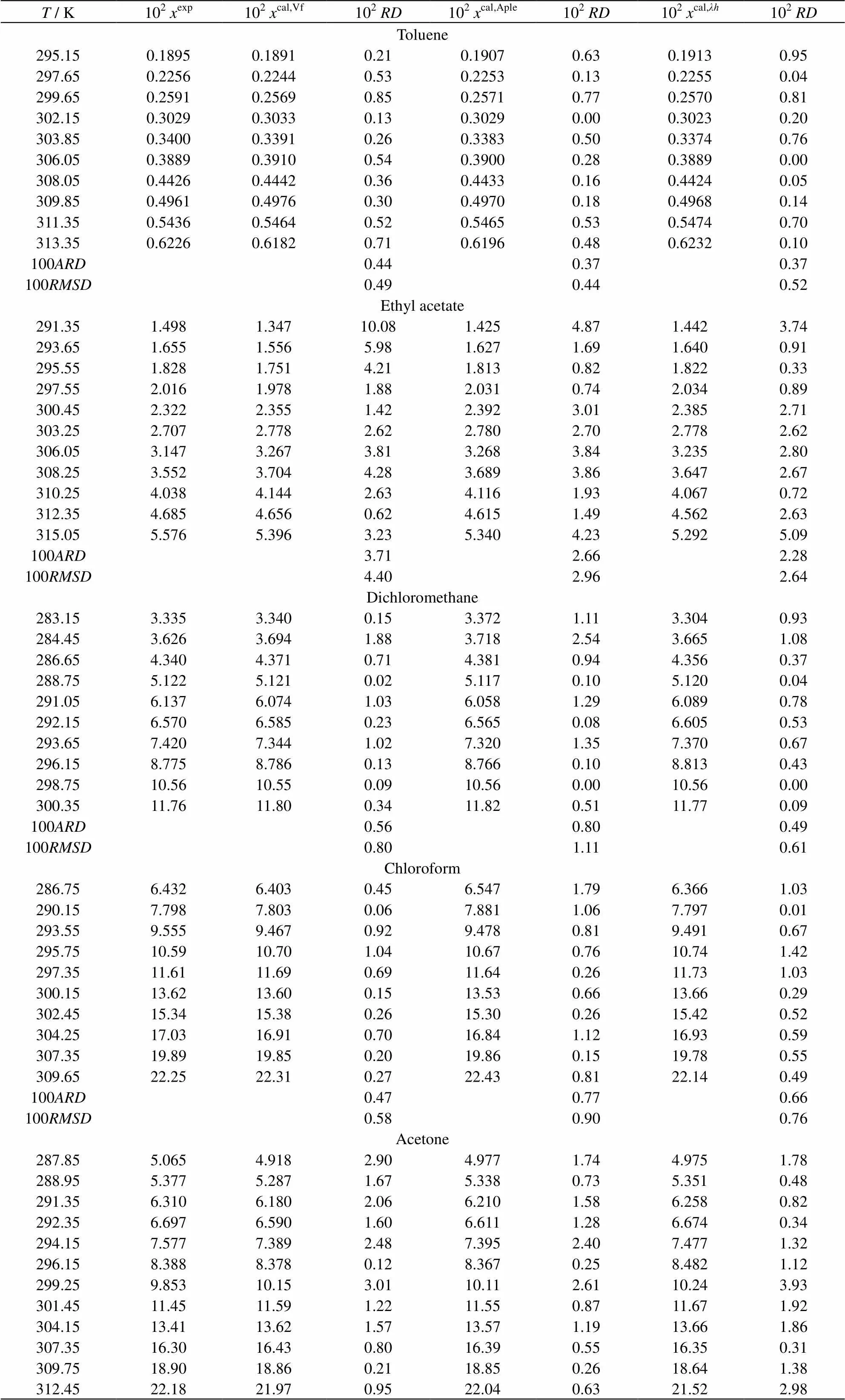
表1 1-苄基-4-羟甲基-1H-1,2,3-三氮唑在不同溶剂中的溶解度及模型关联结果
continued
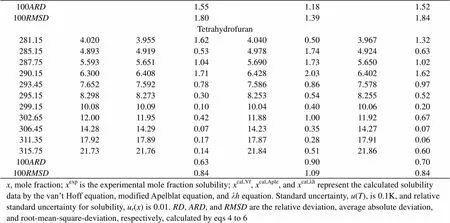
100ARD1.551.181.52 100RMSD1.801.391.84 Tetrahydrofuran 281.154.0203.9551.624.0400.503.9671.32 285.154.8934.9190.534.9781.744.9240.63 287.755.5935.6511.045.6901.735.6501.02 290.156.3006.4081.716.4282.036.4021.62 293.457.6527.5920.787.5860.867.5780.97 295.158.2988.2730.308.2530.548.2550.52 299.1510.0810.090.1010.040.4010.060.20 302.6512.0011.950.4211.881.0011.920.67 306.4514.2814.290.0714.230.3514.270.07 311.3517.9217.890.1717.870.2817.910.06 315.7521.7321.760.1421.840.5121.860.60 100ARD0.630.900.70 100RMSD0.841.090.84 x, mole fraction; xexp is the experimental mole fraction solubility; xcal,Vf, xcal,Aple, and xcal,λh represent the calculated solubility data by the van’t Hoff equation, modified Apelblat equation, and λh equation. Standard uncertainty, u(T), is 0.1K, and relative standard uncertainty for solubility, ur(x) is 0.01. RD, ARD, and RMSD are the relative deviation, average absolute deviation, and root-mean-square-deviation, respectively, calculated by eqs 4 to 6
式中,、、、、、、分别为所对应方程的模型参数,其值列于表2中,式(3)中m为BHMT的熔点,经WRS-1B熔点仪测定,m= 351.85 K。

表2 van’t Hoff方程、Apelblat方程以及λh方程参数的关联结果
分别采用相对偏差、总平均相对偏差和均方根偏差来表示关联方程的拟合效果:
式中,exp和cal分别为溶解度的实验测定值和采用上述模型方程所得的溶解度计算值,结果见表1。其中,cal,Vf、cal,Apel、和cal,分别为van’t Hoff方程、Apelblat方程、方程的溶解度计算值。
从表1中的数据可以得出:BHMT在甲苯、四氢呋喃、丙酮、乙酸乙酯、三氯甲烷、二氯甲烷中的溶解度均随温度的升高而增大,且在甲苯中的溶解质量最小,在丙酮中的溶解质量最大。BHMT在中的溶解度数据用van’t Hoff、Apelblat和方程关联的平均相对偏差均大于甲苯、二氯甲烷、四氢呋喃和三氯甲烷中的平均相对偏差,可能是因为乙酸乙酯、丙酮与BHMT形成了分子间氢键。用van’t Hoff方程关联的总的平均相对偏差和平均均方根偏差分别为1.23%,1.49%;用Apelblat方程关联的总的平均相对偏差和平均均方根偏差分别为1.11%,1.32%;用模型关联的总的平均相对偏差和平均均方根偏差分别为1.00%,1.20%,由此可以看出,van’t Hoff方程、Apelblat方程,方程均能较好地关联BHMT在所研究体系中的溶解度,其中用方程拟合的效果要稍好于van’t Hoff方程和Apelblat方程。总体而言,在实验所测温度范围内,三种模型均能较好的关联BHMT在所选六种溶剂中的溶解度。
4 结 论
(1) 采用激光监视技术在常压下测定了BHMT在甲苯、丙酮、四氢呋喃、乙酸乙酯、二氯甲烷、三氯甲烷中281.15~315.75 K的溶解度数据。
(2) 采用van’t Hoff方程、Apelblat方程,方程对实验数据进行了关联,三种模型方程均能较好地关联BHMT在所研究体系中的溶解度,且λh方程要优于van’t Hoff方程和Apelblat方程。
(3) 本研究为BHMT制备过程中溶剂的选择、萃取剂的选择以及分离提纯提供基础数据。
符号说明:

a, b¾ van’t Hoff方程参数x¾ 溶解度,摩尔分数 A, B, C¾ Apelblat方程参数λ, h¾λh方程参数 ARD¾ 平均相对偏差,%上标 N¾ 实验点数cal¾ 计算值 RD¾ 相对偏差,%exp¾ 实验值 RMSD¾ 均方根偏差,%下标 T¾ 热力学温度,Km¾ 纯物质的熔点,K
[1] Yap A H, Weinreb S M.-Tosylethylazide:a useful synthon for preparation of N-protected 1,2,3-triazoles via click chemistry [J]. Tetrahedron Lett, 2006, 47(18): 3035 -3038.
[2] LONG Jiang (龙江), LI Xue-ping (李雪平), JIN Su-jing (靳苏静),. Synthesis of 4-{[3-(trimethoxysilyl) propoxy]methyl} -1H-1,2,3-triazole (4-{[3-(三甲氧基硅烷基)丙氧基]甲基}-1H-1,2,3-三氮唑的合成) [J]. Fine Chem (精细化工), 2013, 30(2): 217-220.
运用MRI常规序列评估新生儿缺氧缺血性脑损伤的预后研究较少,本研究发现,T1 flair、T2 flair 和SWI图在短期评价其预后方面作用可以优先考虑使用,而中远期价值仍有待于下一步深入研究。
[3] Song M K, Li H P, Li J H,. Tetrazole-based, anhydrous proton exchange membranes for fuel cells [J]. Adv Mater, 2014, 26(8): 1277-1282.
[4] Granados-Focil S, Woudenberg R C, Yavuzceti O,. Water-free proton-conducting polysiloxanes: a study on the effect of heterocycle structure [J]. Macromolecules, 2007, 40(24): 8708-8713.
[5] Dachb I, Rengifo H R, Turro N J,. Cross-linked “matrix-free” nanocomposites from reactive polymer-silica hybrid nanoparticles and functional materials [J]. Macromolecules, 2010, 43(16): 6549-6552.
[6] Maksikova A V, Sukhanov G P, Vereshchagin L I,. Synthesis of triazole and tetrazole ethers [J]. Izv Vyssh Uchebn Zaved, Khim Khim Tekhnol, 1984, 27(2): 172-177.
[7] Vereshchagin L I, Golobokovat V, Pokatilov F A,. The curtius reaction in the synthesis of noncondensed polynuclear azoles [J]. Chem Heterocycl Compd, 2011, 47(4): 456-463.
[8] Golobokova T V, Pokatilov F A, Proidakov A G,. Synthesis of polynuclear azoles linked through carbamate and urea bridges [J]. Russ J Org Chem, 2012, 48(4): 566-574.
[9] Golobokova T V, Pokatilov F A, Proidakov A G,. Synthesis of polynuclear azoles linked by ether tethers [J]. Russ J Org Chem, 2013, 49(1): 130-137.
[10] Barsoum D N, Brassardc J, Deeb J H A,. Synthesis of 5-Iodo-1,2,3-triazoles from organic azides and terminal alkynes: ligand acceleration effect, substrate scope, and mechanistic insights [J]. Synthesis, 2013, 45(17): 2372-2386.
[12] Stefani H A, Canduzini H A, Manarin F. Modular synthesis of mono, di, and tri-1,4-disubstituted-1,2,3-triazoles through copper-mediated alkyne–azide cycloaddition [J]. Tetrahedron Lett, 2011, 52(46): 6086-6090.
[13] Dubrovina N V, Domke L, Shuklov I A,.New mono- and bidentate p-ligands using one-pot click-chemistry: synthesis and application in Rh-catalyzed hydroformylation [J]. Tetrahedron, 2013, 69(41): 8809-8817.
[14] Jlalia I, Beauvineau C, Beauvière S,.Automated synthesis of a 96 product-sized library of triazole derivatives using a solid phase supported copper catalyst [J]. Molecules, 2010, 15(5): 3087-3120.
[15] Shin J A, Lim Y G, Lee K H,. Copper-catalyzed azide-alkyne cycloaddition reaction in water using cyclodextrin as a phase transfer catalyst [J]. J Org Chem, 2012, 77(8): 4117-4122.
[16] JIA Xue-ting (贾雪婷), YANG Yi-chen (杨益辰), LIU Guo-zhu (刘国柱),. Measurement of the solubilities of 2 - ethylanthraquinone and 2-amylanthraquinone in TMB/DIBC mixed solvents and their correlation with thermodynamic equations (2-乙基和2-戊基蒽醌在TMB/DIBC中溶解度的测定与关联) [J]. J Chem Eng of Chinese Univ (高校化学工程学报), 2014, 28(6): 1183-1189.
[17] XU Qing-qing (许青青), SU Bao-gen (苏宝根), CHEN Wei (陈蔚),. Determination, correlation and prediction of solubilities of desmosterol in five organic solvents (链甾醇在五种有机溶剂中溶解度的测定、关联及预测) [J]. J Chem Eng of Chinese Univ (高校化学工程学报), 2014, 28(3): 443-448.
[18] LI Yu-gang (李玉刚), KONG Ling-qi (孔令启), MA Lei (马磊),. Measurement and correlation of the solubilities of isophthaIonitrile in four solvents (间苯二甲腈在四种溶剂中溶解度的测定及关联) [J]. J Chem Eng of Chinese Univ (高校化学工程学报), 2011, 25(3): 390-394.
[19] ZHOU Cai-rong (周彩荣), SHI Xiao-hua (石晓华), FENG Wei (冯伟),. Measurement and correlation of solubilities of neopentyl glycol in solvents (新戊二醇在溶剂中溶解度的测定及关联) [J]. J Chem Eng of Chinese Univ (高校化学工程学报), 2010, 24(3): 365-369.
[20] Wang X M, Qin Y N, Zhang T W,. Measurement and correlation of solubility of azithromycin monohydrate in five pure solvents [J]. J Chem Eng Data, 2014, 59(3), 784-791.
[21] LIU Guang-qi (刘光启), MA Lian-xiang (马连相), LIU Jie (刘杰). Handbook of substances properties data in chemical and engineering (inorganic Vol) (化学化工物性数据手册) (无机卷) [M]. Beijing (北京): Chemical Industry Press (化学工业出版社), 2002.
Measurement and Correlation of 1-Benzyl-4-Hydroxymethyl-1H-1,2,3-Triazole Solubility
SHEN Le, LI Hui-ping, GAO Jiang-tao, LI Huan-xin
(School of Chemical Engineering and Energy, Zhengzhou University, Zhengzhou 450001, China)
The solubility of 1-benzyl-4-hydroxymethyl-1H-1,2,3-triazole (BHMT) in toluene, tetrahydrofuran, acetone, ethyl acetate, chloroform and dichloromethane was measured using a laser monitoring technique within a temperature range between 281.15~315.75 K under atmospheric pressure. The results show that the solubility of BHMT in those selected solvents increases with the increase of temperature but it varies greatly in different solvents. Van’t Hoff equation, modified Apelblat equation andequation were used in data regression and the average relative deviations are 1.23%, 1.11%, 1.00%, respectively. These results indicate that the solubility data can be well correlated by these three models and theequation provides the best fitting result. The experimental results and correlation models can be used as essential data for solvent selection of BHMT extraction and crystallization.
solubility; 1-benzyl-4-hydroxymethyl-1H-1,2,3-triazole; solubility model; laser monitoring observation technique
1003-9015(2016)01-0001-06
O645.12;TQ252.6
A
10.3969/j.issn.1003-9015.2016.01.001
2015-03-11;
2015-05-24。
河南省国际合作项目(104300510009)。
沈乐(1990-),男,湖北武汉人,郑州大学硕士生。通讯联系人:李惠萍,E-mail:huipingli@zzu.edu.cn

