以CO2作为可再生能源储存介质的零碳排放电厂过程模拟
盖少磊,赵 欢,耿秀振,辛斌斌
(沈阳航空航天大学 热能工程研究所,沈阳 110136)
以CO2作为可再生能源储存介质的零碳排放电厂过程模拟
盖少磊,赵欢,耿秀振,辛斌斌
(沈阳航空航天大学 热能工程研究所,沈阳 110136)
利用可再生能源将CO2和H2O转化为液体燃料可应用于零碳排放电厂,形成“可再生能源+CO2+H2O→液体燃料→电力+CO2+H2O”的循环利用模式。CO2和H2O的转化主要有3条路径:CO+H2、CO2+H2以及CO2+H2O,其中CO和H2来自CO2和H2O的电解,液体产物为甲醇。为研究3条转化路径以及零碳排放电厂,利用Aspen Plus进行建模并做热力学分析。结果表明若CO2的转化率高于42%时,电催化转化CO2和H2O为合成甲醇的最佳路径;若CO2的转化率低于42%时,则CO2和CO的催化加氢同为最优路径。零碳排放电厂CO2的排放降低到62.5 kg/MW,仅占超临界燃煤机组排放量的7.29%。
二氧化碳减排;零碳排放;液体燃料;可再生能源;Aspen Plus
近年来,将CO2和H2O转化为燃料尤其是液体燃料成为了研究热点,这为实现CO2的减排提供了一条循环利用的新路径。此种液体燃料如甲醇等,相较于气体燃料更易于储存和运输,且其应用于汽车、船舶等终端热机可在一定程度上实现CO2的减排。若将液体燃料应用于电厂,则可极大地缓解CO2排放的压力。基于此,提出了零碳排放电厂的概念[1-2]。如图1所示,这一新概念技术将CO2-液体燃料-CO2作为零碳排放电厂的运行模式,并利用可再生能源,如太阳能、风能等作为催化反应的输入能源。所生产的液体燃料一部分直接进入发电系统,一部分则储存起来作为可再生能源减少时的补充,以维持电力输出的稳定性。而液体燃料燃烧的产物则是二氧化碳和水,可被直接循环到催化反应器进行再次催化转化。这样,零碳排放电厂不仅实现了CO2的循环利用,避免了直接向大气中排放的问题,更实现了将不稳定的可再生能源转化为稳定的电力输出的目标。
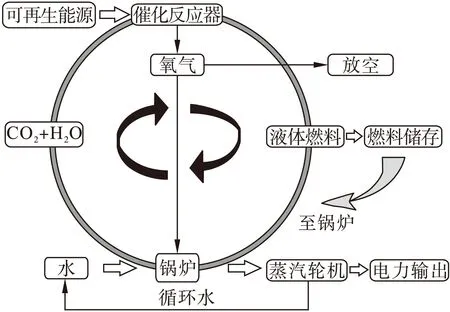
图1 零碳排放电厂循环示意图
零碳排放电厂的关键是获得一种液体燃料,其不仅可由CO2轻易转化得到,而且具有良好的燃烧性能。然而实际的转化产物将包含多种不同的成分,为了简化模拟,此处假设甲醇是唯一的产物。作为前景广阔的液体燃料候选者,甲醇可由CO2根据如下几种技术路线合成:
(1)工业上CO2与CH4首先催化重整为合成气,然后在F-T催化转化反应器中转化为甲醇[3-4]。然而,此技术路线需要消耗大量的化石能源甲烷。
(2)CO催化加氢合成甲醇是一个比较容易实现的反应,其中H2来自H2O的电解,CO来自CO2的催化还原。这一路线还需要解决如何高效地把CO2向CO转化的问题[5]。
(3)近年来,研究人员也致力于实现CO2的直接催化加氢[6-8],这一路线不需考虑CO2向CO高效转化的问题。
(4)不少学者正在研究如何实现CO2和H2O的直接转化[9-10]。
路径(1)中因大量消耗化石能源CH4,因此将不对其进行研究。对于甲醇合成的其它路径,利用Aspen Plus分别建模并进行热力学分析,基于分析结果对整体零排放电厂进行过程模拟。
1 甲醇合成路径建模与参数设置
1.1路径建模
(1)CO催化加氢
如图2(a)所示,R1是CO2和H2O的共电解池,R2是F-T催化加氢反应器。在电解过程中,CO和H2产生于阴极一侧,而O2则产生于阳极一侧并由此排出。合成气经闪蒸脱除水蒸气后进入R2进行催化加氢反应,并得到目标产物液体燃料甲醇。由于催化加氢过程中没有水产生,因此由R2得到的产物经FL2闪蒸分离后便得到较纯的甲醇。
(2)CO2催化加氢
与CO2和H2O的共电解相比,CO2催化加氢合成甲醇在热力学上更可行。如图2(b)所示,R1是H2O电解槽,R2是F-T催化加氢反应器,而RAD1,RAD2是蒸馏模块。CO2与来自H2O电解产生的H2混合后进入R2催化加氢反应器反应生成甲醇。在此反应过程中因为会有水产生,所以由R2得到的产物需经过多次蒸馏才能得到纯度较高的甲醇燃料。
(3)CO2和H2O直接反应生成甲醇
图2(c)是光催化转化(PhC)CO2生产甲醇的工艺流程图,R1是光催化反应器,CO2和H2O将在其中反应生成甲醇等目标产物。来自R1的反应产物经FL1闪蒸分离后,未反应的CO2、O2以及其它气体产物将被循环通入R1进行再次反应,而液体燃料和水溶液的混合物需经过多级蒸馏模块RAD后才可得到纯度一定的液体燃料。电催化转化(ElC)CO2和H2O生产甲醇的工艺流程图如图2(d)所示,R1是电催化反应器,由两个反应腔A、B组成,A反应腔通入水溶液并置入正电极;B反应腔则通入气态CO2,同时置入负电极。A、B反应腔被质子交换膜(PEM)隔开。水在阳极电解产生O2和大量质子,随后质子经PEM到达反应腔B与吸附在催化剂表面的CO2反应生成甲醇等液体燃料。由于在电催化的正常运行中会产生大量的水,另外A反应腔中少量水也会穿越PEM到达B反应腔,因此产物经FL1闪蒸分离后还需经过多级蒸馏,进而得到一定纯度的液体甲醇燃料。
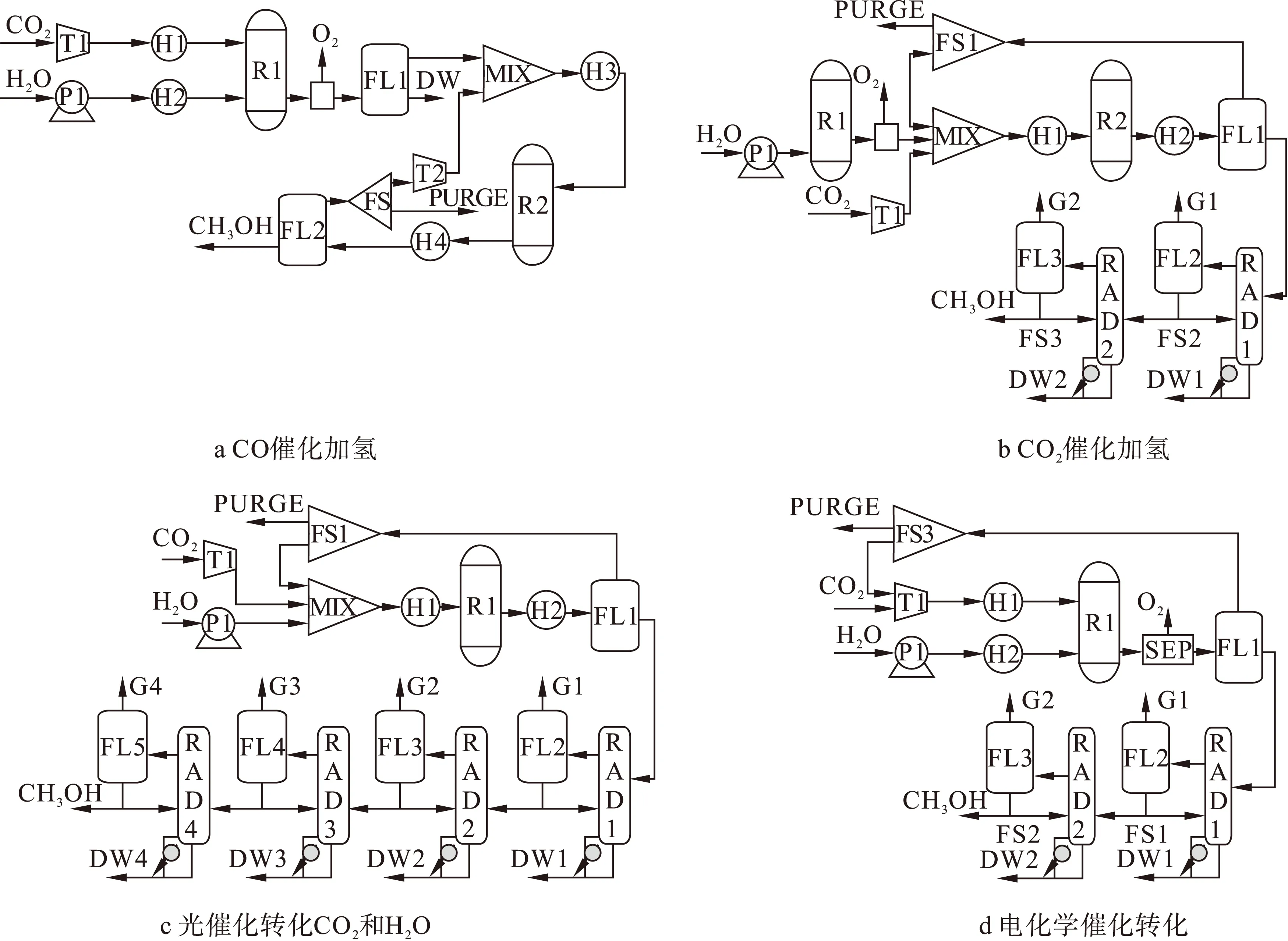
图2 甲醇工艺流程图
1.2参数设置
由于各路径在实现CO2和H2O的转化时所能达到的转化率不同,因此为了较好的对比研究,在模拟中假设各路径的转化率均为30%。此外,为了减小各路径的不同反应参数对结果的影响,取F-T反应器的运行条件为210 ℃和40 bar[11-12]。而对光催化反应器的反应条件设置基于两种假设:(1)基于刘媛媛等人[13]研制的CO2光催化反应器,为进一步提高CO2在水中的溶解度,取运行压力为40 bar,运行温度为环境温度;(2)光催化反应器的一个关键因素是有效的受光面积,由Du[14]等人开发的内部辐照结构化反应器(IIMR)提供一种可有效增大受光面积的方法,本模拟研究假设此光催化反应器采用了IIMR的反应器设计。对于电催化反应器,采用质子交换膜(PEM)的电催化反应器可将CO2和H2O分离,且反应生成的O2将仅在H2O溶液一侧排出。这一方法的应用由Genovese[15]所报道,其不仅有利于液体燃料的分离收集,且完美解决了CO2在水溶液中溶解度的问题,其反应温度和压力分别为室温和40 bar。
2 结果和讨论
2.13种甲醇合成路径的比较
F-T反应器中所进行的反应为放热反应,而由CO2和H2O电解制CO和H2的过程则为吸热反应。因电解池的电解效率接近100%,因此CO2和H2O分子分解的能量最低值为以下反应的焓变值:
(1)
(2)
利用商业软件Aspen Plus对以上甲醇合成路径进行建模,并做热力学分析。结果表明,当CO2转化率低于42%时,光催化转化路径的能耗最低;而在CO2转化率为42%左右时,几种路径的能耗彼此接近(见图3a;但随着CO2转化率的进一步提高,光催化路径的能耗迅速攀升,电催化路径的能耗则持续降低,并在60%以后成为能耗最低路径。图3b中,热负荷为各路径中催化反应器所消耗的能量,而功率为压缩机所消耗的能量,随着CO2转化率的不断提升,催化反应器所消耗的能量即热负荷将呈线性增长的趋势。而由功率变化曲线可知,光催化路径能耗上升的主要因素为物流压缩功率的不断增加,这是因为随着CO2转化率的提高,O2的产量亦不断升高,且O2与副产物H2以及其它气体产物混合后经压缩机压缩并循环至反应器,这一过程严重增加了压缩机的负担。而电催化所产生的O2不与其它产物相混合,但副产物H2仍然无法消除,其将与未反应的CO2一同进入循环系统。随着CO2转化率的提高,甲醇的电流效率不断增加,而副产物H2则愈来愈低。因此,在电催化路径中循环压缩机的负载逐渐降低。对于CO2和CO的催化加氢路径,随着CO2转化率的提升二者热负荷始终保持近似相等。
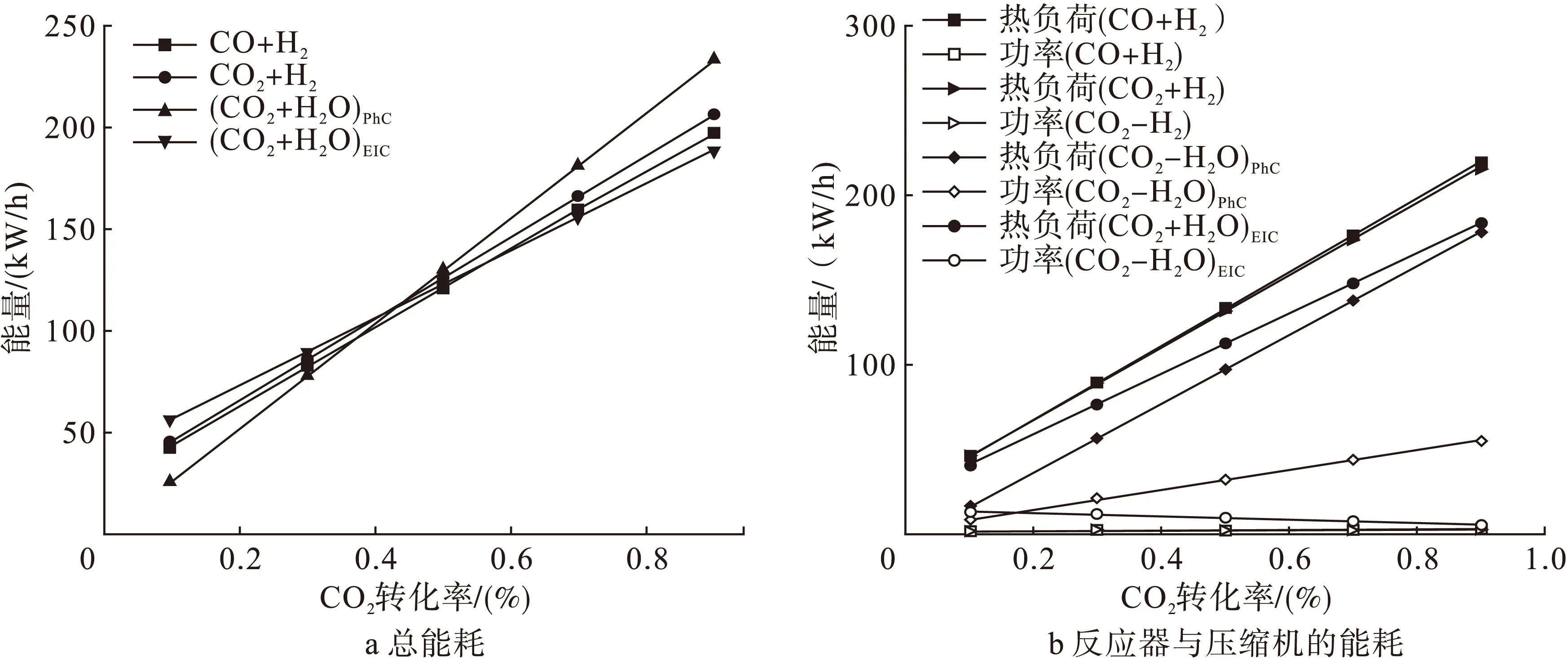
图3 不同路径合成甲醇的能耗图
除能耗之外,还需要考虑甲醇的纯度问题。由于光催化转化CO2和H2O的产物甲醇与水溶液相互混合,因而甲醇在产率不高时极难与水溶液分离。与其他路径相比,在甲醇提纯设备和运行条件一致情况下,要使甲醇达到可供燃烧的浓度,仅催化路径就需要更多的蒸馏模块。而CO2和CO催化加氢以及电催化的产物都不与水溶液混合,且在反应过程中只有少量甚至没有水生成,因此所得到的甲醇浓度非常高。结合各路径的能耗因素分析,当CO2的转化率能够达到大于42%时,电催化转化CO2和H2O的路径为最佳路径;而当转化率小于42%时,由能耗来看CO催化加氢比CO2略低,但前者在电解生成CO的过程中又比CO2成本略高,综合来说CO和CO2的催化加氢制甲醇同为最好的选择,且在工业生产中CO2和CO的催化加氢是同时发生的,此外其CO2的净转化率已达30%以上[16]。因此,在电催化转化CO2和H2O制甲醇还未得到突破之前,CO2和CO的催化加氢仍然是完成零碳排放电厂的最佳选择。
2.2零碳排放电厂的过程模拟
2.2.1建模
据零碳排放电厂的概念及以上对于甲醇合成各路径的分析,CO2、CO和H2(6.4∶8.6∶60)作为合成甲醇的原料气,其中CO和H2来自CO2和H2O的电解,而输入能源则来自太阳能光伏发电。零碳排放电厂流程图如图4所示,R1为CO2和H2O的共电解槽,电解产物经FL1闪蒸得到CO2、CO和H2混合气后通入F-T催化反应器合成甲醇,其中F-T反应器采用目前较为完善的甲醇合成动力学模型,且模型方程和参数取自Van-Dal等人的研究结果[16]。所得粗甲醇经闪蒸分离后还需经过多次蒸馏达到一定纯度的精甲醇,而在F-T中未反应的原料气将会被循环至反应器中再次反应,所生产的精甲醇一部分直接供给超临界发电机组,另一部分则储存起来以备夜间维持发电机组的正常运转。为满足超临界发电机组的运行条件(表1[17]),将煤的质量流量按热值换算为甲醇的质量流量,即为368.27 t/h。
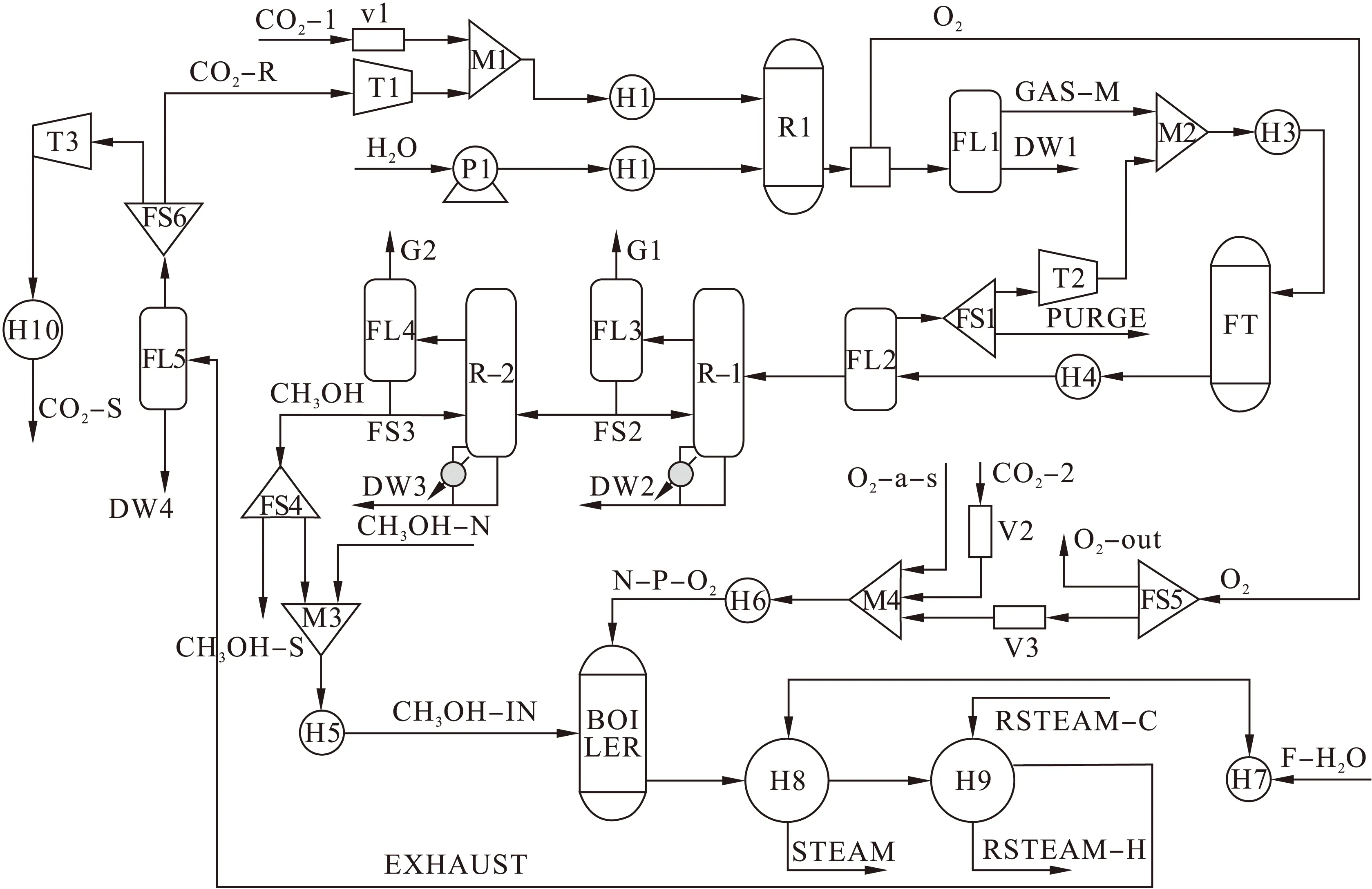
R1:CO2和H2O的共电解槽;F-T:CO2和CO的催化加氢反应器;BOILER:锅炉;H1-H9:换热器;FL1-FL5:气液闪蒸器;R-1,R-2:甲醇蒸馏器;T1-T3压缩机;P1:泵;M1-M4:物流混合器;FS1-FS6:物流分裂器;V1-V3:气体阀门图4 零碳排放电厂模拟流程图
太阳能在不同时间、不同地形、不同纬度等条件下的日照时长都存在着变化,为简化模拟,根据当地直射太阳辐射能量DNI=945W/m2和年平均太阳辐射能量I=2 717 kWh/(m2·y),可得出年平均日照时长数H=I/DNI=2 875 h,则可知日平均日照时长数为7.87 h。在7.87 h内,甲醇的产量必须同时满足日间和夜间发电机组对甲醇的需求量,因此在日间66.7%左右的甲醇将被储存起来。在日间,CO2和H2O电解产生的O2一部分可用于提供锅炉中甲醇富氧燃烧所需的氧化剂,而一部分氧气则必须被安全排放到大气中,因为储存O2不仅技术要求苛刻而且成本极高,所以夜间发电机组运行时使用富氧燃烧技术需利用来自空气分离机的氧气。理论上利用低温空气分离技术可以得到纯度为95%的氧气[18],且每生产1.5 mol氧气仅消耗28.5 kJ的能量,仅占燃烧1 mol甲醇所释放能量的4.5%。
2.2.2系统优化
为了得到零排放电厂的最佳运行参数,利用Aspen Plus中灵敏度功能分别分析了F-T反应器的运行温度和压力对甲醇产量的影响。净热负荷为F-T反应器所消耗的可再生能源,因CO2和CO的催化加氢反应为放热反应,因此热负荷为负值,甲醇的产率越高则净热负荷的绝对值越大,反之则净热负荷的绝对值越小。显而易见,F-T反应器温度和压力对反应的高效进行有着至关重要的作用,但两种参数过高或过低都将对甲醇的产率产生影响。当反应压力低于50 bar时,甲醇产率随着压力的升高而快速升高,而当压力继续高于50 bar时,甲醇产率则迅速降低。同样的,反应温度和甲醇的产率也有着类似的关系。如图5所示,甲醇峰值产量出现在50 bar、330 ℃条件下。
除温度和压力外,进入锅炉的甲醇质量流量也是影响系统正常运行的重要参数。采用富氧燃烧技术,甲醇可更充分地释放其化学能,所以在减小甲醇的质量流量至原值的75%时仍可得到足量的过热蒸汽。但当甲醇的质量流量继续减小时,则无法保证再热蒸汽出口温度达到569 ℃(图6a),从而严重影响电力的稳定输出。此时,若通过有效的热管理技术将H3、H10和F-T反应器等的废热加以利用,如锅炉给水和进气的预热等,可进一步减小甲醇进入锅炉的质量流量。这样,最终发电机组的甲醇消耗量降为日间276 t/h,夜间280 t/h。
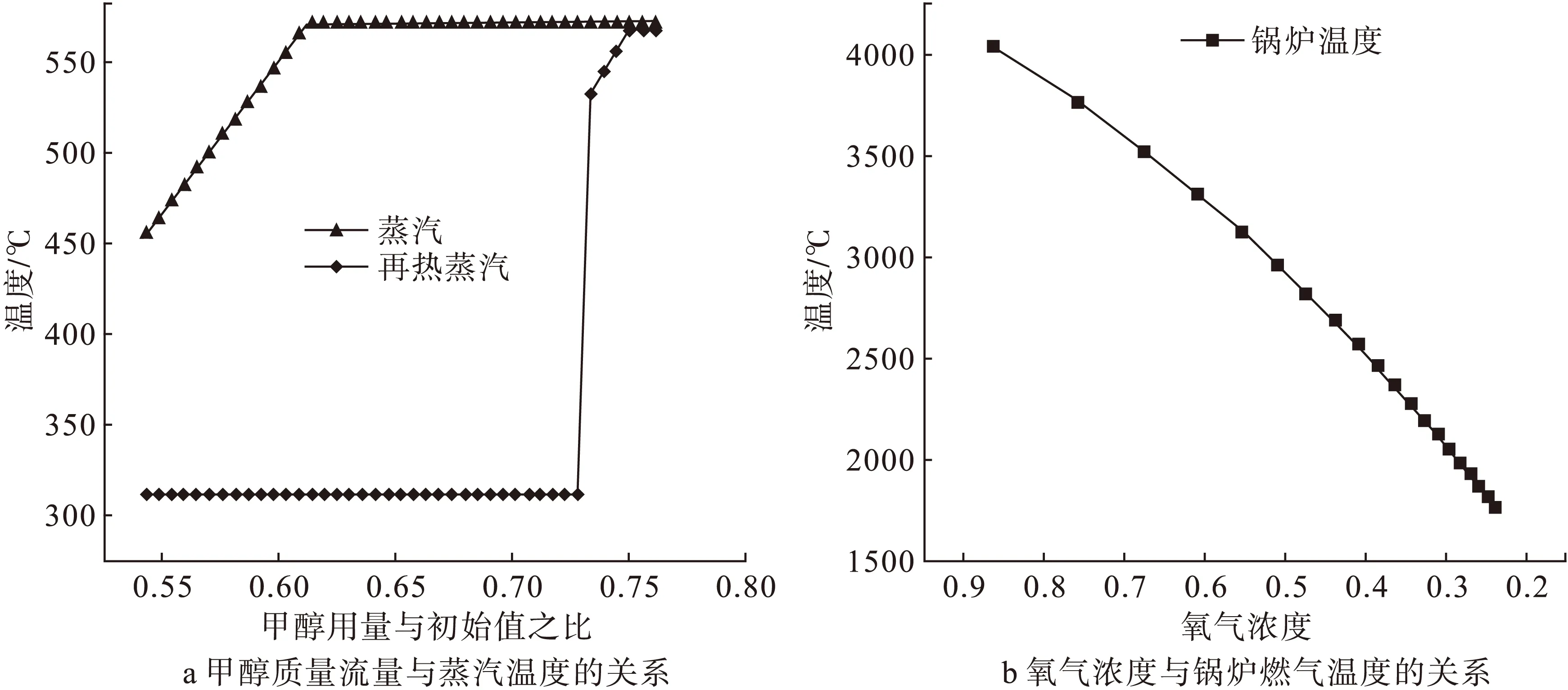
图6 影响发电机组运行的因素
另一方面,采用富氧燃烧技术会使火焰温度急剧上升,这对锅炉材料性能和耐久度等都有着极大的危害。因此在不减少甲醇质量流量的情况下,通过向氧气中引入过量CO2稀释燃烧热的方法来降低燃气温度。由图6b可知,当氧气浓度降为25%时,燃气温度降到1 500 ℃左右。
此外,由于驰放气PURGE中存在大量未转化的CO、H2和CO2,而H2和CO的大量排放会直接导致电解槽能耗的急剧攀升,因此驰放气中CO和H2的回收利用至关重要。利用膜分离技术可较好实现CO2[19-20]、CO[21]和H2[22]的分离回收。且其工作温度小于100 ℃,可利用系统中的废热对膜分离设备提供所需能量。假设对CO和H2的回收率为100%,那么电解槽对CO和H2的产量可分别降低14 262 mol/h和90 405 mol/h。
2.2.3质能平衡
零碳排放电厂的一个重要评价指标是CO2的排放量,因此对于系统的碳平衡计算显得尤为重要。CO2作为系统中能量载体的循环工作介质,其输入输出将只与系统的碳损失相关,其中包括CO2、CO和甲醇,因此碳平衡计算公式可写作:
CO2 input=CO2 output+COoutput+CH3OHoutput
(3)
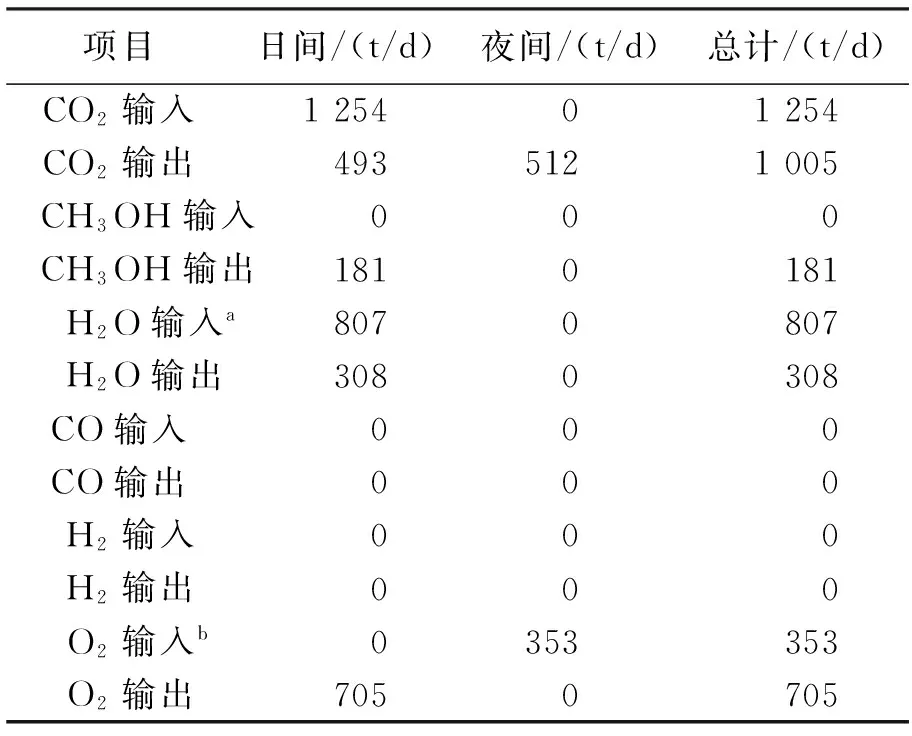
表2 催化加氢法NZCE电厂质量平衡
a不计发电机组蒸汽用水量;b O2来自于空分机。
将表2中的数据代入式(3)得出,零碳排放电厂每日净CO2输入量为1 254 t/d,包括了生产过程中的CO2、CO和甲醇的排放。而对应排放进大气的CO2量仅为62.5 kg/MWh,仅占目前最先进的超临界发电机组排放量的7.29%。而水的质量衡算可以相同的方法得出,其中水的损耗包括甲醇、水以及氢气。由表2中数据可知每日水的消耗量为807 t/d。
表3列出了零碳排放电厂的各个主要模块的能量收支情况。系统中CO2、CO和H2的膜回收系统、空气分离系统等的能量可通过有效的热管理技术将废热如H1、F-T和FL5处的释热回收再利用,从而避免了额外的能量输入。蒸汽经过蒸汽轮机后仍然携带大量的热能,这一部分能量一般用来对锅炉给水的预热。而FL1中的运行温度过低,其所释放的大量低品质能量将无法再次收集利用。电厂可再生能源的输入均是电能的形式,主要被电化学催化反应器、压缩机、泵和部分加热器所消耗。而电厂的功率输出则是670 MW,因此电厂能量效率可由式(4)计算而得:
(4)
其中P是电厂的输出功率,Er是每日输入进电厂系统的可再生能源,包括R1、T1、T2、T3、P1、H5和H6,据表3中相应模块的能量值加和后得到Er=68 983.1 MWh。因此,将P和Er代入式(3)、(4)中得到在CO2转化率为33%[16]时NZCE电厂能量效率η=23.3%。
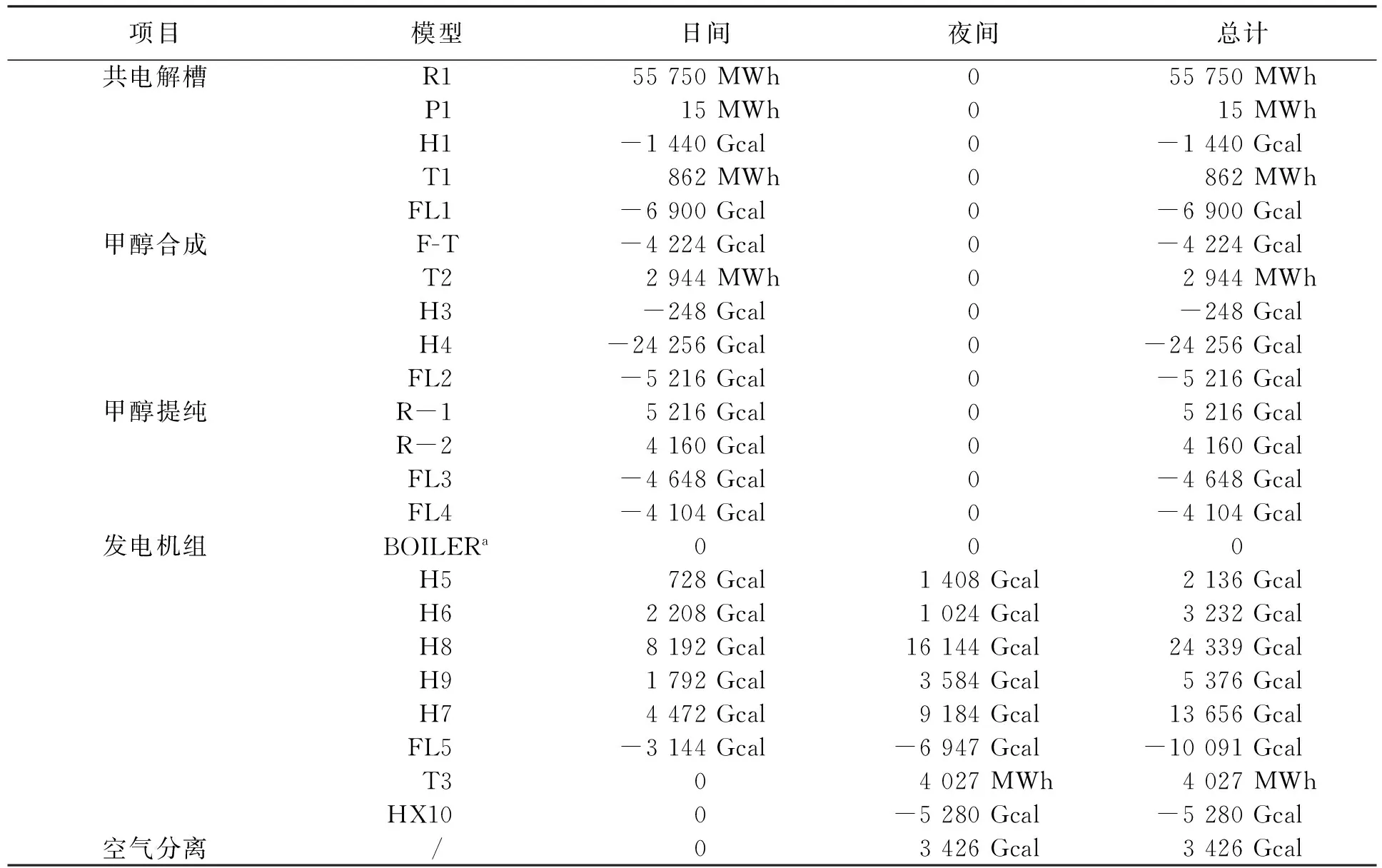
表3 催化加氢法NZCE电厂能量平衡
a BOILER 假定为绝热燃烧。
3 结论
(1)利用Aspen Plus对CO+H2、CO2+H2以及CO2+H2O等几种甲醇合成的路径进行合理建模并做了热力学分析。结果表明,在仅考虑能耗的情况下,若CO2的转化率高于42%时,电催化转化CO2和H2O为合成甲醇的最佳路径;而若CO2的转化率低于40%时,则CO2和CO的催化加氢同为最优路径。
(2)提出了以CO2和H2O转化而成的液体燃料为能源介质的零碳排放电厂的概念,形成“可再生能源+CO2+H2O→液体燃料→电力+CO2+H2O”的CO2循环利用模式。采用CO2和CO的催化加氢作为合成甲醇的路径,对整体零碳排放电厂做系统建模分析,结果表明CO2的排放可降低到62.5 kg/MW,仅占超临界燃煤机组排放量的7.29%,但因大量能量以废热的形式浪费掉,因此系统净能量效率只有23.3%。
[1]CHENDING LUO,NA ZHANG.Zero CO2emission SOLRGT power system[J].Energy,2012,45(1):312-323.
[2]MUHAMMAD TAHIR,NORAISHAH SAIDINA AMIN.Recycling of carbon dioxide to renewable fuels by photocatalysis:Prospects and challenges[J].Renewable and Sustainable Energy Reviews,2013,25(5):560-579.
[3]KATHIRASER Y,WANG Z,KAWI S.Oxidative CO2reforming of methane in La0.6Sr0.4Co0.8Ga0.2O3-δ(LSCG)hollow fiber membrane reactor[J].Environmental Science and Technology,2013,47(24):14510-14517.
[4]BURTRON H.DAVIS.Overview of reactors for liquid phase fischer-tropsch synthesis[J].Catalysis Today,2002,71(3-4):249-300.
[5]JIN SHI,FENG SNI,NING SONG,et al.A novel electrolysis cell for CO2reduction to CO in ionic liquid/organic solvent electrolyte[J].Journal of Power Sources,2014,259(4):50-53.
[6]SOFIANE ARAB,JEAN-MARC COMMENGE,JEAN-FRANÇIS PORTHA,et al.Methanol synthesis from CO2and H2in multi-tubular fixed-bed reactor and multi-tubular reactor filled with monoliths[J].Chemical Engineering Research and Design,2014,92(11):2598-2608.
[7]DANTE L.CHIAVASSA,SEBASTIN E.COLLINS,ADRIAN L.BONIVARDI,et al.Methanol synthesis from CO2/H2using Ga2O3-Pd/silica catalysts:Kinetic modeling[J].Chemical Engineering Journal,2009,150(1):204-212.
[8]LI LI,DONGSEN MAO,JUN YU,et al.Highly selective hydrogenation of CO2to methanol over CuO-ZnO-ZrO2catalysts prepared by a surfactant-assisted co-precipitation method[J].Journal of Power Sources,2015,279(1):394-404.
[9]NAVEED AHMED,MOTOHARU MORIKAWA,YASUO IZUMI.Photocatalytic conversion of carbon dioxide into methanol using optimized layered double hydroxide catalysts[J].Catalysis Today,2012,185(1):263-269.
[10]CARLOS CARLESI,DANILO CARVAJAL,DREIDY VASQUEZ,et al.Analysis of carbon dioxide-to-methanol direct electrochemical conversion mediated by an ionic liquid[J].Chemical Engineering and Processing:Process Intensification,2014,85:48-56.
[11]GRAAF G H,WINKELMAN J G M,STAMHUIS E J,et al.Kinetics of the three phase methanol synthesis[J].Chemical Engineering Science,1988,43(8):2161-2168.
[12]NONAM PARK,PARK M J,LEE Y J,et al.Kinetic modeling of methanol synthesis over commercial catalysts based on three-site adsorption[J].Fuel Processing Technology,2014,125(125):139-147.
[13]LIU Y Y,HUANG B B,YING DAI,et al.Selective ethanol formation from photocatalytic reduction of carbon dioxide in water with BiVO4 photocatalyst[J].Catalysis Communications,2009,11(3):210-213.
[14]PENG DU,JOANA T.CARNEIRO,JACOB A.Moulijn,et al.A novel photocatalytic monolith reactor for multiphase heterogeneous photocatalysis[J].Applied Catalysis A:General,2008,334(1-2):119-128.
[15]CHIARA GENOVESE,CLAUDIO AMPELI,SIGLINDA PERATHONER,et al.A gas-phase electrochemical reactor for carbon dioxide reduction back to liquid fuels[J].Chemical Engineering Transactions,2013,32(11):289-294.
[17]YANG Y P,WANG L G,DONG C Q,et al.Comprehensive exergy-based evaluation and parametric study of a coal-fired ultra-supercritical power plant[J].Applied Energy,2013,112(4):1087-1099.
[18]QIAN FU,YASUKI KANSHA,CHUNFENG SONG,et al.A cryogenic air separation process based on self-heat recuperation for oxy-combustion plants[J].Applied Energy,2016,162:1114-1121.
[19]ERIK SJÖBERG,SIMON BARNES,DANIL KORELSKIY,et al.MFI membranes for separation of carbon dioxide from synthesis gas at high pressures[J].Journal of Membrane Science,2015,486:132-137.
[20]ARIJIT MONDAL,MRIDUSMITA BAROOAH,BISHNUPADA MANDAL.Effect of single and blended amine carriers on CO2separation from CO2/N2mixtures using crosslinked thin-film poly(vinyl alcohol)composite membrane[J].International Journal of Greenhouse Gas Control,2015,39:27-38.
[21]DIMARTINO S P,GLAZER J L,HOUSTON C D,et al.Hydrogen/carbon monoxide separation with cellulose acetate membranes[J].Gas Separation & Purification,1988,2(3):120-125.
[22]STANISLOWSKI J J,HOLMES M J,SNYDER A C,et al.Advanced CO2Separation technologies:coal gasification,warm-gas cleanup,and hydrogen separation membranes[J].Energy Procedia,2013,37:2316-2326.
(责任编辑:吴萍英文审校:赵欢)
Process simulation of a zero carbon emission power plant using CO2as storage medium of renewable energy
GAI Shao-lei,ZHAO Huan,GENG Xiu-zhen,XIN Bin-bin
(Thermal Energy Research Centre,Shenyang Aerospace University,Shenyang 110136,China)
Liquid fuel converted from CO2and H2O using renewable energy was utilized in zero carbon emission power plants,forming a closed cycle of “renewable energy(unstable energy supply)+CO2+H2O→liquid fuels→electricity(stable energy supply)+CO2+H2O”.Three main routes were considered for the conversion of CO2and H2O∶CO+H2,CO2+H2and CO2+H2O,in which CO and H2come from the electrolysis of CO2and H2O,and electrolytic liquid product was methanol.To investigate these three conversion routes and the zero carbon emission power plant,Aspen Plus software was used to build proper models and conduct the thermodynamic analysis.The results show that when the conversion of CO2is higher than 42%,the best route of methanol synthesis is the electrocatalytic conversion of CO2and H2O;while when CO2conversion is lower than 42%,the optimal route is the hydrogenation of CO2and CO.The simulation result also confirms that CO2emission for the zero carbon emission power plant only decreases to 62.5 kg/MW,which is just 7.29% of that for the super critical coal-fired power plant.
CO2emission mitigation;zero carbon emission;liquid fuel;renewable energy;Aspen Plus
2015-10-23
国家自然科学基金(项目编号:51404154)
盖少磊(1988-),男,陕西富平人,硕士研究生,主要研究方向:CO2的综合利用,E-mail: shaolei_gai@163.com;赵欢(1982-),女,辽宁沈阳人,副教授,主要研究方向:洁净煤技术,E-mail:phd_zhaohuan@163.com。
能源与环境工程
2095-1248(2016)04-0089-08
TK01+9
A
10.3969/j.issn.2095-1248.2016.04.016

