胆舒滴丸质量标准研究
周维,胡昌江,冯健
(四川新绿色药业科技发展股份有限公司,四川 彭州 611930)
胆舒滴丸质量标准研究
周维,胡昌江*,冯健
(四川新绿色药业科技发展股份有限公司,四川 彭州 611930)
目的:建立胆舒滴丸的质量标准。方法:采用薄层色谱法对胆舒滴丸中的薄荷脑进行定性研究;采用气相色谱法对胆舒滴丸进行特征图谱研究及含量测定。结果:薄层色谱鉴别特征明显,专属性强;胆舒滴丸不同批次的气相色谱图均有8个特征峰,均具有较好的分离度;薄荷脑在0.104~0.780 μg呈现良好的线性关系,回归方程为Y=1 827.0X-2×10-13,相关系数为r=1.000 0。结论:所建立的质量标准能有效地对胆舒滴丸进行鉴别,并准确地进行含量测定。
胆舒滴丸;薄荷脑;特征图谱;质量标准;含量测定
胆舒滴丸是以薄荷素油为原料制成的中药制剂,用于慢性结石性胆囊炎、慢性胆囊炎及胆结石肝胆郁结、湿热胃滞证[1]。薄荷素油主要成分为L-薄荷脑、(-)-薄荷酮、胡薄荷酮、桉油精、异薄荷酮等[2]。为了有效地控制胆舒滴丸的质量,本文建立薄层色谱法对其进行定性鉴别,气相色谱法考察其特征图谱及含量。通过方法学考察得出,所建方法专属性强、灵敏度高、方法稳定,可用于胆舒滴丸的质量控制。
1 仪器与试药
1.1 仪器
薄层自动成像仪(TLC Visualizer,CAMAG);半自动点样仪(linamat5,CAMAG);万分之一天平(BS110S,赛多利斯);超声清洗器(KQ-250B型,昆山超声电子有限公司);气相色谱仪(78090B,安捷伦);色谱柱(安捷伦);
1.2 试药
桉油精、薄荷脑、胡薄荷酮、(-)-薄荷酮(中国食品药品检定研究院,批号分别为110788-201105,110728-200506,111706-201205,111705-201105);胆舒滴丸(四川新绿色药业科技发展股份有限公司,批号分别为1312001,312002,1312003,140501,140502,140503,150401,150402,150403);其他试剂、试药均为分析纯
2 方法与结果
2.1 薄层色谱鉴别
取本品10丸,研细,加乙酸乙酯10 mL,超声处理5 min,滤过,滤液作为供试品溶液。另取薄荷脑对照品,加乙酸乙酯制成质量浓度为4 mg·mL-1的溶液,作为对照品溶液。照薄层色谱法(《中华人民共和国药典》2010年版一部附录Ⅵ B)试验,吸取上述两种溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚60~90 ℃-乙酸乙酯(7∶1)为展开剂,展开,取出,晾干。喷以5%香草醛乙醇溶液-硫酸(100∶5)的混合溶液,在105 ℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点[3-4]。结果见图1。
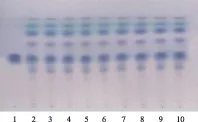
注:1.薄荷脑;2.1312001;3.1312002;4.1312003;5.140501;6.140502;7.140503;8.150401;9.150402;10.150403。图1 胆舒滴丸薄层鉴别图
2.2 特征图谱
2.2.1 色谱条件与系统适用性试验 以聚乙二醇20 M为固定相的毛细管柱(柱长为30 m,内径为0.53 mm,膜厚度为1 μm);柱温为程序升温:初始温度为115 ℃,保持5 min,以4 ℃·min-1的速率升温至200 ℃,保持3 min;进样口温度为230 ℃;检测器温度为230 ℃;分流进样,分流比为10∶1。理论板数按薄荷脑峰计算应不低于50 000。见图2。
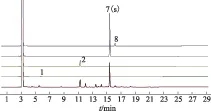
注:1.桉油精;2.(-)-薄荷酮;7.薄荷脑;8.胡薄荷酮。下同。图2 胆舒滴丸对照图谱
2.2.2 参照物溶液的制备 取桉油精对照品、(-)-薄荷酮对照品、薄荷脑、胡薄荷酮对照品[5],精密称定,分别加无水乙醇制成质量浓度为2 mg·mL-1的溶液,即得。
2.2.3 供试品溶液的制备 取本品5丸,精密称定,置50 mL量瓶中,加水4 mL,超声处理使溶散,加入无水乙醇30 mL,超声处理(功率200 W,频率40 kHz)5 min,放冷,加无水乙醇至刻度,摇匀,滤过,取续滤液,即得。
2.2.4 特征图谱方法学考察 稳定性:取同一供试品溶液,分别于0、4、8、12、24 h测定,对其中的特征峰进行分析,各色谱峰相对保留时间的RSD均小于0.3%,结果表明,供试品溶液在24 h内稳定。
精密度:取同一供试品溶液,连续进样6次,每次1 μL,各色谱峰相对保留时间的RSD均小于2.0%,符合特征图谱研究的技术要求,表明该方法进样精密度良好。
重复性:取同一批胆舒滴丸样品6份,分别按照2.2.3项下方法制备供试品溶液,分别进样,结果各色谱峰的相对保留时间的RSD均小于2.0%,表明该方法重复性好。
2.2.5 胆舒滴丸对照特征图谱的建立和分析 按照2.2.3项下分别制备9批胆舒滴丸供试品溶液进行检测,采用中药色谱指纹图谱相似度评价系统(2012版)进行分析,根据相对保留时间稳定、各批次样品均能检出,且峰相对较高的原则,以7号峰为参照确定8个重复性较好的峰作为特征峰,并进行多点校正,自动匹配后生成对照特征图谱。9批胆舒滴丸特征图谱见图3,所得对照特征图谱见图4,各共有峰的相对保留时间见表1。各特征峰与S峰的相对保留时间分别为:0.37(峰1)、0.73(峰2)、0.78(峰3)、0.87(峰4)、0.90(峰5)、0.92(峰6)、1.00(峰S)、1.05(峰8)。
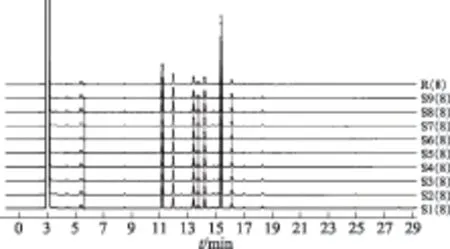
图3 9批胆舒滴丸特征图谱
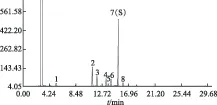
图4 胆舒滴丸对照特征图谱
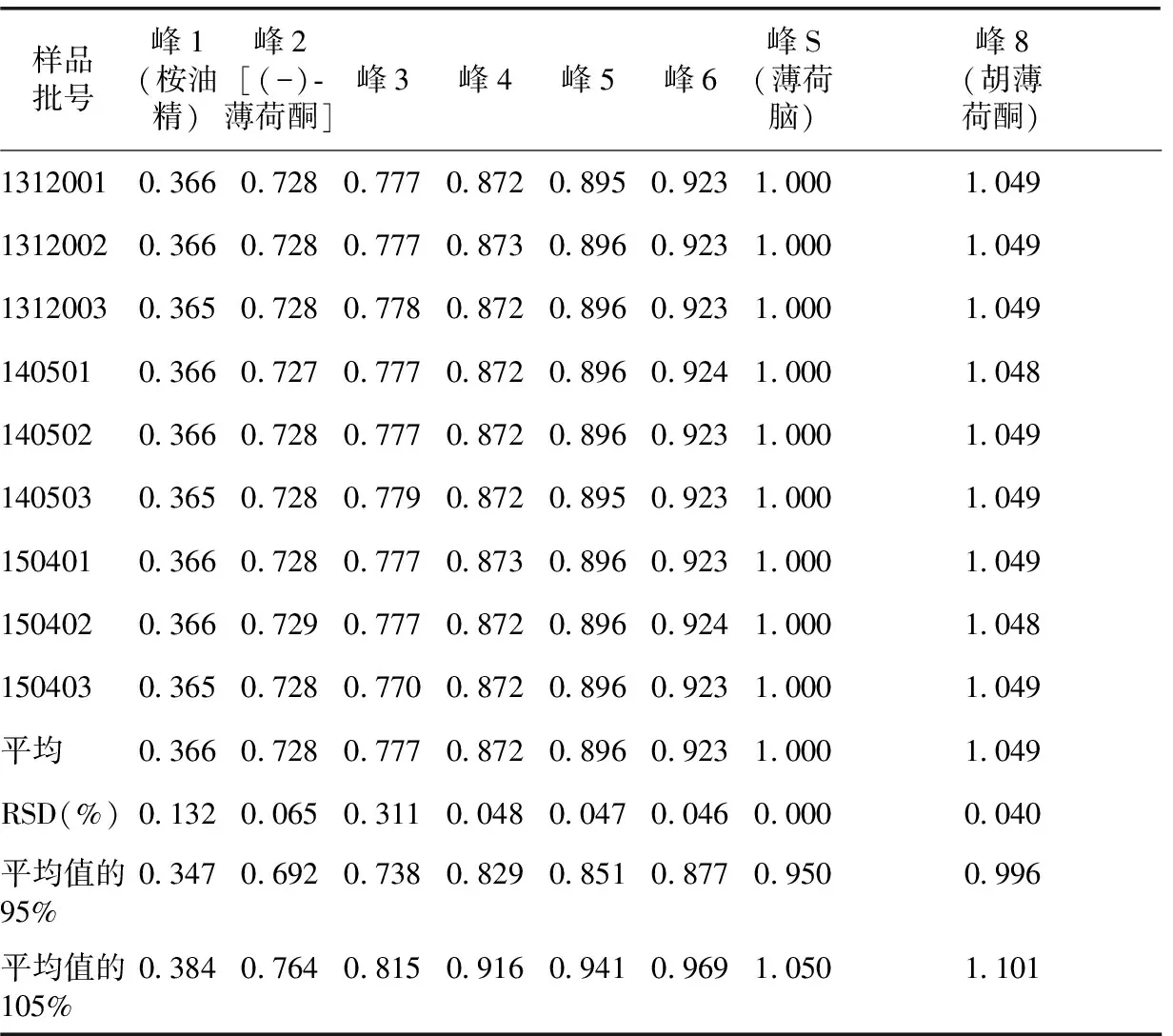
表1 9批胆舒滴丸特征图谱共有峰的相对保留时间
2.3 含量测定
2.3.1 色谱条件与系统适用性试验 同2.2.1色谱条件。
2.3.2 对照品溶液的制备 取薄荷脑对照品,精密称定,加无水乙醇制成每质量浓度为0.2 mg·mL-1的溶液,即得。
2.3.3 供试品溶液的制备 同2.2.3供试品溶液的制备方法。
2.3.4 空白供试品溶液的制备 原方法去除薄荷素油,依法制成阴性制剂。取5丸,按照2.2.3项下方法制备空白供试品溶液,依法测定。结果在色谱图薄荷脑色谱峰位置无吸收峰,空白制剂色谱图对待测峰的测定无干扰。
2.3.5 标准曲线的制备 分别精密吸取薄荷脑对照品溶液(0.52 mg·mL-1)0.2、0.5、0.8、1、1.5 μL,注入气相色谱仪,测定峰面积,以进样量(X,μg)为横坐标,以峰面积值(Y)为纵坐标,绘制标准曲线,计算回归方程:Y=1 827.0X-2×10-13,相关系数r=1.000 0,表明薄荷脑在0.1~0.75 μg进样量与峰面积值呈良好的线性关系。
2.3.6 精密度试验 精密吸取薄荷脑对照品溶液(0.52 mg·mL-1)1 μL,连续进样6次,薄荷脑峰面积的RSD为1.0%,表明本方法进样精密度良好。
2.3.7 重复性试验 取同一批次胆舒滴丸5丸,共6份,置具塞锥形瓶中,按照2.3.3项下方法处理成6份供试品溶液,进行测定,薄荷脑峰面积的RSD为1.5%,表明本方法重复性良好。
2.3.8 稳定性试验 取同一供试品溶液,分别于0、4、8、12、24 h测定,对其中的特征峰进行分析,薄荷脑峰面积的RSD为0.6%,结果表明,供试品溶液在24 h内稳定。
2.3.9 加样回收试验 取已知含量的样品(批号:1312001,薄荷脑的含量为1.95 mg/丸,)3丸,共6份,精密称定,分别精密加入薄荷脑对照品溶液(0.52 mg·mL-1)10 mL,依法测定。计算回收率为100.6%,RSD为2.2%,表明此方法准确性良好。
2.3.10 样品的含量测定 依法对9批胆舒滴丸进行薄荷脑的含量测定,结果见表2。
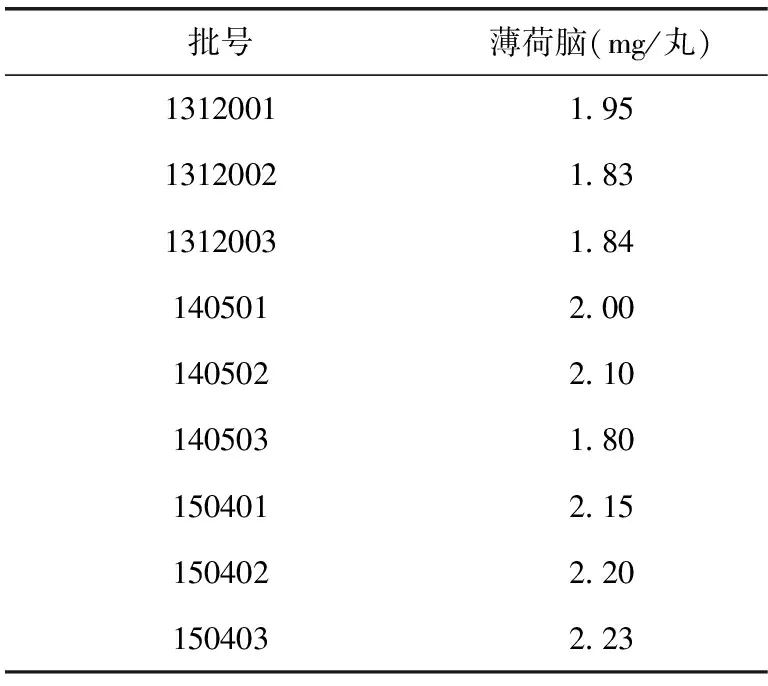
表2 各批次胆舒滴丸中薄荷脑的含量(n=2)
3 讨论
胆舒滴丸是以薄荷素油为主要原料制成的滴丸剂。薄荷素油主要成分为L-薄荷脑、(-)-薄荷酮、胡薄荷酮、桉油精、异薄荷酮等,其中以薄荷脑含量最高,故以薄荷脑为薄层色谱鉴别和含量测定的指标成分,以桉油精、(-)-薄荷酮、薄荷脑、胡薄荷酮为参照物,采用薄层色谱法和气相色谱法对胆舒滴丸进行鉴别、含量测定及特征图谱研究。
特征图谱可从整体上实现质量控制,有利于中药质量稳定和有效。2015年版《中华人民共和国药典》一部收载的薄荷素油指纹图谱项下,对薄荷素油进行了指纹图谱检测。为了提高胆舒滴丸的质量标准,特进行胆舒滴丸的特征图谱研究,确定了8个特征峰,其中4个峰得到指认。
根据9批胆舒滴丸含量测定数据,以9批薄荷脑含量的80%为限量标准,暂定本品每丸含薄荷素油以薄荷脑(C10H20O)计,不得少于1.6 mg。
[1] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2010.
[2] 刘红杰,金若敏.薄荷油研究进展[J].山东中医药大学学报,2006,30(6):502.
[3] 朱亮,包贝华,周灵君.胆舒滴丸的质量标准研究[J].江苏中医药,2007,39(8):68-69.
[4] 刘军,袁杰,吕雄文.枇杷止咳颗粒中枇杷叶、薄荷脑和罂粟壳薄层鉴别的研究[J].安徽医药,2011,15(12)1498-1500.
[5] 桂新,周荣汉.国产野生薄荷挥发油化学组分变异及其化学型[J].植物资源与环境,1998,7(3):13-18.
StudyonQualityStandardsofDanshuDrippingPills
ZHOU Wei,HUChangjiang*,FENGJian
(SichuanNeo-greenPharmaceuticalTechnologyDevelopmentCo.Ltd,Sichuan,Pengzhou611930,China)
Objective:To establish the quality standard for establishing the quality of Danshu dripping pills.Methods:Characteristic identification of Danshu dripping pill was performed by TLC,and content determination and the characteristics chromatograms was performed by gas chromatography.Results:The identification of TLC was obvious and specific.There were 8 characteristic chromatographic peaks with good separation in different batches of Danshu dripping.Menthol showed a good linear relationship in 0.104~0.78 μg.The regression equation wasY=1827.0X-2*10-13.The correlation coefficient was r=1.0.Conclusion:The established quality standard can be effective for the identification and accurate determination of the content of Danshu dripping pills.
Danshu dripping pills;menthol;fingerprint chromatogram;quality standards;determination of content
2015-07-02)
*
胡昌江,教授,博士研究生导师,研究方向:中药炮制原理及饮片质量标准研究;E-mail:wind_61@163.com
10.13313/j.issn.1673-4890.2016.5.022

