经导管主动脉瓣置换术后心肌损伤的荟萃分析
朱 灏 任晓敏 潘道蓉 庞 思 田乃亮 张瑶俊
经导管主动脉瓣置换术后心肌损伤的荟萃分析
朱灏任晓敏潘道蓉庞思田乃亮张瑶俊
目的:系统评价经导管主动脉瓣置换术后心肌损伤的发生率及预测因子。方法:全面检索PubMed、Springer、Elsevier-SDOL、EMbase、SSCI、CNKI、VIP、中国生物医学文献数据库、万方数据资源系统,收集2009年1月至2015年11月发表的主动脉瓣置换术后心肌损伤的研究文献。利用疾病患病率或发病率质量准则评价文献质量,运用Comprehensive Meta-Analysis 2.0软件进行荟萃分析。结果:最终纳入9个研究,均为非随机对照研究,共包含2 423例接受经导管主动脉瓣膜置换术的严重主动脉瓣狭窄患者。术后心肌损伤的总体发生率为20.5%(95%CI:18.5~22.7)。经导管主动脉瓣膜置换术后发生心肌损伤的独立预测因子包括:经心尖途径、早期手术经验不足、瓣膜栓塞或需要置入第2个瓣膜、大出血或致命性出血、冠状动脉粥样硬化性心脏病病史、手术时间、术前存在肾功能不全。结论:经导管主动脉瓣置换术后心肌损伤的总体发生率高达20.5%,可能对预后产生不良影响,应当针对其预测因子进行早期干预以改善患者预后。
经导管主动脉瓣置换术;心肌损伤;预测因子;荟萃分析
严重主动脉瓣狭窄患者经导管主动脉瓣置换(transcatheter aortic valve replacement,TAVR)术后的临床转归已得到明显改善,目前全世界已有超过80 000例接受该手术治疗的患者,为有外科手术禁忌的高龄患者带来了福音[1]。2014年,美国针对CoreValve瓣膜的关键试验(Pivotal Trial)[2]首次表明,TAVR在外科手术风险升高的严重主动脉瓣狭窄患者中疗效优于外科瓣膜置换术,明显降低了患者的1年死亡率(14.2%对19.1%)。同年Sapien XT瓣膜的安全性和有效性也得到了随机多中心PARTNER Ⅱ试验[3]和欧洲PREVAIL TA研究[4]的证实。2015年新一代Sapien 3瓣膜在1 076例有中危手术风险的患者中取得了良好的疗效,其30 d全因死亡率为1.1%,而早期PARTNER A试验中为5.2%[5],这表明手术条件和设备改善使TAVR的适应证扩展至外科手术的中危患者。未来TAVR手术可能会替代外科手术[6]。
然而TAVR手术仍存在不少并发症,影响患者预后[7]。围手术期心肌梗死是TAVR术后常见的并发症之一,本文旨在系统综述和分析重度主动脉瓣狭窄患者接受TAVR术后心肌损伤的发生率和预测因子。
1 资料和方法
本研究严格按照Cochrane协作网的PRISMA声明进行荟萃分析。
1.1纳入和排除标准
纳入标准:(1)研究类型为临床随机对照研究或注册登记研究;(2)研究对象为所有接受TAVR的外科手术高风险的患者;(3)研究报道了TAVR术后心肌损伤的发生率和预测因子。排除标准:(1)研究未给出TAVR术后心肌损伤标志物升高的具体数据;(2)研究未报道TAVR术后心肌损伤的发生率;(3)无法提取数据的研究。
1.2检索策略
使用主题词结合自由词进行检索。中文检索词包括:“主动脉瓣置换术”、“经导管主动脉瓣置换术”、“经导管主动脉瓣植入术”。英文检索词包括:“aortic valve replacement”、“transcatheter aortic valve replacement”、“transcatheter aortic valve implantation”、“myocardial injury”、“myocardial infarction”。系统检索PubMed、Springer、Elsevier-SDOL、EMbase、SSCI、VIP、CNKI、中国生物医学文献数据库、万方数据资源系统中2009年1月至2015年11月发表的文献。同时回顾参考文献和早期荟萃分析,纳入符合标准的研究。
1.3资料提取和质量分析
提取资料包括纳入研究基本情况(设计方案、样本量)、研究对象的年龄、性别、手术途径、心肌损伤定义、冠状动脉粥样硬化性心脏病(冠心病)病史、使用自膨胀式瓣膜等基线资料和心肌损伤的发生率、预测因子。质量分析采用Loney等提出的观察性研究的质量评价准则进行评分,得分范围0~7分,得分越高,表示文献质量越好。
1.4统计学分析
本研究对照Cochrane手册的系统评价指南,进行标准的数据提取和计算。采用随机效应模型(DerSimonian and Laird模型,D-L模型)计算95%CI,设定显著水平为0.05(双侧),并用森林图展示假设检验结果。使用I2检验分析异质性,当I2>50%时,认为存在显著异质性。敏感性分析通过每次剔除一个研究并重新进行分析。所有统计分析均采用Comprehensive Meta-Analysis Software 2.0软件完成。
2 结果
2.1纳入文献的基本情况
初检文献合计28篇,通过阅读题目、摘要和全文,初筛后获得文献15篇。排除评述3篇,会议摘要2篇,无法提取数据的文献1篇。最终确定9篇文献符合纳入条件。所有纳入的文献均为英文文献,研究地点分别在美国、瑞典、加拿大、德国、荷兰、意大利等,其中5篇对TAVR术后心肌损伤发生的独立预测因子进行了分析。本荟萃分析包括2 423例接受TAVR术的患者。文献质量评价及患者基线特征见表1,质量评分中位数为4分,最低为Carrabba等[8]的研究,为3分,是中等质量文献,其他文献的评分数≥4,为高质量文献。
2.2心肌损伤的发生率及预测因子
通过随机效应模型对入选研究进行荟萃分析,结果显示TAVR术后心肌损伤的总体发生率为20.5%(95%CI:18.5~22.7,P<0.001),见图1。TAVR术后发生心肌损伤的独立预测因子包括经心尖途径、早期手术经验不足、瓣膜栓塞或需要置入第2个瓣膜、大出血或致命性出血、冠心病病史、手术时间较长、术前存在肾功能不全(见表2)。

表1 入选研究的基线特征和文献质量
注:NA为不能提取数据;TA为经心尖;VARC为瓣膜学术研究协会
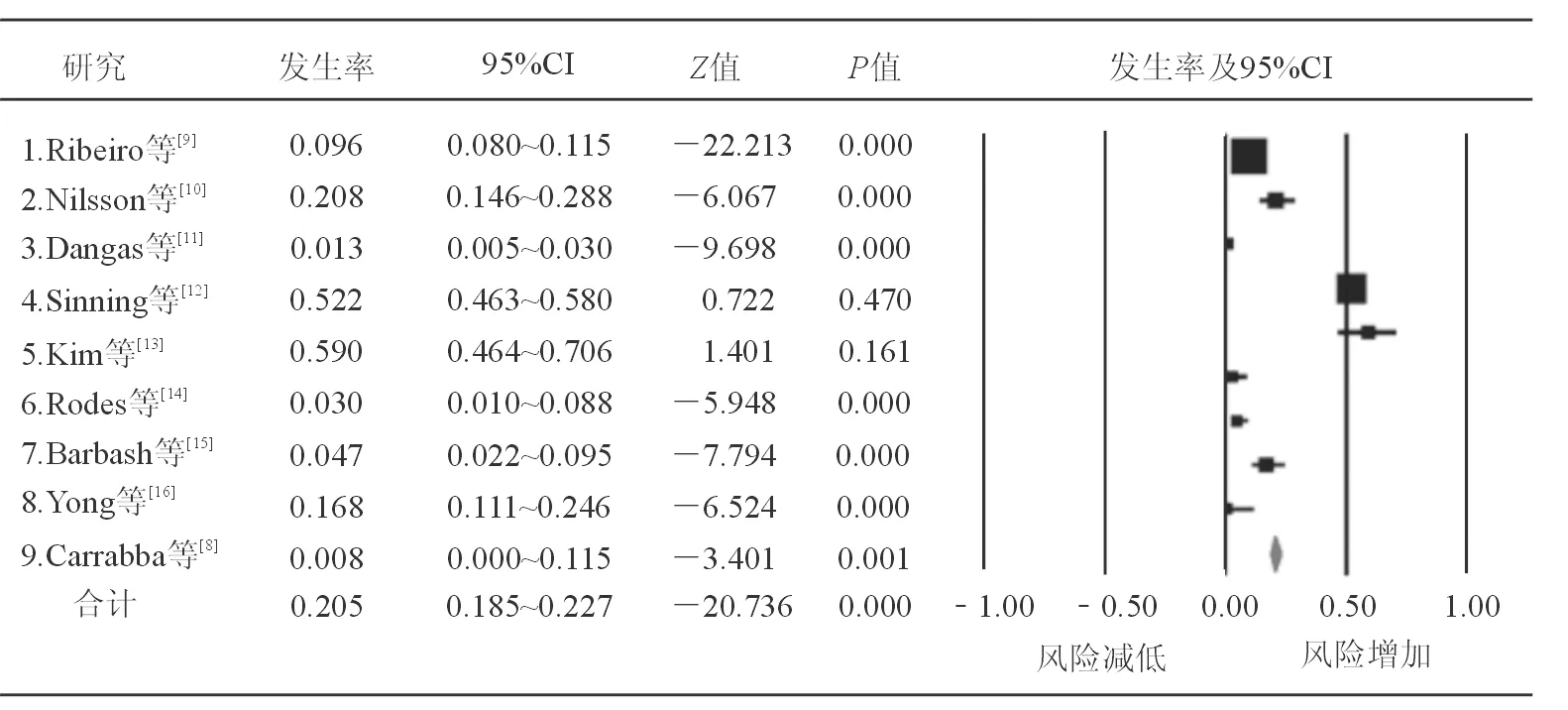
图1 TAVR术后心肌损伤发生率的荟萃分析
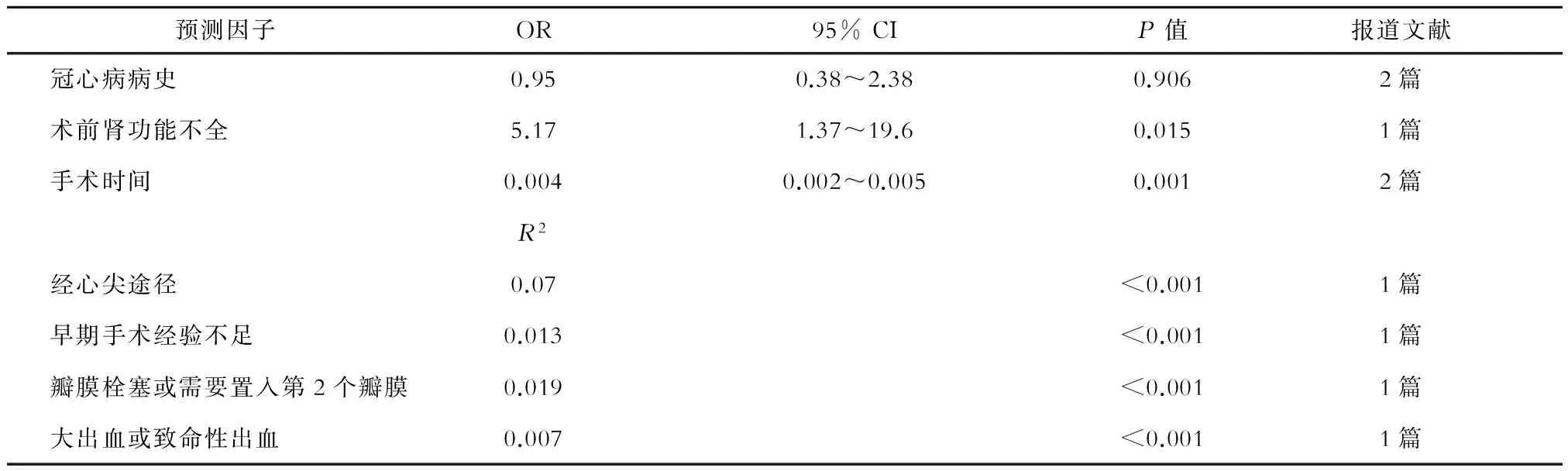
预测因子OR95%CIP值报道文献 冠心病病史0.950.38~2.380.9062篇 术前肾功能不全5.171.37~19.60.0151篇 手术时间0.0040.002~0.0050.0012篇R2 经心尖途径0.07<0.0011篇 早期手术经验不足0.013<0.0011篇 瓣膜栓塞或需要置入第2个瓣膜0.019<0.0011篇 大出血或致命性出血0.007<0.0011篇
2.3敏感性分析
每次删除一个研究,使用固定效应模型评价其对荟萃分析结果的影响,结果未发现某一研究使总体结局产生统计学改变。使用固定效应模型和随机效应模型所得结果相似,说明合并结果稳定性好,基本可靠。
3 讨论
2011年瓣膜学术研究协会(Valve Academic Research Consortium,VARC)对围手术期心肌梗死作出了明确定义[17]:术后72 h内出现新发缺血症状(如胸痛、呼吸困难等),并且心肌损伤标志物升高(推荐使用肌酸激酶同工酶,术后峰值超过参考上限值的10倍或者超过5倍并且至少有2个导联出现病理性Q波)。然而回顾本文所纳入的各项研究发现,大部分研究中符合严格定义的围手术期心肌梗死的报道较少,大多采取“心肌损伤”这一观察终点。这是因为这些研究中发现符合心肌梗死心肌酶学标准的患者并非都合并有缺血症状,并且缺血症状的报道具有很大的主观性,导致研究中对心肌梗死报道较少[18]。采用“心肌损伤”作为研究指标,并且利用心肌损伤标志物来定量分析和讨论手术对于心肌损伤的影响程度,成为了许多研究者的共识。本研究对各研究文献中心肌损伤标志物水平升高至符合心肌梗死标准的所有患者进行分析,而不论该患者是否出现缺血症状。本研究发现,并不是所有的研究都采用了VARC定义来获取TAVR术后心肌损伤相关的数据,也有部分研究采用了VARC-2定义[19]。因为考虑到在实际应用中使用经心尖途径手术时,使用体外循环会导致心肌受损,所以在2013年VARC-2定义中更新围术期心肌梗死标准为:心肌损伤标志物升高必须符合肌酸激酶同工酶升高5倍或肌钙蛋白升高15倍。
Carrabba等[8]的研究中,TAVR术后心肌损伤的发生率为0.8%,该研究根据VARC定义采用肌酸激酶同工酶或肌钙蛋白较基线水平升高作为诊断标准,患者均未采用经心尖途径手术,因此TAVR术后心肌损伤的发生率较低。而Kim等[13]研究报道的TAVR术后心肌损伤的发生率为59%,该研究采用VARC-2定义作为诊断围手术期心肌梗死的标准,结果发现根据术后72 h内肌钙蛋白峰值升高15倍这一标准,有59%的患者心肌损伤符合围手术期心肌梗死。该研究中有42.6%的患者采用了经心尖途径的手术方式,这可能与术后心肌损伤标志物水平升高直接相关。本研究发现,TAVR术后心肌损伤的总体发生率为20.5%,这表明目前TAVR术后的心肌损伤发生率仍较高。
研究发现,TAVR术后心肌损伤与术后9个月患者死亡率升高相关。研究TAVR术后心肌损伤的预测因子有助于更深入地了解其发生机制,并采取预防或针对性治疗措施,改善患者预后[14]。TAVR术后引起心肌损伤的原因很多。本研究发现,TAVR术后发生心肌损伤的独立预测因子包括经心尖途径、早期手术经验不足、瓣膜栓塞或需要置入第2个瓣膜、大出血或致命性出血、冠心病病史、手术时间、术前存在肾功能不全。首先,经心尖途径的手术方式对心肌损伤的风险较大。经心尖途径因需要体外循环支持,而体外循环时血液暴露于氧合器,使用肝素、鱼精蛋白、麻醉及手术异物均会引起补体激活和单核/巨噬细胞激活,进而诱发大量炎性细胞因子释放,引起心肌损伤。并且经心尖途径的手术时间较长,进一步延长了血流灌注不足的时间。其次,早期手术经验不足主要表现在球囊膨胀式瓣膜置入时,需要快速心室起搏的支持,这一操作会引起术中低血压和低血流灌注,而使用自膨胀式瓣膜时,则往往存在瓣膜型号偏大,置入过程中更易发生心肌机械压迫和损伤[15]。瓣膜栓塞或置入第2个瓣膜都会使原有的管腔面积变小,形成类似主动脉缩窄的情况,从而影响心肌灌注和心功能。其他如大出血或致命性出血、冠心病病史等均与手术中或术后缺血再次加重相关[9]。目前认为,术前肾功能不全所导致的心肌损伤与心肾综合征机制相似[15]。因此,任何导致心肌供血不足或机械损伤的因素,都会导致心肌损伤,反复缺血更会影响患者术后的心功能状态,这在最近发表的关于TAVR术后心肌核磁共振显像的研究中得到证实[14]。
本研究存在一定的局限性:(1)入选的文献均为非随机对照研究,样本量较小;(2)对于心肌损伤的定义没有统一;(3)入选文献中缺乏相应的原始心肌损伤标志物升高的数据;(4)并非所有纳入研究都可以提取完整和适合的数据,存在一定的偏倚。TAVR术后心肌损伤的发生机制及预防措施均需进一步研究。
[1]崔玲,白元,秦永文.主动脉瓣狭窄治疗策略的选择[J].国际心血管病杂志,2014,41(2):65-68.
[2]Adams DH,Popma JJ,Reardon MJ.Transcatheter aortic-valve replacement with a self-expanding prosthesis[J].N Engl J Med,2014,371(10):967-968.
[3]Kodali S,Pibarot P,Douglas PS,et al.Paravalvular regurgitation after transcatheter aortic valve replacement with the Edwards sapien valve in the PARTNER trial:characterizing patients and impact on outcomes[J].Eur Heart J,2015,36(7):449-456.
[4]Walther T,Thielmann M,Kempfert J,et al.PREVAIL TRANSAPICAL:multicentre trial of transcatheter aortic valve implantation using the newly designed bioprosthesis (SAPIEN-XT) and delivery system (ASCENDRA-Ⅱ)[J].Eur J Cardiothorac Surg,2012,42(2):278-283.
[5]Smith CR,Leon MB,Mack MJ,et al.Transcatheter versus surgical aortic-valve replacement in high-risk patients[J].N Engl J Med,2011,364(23):2187-2198.
[6]丛欣鹏,李新明.经导管主动脉瓣植入术研究现状及进展[J].国际心血管病杂志,2014,41 (3):154-157.
[7]郭丽娜,施仲伟.经导管Edwards-Sapien主动脉瓣植入术临床应用[J].国际心血管病杂志,2011,38(4):209-212.
[8]Carrabba N,Valenti R,Migliorini A,et al.Prognostic value of myocardial injury following transcatheter aortic valve implantation[J].Am J Cardiol,2013,111(10):1475-1481.
[9]Ribeiro HB,Nombela-Franco L,Munoz-Garcia AJ,et al.Predictors and impact of myocardial injury after transcatheter aortic valve replacement:a multicenter registry[J].J Am Coll Cardiol, 2015,66(19):2075-2088.
[10]Nilsson L,Appel CF,Hultkvist H,et al.Evaluation of the valve academic research consortium-2 criteria for myocardial infarction in transcatheter aortic valve implantation:a prospective observational study[J].PLoS One, 2015,10(6):e0130423.
[11]Dangas GD,Lefevre T,Kupatt C,et al.Bivalirudin versus heparin anticoagulation in transcatheter aortic valve replacement.A randomized phase 3 trial[J].J Am Coll Cardiol, 2015,66(25):2860-2868.
[12]Sinning JM,Hammerstingl C,Schueler R,et al.The prognostic value of acute and chronic troponin elevation after transcatheter aortic valve implantation[J].EuroIntervention,2016, 11(13):1522-1529.
[13]Kim WK,Rolf A,Liebetrau C,et al.Detection of myocardial injury by CMR after transcatheter aortic valve replacement[J].J Am Coll Cardiol,2014,64(4):349-357.
[14]Rodes-Cabau J,Gutierrez M,Bagur R,et al.Incidence,predictive factors,and prognostic value of myocardial injury following uncomplicated transcatheter aortic valve implantation[J].J Am Coll Cardiol,2011,57(20):1988-1999.
[15]Barbash IM,Dvir D,Ben-Dor I,et al.Prevalence and effect of myocardial injury after transcatheter aortic valve replacement[J].Am J Cardiol,2013,111(9):1337-1343.
[16]Yong ZY,Wiegerinck EM,Boerlage-van DK,et al.Predictors and prognostic value of myocardial injury during transcatheter aortic valve implantation[J].Circ Cardiovasc Interv,2012, 5(3):415-423.
[17]Leon MB,Piazza N,Nikolsky E,et al.Standardized endpoint definitions for transcatheter aortic valve implantation clinical trials:a consensus report from the Valve Academic Research Consortium[J].J Am Coll Cardiol,2011,57(3):253-269.
[18]Fearon WF,Yeung AC.Clinical relevance of myocardial injury after transcatheter aortic valve replacement[J].J Am Coll Cardiol,2015,66(19):2089-2091.
[19]Kappetein AP,Head SJ,Genereux P,et al.Updated standardized endpoint definitions for transcatheter aortic valve implantation:the Valve Academic Research Consortium-2 consensus document[J].J Thorac Cardiovasc Surg,2013,145(1):6-23.
(收稿:2015-12-07修回:2016-05-24)
(本文编辑:梁英超)
Meta-analysis of myocardial injury in patients with aortic stenosis undergoing transcatheter aortic valve replacement
ZHU Hao,REN Xiaomin,PAN Daorong,PANG Si,TIAN Nailiang,ZHANG Yaojun.
Department of Cardiology,Nanjing First Hospital,Nanjing Medical University,Jiangsu 210006,China
Objective:To systematically review the incidences,predictors of myocardial injury in patients undergoing transcatheter aortic valve replacement (TAVR).Methods:We searched PubMed,Springer,Elsevier-SDOL,EMbase,SSCI,VIP,CNKI,Chinese biomedical literature database,Wanfang data resource between January 2009 and November 2015 for the publications or reports regarding the myocardial injury after TAVR.The quality of enrolled studies was assessed using Loneycriteria.Meta-analyses were performed by Comprehensive Meta-Analysis Version 2.0 software.Results:Nine eligiblenon-randomized controlled registries with a total of 2 423 patients with severe aortic stenosis undergoing TAVR were included in the present meta-analysis.The incidence of myocardial injury after TAVR was 20.5% (95%CI:18.5~22.7).The independent predictors of myocardial injury after TAVR reported in these studies included:transapical approach,early experience,valve embolization/second valve,major or life threatening bleeding,history of coronary heart disease,procedure time,baseline renal insufficiency.Conclusion:The estimated incidence of myocardial injury after TAVR was as high as 20.5%,which may result in a poor prognosis.Identification and management of predictive factors of myocardial injury could help to improve the prognosis of patients.
Transcatheter aortic valve replacement; Myocardial injury; Predictor; Meta-analysis
210006南京医科大学附属南京医院(南京市第一医院)心血管内科
田乃亮,Email:tiannailiang@163.com
10.3969/j.issn.1673-6583.2016.03.016

