减肥类保健食品化学添加成分酚酞检测卡的研制
姚世平 刘光中 姚洪涛 周 轶 李心乐* 刘春秀 关 苗
减肥类保健食品化学添加成分酚酞检测卡的研制
姚世平①刘光中①姚洪涛①周 轶①李心乐①*刘春秀①关 苗①
目的:研制一种适合现场快速鉴定减肥类保健食品中酚酞的检测卡。方法:依据酚酞在碱性体系中反应形成粉红色醌式结构物原理,通过物理吸附将碱性体系中的有效组分附着到中性滤纸的材质上制备酚酞检测卡。酚酞检测卡与标准色阶图谱对比进行定性分析,与食品中危害因子及非法添加药物智能化综合检测仪配合;根据反射光谱法原理,将0.50 mg/g、1.00 mg/g、2.00 mg/g、3.00 mg/g和6.00 mg/g酚酞标准品与碱性体系反应生成醌式结构物浓度值内部拟合形成标准曲线,可定量分析确定待检品中酚酞的浓度。结果:酚酞检测卡在食品中危害因子及非法添加药物智能化综合检测仪检测以及同药典液相检测方法进行对比实验的结果符合率为90%~98%,证实酚酞检测卡具备较高的灵敏度。结论:研制的酚酞检测卡即可定性检测又可定量检测分析,适合各种快速检测减肥类保健食品酚酞含量的要求。
检测卡;酚酞;保健食品;试纸;快速;减肥类
[First-author's address] Beijing times Ken hengye technology development co., LTD, Beijing 100020, China.
酚酞商品名为果导片,是一种弱的有机酸,医用为接触性泻药,其刺激结肠黏膜增强并阻止肠内液体吸收,将水和电解质在结肠蓄积产生缓泻作用而促进排便。在临床上作为习惯性顽固便秘的处方药,但不宜长期使用。若长期服用酚酞可导致营养物质的丢失,而引起贫血、水电解质失衡体重过低、抵抗力下降以及营养不良等并发症[1-2]。酚酞化学名为3,3-双(4-羟基苯基)-1(3H)-异苯并呋喃酮,其分子式为C20H14O4,属于晶体粉末状,几乎不溶于水,易溶于乙醇。
目前,减肥类保健食品中酚酞基本采用拉曼光谱、高效液相色谱、薄层色谱法、液-质谱串联及分光光度计法[3-8]等方法检测,这些检测方法均有检测成本高、耗时较长及检测人员专业素质要求高等缺点[9-16]。为此,本研究研制一种适合现场快速鉴定减肥类保健食品中酚酞的检测卡。因酚酞常用做酸碱指示剂,其在酸性和中性溶液中为无色,在pH值>10的碱性环境中呈粉红色醌式结构物,故利用该显色原理制备酚酞检测卡[17-22]。酚酞检测卡与标准色阶图谱目测进行定性分析,配合食品中危害因子及非法添加药物智能化综合检测仪可以进行定量分析,由于其便携、操作简单以及可降低漏检率和错检率等特点,适用于现场快速鉴别检测减肥类保健食品中的化学药物成份。
1 仪器与材料
1.1仪器设备
UV2600型分光光度计(日本岛津企业管理有限公司);1220型高效液相色谱(济南赛畅科学仪器有限公司安捷伦科技有限公司);DZF6053型真空干燥箱(上海-恒科技有限公司);AT261精密电子天平(瑞士Mettle梅特勒仪器公司),UB-7型酸度计(德国赛多利斯股份有限公司);ZQ2000型微电脑自动斩切机(上海金标生物科技有限公司);XH-C型涡旋混匀器(金坛市自塔新宝仪器厂);食品中危害因子及非法添加药物智能化综合检测仪(北京倍肯恒业科技发展股份有限公司)。
1.2材料
酚酞100 mg(中国食品药品检定研究所);氢氧化钠、碳酸氢钠、氢氧化钾、烷基糖苷、十二烷基硫酸钠(SDS)、无水乙醇及活性炭均属国药集团化学试剂有限公司,分析纯;水为超纯水。材质为中性滤纸。
2 实验方法
2.1分光光度计法
2.1.1酚酞成分的鉴定实验
根据2015版药典进行酚酞成分的鉴定实验[23]。
(1)取酚酞数毫克,加氢氧化钠试液或热的碳酸钠试液2 ml,即溶解成红色的溶液;再加过量的碱液,红色随即消失。
(2)取含量测定溶液,采用紫外-可见分光光度法(通则0401)进行测定:①取酚酞标准品约38 mg,精密称定,置100 ml量瓶中,加入乙醇约60 ml,振摇使其溶解,加入0.01 mol/L盐酸溶液10 ml混匀,再用乙醇将其稀释至刻度后摇匀;②精密量取测定溶液10 ml,置入100 ml量瓶中,加入乙醇10 ml混匀,再用0.01 mol/L盐酸溶液稀释至刻度后摇匀;③采用紫外-可见分光光度法(通则0401),在275 nm的波长处测定吸光度,按C20H14O4的吸收系数为134进行计算;④在275 nm的波长处有最大吸收,在259 nm的波长处有最小吸收。
2.1.2酚酞醌式结构物检测实验范围
分别取酚酞标准品0、0.50 mg/g、1.00 mg/g、2.00 mg/g、3.00 mg/g、6.00 mg/g及8.00 mg/g稀释6倍后进行标准曲线的绘制,通过对比其OD值的变化区间,确定酚酞碱性体系显色后的检测范围。
2.2酚酞检测卡
2.2.1酚酞检测卡的制备
准确裁取中性滤纸8 cm×8 cm充分浸泡到试纸显色液,试剂显色液由氢氧化钠(0.001 mol/L)、氢氧化钾(0.02 mol/L)、碳酸氢钠(0.05 mol/L)、烷基糖苷(APG0810,5%)及十二烷基硫酸钠(SDS,2%);各组的体积配比为10∶5∶4∶1∶2;浸泡5 min后取出37 ℃烘干2 h备用。将处理好的试纸按照2 cm×0.4 cm裁剪成小条贴在底板上,制备成酚酞检测卡,铝箔袋密封保存。
2.2.2酚酞标准色阶的制备
配置0、0.50 mg/g、1.00 mg/g、2.00 mg/g、3.00 mg/g及6.00 mg/g酚酞标准系列溶液,按照酚酞检测方法分别测定,将显色后的试纸条用数码相机拍摄后制成标准色阶图谱。
2.2.3酚酞标准曲线的绘制
量取酚酞标准系列溶液0、0.50 mg/g、1.00 mg/ g、2.00 mg/g、3.00 mg/g及6.00 mg/g,按照检测方法,将显色后的酚酞检测卡放入食品中危害因子及非法添加药物智能化综合检测仪中进行测定,依据发射光谱原理读取对应灰阶色度值绘制标准曲线进行定量检测分析。
2.2.4三种保健食品样品
2.2.4.1样品前处理
(1)针对减肥咖啡类保健食品的前处理方法:称取0.5 g样品,放入10 ml离心管内,加入3 ml提取液和0.1 g提取物,振荡2 min,静置15 min后用0.45 µm微孔滤膜过滤,取滤液并加入等体积的纯净水,得到减肥咖啡类样品1~5。
(2)针对减肥茶保健食品的前处理方法:取约0.50 g样品碾碎,放入10 ml离心管内,加入3 ml提取液和0.25 g提取物,振荡2 min,静置15 min后用0.45 µm微孔滤膜过滤,取滤液并加入等体积的纯净水,得到减肥茶类样品1~5。
(3)针对左旋肉碱片剂减肥保健食品的前处理方法:取约0.5 g样品碾碎,放入10 ml离心管内,加入3 ml提取液和0.1 g提取剂及0.1 g提取物,先振荡2 min,之后每隔10 min振荡1 min,重复3次,静置10 min后用0.45 µm微孔滤膜过滤,取滤液并加入等体积的纯净水,得到减肥片剂样品1~5。
2.2.4.2加标实验
(1)针对减肥咖啡类、减肥茶类保健食品的加标方法:取约0.50 g样品碾碎,加入2.00 mg/g酚酞标准溶液1.0 ml,放入10 ml离心管内,加入3 ml提取液和0.25 g提取物,振荡2 min,静置15 min后用0.45 µm微孔滤膜过滤,取滤液并加入等体积的纯净水,分别记为减肥咖啡加标液1~5和减肥茶加标液1~5。
(2)针对左旋肉碱片剂减肥保健食品的加标实验方法:取约0.5 g样品碾碎放入10 ml离心管内,加入2.00mg/g酚酞标准溶液1.0 ml后混匀,加入3 ml提取液和0.1 g提取剂及0.1 g提取物,先振荡2 min,每隔10 min,振荡1 min,重复3次,最后静置10 min后,用0.45 µm微孔滤膜过滤,取滤液并加入等体积的纯净水,为减肥片剂加标液1~5。
2.3高效液相色谱方法
2.3.1酚酞标准品及样品色谱检测条件
通过文献分析确定液相检测条件。色谱柱:ZORBAX SB-C18柱(5 µm,4.6×150 mm,Agilent);流动相:水-乙腈(70∶30,v/v);检测波长为230 nm;柱温为30 ℃;进样量为10 µl;流速为1.0 ml/ min;检测时间为30 min。
2.3.2酚酞液相标准曲线的绘制
分别精确量取酚酞标准溶液0、0.50 mg/g、1.00 mg/g、2.00 mg/g、3.00 mg/g和6.00 mg/g稀释至检测范围,依据上述色谱条件检测出峰时间及峰面积。
2.3.3酚酞样品处理
(1)供试品溶液制备。将待检减肥类保健食品胶囊其1颗内容物约0.45 g,置于100 ml棕色容量瓶中,取甲醇溶解,超声处理10 min后定容摇匀,取续滤液为供试品溶液。
(2)对照品溶液制备。称定105 ℃干燥至恒重的酚酞对照品10 mg,置100 ml棕色容量瓶中,加入甲醇超声溶解,制备成100 µg/ml。精确量取100 µg/ml的酚酞标准溶液10 ml,用无水甲醇定容到100 ml容量瓶中制备成10 µg/ml。加甲醇适量超声溶解,加甲醇至刻度摇匀,即为对照品溶液。
(3)液相加标实验。取0.50 g碾碎样品于检测管中,加入2.0 mg/g酚酞标准溶液0.5 ml,置于200 ml棕色容量瓶中,取200 ml色谱甲醇溶解,超声处理10 min后定容摇匀,取得滤液,即为待检样品加标液。
3 实验结果
3.1分光光度法实验
3.1.1酚酞成分的鉴定
根据2015版药典进行酚酞成分的鉴定实验结果。
(1)将酚酞原溶液与pH值为12的碱性体系混合反应生成的醌式结构物显粉红色,再次滴加碱液变为无色。在分光光度计上200~900 nm进行光谱扫描,其分别有2个吸收峰:λ=553 nm,OD=0.214 ABS;λ=312 nm,OD=3.117 ABS;通过与酚酞原溶液出峰条件对比显示,λ为553 nm时为酚酞醌式结构物的最大吸收峰,可通过对比553 nm处OD的变化值作为判定依据,如图1所示。
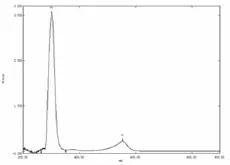
图1 酚酞显色后醌式结构物UV图谱
(2)取酚酞标准品38 µg/ml的乙醇(0.01 mol/L的盐酸溶液)200~500 nm下的光谱扫描,λ=283.60 nm,OD=0.144 ABS,证实酚酞紫外吸收峰为283.60 nm,如图2所示。
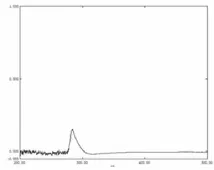
图2 酚酞原溶液UV图谱
3.1.2酚酞醌式结构物检测范围
分别取酚酞标准溶液0、0.50 mg/g、1.00 mg/ g、2.00 mg/g、3.00 mg/g、6.00 mg/g和8.00 mg/ g,稀释6倍后按照3.1.1(1)显色后进行标准曲线的绘制,通过对比其OD值的变化区间,初步确定酚酞碱性体系显色后的检测范围(见表1)。
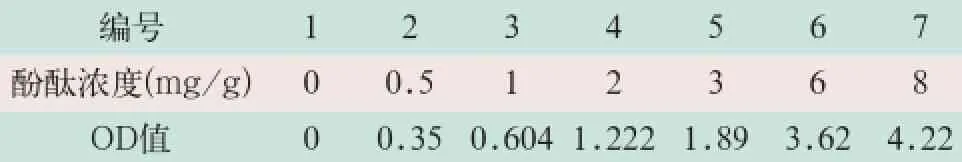
表1 酚酞浓度与显色醌式结构物OD数据
实验对比显示,酚酞与其在碱性条件下生成的粉红色醌式结构物成正比,以酚酞标准品浓度做横坐标,粉红色醌式结构物OD为纵坐标,得到的回归方程为公式1:

相关系数为0.999表明在0~6.0 mg/g的酚酞与其粉红色醌式结构物成一元关系,因浓度为6.00 mg/g 与8.00 mg/g显色后OD区分度不大,因此酚酞检测的显色反应范围为0~6.00 mg/g(如图3所示)。
3.2酚酞检测卡
酚酞检测卡由底板、吸水纸和酚酞试纸构成,如图4所示。
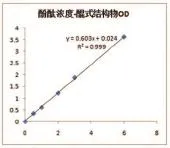
图3 酚酞浓度和显色醌式结构物线性关系图
图4 酚酞检测卡示意图
3.2.1标准色阶图谱的构成
将酚酞标准溶液与碱反应生成的醌式结构物变色情况用数码相机拍摄后制备(如图5所示)。

图5 标准色阶图谱
3.2.2酚酞标准曲线的制备
取0、0.50 mg/g、1.00 mg/g、2.00 mg/g、3.00 mg/g和6.00 mg/g酚酞标准溶液各70 µl分别滴加到酚酞检测卡上反应15 min,放置于食品中危害因子及非法添加药物智能化综合检测仪进行检测,检测结果见表2。
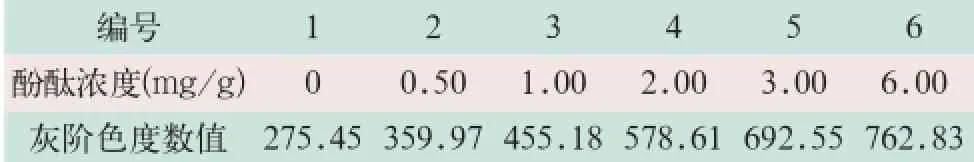
表2 酚酞检测卡显色后在食品中危害因子及非法添加药物智能化综合检测仪上灰阶色度值
检测显色结果如图6所示。

图6 酚酞检测卡梯度显色情况示图
检测酚酞浓度-灰阶色度值的线性关系结果如图7所示。
在食品中危害因子及非法添加药物智能化综合检测仪读取灰阶色度值。本研究中图6、图7显示,酚酞检测卡检测范围为0~6.00 mg/g,检测结果经过目测对比标准色阶图谱可定性,与食品中危害因子及非法添加药物智能化综合检测仪可进行定量分析。
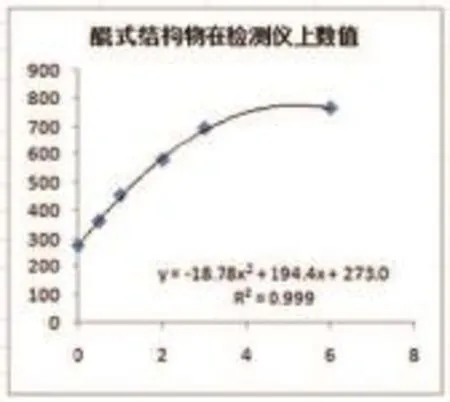
图7 酚酞标液与灰阶色度值线性关系示图
3.2.3三种保健类食品样品检测
3.2.3.1酚酞检测卡样品检测结果
将减肥咖啡、减肥茶及减肥片剂三类减肥保健食品各取5个样品用酚酞检测卡进行平行实验,取检测结果平均值,故减肥咖啡类保健食品中酚酞含量为1.15 mg/g,其变异系数(coefficient of variation,CV)为4.00%;减肥茶保健食品中酚酞含量为0.53 mg/g,其CV为4.39%;减肥片剂中酚酞含量为1.69 mg/g,其CV为3.49%。酚酞检测卡样品检测结果见表3。
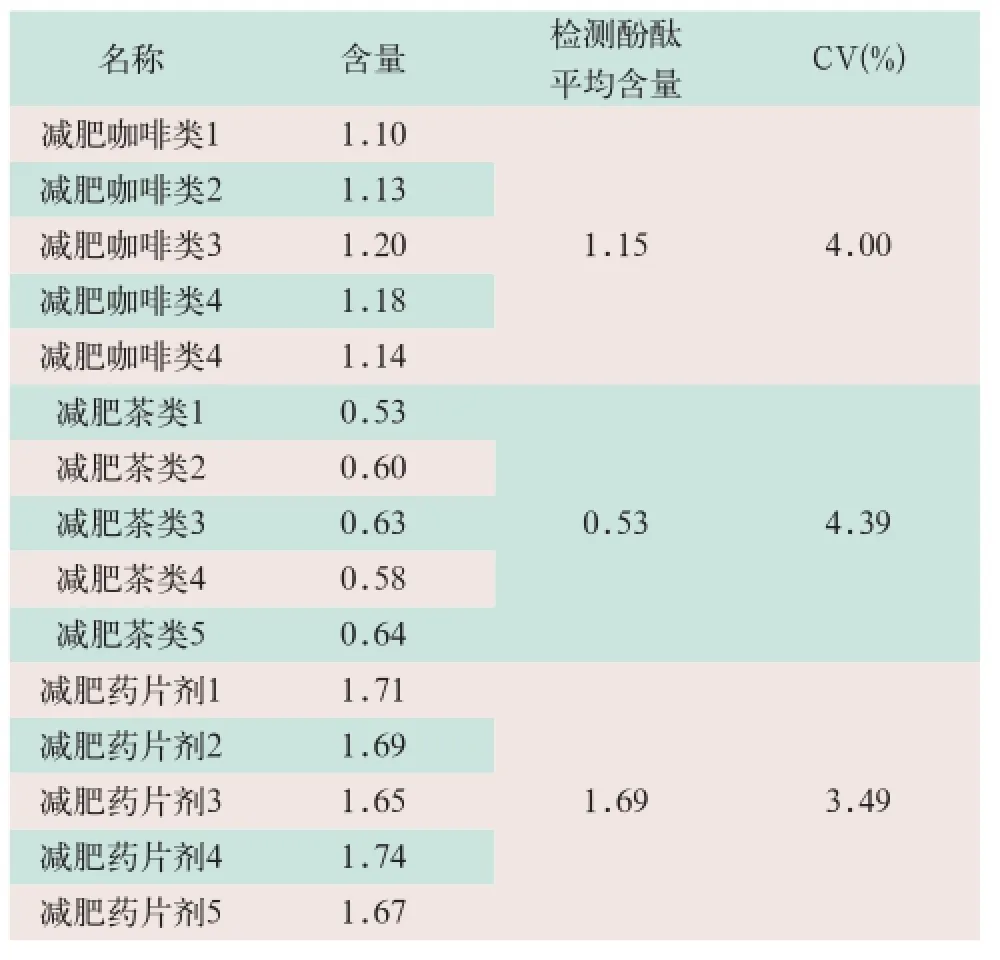
表3 酚酞检测卡样品加标情况一览表(mg/g)
3.2.3.2加标实验结果
分别在减肥咖啡、减肥茶及减肥片剂三类减肥保健食品进行检测的样品中添加2.00 mg/g的酚酞,其酚酞检测卡样品加标检测结果见表4。
3.3高效液相色谱检测
3.3.1酚酞标准品及样品色谱检测条件
实验结果显示,酚酞标准品在高效液相色谱中共检测30 min,出峰时间为8.621 min,峰面积为243.16,对称因子为0.90,其色谱图如图8所示。
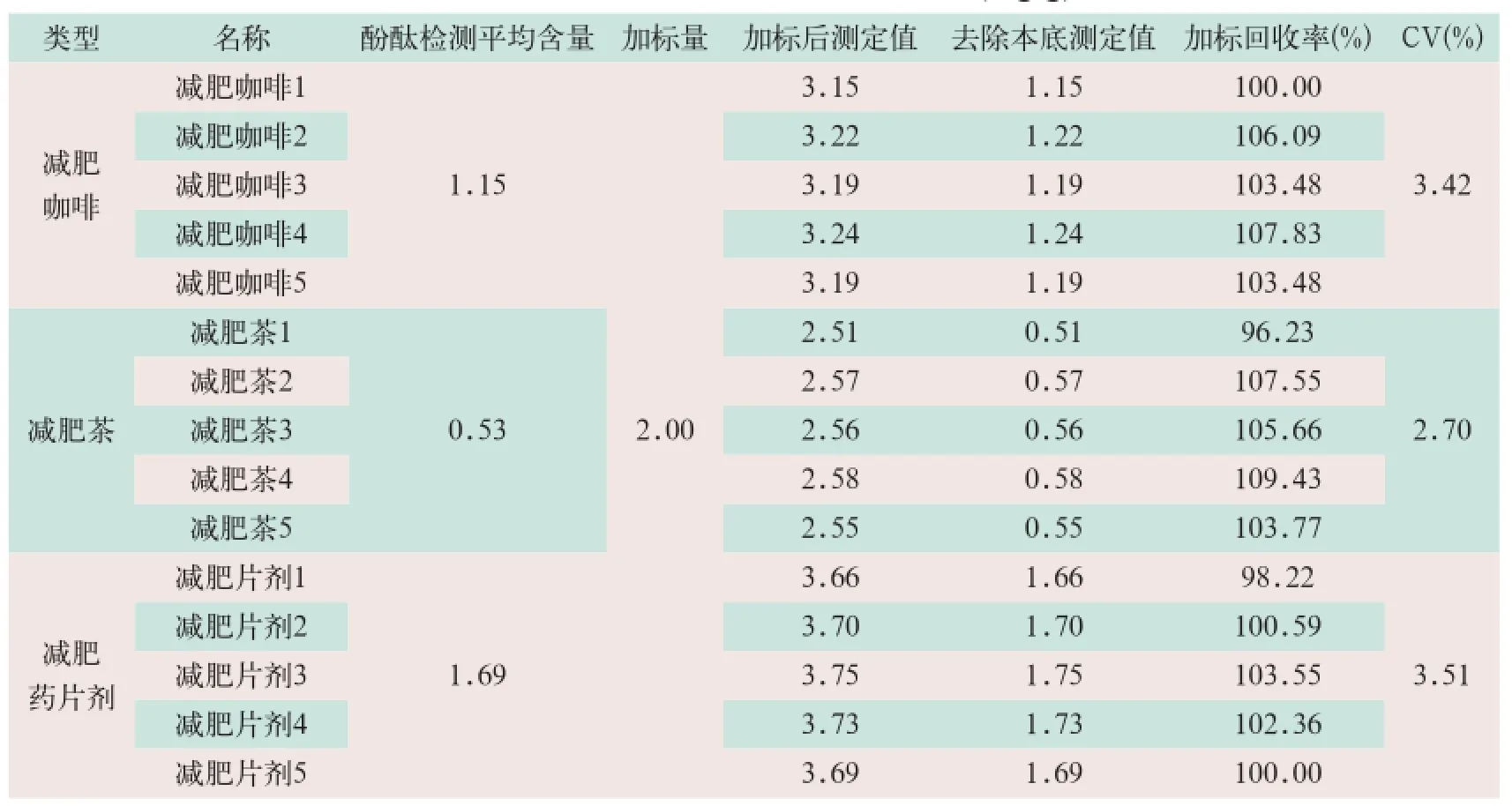
表4 酚酞检测卡样品加标检测结果(mg/g)
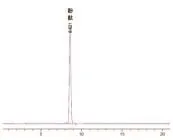
图8 酚酞标准溶液出峰图谱
3.3.2酚酞液相标准曲线的绘制
分别精确量取酚酞标准溶液0、0.50 mg/g、1.00 mg/g、2.00 mg/g、3.00 mg/g和6.00 mg/g,稀释至检测范围,依据上述色谱条件检测出峰时间及峰面积,见表5,如图9所示。
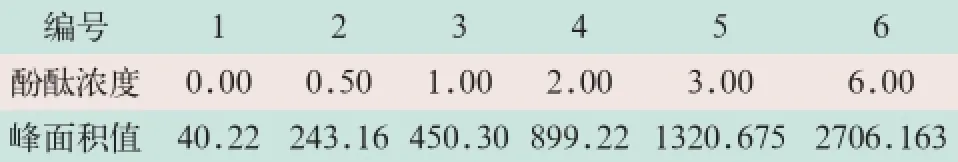
表5 酚酞液相标准曲线参数(mg/g)
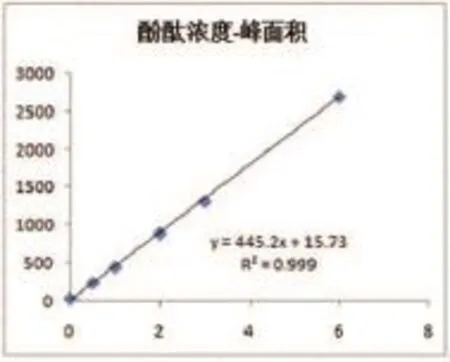
图9 酚酞浓度—液相峰面积线性关系图
图9显示,以酚酞溶液浓度为横坐标,酚酞在8.63 min出峰时间为纵坐标,其呈正比关系建立标准曲线方程,其一元线性方程为Y=445.2X+15.73, R2=0.999。
3.3.3样品
3.3.3.1样品测定结果
按照色谱检测条件进行样品前处理及三种样品的酚酞含量检测,其检测结果见表6。
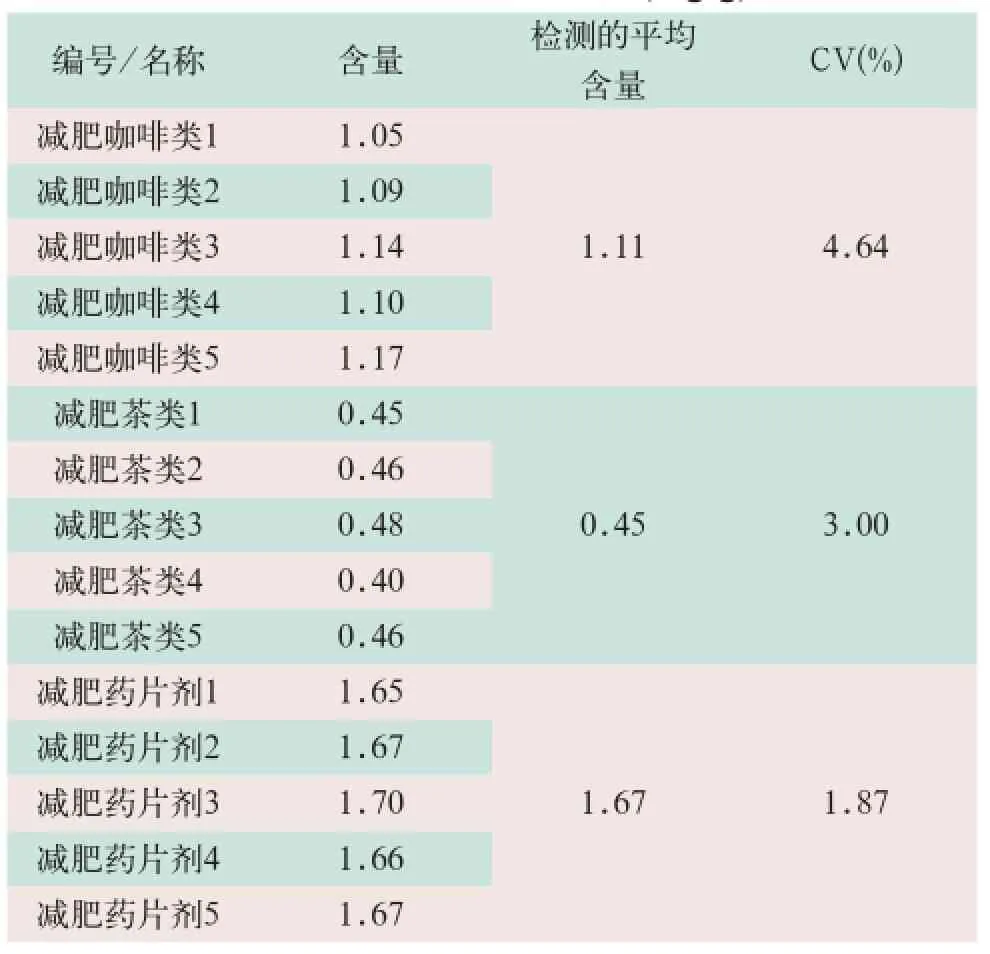
表6 酚酞液相检测结果(mg/g)
将减肥咖啡类、减肥茶类和减肥片剂类三种保健食品分为5个样品,采用酚酞高效液相色谱方法进行平行实验,取检测结果的平均值,故减肥咖啡中酚酞含量为1.11 mg/g,CV为4.64%;减肥茶中酚酞含量为0.45 mg/g,CV为3.00%;减肥片剂中酚酞含量为1.67 mg/g,CV为1.87%。
3.3.3.2加标实验方法
按照2.3.2进行样品加标检测实验,高效液相色谱检测减肥咖啡中酚酞的含量为1.11 mg/g,其加标回收率为98%~110%,其平均的CV为4.12%;减肥茶中酚酞含量为0.45 mg/g,其加标回收率为95%~110%,CV为2.55%;减肥药片剂中酚酞含量为1.67 mg/g,其加标回收率为95%~110%,CV为3.35%。见表7。
高效液相色谱方法与酚酞检测卡共同检测减肥类保健食品并进行对比实验,高效液相色谱方法的样品中加标2.00 mg/g时,加标回收率均为95%~110%,其检测CV为2.00%~4.00%;酚酞检测卡加标回收率为95%~110%,其检测CV为2.50%~4.50%,通过对比可知,酚酞检测卡精密度、加标回收率等检测性能等效于药典标准方法(见表8)。
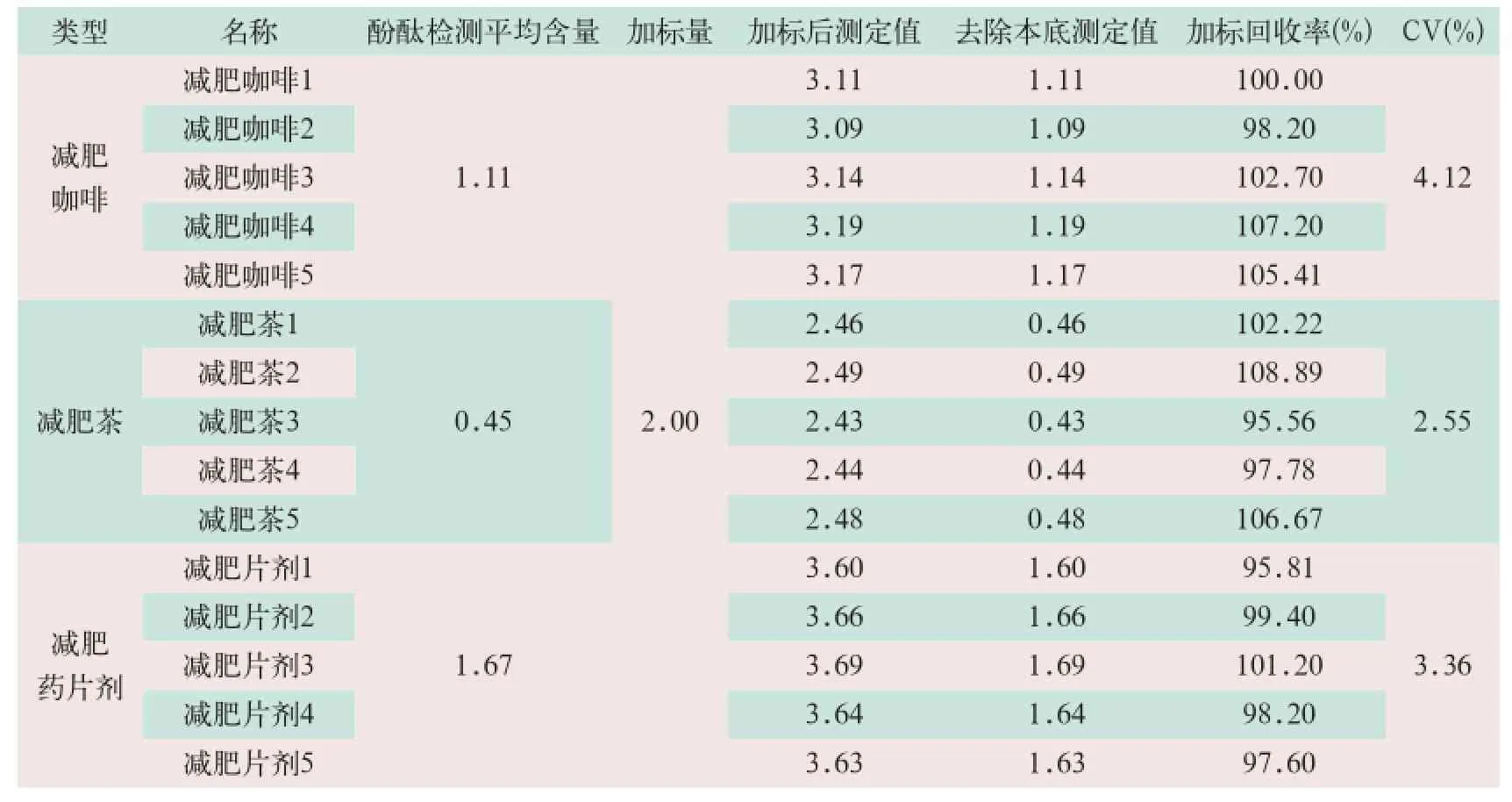
表7 酚酞液相加标检测结果(mg/g)

表8 酚酞检测卡与高效液相色谱检测结果对比(mg/g)
4 结论
本研究参照2015药典方法经过工艺改良制备的酚酞检测卡,鉴定减肥保健类食品中的非法添加化学药物酚酞。酚酞检测卡灵敏度为0.50 mg/g,检测范围为0~6.00 mg/g,检测时间为15 min,样品前处理时间与样品检测总时间≤30 min,既可与标准色阶图谱比较可定性分析,又可与食品中危害因子及非法添加药物智能化综合检测仪配合定量的检测。酚酞检测卡可现场直接检测,因针对不同组分的样品,采用针对性的前处理方法,避免了快检中容易出现的误检、漏检问题。酚酞检测卡具有快速、准确及操作简单等特点,适用于卫生执法现场对保健食品检测,为一线食品安全执法提供科学依据。
[1]余翠琴,张凡.慎用泻药[J].中国临床药学杂志,2002(9):307-308.
[2]张谊,张秀娟.滥用泻药可致生命危险[J].首都医药,2005(15):35.
[3]甘盛,韩婷,李志成,等.减肥中成药中非法添加酚酞的拉曼光谱快速检测[J].中国实验方剂学杂志,2014,11(1):20-21.
[4]袁春晖,冯家力,潘振球,等.保健减肥食品中酚酞的测定方法研究[J].中华预防医学杂志,2006,40(5):362-364.
[5]马微,王海波,马强,等.减肥保健食品中非法添加酚酞和西布曲明的同时检测[J].食品科学,2010,31(4):23-24.
[6]黄诺嘉,杨文红,黄奕滨.减肥类中成药、保健食品、食品中非法添加酚酞、西布曲明等化学成分的快筛检测方法研究[J].食品与药品,2011,13(2):114-117.
[7]姚莉,陈景国,陈冬.减肥类保健品中非法添加化学药品的快速筛查[J].淮海医药,2012,30(6):110-111.
[8]黄诺嘉,杨文红,黄奕滨.减肥产品中非法添加酚酞的检测方法研究[J].今日药学,2010,20(12):23-29.
[9]胡青,崔益泠,王珂,等.减肥类保健食品中非法添加酚酞定性定量检测方法的研究[J].中国药学杂志,2007,42(8):624-626.
[10]黄芳,吴惠勤,黄晓兰,等.高效液相色谱-串联质谱法同时测定保健品中非法添加的六种减肥化学品[J].分析测试学报,2013,32(6):12-15.
[11]毛庆,张小松.中成药和保健品中非法添加减肥类化学物质的快检[J].中国药业,2010,19(18):41-42.
[12]宋景梅.紫外分光光度法测定酚酞及酚酞片的含量[J].药物分析杂志,1990,10(2):115-118.
[13]秦宗会,谢兵.紫外光谱法测定曲美胶囊中的盐酸西布曲明[J].光谱实验室,2005,22(5):1025-1027.
[14]祁爱桂,李桂兰,陈静.紫外法与间接碘量法测定酚酞片含量的比较[J].黑龙江医药,1995,8(4):212-214.
[15]程民.HPLC法测定酚酞含片的含量[J].安徽医药,2007,11(8):713-713.
[16]季颖,施荟,江志强,等.液质联用测定犬血浆中盐酸西布曲明浓度和药动学[J].中国临床药学杂志,2006,15(6):365-368.
[17]Sayin T,Güldal M.Sibutramine:possible cause of a reversible cardiomyopathy[J].Int J Cardiol,2005,99(3):481-482.
[18]Clark DW,Harrison-Woolrych M.Sibutramine may be associatedwith memory impairment[J]. BMJ,2004,329(7478):1316.
[19]Wooltorton E.Obesity drug sibutramine (Meridia):hypertension and cardiac arrhythmias[J]. CMAJ,2002,166(10):1307-1308.
[20]Radhakrishna T1,Narayana CL,Rao DS,et al. LCmethod for the determination of assay and purity of sibutramine hydrochloride and its enantiomers by chiral chromatography[J].J Pharm Biomed Anal,2000,22(4):627-639.
[21]Li Ding,Xinyu Hao,Xin Huang,et al.Simultaneous determination of sibutramine and its N-desmethyl metabolites in human plasma by liquid chromatography-electrospray ionizationmass spectrometry method andclinical applications[J].Chromatography B,2003,492:241-248.
[22]Chen J,Lu W,Zhang Q,et al.Determination of the active metabolite of sibutramine by liquid chromatography-electrospray ionization tandem mass spectrometry[J].J Chromatogr B Analyt Technol Biomed Life Sci,2003,785(2):197-203.
[23]国家药典委员会.中华人民共和国药典(二部)[M].北京:北京医药科技出版社,2015.
The development of chemical ingredients of phenolphthalein test card in health weight-reducing food/
YAO Shi-ping, LIU Guang-zhong, YAO Hong-tao, et al//
China Medical Equipment,2016,13(8):11-17.
Objective: To develop a rapid detection card of Phenolphthalein illegal add chemicals in the health weight-reducing food suitable for rapid identification on site. Methods:On the basis of phenolphthalein pink complex principle in alkaline system reaction, the effective components of alkaline system attached to the neutral filter material on the preparation of phenolphthalein test card by physical adsorption. The qualitative analysis was analyzed between phenolphthalein test card and standard color order spectrum, which coordinated with harmful factors in food and illegal add drugs intelligent integrated detector. According to the principle of reflection spectroscopy,phenolphthalein standard reaction of 0.50mg/g, 1.00mg/g, 2.00mg/g, 3.00mg/g and 6.00mg/g and alkaline system generated inside the complex density form standard curve fitting, in order to analyze the concentration quantitatively to determine the quarantine of phenolphthalein. Results: Using phenolphthalein test card harmful factors in food drugs, illegal add intelligent integrated detector test results and comparative experiments with pharmacopoeia liquid phase detection method, the coincidence rate were from 90% to 98%, confirming phenolphthalein dipstick test card has higher sensitivity. Conclusion: Development of phenolphthalein inspection card can be used in qualitative test and quantitative analysis, suitable for all kinds of rapid detection of the requirements of the content of phenolphthalein health weight-reducing food.
Test card; Phenolphthalein; Health food; Test paper; Rapid; Slim chemical composition
1672-8270(2016)08-0011-07 [中图分类号]R155.51
A
姚世平,男,(1963- ),硕士,高级工程师。北京倍肯恒业科技发展股份有限公司董事长兼总裁,从事医疗装备、食品安全和药品检测工作。
10.3969/J.ISSN.1672-8270.2016.08.004
①北京倍肯恒业科技发展股份有限公司 北京 100020
lixinle@biochemgroup.net
2016-03-02

