Hr基因敲除小鼠模型的构建和表型分析
朱奎成,徐存拴,陈莹莹,王纯耀,章金涛
(1.河南师范大学生命科学学院,新乡 453007;2.郑州大学实验动物中心,郑州 450052)
Hr基因敲除小鼠模型的构建和表型分析
朱奎成1,2,徐存拴1,陈莹莹2,王纯耀2,章金涛2
(1.河南师范大学生命科学学院,新乡453007;2.郑州大学实验动物中心,郑州450052)
目的建立基因敲除小鼠以深入研究无毛基因(hairless,Hr)的功能。方法利用类转录激活因子效应因子核酸酶 (transcription activator-like effector nucleases,TALENs) 技术,制备Hr基因敲除小鼠,观察基因敲除小鼠毛发生长发育规律,并取部分皮肤组织石蜡切片,显微镜下分析结果。结果获得一个在Hr基因编码区86~87位有2个碱基缺失的首建鼠,产生了TGA终止密码子。通过与野生型鼠杂交获得阳性子代,进行同窝交配,传至第2代小鼠14 d开始脱发,30 d左右毛发脱净,并终身保持无毛。皮肤组织学观察发现真皮内形成大小不等的包囊。研究结果表明成功建立的Hr基因敲除小鼠表现出毛发生长异常。结论证明了无毛基因与毛发生长发育的密切关系,为研究Hr基因的精确功能提供了良好的动物模型。
无毛基因;基因敲除;小鼠;表型
脱发或称秃发是一种常见的人类疾病。毛发生长和脱落的调节是一个高度复杂的过程,受到许多基因的调控[1]。寻找影响毛发生长和脱落的重量级因子,将为阐明毛发生长周期的调控机制,研发有效治疗脱发性疾病的药物提供新的思路和治疗手段。无毛小鼠(hairless mice)是一种皮肤和被毛结构发生异常变化的小鼠,该种小鼠出生后第一次毛发生长正常,大约在14 d开始从头部向尾部脱毛,正常情况下1周内被毛全部脱净,并终生保持无毛状态,其表型类似于人的丘疹性无毛症(papular atrichia)[2],是皮肤病及毛发生长研究的良好实验动物模型,由于无毛小鼠的无毛表型是因为一个被定位于14号染色体上的功能基因突变所致[3],因此,该基因被命名为“无毛基因”(hairless gene,Hr)。近十年来,有关小鼠Hr基因等位自发突变动物的报道达16个之多,这些研究结果揭示了Hr基因突变与多样化表型之间的复杂关系[4-5],成为研究毛发生长脱落机制的重要实验材料,但进展缓慢。作者认为,建立遗传突变动物,进一步分析无毛基因的精确功能和毛囊周期的调控途径有助于探明Hr基因致脱发的发病机制,并为人的脱发、斑秃等毛发疾病研究提供重要的新线索。本研究利用 TALENs 技术建立了Hr基因敲除的小鼠模型提供基础资料。
1 材料和方法
1.1实验动物
C57BL/6J小鼠购于北京维通利华实验动物技术有限公司 ( SCXK( 粤) 2013-0032)。饲养于郑州大学实验动物中心SPF级动物房,许可证号:SYXK(豫)2016-0002。饲料购自郑州大学实验动物中心,经60Co辐照灭菌。
1.2TALENs 载体的构建和体外转录
根据NCBI 上Hr基因序列,利用TALEN 在线设计工具( http://zifit.partners.org/ZiFiT//ChoiceMenu.aspx) 设计基因敲除位点。左右靶点的识别模块经golden gate 方法组装完成后,克隆到载体上构建成pRP[TALEN]-Hygro-CMV>22nt_TGTGAACGGCATTGT GGGACAG真核表达载体。线性化后,在T7 启动子的作用下体外转录为mRNA注射到C57BL/6J的受精卵中,挑选注射后状态良好的受精卵,移植到假孕母鼠的输卵管内,待其自然生下F0代小鼠。
剪取经原核注射产生的1周龄首建鼠的鼠尾组织,提取基因组DNA,利用引物扩增目的片段,PCR 上游引物为:5′- CTCATGCTTTGTCCTTACCCTCC AG-3′,下游引物为:5′-CACCAGTGAGAGTGTGTCC TTGGG-3′,对扩增出的PCR产物进行测序,与C57BL/6J小鼠基因目的序列比对,分析靶点序列缺失情况。
1.3基因敲除小鼠繁殖及表型分析
显微注射获得F0代小鼠分别与野生型的C57BL/6J交配,对交配获得的F1代小鼠进行基因型鉴定,分别建系。将来自同一只F0的阳性F1代小鼠同胞交配,可获得F2代小鼠,对F2代小鼠进行基因型鉴定。理论上F2代小鼠中25%的几率为Hr-/-纯合子小鼠。
出生后每天观察小鼠被毛及皮肤形态的变化,详细记录。皮肤组织学观察:动物颈椎脱臼法处死,取背部中央皮肤, 体积分数10%甲醛溶液固定,脱水, 石蜡包埋, 切片,HE染色, 显微镜下观察, 拍照。
2 结果
2.1Hr敲除小鼠的构建及PCR 鉴定
根据小鼠Hr核酸序列信息,针对外显子设计两处相邻的靶序列进行TAL识别模块构建,将这两个相邻靶点识别模块融合克隆到FokI 的N-末端,形成真核表达载体,原核注射到C57BL/6J小鼠的受精卵中,移植到假孕鼠子宫内,共出生13只幼仔,剪取7日龄的鼠尾组织,提取基因组DNA,PCR 扩增,测序与C57BL/6J小鼠基因序列比较,其中10#小鼠在Hr编码区86~87位共2个碱基的缺失,产生了TGA终止密码子(图1)。
2.2基因敲除小鼠繁殖及表型初步分析2.2.1形态观察:基因敲除小鼠出生后被毛生长正常,与有毛小鼠无法区分。大约2周左右,基因敲除纯合子小鼠开始从背部开始脱毛(图2 A),然后延伸至头颈部及尾部。1月龄时毛发基本脱落殆尽,仅保留极少分散毛发,皮肤为肉色偏红, 皮肤薄,头、颈部有较细的皮肤皱纹(图2 B),并随年龄增长,皮肤变厚,颜色加深,更加松弛并终身保持无毛状态。2.2.2组织学:14日龄敲除小鼠皮肤可见毛囊上部的毛管部宽大形成椭圆囊,毛囊解体,毛球部和毛乳头滞留于真皮内(图3 A)。1月龄敲除小鼠皮肤小囊内含一些角化碎屑样物质,真皮层中见几排大小不等的包囊(图3 B)。14日龄(图3 C)和1月龄(图3 D)对照小鼠真皮中见多量发育正常的毛囊。

A: -示碱基缺失部分;B: 上图为正常C57BL /6J小鼠,下图为基因敲除小鼠;箭头示碱基缺失位点。图1 测序结果序列比对图(A)和测序图(B)A: The short dotted lines represent the knockout bases. B: Sequence comparison and sequence map of different mice. The wild-type sequence is shown at the top. The arrow shows deletion sites.Fig.1 Sequence comparison and sequence map

A: 14日龄敲除小鼠全身毛发稀疏;B: 1月龄敲除小鼠毛发基本脱净。图2 转基因小鼠脱毛规律及皮肤表型的变化A: Note the sparse hair at 14 days of age. B: Hair is almost completely missing at one month of age.Fig.2 Hair loss in the hr knockout mice and changes of the skin phrnotype
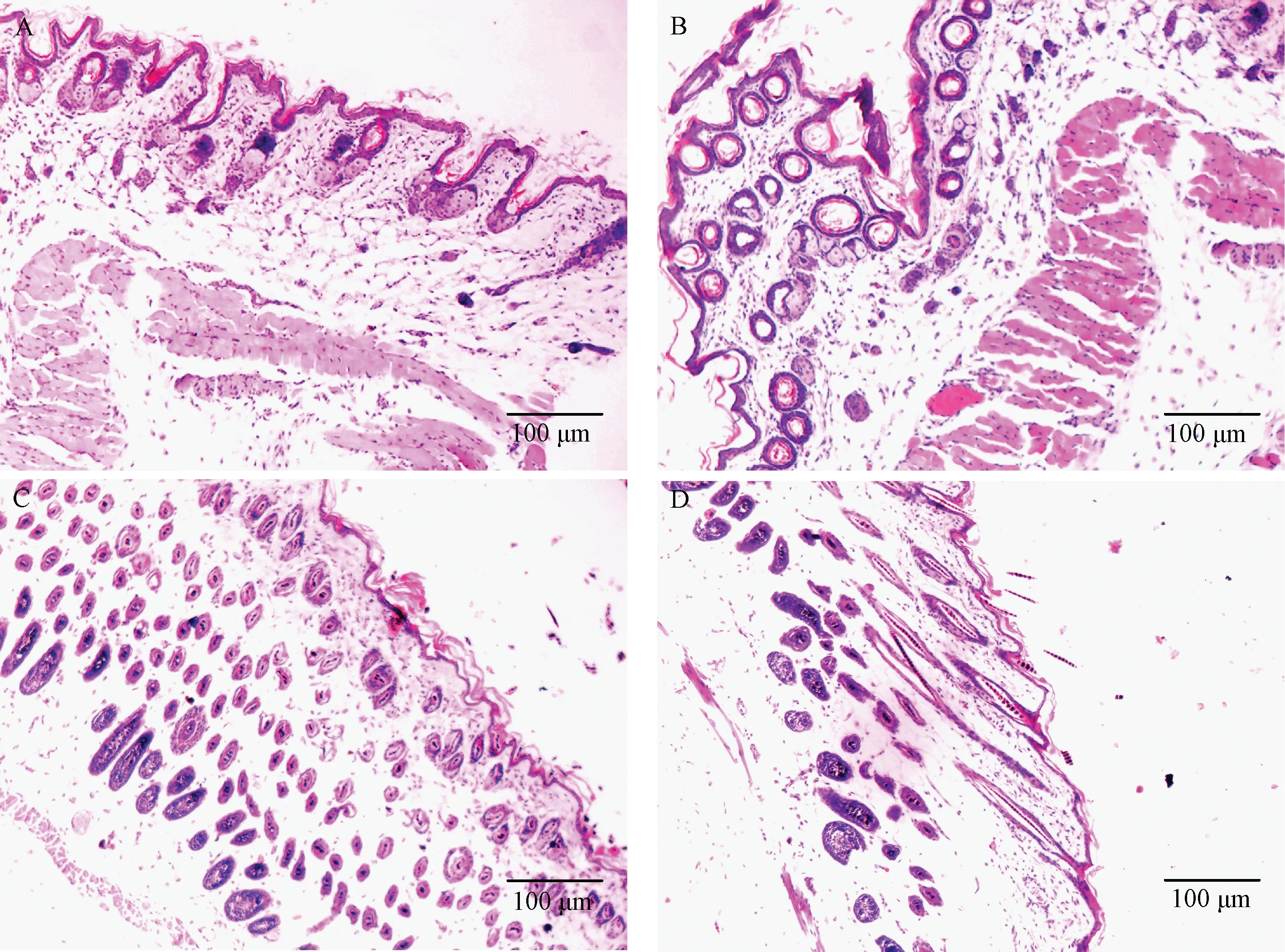
A: 14日龄敲除小鼠毛囊上部的毛管部宽大形成椭圆囊。B: 1月龄敲除小鼠真皮深层及皮下组织有几排大小不等的包囊。C:14日龄C57BL /6J小鼠毛囊。D:1月龄C57BL /6J小鼠毛囊。图3 基因敲除和C57BL /6J小鼠皮肤组织学观察(HE,标尺=100 μm)A: The widened hair canals of upper follicle form multiple utricles in a 14-day-old Hr knockout mice. B: Note the several rows of dermal cysts in a 1-month-old Hr knockout mouse. C: Normal hair follicles in a 14-day old control mouse. D: Hair follicles in a wild-type mouse developed normally at day 30.Fig.3 Histologic appearance of skin in the Hr knockout mice(HE,Bar=100 μm)
3 讨论
无毛基因是一个多效基因,位点的突变,不仅造成完全和持久的无毛,而且还导致免疫与繁殖的异常(Ignatieva et al,1988)、淋巴瘤易感性的增高(Meier et al,1969)、二口恶英毒性敏感性的增加等[6]。到目前为止,无毛基因已发现了16个等位基因,如hairless(hrhr)突变、rhino(hrrh)突变、Hrrh-J突变、Hrrh-R突变等。不同等位基因间即具有共同特征,如程序化的脱毛方式,皮肤皱褶,育仔困难,免疫受损,真皮包囊出现等[7]。目前,通过建立转基因动物模型来研究基因的生物学功能,已越来越普遍地被研究者所接受[8]。基因敲除是证明基因功能不可缺少的逻辑环节,是研究基因功能最直接有效的方法之一。TALEN 作为一种高效的基因编辑工具, 当其在基因组上产生双链断裂后,可以通过NHEJ修复方式产生基因敲除[9]。
课题组采用用TALENs 技术构建了Hr基因敲除小鼠,测序发现hr编码区86~87位共2个碱基的缺失,产生了TGA终止密码子。基因敲除小鼠生长发育观察发现,小鼠出生后14 d开始从头颈部、背部、尾部开始脱毛,表现为稀毛特征,最后全身脱净,并终生保持无毛状态。皮肤组织学观察发现毛发生长缺陷,皮肤内毛囊瓦解,并形成许多椭圆囊及真皮包囊,与无毛基因自发突变研究结果一致[10]。本研究敲除小鼠的获得说明Hr基因影响了毛囊的正常生长发育,机理可能在于基因缺失致其基因产物-无毛蛋白的丧失,无毛蛋白是一个H3K9去甲基化酶,可通过直接控制其靶基因,调节表皮的内稳态[11]。利用本试验建立的基因敲除小鼠模型,对深入了解Hr基因在毛发生长发育中表达调控的分子机制,鉴别控制毛发生长的关键基因并研究它的作用机制,可能为最终揭开人类脱发的奥秘,发展有效治疗药物,解决毛发再生难题提供了有价值的材料。
[1]Stenn KS, Paus R. Controls of hair follicle cycling [J]. Physiol Rev, 2001, 81: 449-494.
[2]Porter RM. Mouse models for human hair loss disorders [J]. J Anat, 2003, 202: 125-131.
[3]Jones JM, Elder JT, Simin K, et al. Insertional mutation of the hairless locus on mouse chromosome 14 [J]. Mamm Genome,1990, 4(11): 639-643.
[4]Yip L, Horev L, Sinclair R, et al. Atrichia with papular lesions: a report of three novel human hairless gene mutations and a revision of diagnostic criteria [J]. Acta Derm Venereol, 2008, 88: 346-349.
[5]Benavides F, Oberyszyn TM, VanBuskirk AM, et al. The hairless mouse in skin research [J]. J Dermatol Sci, 2009, 53: 10-18.
[6]Kim JE, Song D, Kim J, et al. Oral supplementation with cocoa extract reduces UVB-induced wrinkles in hairless mouse skin [J]. J Invest Dermatol, 2015, 11: 455-457.
[7]王冬平, 栾蓉晖, 李善如, 等. BALB/c突变无毛小鼠特异性免疫功能的研究 [J]. 中国实验动物学报, 2003, 11(1): 23-25.
[8]孙振红, 苗向阳, 朱瑞良, 等. 动物转基因新技术研究进展 [J]. 遗传, 2010, 32(6): 539-547.
[9]Miller JC, Tan S, Qiao G, et al. A TALE nuclease architecture for efficient genome editing [J]. Nat Biotechnol, 2011, 29(2): 143-148.
[10]章金涛, 付淑莉, 王纯耀, 等. 无毛小鼠不同年龄皮肤结构的比较研究 [J]. 中国实验动物学报, 1998, 6(1): 37-41.
[11]Liu L, Kim H, Casta A. Hairless is a histone H3K9 demethylase [J]. FASEB J, 2014, 8: 1534-1542.
Construction of a Hr mutant knockout mouse model and phenotypic analysis
ZHU Kui-cheng1,2,,XU Cun-shuan1,WANG Chun-yao2,CHEN Ying-ying2,ZHANG Jing-tao2
(1. College of Life Science, Henan Normal University, Xinxiang 453007, China;2. Laboratory Animal Center of Zhengzhou University, Zhengzhou 450052)
ObjectiveTo establish aHrmutant knockout mouse model to study the function ofHrgene. Methods Transcription activator-like effector nucleases ( TALENs) technique was used to disrupt the mouseHrlocus,creating heritable mutations that eliminateHrfunction to explore the effects ofHron hair development and provide a good model to study the function of Hrgene.The phenotype of Hr-/-mice was observed after birth and skin histology of the transgenic mice was studied by light microscopy. ResultsIt was shown that a F0 mouse with the 2-bp deletion inHrgene ranging from 86 to 87 base pairs was obtained. The male mice with clear deletion of theHrfragment and with obvious frame shifting were mated with wild-type female mice, and F1mice were achieved.The heterozygous males mated with females to generate the F2homozygous mice. The first hair coat ofHr-/-mice developed normally. Beginning from 14 days after birth, however, there was a rapid hair loss. The mices were completely hairless except for a few vibrissae at 30 days. Histologically, two characteristic structures appeared, the utriculus and dermal cyst. ConclusionsThe results suggest thatHr-/-mice are successfully created using TALENs, and Hr is important for regulating hair development, which could explain at least in part the hair loss and be applied to study the mechanism of hair growth and development disorder.
Hr;Knockout;mouse;Phenotype
国家自然科学基金(编号:31372270)。
朱奎成(1975-),男,在读博士,副教授。研究方向:动物学。Email:kuicheng123@126.com。
1.徐存拴(1958-),男,博士,教授,研究方向:细胞分化调控;2.章金涛(1968-),男,博士,教授,研究方向:遗传学。
研究报告
R-33
A
1671-7856(2016) 08-0075-04
10.3969.j.issn.1671-7856.2016.08.012
2016-04-04

