超高效液相色谱串联四极杆飞行时间质谱快速筛查猪肉中29种抗菌药物的残留
郝 杰,姜 洁,邵瑞婷,路 勇,冯 楠
(北京市食品安全监控和风险评估中心,北京 100041)
超高效液相色谱串联四极杆飞行时间质谱快速筛查猪肉中29种抗菌药物的残留
郝杰,姜洁*,邵瑞婷,路勇,冯楠
(北京市食品安全监控和风险评估中心,北京 100041)
采用超高效液相色谱串联四极杆飞行时间质谱仪(UPLC-Q-TOFMS)建立了猪肉中磺胺、喹诺酮、大环内酯、林可酰胺等4类29种抗菌类药物残留的筛查数据库;并结合快速高通量的前处理方法实现了猪肉中抗菌类药物的快速筛查测定。样品经Mcllvaine缓冲液提取,HLB固相萃取柱净化,采用BEH C18UPLC色谱柱分离,梯度洗脱,采用全信息串联质谱扫描模式(MSE)进行检测,精确质量数的母离子定量。结果表明:29种抗菌药物的定量限(LOQ,S/N≥10)为0.5~10 μg/kg,高、中、低3个添加水平平均回收率为50.10%~118.33%,相对标准偏差(RSD)为0.31%~14.90%,该方法能够达到高通量、多组分、快速开放的筛查目的,可用于猪肉基质中抗菌药物的批量快速筛查工作。
飞行时间质谱,抗菌药物,快速筛查
抗菌药物是指能抑制或杀灭细菌,用于预防和治疗细菌性感染的药物。其中包括人工合成或半合成类的药物以及微生物(细菌、真菌和放线菌属)的代谢产物-抗生素。从化学结构和作用机理上,合成药物又可分为磺胺类、喹诺酮类、硝基咪唑类、硝基呋喃类等;抗生素又可分为β-内酰胺类、大环内酯类、林可酰胺类、氨基糖苷类、四环素类、氨酰醇类等[1]。
近年来,各类抗菌药物在现代畜牧生产中的使用量明显增加、使用范围明显扩大,由此带来了许多食品安全风险的隐患[2-5]。动物源性食品中抗菌类药物残留的问题日渐突出,对消费者造成了严重的健康威胁,国内外都开始关注并采取了各种措施控制抗菌药物的滥用[6-10]。我国制定了关于食品中抗菌类药物的残留限量,例如所有动物食品中磺胺类药物总量最大残留为100 μg/kg,对林可酰胺类及大环内酯类药物的最大残留限量为40~1500 μg/kg,牛奶和畜类肌肉中喹诺酮类药物的最大残留量为30~400 μg/kg[11]。
目前,食品中抗菌药物的检测多为液相色谱串联质谱法,其中又以串联四极杆质谱方法居多[12-15]。前处理方法多为固相萃取法和基质分散固相萃取法[16-17]。这些方法都相对比较独立,只能完成某一类物质的检测,且方法固定不开放,一旦定型,很难再加入新的检测物质。无法满足食品安全突发事件快速处置工作所要求的高效率、多组分、开放性等要求。
高分辨飞行时间质谱(time of flight mass spectrometry,TOFMS)近年来在食品安全分析领域的应用越来越广泛,与低分辨的串联四极杆质谱相比,其具有定性准确,精确质量数,方法开放等优势,Oertelli等研究了基于UPLC-TOFMS的牛奶中150种兽药残留的快速多残留筛查方法[18],高馥蝶等利用UPLC-Q-TOFMS对牛奶中42种农、兽药残留[19],张洁等利用UPLC-Q-TOFMS建立牛奶中19种抗菌药物的筛查方法[20]。
本文使用高分辨飞行时间质谱进行猪肉中磺胺类,喹诺酮类,林可酰胺类,大环内酯类等4类29种抗菌药物同时检测方法的研究,建立了基于精确质量数的筛查数据库和优化的定量方法,满足了食品安全风险突发事件的快速应急处理工作中高通量、高可靠性确证和定量分析的要求。为相关工作提供了可靠的技术保障。
1 材料与方法
1.1材料与仪器
磺胺二甲嘧啶(纯度99.0%)、磺胺地索辛(纯度99.5%)、磺胺甲基嘧啶(纯度99.2%)、磺胺嘧啶(纯度99.5%)、磺胺间甲氧嘧啶(纯度98.5%)、磺胺对甲氧嘧啶(纯度98.0%)、磺胺多辛(纯度99.0%)、磺胺噻唑(纯度99.5%)、磺胺甲噁唑(纯度99.0%)、磺胺吡啶(纯度99.0%)、磺胺二甲异噁唑(纯度99.0%)、磺胺喹噁啉(纯度98.0%)、磺胺醋酰(纯度99.5%)、磺胺氯哒嗪(纯度100.0%)、磺胺甲氧哒嗪(纯度99.2%)、盐酸二氟沙星(纯度98.0%)、奥比沙星(纯度99.0%)、司帕沙星(纯度98.9%)、马波沙星(纯度99.0%)、盐酸沙拉沙星(纯度95.5%)、甲磺酸丹诺沙星(纯度93.5%)、氟罗沙星(纯度98.0%)、培氟沙星(纯度99.0%)、依诺沙星(纯度99.0%)、林可霉素(纯度98.0%)、克林霉素(纯度98.0%)、螺旋霉素(纯度96.0%)、红霉素(纯度95.3%)、替米考星(纯度95.3%)、泰乐菌素(纯度96.0%)均购自于德国Dr. Ehrenstofer GmbH公司。
乙腈、甲醇、乙酸铵、正己烷,色谱纯美国Thermo Fisher公司;甲酸,色谱纯德国CNW Technology GmbH公司;无水硫酸钠分析纯,北京化学试剂厂;亮氨酸脑啡肽美国Waters公司;HLB固相萃取柱150 mg/6 mL、MCX固相萃取柱150 mg/6 mL QuEChERS提取管(内含1.5 g无水硫酸钠和6 g无水硫酸镁)、QuEChERS净化管(内含150 mg无水硫酸镁,50 mg PSA,50 mg C18)美国Waters公司。实验用水为Milli-Q制备的超纯水。
Waters Acquity UPLC超高效液相色谱系统、Waters Synapt G2四极杆串联飞行时间质谱仪,配有电喷雾离子源及Masslynx 4.1 SCN791软件系统美国Waters公司;Milli-Q纯水仪美国Millipore公司;3K18高速冷冻离心机美国Sigma公司;固相萃取装置美国Waters公司。
1.2标准溶液的配制
各标准品于10 mL棕色容量瓶中用甲醇溶解,并定容到刻度,配制成1000 μg/mL的标准储备液,转入棕色样品瓶中于-20 ℃保存。
1.3样品前处理
猪肉肌肉组织样品经处理均质后,称取5.0 g样品于离心管中,加入10 mL Mcllvaine缓冲液,涡旋振荡1 min至充分混匀,超声波提取20 min,于4 ℃下10000 r/min离心10 min,取出上清液,残渣用10 mL Mcllvaine缓冲液再提取一遍,合并上清液待用。
HLB固相萃取柱用5 mL甲醇,5 mL水活化,取10 mL上清液上柱,保持上柱速度不超过3 mL/min,用5 mL 5%甲醇淋洗小柱,使用正向氮气流压干后用6 mL甲醇洗脱并收集洗脱液,洗脱液于室温下用氮气吹干,用1 mL流动相A∶流动相B=9∶1(v∶v)复溶,再加入1 mL正己烷,充分涡旋后,4 ℃ 14000 r/min离心10 min,取下层液体过0.22 μm聚四氟乙烯滤膜,待仪器分析。
1.4色谱条件
液相色谱柱:Waters Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm);流速0.45 mL/min;柱温45 ℃;流动相:A 1 mol/L pH5.0乙酸铵溶液10 mL+990 mL水,B 1 mol/L pH5.0乙酸铵溶液10 mL+990 mL甲醇;梯度洗脱条件:0~0.25 min 98% A,0.25~12.25 min 98%~1% A,12.25~13.00 min 1% A,13.00~13.01 min 1%~98% A,13.01~17.00 min 98% A;进样量5 μL,进样温度10 ℃。
1.5质谱条件
电喷雾离子源;毛细管电压3.0 kV;离子源温度120 ℃;萃取电压4.0 V;锥孔电压20.0 V;锥孔气流量50 L/h;脱溶剂气温度550 ℃;脱溶剂气流量1000 L/h。采用全信息串联质谱法(MSE)采集数据,质量扫描范围m/z 50~1000;低场碰撞能量4 eV;高场碰撞能量10~45 eV。实验中使用亮氨酸脑啡肽(2 ng/mL,乙腈∶水=1∶1稀释)进行质量数实时校正。
2 结果与分析
2.1前处理方法的优化
2.1.1提取溶剂的优化考虑到29种化合物的快速筛查需要通用、快速、回收率优化的前处理方法,本研究考察的前处理方法需要均能有效净化基质中的干扰。选取总体回收率较差的磺胺二甲异恶唑、磺胺氯哒嗪、培氟沙星、红霉素、泰乐菌素5种化合物作为依据,考察了乙腈、0.1%乙酸乙腈、乙酸乙酯、Mcllvaine缓冲液等不同提取液的回收率。结果如图1所示。
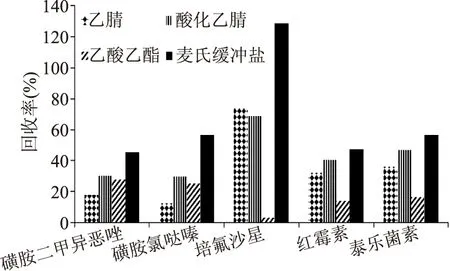
图1 不同提取溶剂的提取效率Fig.1 Recoveries of different extract solvent注:加标水平20 μg/kg,其余化合物的回收率均好于此五种,图2同。
结果表明,使用Mcllvaine缓冲液作为提取溶液,在均为2次提取的情况下,可以达到较好的回收率,其中最差的5种化合物回收率也能保持在45%以上。
2.1.2净化条件的优化考察了HLB固相萃取柱,MCX固相萃取柱、QuEChERS基质分散固相萃取以及QuEChERS基质分散固相萃取+0.1 g Na2EDTA共四种净化条件的效果。以总体回收率较差的磺胺二甲异恶唑、磺胺氯哒嗪、培氟沙星、红霉素、泰乐菌素5种化合物作为依据进行评价,结果如图2表示:
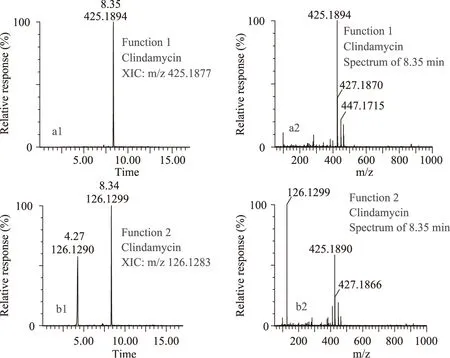
图3 克林霉素的质谱分析图Fig.3 Total ion chromatogram and spectrogram of Clindamycin

图2 不同净化条件的净化效果Fig.2 Recoveries of different clean-up method
实验发现,使用MCX柱净化,在红霉素和泰乐菌素的回收率上相近甚至稍优于HLB柱,但由于其在磺胺类化合物的低回收表现,并不如HLB柱适用,而QuEChERS方法的稀释倍数过大,影响了其方法的检出限。另外,在QuEChERS提取管中加入Na2EDTA可见明显改善了各类化合物的回收率,推测Na2EDTA消除了易于目标化合物形成螯合物的金属离子的影响,起到了优化净化的效果,这也解释了在提取溶剂中含有Na2EDTA的Mcllvaine缓冲液的提取效率要优于其他溶剂。
综上所述,使用Mcllvaine缓冲液作为提取溶剂,选择HLB固相萃取柱作为净化方法,可以得到29种抗菌类药物较好的前处理提取-净化效果,目标化合物的回收率均在50%以上。
2.2色谱-质谱分析
2.2.1飞行时间质谱仪的校正在实验工作开展之前,使用甲酸钠对仪器质量轴进行校正,将仪器的测定质量误差控制在5 ppm之内。实验过程中,使用亮氨酸脑啡肽(C28H37N5O7,单一同位素精确质量数555.2693)进行实时校正。质谱方法分为3个通道(Function),通道1为低场碰撞能量采集母离子信息,通道2为高场碰撞能量采集碎片离子信息,通道3为亮氨酸脑啡肽实时质量数矫正通道。
2.2.2筛查信息数据库的建立本研究根据国家相关的动物源性食品中抗菌药物使用相关标准,选取了4类共29种常用抗菌药物,这些化合物的相对分子质量和理化性质各有不同。
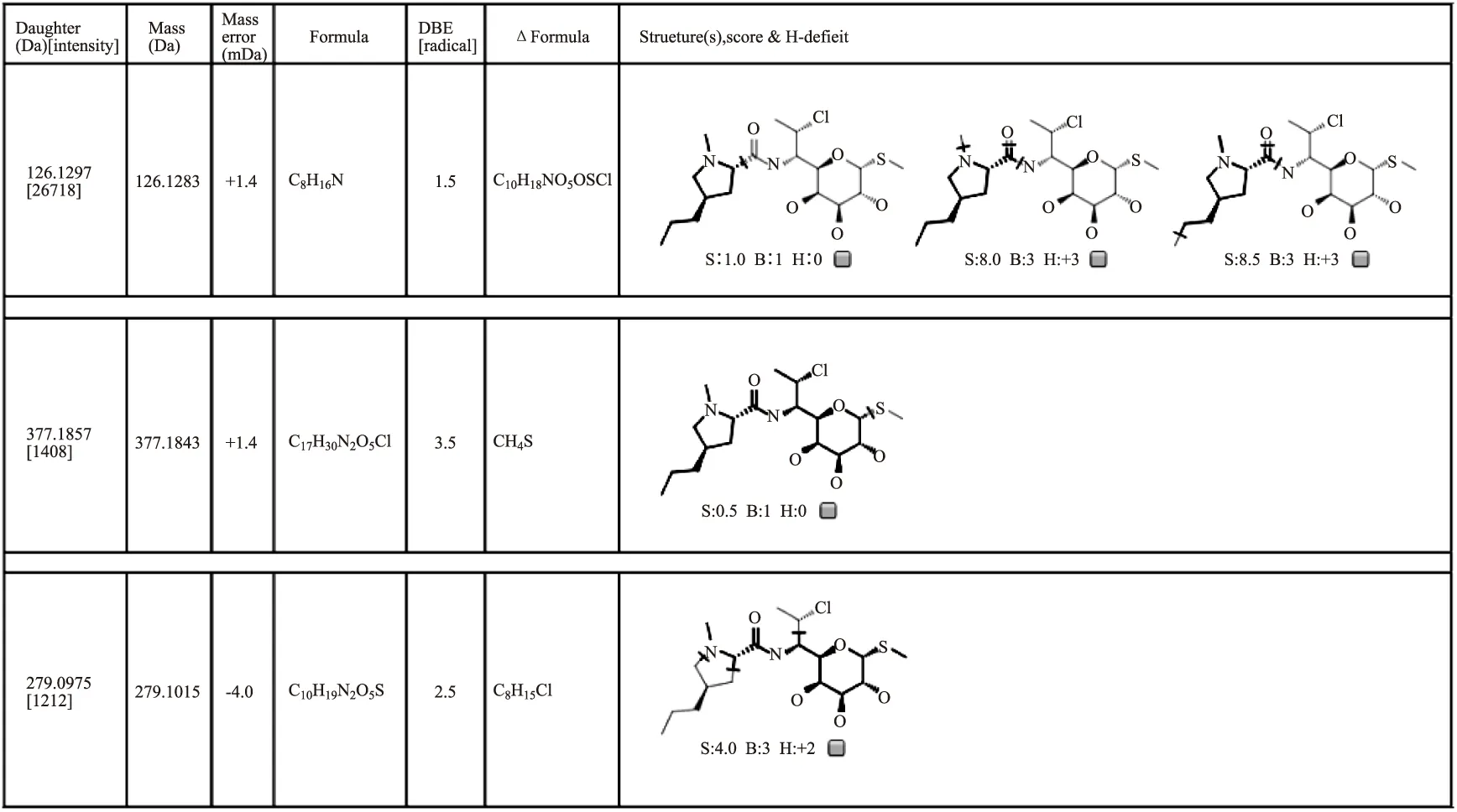
图4 克林霉素的碎片分析结果Fig.4 Product ion analysis result of Clindamycin by massfragment
用前处理过程中的复溶液(流动相A∶流动相B=9∶1 v∶v)将29种药物分别配制成100 ng/mL的单个标准工作溶液,经色谱进入飞行时间质谱仪,根据化合物分子式与加合离子状态推算母离子的质荷比,在±20 mu的偏差下提取该质荷比的XIC,确定该化合物的保留时间。以克林霉素(C18H33ClN2O5S,相对分子质量424.1799)为例,图3a1是克林霉素的1通道(低场碰撞能量=4 eV)提取离子流图,可以得到在固定色谱条件下克林霉素的保留时间为8.35 min,图3a2为克林霉素的1通道8.35 min处的质谱图,克林霉素的母离子电离形式为[M+H]+,母离子质荷比m/z 425.1877。通过Elemental Composition的同位素模型对图3a2中425.1894质谱峰进行分析(结果如图3a3),可以得到同位素分布的iFit置信值为99.11%,为所有可能化学式中理论同位素峰匹配度最高的一个,该质谱峰(m/z 425.1894)即为克林霉素的[M+H]+峰。
图3b2为克林霉素的2通道(高场碰撞能量=10~45 eV)下,8.35 min处的质谱图,在Mass Fragment软件中导入化合物结构式,经软件自动对高低场碰撞能量质谱图进行对比,得到三个较易形成,丰度较高的碎片离子信息,分别为m/z 126.1283,m/z 377.1843,m/z 279.1015。图3b1为2通道下m/z 126.1283的提取离子流图。
图4为massfragment对克林霉素在MSE模式下子离子的分析图。对找到丰度较大的碎片离子(m/z 126.1297,m/z 279.0975,m/z 377.1857)进行分析,对比从结构式得到的理论碎片,所检测到的碎片与理论碎片符合,并且从结构式的断裂形式上可以看出,这些碎片都较易形成,因此可以确定这几个碎片作为筛查方法中克林霉素的碎片离子。
结合上述论证,可以得到克林霉素在固定色谱-质谱条件下,保留时间为8.35 min,母离子精确分子量为425.1877,碎片离子为m/z 126.1283,m/z 377.1843,m/z 279.1015。建立成文本形式的数据库后,利用MassLynx中ChromaLynx XS组件的识别筛查功能,对比保留时间(偏差0.2 min以内),母离子精确分子量(偏差20 mu以内),碎片离子精确分子量(偏差20 mu以内),同位素峰匹配度(最高且>80%)四个参数,来对样品中的目标化合物做定性判定。29种化合物的色谱及质谱采集参数见表1。
2.2.3仪器定量方法的建立根据欧盟2002/657/EC[21]要求,高分辨质谱仪得到的母离子得分为2.0,子离子为2.5,因此在定量方法中,一个母离子与一个子离子即可满足4分的定性要求。在质量误差为20 mu窗口内提取母离子,以浓度与母离子峰面积响应值进行线性回归定量。
2.3方法学验证
2.3.1标准曲线的绘制根据29种抗菌药物响应的强弱,配制不同的质量系列浓度的混合标准工作溶液,29种化合物的线性范围由1~100 ng/mL,相关系数均大于0.99。线性方程、相关系数和线性范围见表2。
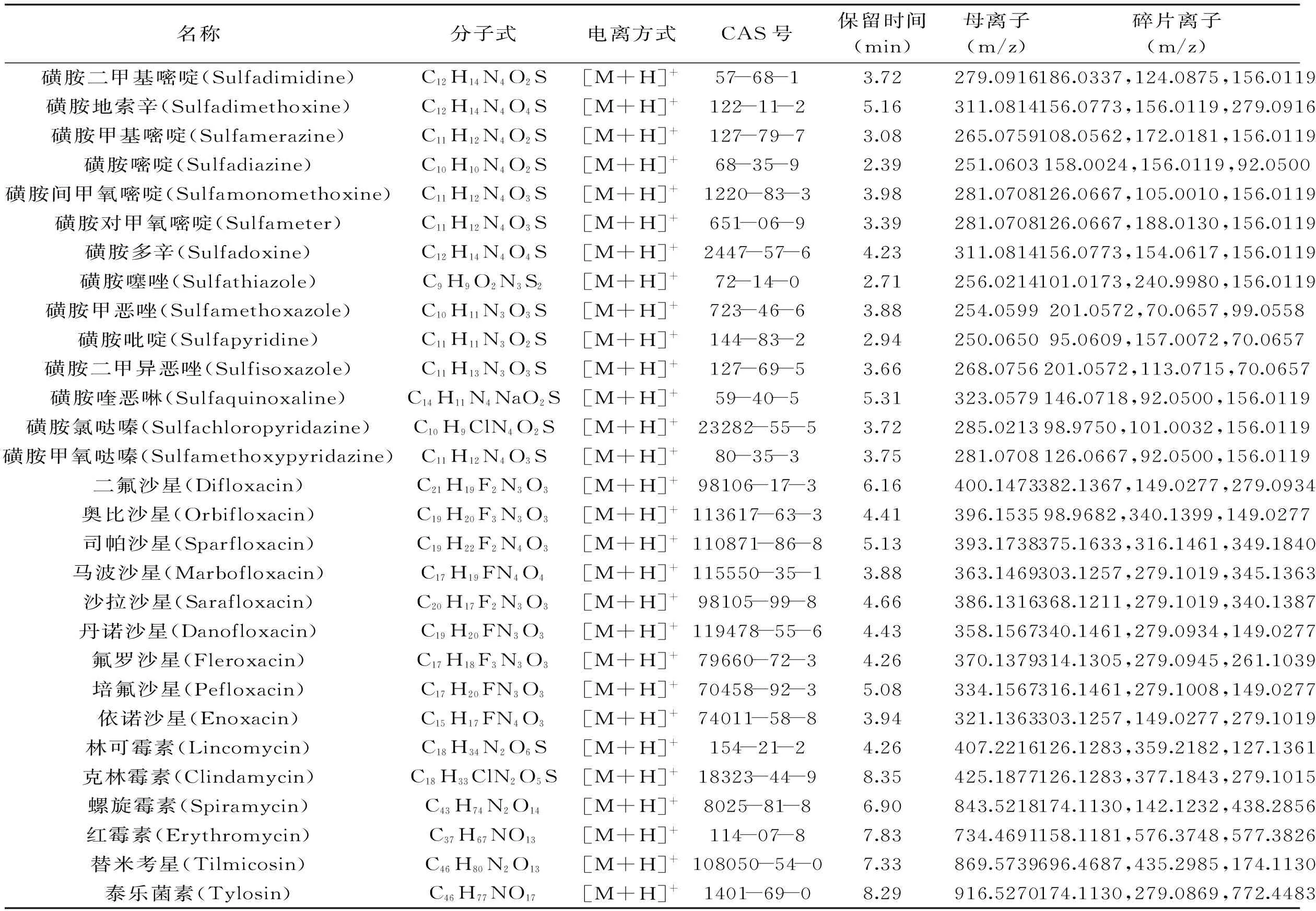
表1 29种抗菌药物的色谱及质谱采集参数
2.3.2方法的检出限和回收率研究了猪肉中,29种抗菌药物筛查方法的检出限及回收率。取空白样品,添加不同系列水平的混合标准溶液,绘制基质加标工作曲线。在基质中加入不同量的混合标准溶液,制成加标阳性样品,进行前处理,将得到的样品上机检测,得到信噪比至少10∶1的目标化合物的最低加标浓度。即为本方法在基质中的检出限。取空白基质,添加3个不同水平浓度的加标量,经过前处理并上机检测,每个浓度水平做6组平行实验,计算回收率及相对标准偏差。方法检出限、回收率和相对标准偏差见表3。
其中磺胺多辛、磺胺氯哒嗪在各水平下的加标回收率均在60%左右,在后续实验中,尝试在含有Na2EDTA的Mcllvaine缓冲液中加入一定比例的乙腈,二者的回收率有所提高,考虑可能是药物在盐溶液中的溶解性所限,加入乙腈可以提高其溶解度,乙腈的比例有待后续工作继续优化。
红霉素和泰乐菌素等大环内脂类药物在酸性提取液中的提取效率普遍不佳,在pH4.0的Mcllvaine缓冲液中回收率会受到影响,但在各加标水平上依然能稳定在60%左右,且方法检出限在10 μg/kg,可以满足兽药筛查工作的要求。

表2 29种抗菌药物的线性方程、相关系数、线性范围
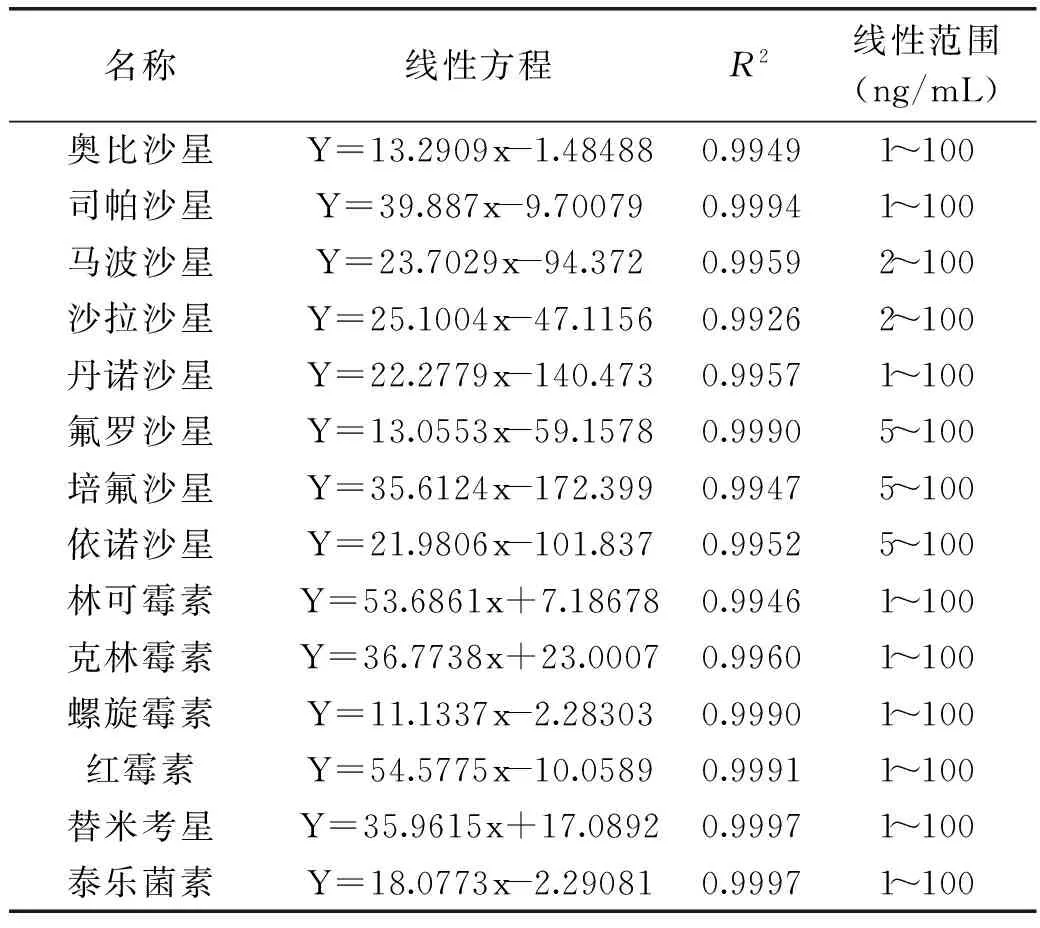
续表
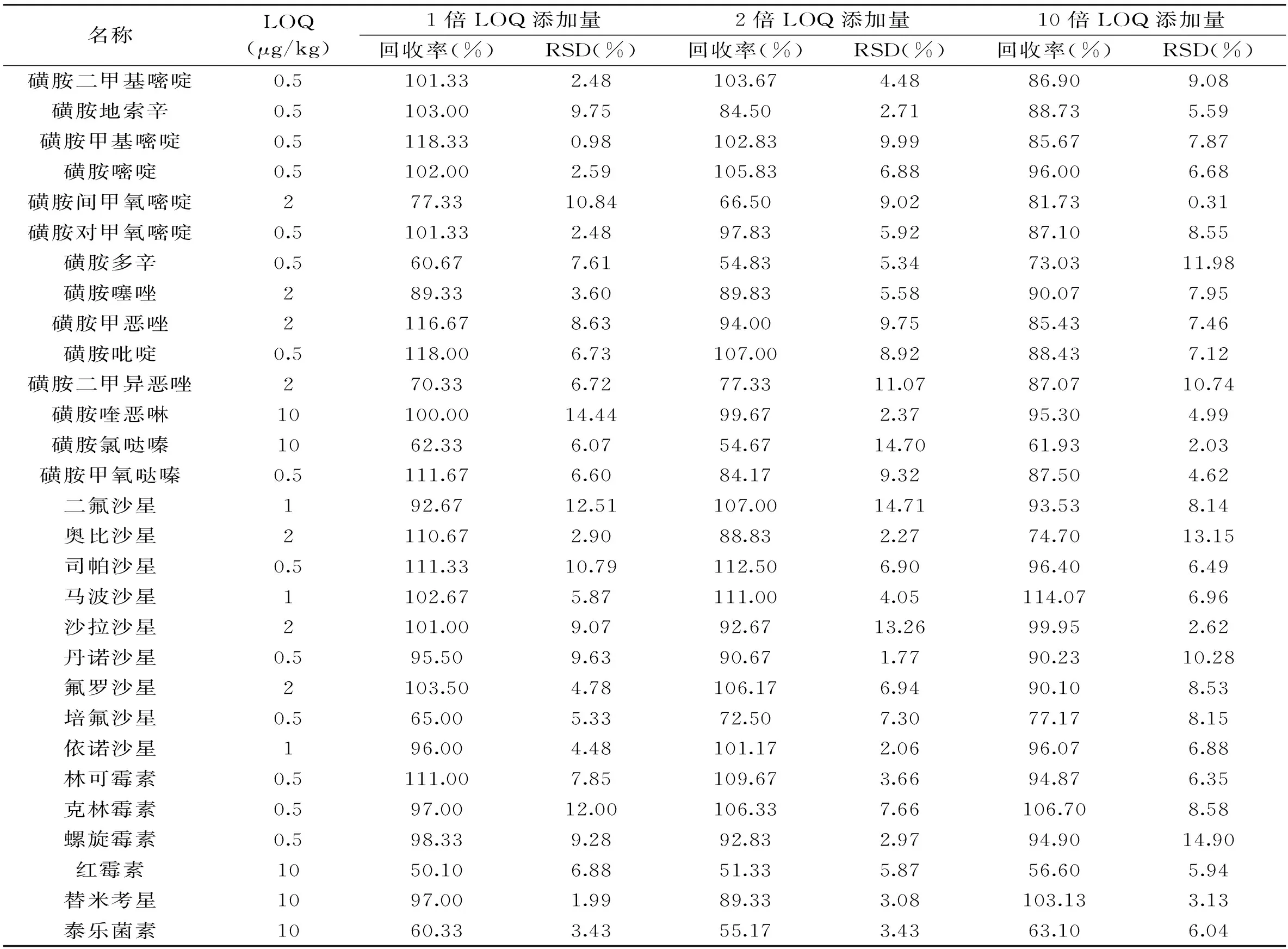
表3 29种抗菌药物的方法检出限、回收率和相对标准偏差
2.4方法应用
应用本方法对市售猪肉进行了筛查,共计21个样本,其中2个样品检出磺胺二甲基嘧啶,含量分别为51,12 μg/kg;1个样品检测出丹诺沙星,含量为12.2 μg/kg。为了验证实验结果,使用国标方法GB/T 21316-2007 《动物源性食品中磺胺类药物残留量的测定 高效液相色谱-质谱质谱法》和GB/T 20366-2006 《动物源产品中喹诺酮类残留量的测定液相色谱-串联质谱法》对检出的阳性样品进行了复测,检测结果磺胺二甲基嘧啶为44,10.8 μg/kg,丹诺沙星为14.9 μg/kg,与本文方法结果吻合。
3 结论
本文利用固相萃取的净化手段,结合超高效液相色谱串联四极杆飞行时间质谱研究建立了猪肉中,磺胺类,喹诺酮类,林可酰胺类,大环内酯类等4类29种抗菌药物的快速筛查方法。该方法准确,灵敏,快捷,方法开放,并且进行了方法学验证应用。适合用于食品安全风险突发事件的快速应急处置工作。
[1]张致平. 抗生素与抗菌药发展史[J]. 首都医药,2004,2:14-16.
[2]高迎春,魏秀丽,蔡芳芹,等. 动物应用抗菌药的风险及防制对策[J]. 中国兽药杂志,2006,40(2):43-48.
[3]刘建华,陈杖榴. 动物性食品中抗菌药残留对人体肠道菌群的影响及其研究模型与方法[J]. 动物医学进展,2003,24(2):37-40.
[4]刘建华,陈杖榴. 动物性食品中抗菌药残留对人体肠道菌群影响的安全性评价[J]. 中国兽药杂志,2003,37(2):33-37.
[5]马驿,陈杖榴. 抗微生物药的残留危害及其合理应用[J]. 中国家禽,2011,33(21):1-7.
[6]Casewell M,Friis C,Marco E,et al. The European ban on growth-promoting antibiotics and emerging consequences for human and animal health[J]. Journal of Antimicrobial Chemotherapy,2003,52:159-161.
[7]Acar J,Rostel B. Antimicrobial resistance:an overview[J]. Review Science Technology Ofiice International des Epizooties,2001,20(3):797-810.
[8]张苗苗. 国内外兽用抗菌药耐药性管理研究[D]. 武汉:华中农业大学,2008.
[9]王华,赵毅,王建华,等. 西安市乳制品中抗菌药的残留检
测[J]. 动物医学进展,2005,26(12):93-96.
[10]World Health Organization. The medical impact of the use of antimicrobials in food animals[R]. Berlin Germany,World Health Organization,1997.
[11]中华人民共和国农业部235号公告[S]. 中国:中华人民共和国农业部,2002.
[12]郭黎明,朱奎,江海洋,等. 超高效液相色谱-串联质谱法同时测定鸡肝中残留的四环素类、磺胺类和喹诺酮类药物[J]. 色谱,2009,27(4):412-416.
[13]周纯洁,赵博,黄思瑜,等. 液相色谱-串联质谱技术在食品中抗菌药物残留分析中的应用[J]. 食品工业科技,2014,35(1):367-370.
[14]包晓丽. 食品中喹诺酮类抗菌药的分析方法比较研究[D]. 浙江:浙江工商大学,2009.
[15]袁中珍. 动物源性食品中16种磺胺类药物残留检测[D].重庆:重庆医科大学,2013.
[16]Chico J,Rubies A,Centrich F,et al. High-throughput multiclass method for antibiotic residue analysis by liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A,2008,1213(2):189-199.
[17]刘洪斌,文一,刘勇军,等. LC-MS/MS法检测牛奶中14中β-内酰胺类抗生素残留[J]. 分析实验室,2014,33(2):221-224.
[18]Ortelli D,Cognard E,Jan P,et al. Comprehensive fast multiresidue screening of 150 veterinary drugs in milk by ultra-performance liquid chromatography coupled to time of flight mass spectrometry[J]. Journal of Chromatography B,2009,877:2363-2374.
[19]高馥蝶,赵妍,邵兵,等. 超高效液相色谱-四级杆-飞行时间质谱法快速筛查牛奶中的农药和兽药残留[J]. 色谱,2012,30(6):560-567.
[20]张洁,严丽娟,潘晨松,等. 超高效液相色谱/高分辨飞行时间质谱法同时检测乳制品中19种抗生素[J]. 色谱,2012,30(10):1031-1036.
[21]European Communities. Commission Decision 2002/657/EC of 12 August 2002 implementing Council Directive 96/23/EC concerning the performance of analytical methods and the interpretation of result[S]. European Communities,2002.
Rapid screening of 29 kinds of antibacterial drugs in pork by UPLC-Q-TOFMS
HAO Jie,JIANG Jie*,SHAO Rui-ting,LU Yong,FENG Nan
(Beijing Municipal Center for Food Safety Monitoring,Beijing 100041,China)
A screening database for 29 kinds of antibacterial drugs including sulfonamides,fluoroquinolones,macrolides and lincosamides in meat was established by ultra-performance liquid chromatography coupled with quadrupole-time of flight mass spectrometry. Combined with a rapid high throughput pretreatment,it can fast screen and test the antibacterial drugs in pork. Samples were extracted by Mcllvaine buffer and cleaned up by HLB solid phase extraction tube. Chromatography method was separated by BEH C18UPLC column,eluted whit gradient solvent,detected by MSEacquisition and quantitative by parent ion with exact mass. The result showed that the LOQs of 29 antibacterial drugs in matrixes were between 0.5 μg/kg and 10 μg/kg. Average recoveries in 3 different spiked levels were 50.10%~118.33%,RSD were 0.31%~14.90%. This method can achieve a high throughput,multi-components,rapid and open screening and appropriate in rapid screening antibacterial drugs in pork.
time of flight mass spectrometry;antibacterial drugs;screening
2015-08-27
郝杰(1984- ),男,硕士,工程师,研究方向:食品安全,E-mail:haojiecrab@126.com。
姜洁(1972- ),女,博士,高级工程师,研究方向:分析化学,E-mail:jybjj2004@126.com。
北京市科技计划项目(Z121100000312014)。
TS207.3
A
1002-0306(2016)11-0293-07
10.13386/j.issn1002-0306.2016.11.052

