离子色谱法测定酒精和甲醇中的四种无机阴离子
韩婷婷,崔 鹤,段小娟,宋 田,姬泓巍,李慧新,蔡 峰,朱倩林
(1.中国海洋大学化学化工学院,山东青岛 266100;2.山东出入境检验检疫局检验检疫技术中心,山东青岛 266002;3.青岛出入境检验检疫局,山东青岛 266001;4.燕山大学理学院,河北秦皇岛 066004)
离子色谱法测定酒精和甲醇中的四种无机阴离子
韩婷婷1,2,崔鹤2,*,段小娟3,宋田4,姬泓巍1,李慧新2,蔡峰2,朱倩林1
(1.中国海洋大学化学化工学院,山东青岛 266100;2.山东出入境检验检疫局检验检疫技术中心,山东青岛 266002;3.青岛出入境检验检疫局,山东青岛 266001;4.燕山大学理学院,河北秦皇岛 066004)
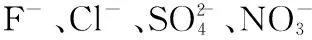
离子色谱法,甲醇,酒精,无机阴离子

1 材料与方法
1.1材料与仪器
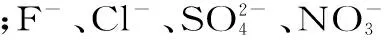
ICS5000+离子色谱仪美国Thermo公司;Milli-Q去离子水制备装置、AG11-HC保护柱、AS15-HC分离柱、AG15-HC保护柱赛默飞世尔科技公司;ASRS-300自循环抑制器美国戴安公司;电导检测器;恒温水浴锅;SK52000LHC超声仪上海科导超声仪器有限公司。
1.2实验方法
1.2.1离子色谱条件色谱柱为AS15-HC分离柱;流动相为40 mmol/L氢氧化钠溶液;流速为1.0 mL/min;柱温为30 ℃;电导检测器;抑制器电流为100 mA;进样量为25 μL。
1.2.3前处理方法称取2.0000 g(精确至0.001 g)试样于100 mL容量瓶中,加入0.5 mL 0.1 mol/L氢氧化钠溶液,恒温水浴蒸至近干,用水定容至刻度,振荡10 min,静置60 min稳定后,经滤膜过滤,待上机测定。
2 结果与讨论
2.1离子色谱条件的选择
2.1.1色谱柱的选择AS11-HC和AS15-HC都是新型高容量阴离子色谱柱,对高浓度基体中的杂质阴离子分析效果较好,常不必进行复杂的前处理去除基体,稀释到合适浓度即可直接测定。实验中分别对AS11-HC和AS15-HC两种阴离子色谱柱进行了选择,采用AS11-HC阴离子色谱柱,以20 mmol/L氢氧化钠溶液做流动相;1.0 mL/min流速;30 ℃柱温;抑制器电流为50 mA;进样量为25 μL,测定5 mg/L标准混合溶液(1.2.1)。实验发现,AS11-HC阴离子色谱柱出峰时间较快,在12 min内可全部出峰,但水负峰距离氟离子太近,会影响到氟离子的测定(图1)。使用AS15-HC阴离子色谱柱,以40 mmol/L氢氧化钠溶液做流动相;流速为1.0 mL/min;柱温为30 ℃;抑制器电流为100 mA;进样量为25 μL,测定5 mg/L标准混合溶液(1.2.1)。结果表明,水负峰和氟离子的保留时间相差1 min,不影响氟离子的测定,但对流动相要求较高,在40 mmol/L的流动相下四种离子完全分离需要23 min(图2)。综合考虑,最终选择AS15-HC离子色谱柱。
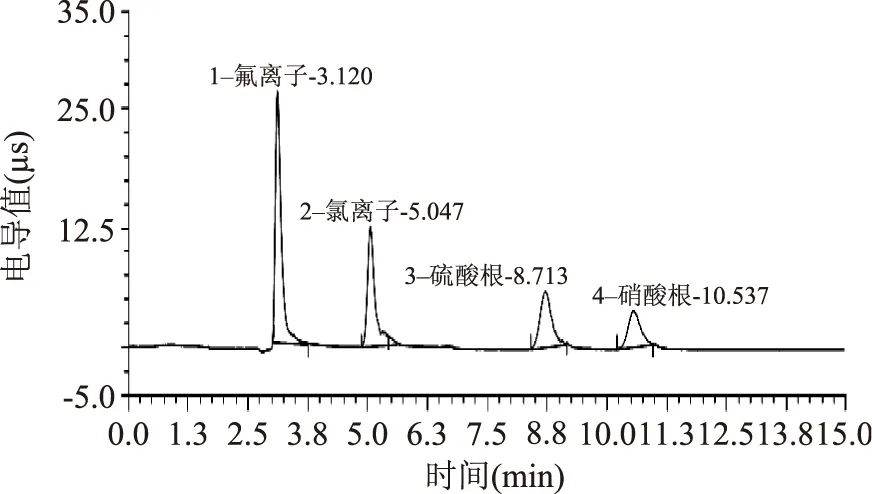
图1 AS11-HC测定四种阴离子的标准色谱图Fig.1 Chromatogram of the four types of anions by AS11-HC
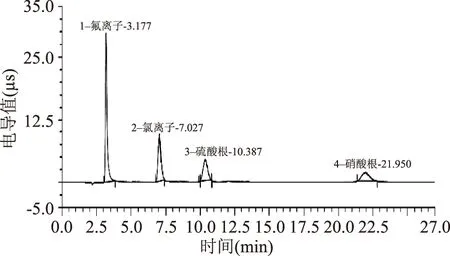
图2 AS15-HC测定四种阴离子的标准色谱图Fig.2 Chromatogram of the four types of anions by AS15-HC

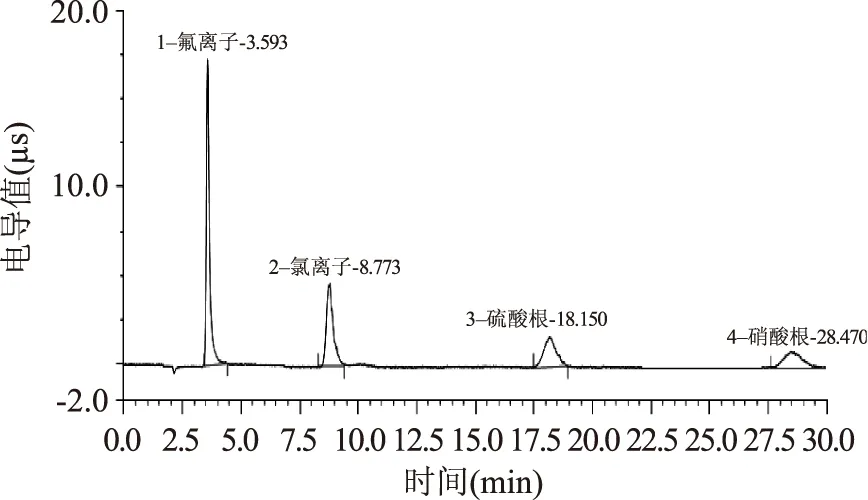
图3 淋洗液为30 mmol/L氢氧化钠溶液时的四种阴离子色谱图Fig.3 Chromatogram of the four types of anions in the eluent of 30 mmol/L sodium hydroxide solution
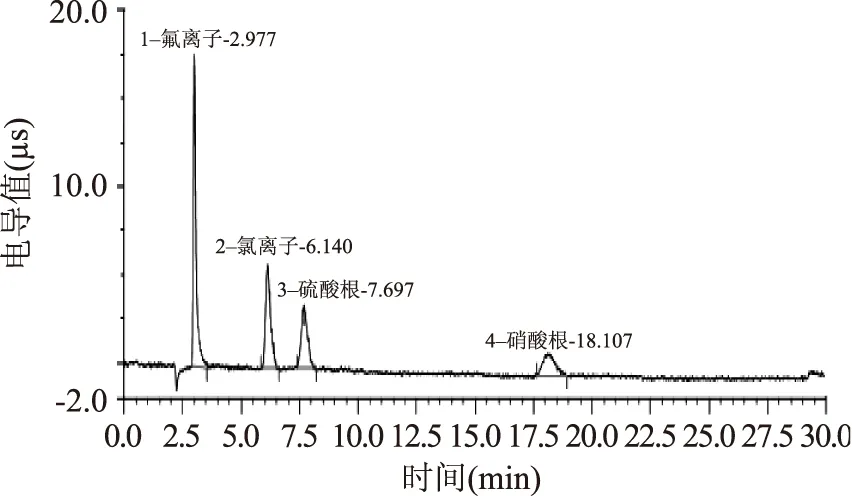
图4 淋洗液为50 mmol/L氢氧化钠溶液时的四种阴离子色谱图Fig.4 Chromatogram of the four types of anions in the eluent of 50 mmol/L sodium hydroxide solution

图5 淋洗液为40 mmol/L氢氧化钠溶液时的四种阴离子色谱图Fig.5 Chromatogram of the four types of anions in the eluent of 40 mmol/L sodium hydroxide solution
2.2前处理条件的选择
酒精和甲醇与水互溶,原则上可以直接进样分析[15],但是采用AS15-HC阴离子色谱柱直接进样分析酒精和甲醇样品时,由于高含量的背景电导会直接影响四种无机阴离子的测定,故选择加入适量的氢氧化钠溶液,利用氢氧化钠和其中醇根的结合,降低背景电导。在实验过程中我们对氢氧化钠溶液的加入量进行了一系列的探究,结果如下:
加入0.15 mL 0.1 mol/L氢氧化钠溶液时,背景电导太高,影响定量,见图6。

图6 加入0.15 mL 0.1 mol/L氢氧化钠溶液时的样品色谱图Fig.6 Chromatogram of the sample in the 0.15 mL 0.1 mol/L sodium hydroxide solution
加入0.3 mL 0.1 mol/L氢氧化钠溶液时,背景电导虽有所降低但依然较高,见图7。
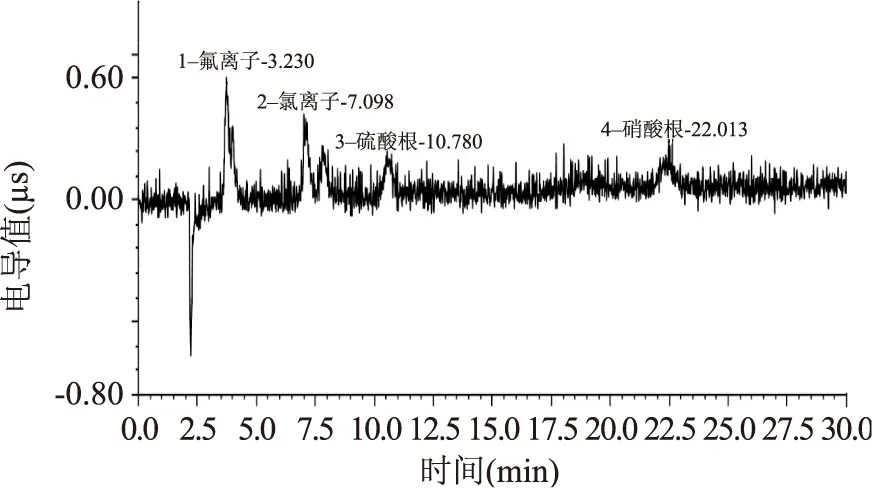
图7 加入0.3 mL 0.1 mol/L氢氧化钠溶液时的样品色谱图Fig.7 Chromatogram of the sample in the 0.3 mL 0.1 mol/L sodium hydroxide solution
经实验,加入0.5 mL 0.1 mol/L氢氧化钠溶液时,被测试样的背景电导较低,可准确定量,见图8。
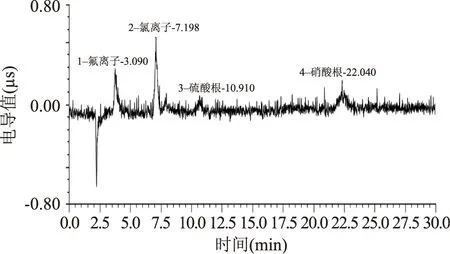
图8 加入0.5 mL 0.1 mol/L氢氧化钠溶液时的样品色谱图Fig.8 Chromatogram of the sample in the 0.5 mL 0.1 mol/L sodium hydroxide solution
2.3方法的线性范围和检出限
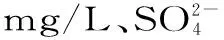

2.4方法的精密度和回收率实验
选取食用酒精、工业酒精、甲醇三种具有代表性的样品,称取2.0000 g(精确至0.001 g),分别进行低、中、高三个浓度添加水平的回收实验,按照上述方法每个水平重复测定6次,计算方法的回收率和相对标准偏差(RSD),结果见表3。4种阴离子均有较高的本底值,测定值为4.12~29.76 mg/kg,回收率在82%~110%之间,相对标准偏差为1.45%~4.64%,证明方法可靠。

表1 4种阴离子的线性范围、线性方程、相关系数和检出限
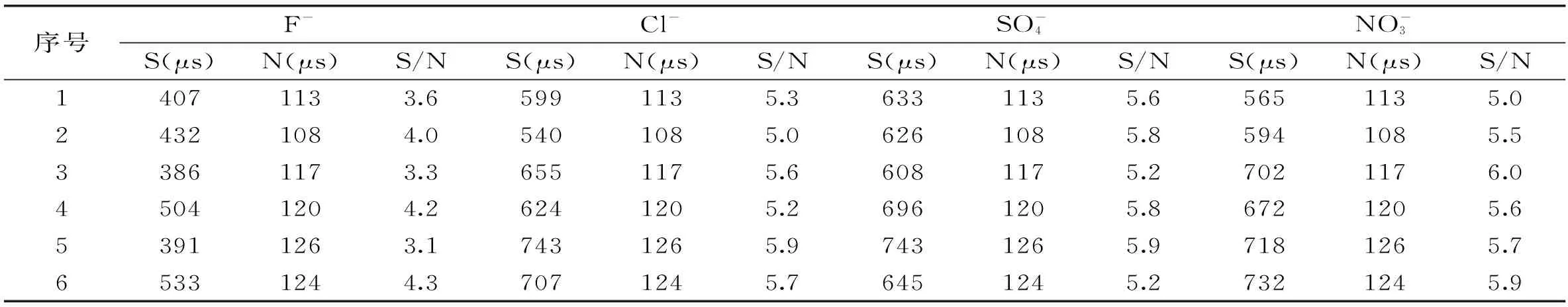
表2 检出限实验
注:S为signal,N为noise。
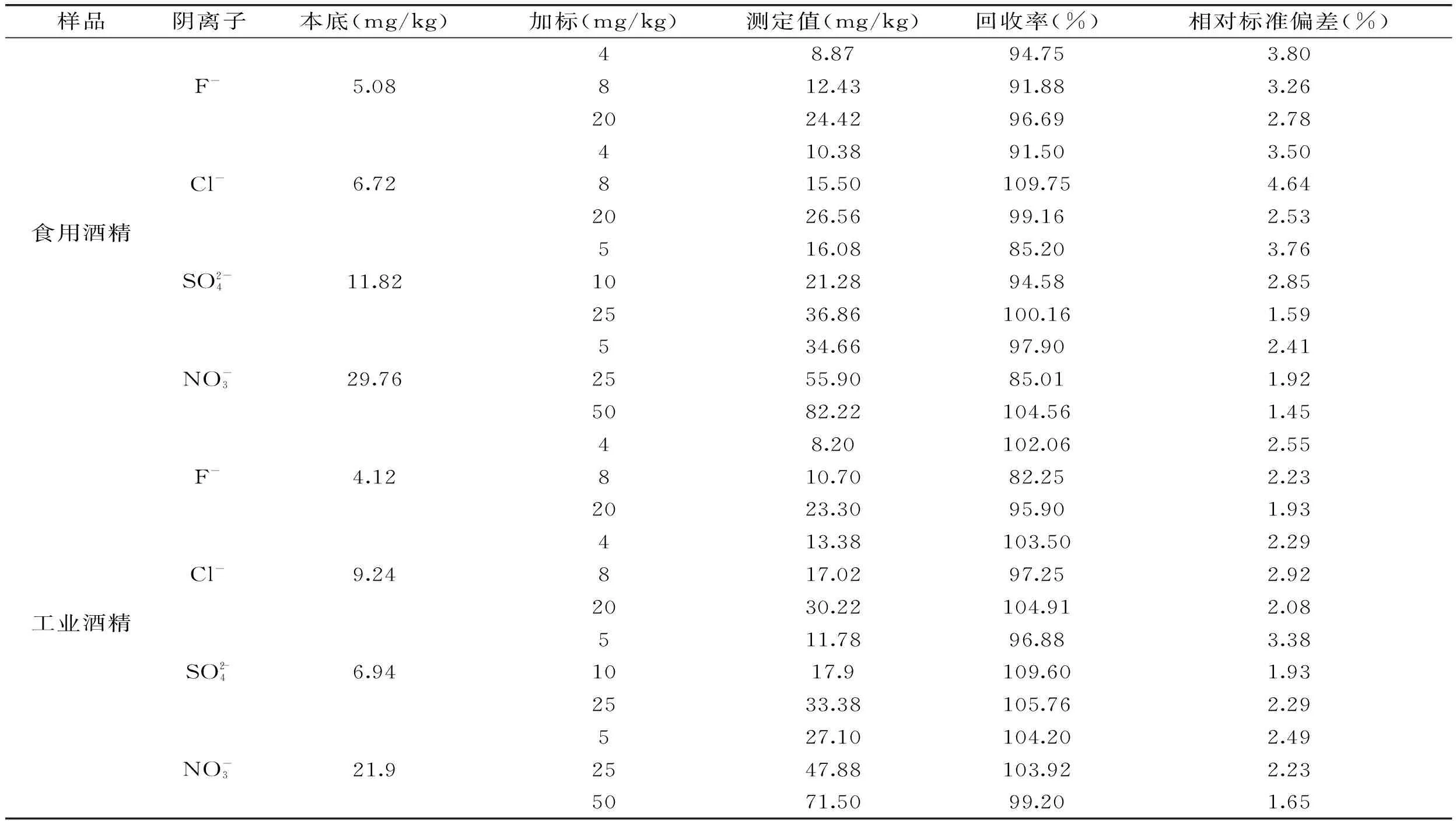
表3 三种样品的本底值、加标回收率和相对标准偏差(n=6)
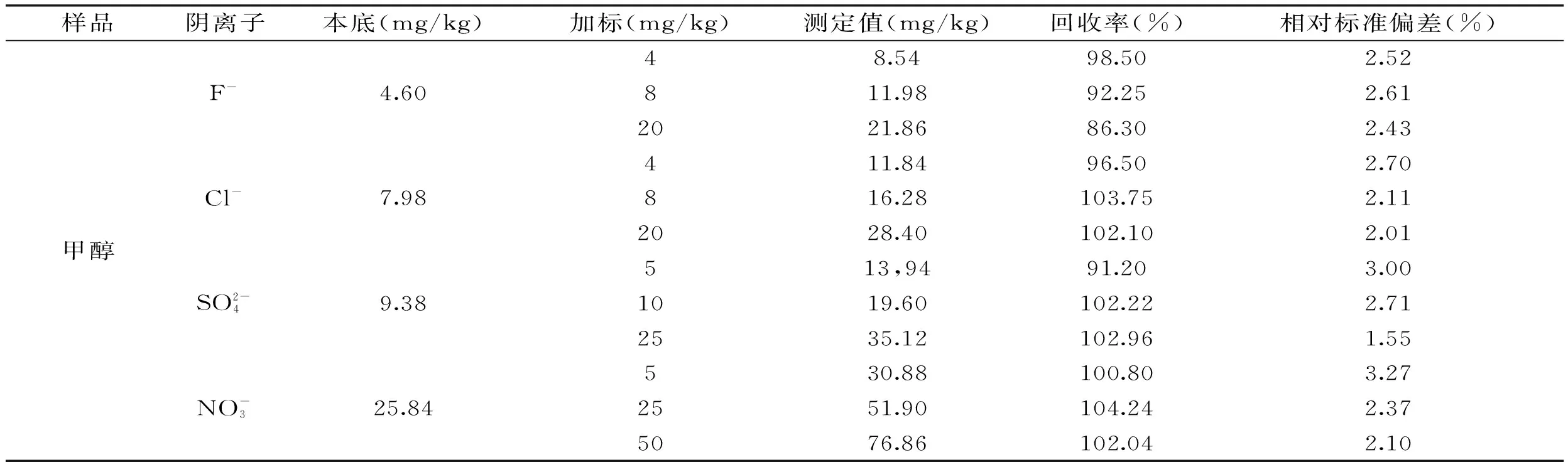
续表
3 结论
本实验采用离子色谱法对酒精和甲醇中氟离子、氯离子、硫酸根离子和硝酸根离子进行分析测试研究,试样中加入0.5 mL 0.1 mol/L氢氧化钠溶液利用水浴将其蒸至近干后定容至刻度,样品前处理过程简单易操作。采用AS15-HC阴离子色谱柱、40 mmol/L氢氧化钠溶液淋洗液;电导检测器、100 mA抑制器电流,23 min内可完成分离检测。通过优化色谱条件,建立了一种简便、准确度高、重现性好、抑制电流低,且采用等度淋洗即可得到很好分离的新方法。该方法对国产离子色谱也具有很强的适用性,为国家制定酒精、甲醇中阴离子限量标准提供参考,同时也为酒精和甲醇生产加工过程中无机阴离子含量控制提供技术支撑。
[1]郭龑茹,朱岩,叶明立. 离子色谱法测定啤酒中的无机阴离子和阳离子[J]. 食品科学,2006,27(4):174-176.
[2]龚殿婷,李凤华,樊占国,等. 光电比浊法测定硼酸中的氯[J]. 材料与冶金学报,2008,03(3):68-72.
[3]佟琦,高丽华. 莫尔法与自动电位滴定法测定水中氯离子含量的比较[J]. 工业水处理,2008(11):69-71.
[4]侯艳文,刘峰. 阴离子交换色谱中淋洗液流速对测定灵敏度影响的讨论[J]. 色谱,1998,16(4):347-350.
[5]李睿姝,于泓,高微,等. 硅胶整体柱离子对色谱快速分析碘离子[J]. 分析实验室,2010,29(3):85-88.
[6]魏益华,张金艳,戴廷灿,等. 离子色谱法测定地沟油和食用油中氯离子含量[J]. 食品科学,2011,12(12):213-215.
[7]杨博锋,汤志旭,高昕. 食品塑料包装材料中单体和添加剂及其检测技术[J]. 食品工业科技,2012,14(14):392-395.
[8]沈敏,冯睿,陈浩,等. 离子色谱法同时测定降水中的9种阴离子[J]. 分析科学学报,2007,23(3):334-336.
[9]商荣宁,张锦梅. 离子色谱法测定食品添加剂磷酸二氢钙中的阴离子[J]. 中国食品卫生杂志,2013,25(1):49-52.
[10]郭宏利,郁鸢,赵申,等. 离子色谱法测定分子筛废水中六亚甲基亚胺的含量[J]. 分析实验室,2013,11(11):26-30.
[11]Maya F,Estela J S,Cerda V. Spectrophotometric determination of chloride in waters using a multisyringe flow injection system[J].Talanta,2008,74(5):1534-1538.
[12]史亚利,刘京生,蔡亚岐,等. 直接进样离子色谱法测定磷酸试剂中痕量无机阴、阳离子[J]. 分析测试学报,2005,24(3):128-130.
[13]侯艳文,牟世芬,侯小平,等. 阴离子交换色谱中淋洗液流速对测定灵敏度影响的讨论[J]. 色谱,1998,16(4):347-350.
[14]林太凤,郑大威,张淑芬,等. 功能饮料中功能因子及其检测方法的研究进展[J]. 食品工业科技,2013,21(21):394-399.
[15]潘丙珍,刘青,庞世琦,等. 离子色谱法测定酒中的有机酸和无机阴离子[J]. 现代食品科技,2013,4(4):876-880.
Determination of four anions in alcohol and methanol by ion chromatography
HAN Ting-ting1,2,CUI He2,*,DUAN Xiao-juan3,SONG Tian4,JI Hong-wei1,LI Hui-xin2,CAI Feng2,ZHU Qian-lin1
(1.College of Chemistry and Chemical Engineering,Ocean University of China,Qingdao 266100,China;2.Shandong Entry-Exit Inspection and Quarantine Technology Center,Qingdao 266002,China;3.Qingdao Entry-Exit Inspection and Quarantine Bureau,Qingdao 266001,China;4.College of Science,Yan Shan University,Qinhuangdao 006004,China)
A comprehensive analytical method based on ion chromatography was developed for the determination of four Inorganic anions in alcohol and methanol. The samples were added proper amount of sodium hydroxide solution,then evaporated to dry in a constant temperature water bath and set the volume to scale. The solution was separated by the AS15-HC separating column with the mobile phase of 40 mmol/L sodium hydroxide solution and 1.0 mL/min flow rate. The results indicated that the calibration curves showed good linear relation for 4 anions(r=0.99902~0.99983). The detection limits for the method were 0.5,0.5,1.0 mg/kg and 1.0 mg/kg respectively. The mean recoveries at three spiked concentration levels(low,middle,high)were 82%~110%,and the relative standard derivations were 1.45%~4.64%(n=6). The method is reliable,simple and convenient,sensitive,universal and reproducible,which could be rapidly applied in the determination of 4 anions in alcohol and methanol.
ion chromatography;methanol;alcohol;inorganic anion
2015-11-19
韩婷婷(1992-),女,硕士,研究方向:仪器分析,E-mail:hantingtingouc@163.com。
崔鹤(1962-),男,博士,研究员,主要从事离子色谱开发研究,E-mail:cuihe88@aliyun.com。
国家重大科学仪器设备开发专项(2012YQ090229)。
TS207.3
A
1002-0306(2016)11-0284-05
10.13386/j.issn1002-0306.2016.11.050

