SD-PMA-ddPCR检测食品中沙门氏菌的研究
王 静,张慧敏,魏 玮,贾俊涛,李春喜,秦 燕
(1.威海出入境检验检疫局检验检疫技术中心,山东威海 264205; 2.山东出入境检验检疫局,山东青岛266500)
SD-PMA-ddPCR检测食品中沙门氏菌的研究
王静1,张慧敏1,魏玮1,贾俊涛2,李春喜1,秦燕1
(1.威海出入境检验检疫局检验检疫技术中心,山东威海 264205; 2.山东出入境检验检疫局,山东青岛266500)
研究将叠氮溴化丙锭(PMA)与微滴数字PCR(ddPCR)技术相结合,建立一种沙门氏菌活菌的检测方法。结果表明,PMA不能完全有效抑制108CFU/mL的沙门氏菌死菌DNA的PCR扩增,0.1% 脱氧胆酸钠(SD)和40.0 μg/mL PMA协同作用,可以有效抑制108CFU/mL的沙门氏菌死菌DNA的PCR扩增,不抑制沙门氏菌活菌DNA扩增的PMA最高浓度是40.0 μg/mL。经过SD和PMA对样品预处理,在不同死、活菌比例下,PMA-ddPCR可以定量检测活菌,避免了死菌DNA的干扰。本方法的检出限为8.0 copy/20 μL。利用PMA-ddPCR检测人工污染鸡肉样品,最低可检出102CFU/mL的沙门氏菌。实验结果证明PMA-ddPCR方法的特异性、精确度、稳定性良好。
叠氮溴化丙锭,脱氧胆酸钠,数字PCR,活菌
随着社会的发展和人们对健康的关注,食品安全成为影响广泛的社会性问题。但食源性疾病暴发事件层出不穷,例如美国多次爆发沙门氏菌污染事件,沙门氏菌是一种常见的食源性致病菌,可使人发生中毒[1-3],主要症状有恶心、呕吐[4-5],严重危害人们的身心健康。因此,定量检测沙门氏菌引起各国的高度关注。
目前,检测沙门氏菌的方法有很多,比如实时荧光聚合酶链式反应[6]、荧光染色[7]等,虽然这些方法相比于传统培养法有一些优势[8-9],但是还存在一些无法克服的缺点,诸如操作繁琐费时,灵敏度低,不能真实反映样品的污染水平[10-11]。因此,开发定量检测活菌的方法很有必要。叠氮溴化丙锭(PMA)是一种能和DNA共价交联的光敏材料,光照可以使PMA的光敏基团转化为氮宾自由基,其可以和DNA发生共价交联,进而阻断DNA分子的PCR扩增,并且PMA只能选择性的渗透死菌的细胞膜,因此PMA被用于和PCR技术相结合定量检测活菌[12-15]。但是有研究发现,PMA不能完全抑制死菌DNA的PCR扩增,可能原因是一些受损细菌细胞碎片阻止PMA渗透进入细胞膜[16]。Wang L J等人[17]利用0.1% 脱氧胆酸钠(SD)处理受损细菌,促进PMA进入死菌细胞内,达到了完全有效抑制死菌DNA的PCR扩增,并且0.1% SD不会对活菌产生影响。
微滴数字PCR(ddPCR)是近年来发展起来的可以定量检测DNA的新方法,通过PCR扩增和荧光信号的积累读取阳性微滴数目,再通过泊松分布计算出样本的DNA分子数目[18-20]。本文首次将PMA与ddPCR技术相结合,开发了高灵敏、高选择性的检测食源性致病菌的新方法。
1 材料与方法
1.1材料与仪器
菌株为沙门氏菌Salmonella(ATCC13311)南京便诊生物科技有限公司;PMA1 mg,美国Biotium公司,溶解于1.0 mL 20%二甲基亚砜(DMSO)溶液,得到1 mg/mL储备液,于-20 ℃避光保存;细菌基因组DNA提取试剂盒北京Tiangen公司;引物、探针由生工生物工程(上海)股份有限公司合成;荧光定量PCR反应体系有关试剂购自罗氏公司;微滴式数字PCR反应体系有关试剂购自美国伯乐公司。
QX200微滴式数字PCR系统美国伯乐公司;7900HT Fast 实时荧光定量PCR(qPCR)系统美国应用生物系统公司;CF16RXII高速冷冻离心机日本日立公司;卤钨灯(500 W)飞利浦灯具(上海)有限公司。
1.2实验方法
1.2.1细菌培养及热灭活菌的制备用接种环沾取甘油管保存的菌液,在营养琼脂平板上划线,于37 ℃下培养24 h。挑取单菌落接种于营养琼脂液体培养基,37 ℃培养至对数生长期。取500 μL菌液沸水浴10 min后,用0.1% SD处理受损细菌,37 ℃条件下温育20 min后,用40.0 μg/mL的PMA处理,混合均匀后暗处孵育15 min,将离心管置于500 W卤钨灯下20 cm处曝光15 min(管口朝上,置于冰上),期间每隔5 min混匀数次,以使样品溶液曝光均匀。随后用试剂盒法提取基因组DNA,进行PCR检测。
1.2.2最佳PMA浓度的选取取500 μL受损细菌于1.5 mL离心管中,利用0.1% SD处理样品同1.2.1,分别加入PMA终浓度为0.0、2.0、5.0、10.0、20.0、40.0、50.0 μg/mL,混合体系振荡5 s后暗处孵育15 min,使PMA最大限度进入受损细胞内。将离心管置于500 W卤钨灯下20 cm处曝光15 min(管口朝上,置于冰上)。随后用试剂盒法提取基因组DNA,进行PCR检测。取500 μL沙门氏菌活菌作为对照组,处理同实验组。
1.2.3最佳曝光时间的选取如1.2.1处理热灭活菌,分别曝光0.0、2.0、5.0、10.0、15.0、20.0 min,随后用试剂盒法提取基因组DNA,进行PCR检测。
1.2.4细菌DNA提取及qPCR和ddPCR检测本实验采取试剂盒法得到基因组DNA。分别利用7900HT Fast 实时荧光定量PCR系统和QX200微滴式数字PCR系统进行检测。参考SN/T 1870-2007合成引物、探针。上游引物(19bp):5′-GCGGCGTTGGAGAGTGATA-3′,下游引物(21bp):5′-AGCAATGGAAAAAGCAGGATG-3′,探针:5′-FAM-CATTTCTTAAACGGCGGTGTCTTTCCCT-TAMRA-3′。
qPCR反应体系(25.0 μL):12.5 μL LightCycler® 480 Probes Master;10 μmol/L上、下游引物各1.0 μL;10 μmol/L探针0.5 μL;模板DNA 2.0 μL;最后用DEPC水补充至25.0 μL。qPCR扩增条件为:95 ℃、3 min;94 ℃、5 s,60 ℃、40 s,40个循环,同时收集FAM荧光。将荧光定量PCR测得CT值代入标准线性方程,即可得到所测菌液浓度值。
ddPCR反应体系(20.0 μL):10.0 μL ddPCRTMSupermix for Probes(No dUTP);10 μmol/L上、下游引物各1.0 μL;10 μmol/L探针0.5 μL;模板DNA 4.0 μL;最后用DEPC水补充至20.0 μL。ddPCR扩增循环条件为:95 ℃,5 min;94 ℃、10 s,60 ℃、45 s,40个循环;98 ℃,10 min。ddPCR数据处理:ddPCR测得浓度值为20.0 μL反应体系中目标基因浓度x(copy/μL),本文中待测菌液浓度值y=5×50x/0.5,其中5为模板(4.0 μL)在反应体系(20.0 μL)中的稀释倍数;试剂盒法提取DNA洗脱液体积为50 μL;待测菌液体积为0.5 mL。
1.2.5qPCR、PMA-ddPCR、SD-PMA-ddPCR检测不同比例活菌的比较配制活菌比例为100%、50%、25%、10%、0%的沙门氏菌菌悬液,分别取500 μL于1.5 mL离心管中,在优化条件下,按照试剂盒法提取基因组DNA,进行qPCR、PMA-ddPCR、SD-PMA-ddPCR检测。
1.2.6SD-PMA-qPCR、SD-PMA-ddPCR检测沙门氏菌的灵敏度将105CFU/mL的沙门氏菌菌液依次稀释10倍制得浓度为105、104、103、102、101CFU/mL菌液。在优化条件下,进行SD-PMA-qPCR、SD-PMA-ddPCR分析实验。
1.2.7SD-PMA-ddPCR的抗干扰性取非沙门氏菌菌株4株(大肠埃希菌、副溶血弧菌、金黄色葡萄球菌、单增李斯特氏菌),经培养后菌落浓度达到108CFU/mL,将上述4株干扰菌和108CFU/mL沙门氏菌混合,在优化条件下,进行SD-PMA-ddPCR检测,分析抗干扰性。
1.2.8SD-PMA-qPCR、SD-PMA-ddPCR检测人工污染样品中沙门氏菌取25 g新鲜鸡肉样品,用均质器制成鸡肉匀浆,利用108CFU/mL死菌污染鸡肉样品,然后用101~106CFU/mL的沙门氏菌菌液进行人工污染,在优化条件下,进行SD和PMA处理之后,进行SD-PMA-qPCR、SD-PMA-ddPCR检测。
2 结果与分析
2.1SD和PMA处理死菌的效果
如图1所示,108CFU/mL热损伤细菌经过SD和PMA处理之后,其CT值明显高于仅用PMA处理的实验组和对照组,说明SD可以进一步破坏死菌的细胞膜,促进了PMA渗透进入死菌细胞膜,从而和DNA共价交联,阻止了DNA的PCR扩增。
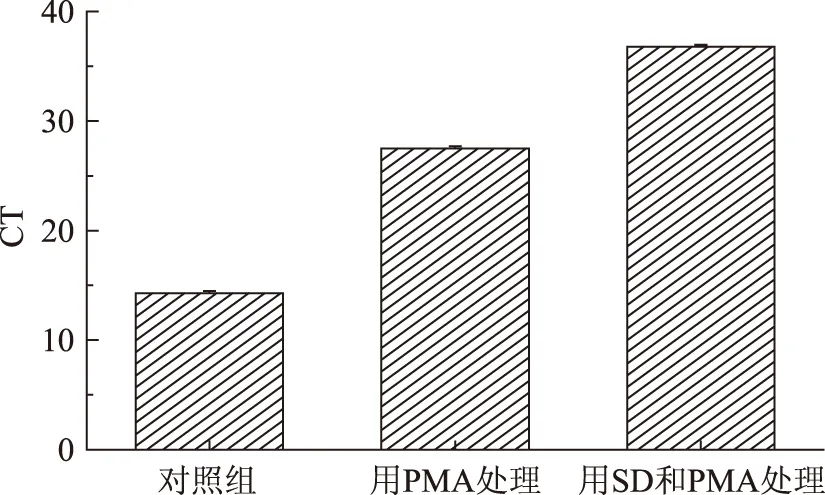
图1 SD协助PMA进入死菌细胞的影响Fig.1 The effect of SD for PMA to enter dead cells
2.2最佳PMA浓度的优化
如图2所示,随着PMA浓度的增大,死菌DNA qPCR扩增的CT值明显升高,当PMA浓度超过40.0 μg/mL时,反应体系的CT值几乎不再发生变化。当PMA浓度为50.0 μg/mL时,相比不加PMA,活菌DNA qPCR扩增的CT值略微增加,可能高浓度PMA影响了活菌DNA的qPCR扩增,本研究选用40.0 μg/mL PMA作为最佳浓度。

图2 PMA 浓度对死菌和活菌的影响Fig.2 Effect of PMA concentration on dead and live bacteria
2.3最佳曝光时间的优化
如图3所示,随着光照时间的增加,体系的CT值迅速升高,光照时间超过15.0 min后,体系的CT值不发生明显变化,本研究选取15.0 min作为最佳光照时间。

图3 曝光时间对PMA 处理死细胞的影响Fig.3 Optimization of different light exposure time

图4 不同沙门氏菌浓度下的CT值Fig.4 CT of different Salmonella cells
2.4qPCR检测沙门氏菌的线性曲线
在0.1% SD、PMA浓度为40.0 μg/mL的条件下,利用qPCR进行了沙门氏菌的检测。如图4所示,随着沙门氏菌含量的增加,CT值明显降低,CT值与沙门氏菌的浓度在102~108CFU/mL范围内呈现良好的线性关系(r=0.9949),其线性回归方程为:y=43.16-3.65x,方程中y代表DNA qPCR扩增的CT值,x代表沙门氏菌的浓度的对数值。该方法的检测限是102CFU/mL(S/N=3)。
2.5qPCR、PMA-ddPCR、SD-PMA-ddPCR检测不同比例活菌的比较
将2.6×108CFU/mL活菌、热灭活菌按照图5所示比例混合后,在优化条件下,进行qPCR、PMA-ddPCR、SD-PMA-ddPCR检测。由图5可见,qPCR测得CT值代入2.4中线性方程计算得出沙门氏菌含量,不论活菌比例如何变化,结果始终为死、活菌的总量;当活菌比例0%时,未经SD处理的菌液进行PMA-ddPCR检测,依然可以检出阳性,说明40.0 μg/mL PMA单独作用下不能完全抑制108CFU/mL死菌的DNA扩增;随着活菌比例的增加,PMA-ddPCR和SD-PMA-ddPCR检出结果也相应增加,但是SD-PMA-ddPCR检出结果与平板计数(Plate count)结果更加接近。
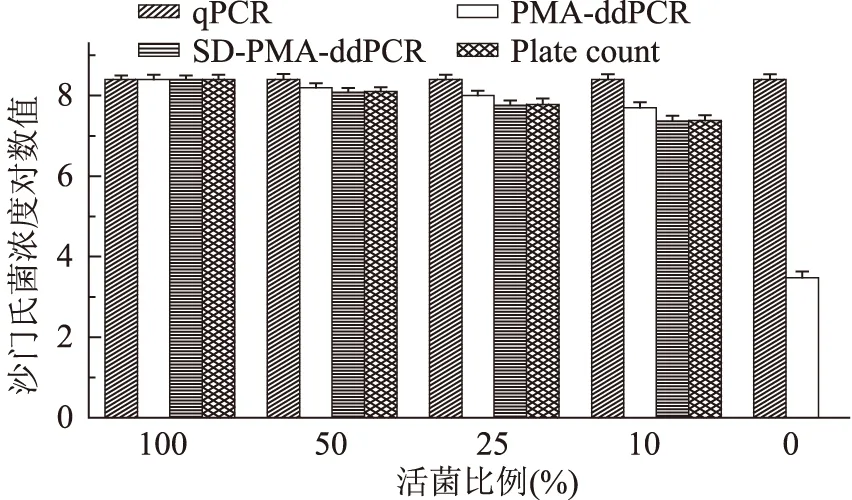
图5 不同热灭活时间下qPCR、PMA-ddPCR、SD-PMA-ddPCR沙门氏菌检测结果Fig.5 The numbers of survivors from qPCR, PMA-ddPCR,SD-PMA-ddPCR
2.6SD-PMA-ddPCR、SD-PMA-qPCR检测沙门氏菌的灵敏度
将原菌液浓度为2.6×105CFU/mL的沙门氏菌10倍梯度稀释,分别标记为S5~S1,进行SD-PMA-ddPCR、SD-PMA-qPCR检测。由图6一维散点图上可以看出S1~S5生成的阳性微滴数分布,阳性微滴数目随着浓度的升高而逐渐增多。ddPCR测得S5~S2的浓度如图7所示,S1未检出,S2测得浓度为0.4 copy/μL,因此该方法检测沙门氏菌基因组DNA的检出限为8.0 copy/20 μL。如图8所示,随着沙门氏菌浓度的稀释,CT值逐渐变大,PMA-qPCR最少可检出102CFU/mL的沙门氏菌。

图6 ddPCR一维散点图Fig.6 The 1D scatterplot of ddPCR

图7 ddPCR反应体系(20 μL)中目标基因浓度Fig.7 Concentration of target genes in reaction system of ddPCR(20 μL)

图8 SD-PMA-qPCR检测沙门氏菌灵敏度Fig.8 Sensitivity of Salmonella by SD-PMA-qPCR detection
2.7SD-PMA-ddPCR的抗干扰性
在4株108CFU/mL非沙门氏菌(大肠埃希菌、副溶血弧菌、金黄色葡萄球菌、单增李斯特氏菌)存在的情况下,SD-PMA-ddPCR检测沙门氏菌得到的结果与沙门氏菌实际结果相近。
2.8SD-PMA-ddPCR检测人工污染样品中沙门氏菌
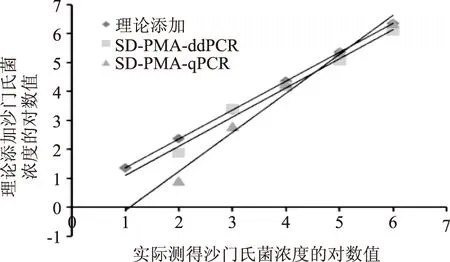
图9 检测人工污染样本中沙门氏菌的比较Fig.9 Salmonella detection of different methods
对不同菌量人工污染的鸡肉样品在优化条件下进行SD-PMA-qPCR、SD-PMA-ddPCR检测,如图9所示,SD-PMA-ddPCR检测人工污染鸡肉样品,最低可检出102CFU/mL沙门氏菌,并且与理论添加值相近;而SD-PMA-qPCR测得CT值代入2.4中线性方程计算得出沙门氏菌含量,与理论添加值偏差较大,说明ddPCR对实际样品的检测效果优于qPCR。SD-PMA-ddPCR对样品检测的RSD均小于5.0%。人工污染死菌的样本37 ℃下放置两周,测得样本的CT值变化小于1.0%。
3 讨论与结论
PMA与ddPCR相结合的方法,可以在死菌存在的条件下定量检测沙门氏菌活菌,消除了“假阳性”结果的出现,SD对样品预处理,使得PMA更容易穿过死菌细胞膜。SD-PMA-ddPCR整个过程快速简便,成功检测鸡肉等样品中沙门氏菌的含量。与SD-PMA-qPCR方法相比,具有准确度高、不需要建立标准曲线等优点,Wang L J等人[16]应用mPCR方法在107CFU/mL热灭活沙门氏菌存在的条件下,定量检测鸡肉等样品中的沙门氏菌。本方法把PMA用量增加了4倍,曝光时间增加了3倍,应用SD-PMA-ddPCR在108CFU/mL热灭活沙门氏菌存在的条件下,定量检测鸡肉等样品中的沙门氏菌,说明PMA浓度的增加和曝光时间延长可以促进PMA与DNA共价交联。SD-PMA-ddPCR方法表现出较好的发展空间,可以进一步应用于其他样品领域的检测。
[1]Gomez T M,Motarjemi Y,Miyagawa S,et al. Foodborne salmonellosis[J]. World Health Statistics,1997,50(1-2):81-89.
[2]Tirado C,Schmidt K. WHO surveillance programme for control of foodborne infections and intoxications,results and trends across greater Europe[J]. Journal of Infection,2001,43(1):80-84.
[3]Majowicz S E,Musto J,Scallan E. The global burden of nontyphoidalSalmonellagastroenteritis[J]. Clinical Infectious Diseases,2010,50(6):882-889.
[4]Burnsa A M,Lawlor P G,Gillian E,et al. GardinerSalmonellaoccurrence and enterobacteriaceae counts in pig feed ingredients and compound feed from feed mills in Ireland[J]. Preventive Veterinary Medicine,2015,121(3-4):231-239.
[5]Zhang H M,Shi L,Guo S Y,et al. Identification and characterization of class 1 integron resistance gene cassettes amongSalmonellastrains isolated from healthy humans in China[J]. Microbiology and Immunology,2004,48(9):639-645.
[6]Master C I,Shallcross J A,Mackey B M,et al. Effect of stress treatments on the detection of Listeria monocytogenes and enterotoxigenicEscherichiacoliby the polymerase chain reaction[J]. Journal of Applied Bacteriology,1994,77(1):73-79.
[7]He X,Hu C,Guo Q,et al. Rapid and ultrasensitiveSalmonellaTyphimurium quantification using positive dielectrophoresis driven on-line enrichment and fluorescent nanoparticleslabel[J]. Biosensors and Bioelectronics,2013(42):460-466.
[8]Aricind A,Bhagwat A A. Simultaneous detection ofEscherichiacoliO157∶H7,ListeriamonocytogenesandSalmonellastrains by real-time PCR[J]. International Journal of Food Microbiology,2003(84):217-224.
[9]Malorny B,Bunge C,Helmuth R. A real-time PCR for the detection ofSalmonellaenteritidis in poultry meat and consumption eggs[J]. Journal of Microbiological Methods,2007,70(2):245-251.
[10]Seo K H,Valentin-Bon I E,Brackett R E. Detection and enumeration ofSalmonellaenteritidis in homemade ice cream associated with outbreak:comparison of conventional and real-time PCR methods[J]. Journal of Food Protection,2006,69(3):639-643.
[11]Whyte P,Gill K M,Collins J,et al. The prevalence and PCR detection ofSalmonellacontamination in raw poultry[J]. Veterinary Microbiology,2002,89(1):53-60.
[12]Nocker A,Sossa-Fernandez P,Burr M D,et al. Use of propidium monoazide for live/dead distinction in microbial ecology[J]. Applied and Environmental Microbiology,2007,73(16):5111-5117.
[13]Cawthorn D M,Witthuhn R C. Selective PCR detection of viableEnterobactersakazakiicells utilizing propidium monoazide or ethidium bromide monoazide[J]. Journal of Applied Microbiology,2008,105(4):1178-1185.
[14]Nocker A,Cheung C Y,Camper A K. Comparison of propidium monoazide with ethidium monoazide for differentiation of live vs. dead bacteria by selective removal of DNA from dead cells[J]. Journal of Applied Microbiology,2006,67(2):310-320.
[15]Forghani F,Langaee T,Eskandari M,et al. Rapid detection of viableBacilluscereusemetic and enterotoxic strains in food by coupling propidium monoazide and multiplex PCR(PMA-mPCR)[J]. Food Control,2015(55):151-157.
[16]Wang L J,Ye C L,Xu H Y,et al.,Development of an SD-PMA-mPCR assay with internal amplification control for rapid and sensitive detection of viableSalmonellaspp.,Shigellaspp. andStaphylococcusaureusin food products[J]. Food Control,2015(57):314-320.
[17]Wang L J,Li P,Zhang Z H,et al. Rapid and accurate detection of viableEscherichiacoliO157∶H7 in milk using a combined IMS,sodium deoxycholate,PMA and real-time quantitative PCR process[J]. Food Control,2014,36(1):119-125.
[18]Morisset D,Stebih D,Milavec M,et al. Quantitative analysis of food and feed samples with droplet digital PCR[J]. PLoS One,2013,8(5):62583-62588.
[19]George D,Czech J,John B,et al. Detection and quantification of chimerism by droplet digital PCR[J]. Chimerism,2013,4(3):102-108.
[20]Beck J,Bierau S,Balzer S,et al. Digital droplet PCR for rapid quantification of donor DNA in thecirculation of transplant recipients as a potential universal biomarker of graft injury[J]. Clinical Chemisty,2013,59(12):1732-1741.
Detection ofSalmonellacells based on SD-PMA-ddPCR
WANG Jing1,ZHANG Hui-min1,WEI Wei1,JIA Jun-tao2,LI Chun-xi1,QIN Yan1
(1.Weihai Entry-exit Inspection and Quarantine Inspection and Quarantine Technology Center,Weihai 264205,China;2.Shandong Entry-exit Inspection and Quarantine Bureau,Qingdao 266500,China)
In this paper,a method to detect liveSalmonellacells was developed based on propidium monoazide(PMA)and ddPCR. The result showed that PMA could not inhibit the DNA PCR amplification of 108CFU/mL deadSalmonellacells,while the combination of sodium deoxycholate(SD)and 40.0 μg/mL PMA could do it. The maximum concentration against DNA amplification from liveSalmonellacells was 40.0 μg/mL. Only liveSalmonellacells were detected by PMA-ddPCR even in the existence of deadSalmonellacells,and the detection limit was 8.0 copy/20 μL. PMA-ddPCR could detect 102CFU/mLSalmonellacells in the polutted sample made by manual work. Furthermore,PMA-ddPCR showed better specificity,accuracy and stability.
propidium monoazide;sodium deoxycholate;ddPCR;live cells
2015-10-08
王静(1975-),女,硕士,高级工程师,研究方向:食品安全,E-mail:15705959793@163.com。
国家质检总局科技计划项目(2014IK114)。
TS207.4
A
1002-0306(2016)10-0067-05
10.13386/j.issn1002-0306.2016.10.004

