气相色谱质谱法测定养殖水体中丁香酚含量不确定度评定
刘海新,余 颖,汤水粉,王丽娟,罗方方
(福建省水产研究所,福建省海洋生物增养殖与高值化利用重点实验室,福建 厦门 361013)
气相色谱质谱法测定养殖水体中丁香酚含量不确定度评定
刘海新,余颖,汤水粉,王丽娟,罗方方
(福建省水产研究所,福建省海洋生物增养殖与高值化利用重点实验室,福建 厦门 361013)
根据测量不确定度评定的基本程序,对本实验室研究建立的气相色谱质谱法测定养殖水体中丁香酚含量结果进行不确定度评定。分析检测过程中引入的不确定度分量,包括标准工作液、样品称量、样液定容、仪器测定、样品前处理重复性等。计算各分量结果并合成相对标准不确定度,在95%置信水平下,包含因子k=2,扩展方法不确定度。结果表明:该检测方法不确定度主要来源于样品前处理过程重复性和仪器测定。因此要确保检测结果的准确可靠,应规范操作、严控工作环境条件,增加平行检测样本数以降低检测方法不确定度。
不确定度;丁香酚;养殖水体;气相色谱质谱
丁香酚(Eugenol)化学名为4-丙烯基-2-甲氧基苯酚,分子式为C10H12O2,广泛存在于丁香油、肉桂叶油、樟脑油、豆蔻油等芳香油中,其药理作用广泛,具有麻醉、抗炎、抗过敏、抗细菌和真菌、抗氧化、促进药物透皮吸收等作用[1]。欧洲食品安全局(EFSA)研究表明,丁香酚具有发育毒性,根据其未观察到不良作用水平(NOAEL),采用100倍安全系数,制定人体食用安全限量为1.0 mg/kg·bw·day[2]。丁香酚对鱼类具有麻醉作用[3-4],其麻醉机理为首先抑制鱼类的脑皮质,使其丧失触觉,然后作用于基底神经节和小脑,并最终作用于脊髓达到麻醉效果[5]。丁香酚因价格低廉、高效、易于购买,而被许多鱼商用于麻醉鱼,以提高长途运输密度。目前,我国尚未批准使用渔用麻醉剂,因此在运输水体中添加使用丁香酚并不违法,但丁香酚在流通环节潜在的风险日益受到人们的关注。水体中丁香酚检测方法标准尚未出台,有学者采用较昂贵的气相色谱-串联质谱仪(GC-MS/MS)检测水体中丁香酚[6]。本研究在参考该检测方法的基础上,优化提取和净化过程、增加固相萃取净化步骤,提高净化效果,采用相对廉价、普及的气相色谱-质谱仪(GC-MS)检测,检测方法相关性能指标符合标准要求。
测量的不确定度是表征合理地赋予被测量之值的分散性,与测量结果相联系的参数,是对测定结果不可信程度或对测定结果有效性的怀疑程度。由于被测量的真值难以准确复现,因此科学合理地进行测量结果不确定度分析,并将其应用于测定结果评定中,对提高检测结果的质量、降低误判风险具有重要意义[7]。本文针对本实验室研究建立的气相色谱质谱法测定水体中丁香酚含量结果,根据《CNAS-GL06化学分析中不确定度的评估指南》[8]和《JJF1059.1-2012测量不确定度评定与表示》[9]规定的基本程序,同时参考水产品中甲基睾酮不确定度评定[10]、苹果中多菌灵残留量测量不确定度分析[7]、葡萄酒中山梨酸含量的不确定度的评定[11]等,对该检测方法测量不确定度进行评定,为科学、准确、合理表述检测结果提供参考。
1 材料与方法
1.1材料与试剂
丁香酚(CAS:97-53-02)和甲基丁香酚(CAS:93-15-2)标准品(纯度≥99%):德国Dr.Ehrenstorfer公司;乙酸乙酯(色谱纯)、正己烷(色谱纯):美国Tedia公司;硅胶固相萃取柱(2 g/6 mL):德国CNW公司;其余试剂均为国产分析纯试剂;水为符合GB/T 6682规定的一级水。
1.2仪器与设备
Thermofisher DSQ气相色谱质谱联用仪:美国Thermofisher公司;电子分析天平AB204-E:瑞士梅特勒托利多公司;R206-B旋转蒸发仪:上海申生科技有限公司;TDL-40B低速台式大容量离心机:上海安亭科学仪器厂。
1.3检测方法
1.3.1标准溶液配制
丁香酚标准储备液和标准中间液:称取丁香酚标准品10.0 mg(精确至0.1 mg),用乙酸乙酯溶解定容于100 mL容量瓶,配制成100 μg/mL的标准储备液,(4±2)℃下避光保存。用1 mL的分度吸量管移取1.00 mL标准储备液,用乙酸乙酯定容到10 mL,配制成10.0 μg/mL的标准中间液,(4±2)℃下避光保存。
100 μg/mL甲基丁香酚内标储备液和10.0 μg/mL内标中间液配制方法和保存条件同丁香酚标准储备液和标准中间液。
内标稀释液:移取10.0 μg/mL的内标中间液1.00 mL,乙酸乙酯定容到10 mL,得到1.00 μg/mL的内稀释液;移取10.0 μg/mL的内标中间液0.40 mL,乙酸乙酯定容到10 mL,得到0.40 μg/mL的内标稀释液,使用时现配现用。
标准工作液:用1 mL的分度吸量管和10 mL的容量瓶,移取适量10.0 μg/mL丁香酚标准中间液,用乙酸乙酯溶液逐级稀释成浓度为0.005、0.01、0.05、0.10、0.15、0.50、1.00 μg/mL的标准工作液。标准工作液定容前,加入1.00 μg/mL的内标稀释液1.00 mL,使得每个浓度标准工作液中内标物浓度均为0.10 μg/mL,使用时现配现用。
1.3.2样品提取和净化
水样经0.45 μm滤膜抽滤,用50 mL量筒量取过滤后的水样20.0 mL于三角瓶中,加入氯化钠1.5~2.0 g,振荡溶解。将水样转入100 mL分液漏斗中,加入20 mL正己烷,剧烈振荡2 min后静置5 min,收集上层有机相于100 mL三角瓶中。用15 mL正己烷重复提取一次,合并两次萃取的有机相。加入4.0~5.0 g无水硫酸钠,旋涡振荡10 s后,转入100 mL鸡心瓶中。用5 mL正己烷洗涤无水硫酸钠,合并正己烷于鸡心瓶中。于37℃减压浓缩至8~10 mL,用于固相萃取。
硅胶固相萃取柱(2 g/6 mL)预先用3 mL正己烷活化,上样,4 mL正己烷淋洗,8 mL乙酸乙酯洗脱,收集洗脱液于玻璃刻度试管中,40 ℃氮吹至1.5 mL,加入0.40 μg/mL内标样液添加液0.5 mL,定容到2 mL,混匀,0.22 μm有机相针式过滤器过滤,供气相色谱-质谱仪测定。
1.3.3仪器条件
1)色谱条件
色谱柱:Thermo TG-1701MS石英毛细管柱(30 mm×0.25 mm×0.25 μm);进样口温度250℃;进样方式:不分流进样;进样量:1 μL;色谱柱升温程序:初始温度为80℃,保持2 min;10℃/min升温至185℃;20℃/min升温至250℃,保持4 min。
2)质谱条件
电离模式:电子轰击电离源(EI),能量:70 eV;离子源温度:250℃;传输线温度:250℃;溶剂延迟10 min。
离子检测方式:选择离子检测(SIM),丁香酚检测离子为:103、131、149、164,定量离子164;甲基丁香酚检测离子:103、147、163、178,定量离子178。
1.3.4结果计算
采用内标法单离子定量,选定浓度与样液相近的标准工作液,按内标法以峰面积比计算。标准工作溶液和样液中的丁香酚和甲基丁香酚响应值均应在仪器线性范围内,水体中丁香酚含量计算公式如下:
(1)
式中:X为试样中目标物质的含量,μg/L;A为样液中丁香酚的峰面积;Cs为标准工作液中丁香酚的浓度,μg/mL;Bs为标准工作液中内标的峰面积;B为样液中内标的峰面积;As为标准工作液中丁香酚的峰面积;Vm为试样体积,mL;V为试样定容体积,mL。
2 结果与分析
2.1不确定度来源
从检测过程和计算公式进行分析,样品测定不确定度来源主要包括以下几个方面:标准工作液引入的不确定度urel(std)、样品称量引入的不确定度urel(m)、样液定容引入的不确定度urel(Vd)、仪器测定引入的不确定度urel(Y)、样品提取净化过程重复性引入的不确定度urel(rep),如图1所示。

2.2各分量不确定的计算
2.2.1标准工作液引入的不确定度urel(std)
根据标准工作液的配制过程,标准工作引入的不确定度包含两个分量:丁香酚标储备液配制引入的不确定度urel(Ceugenol)和标准工作液稀释过程引入的不确定度urel(Vw)。
1)丁香酚标储备液引入的不确定度urel(Ceugenol)
(1)标准物质纯度引入的不确定度urel(P)
丁香酚纯度为99%,最大允许误差为1%,服从正态分布,95%置信水平包含因子k=2,标准不确定度u(P)=0.01/2=5.00×10-3,相对标准不确定度为urel(P)=5.00×10-3。
(2)标准物质称量引入的不确定度urel(Mr)
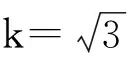
(3)标准储备液定容引入的不确定度urel(Vs)

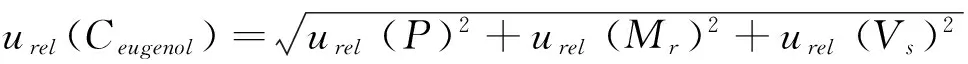
2)标准工作液稀释过程引入的不确定度urel(Vw)
(1)量器校准引入的相对标准不确定度urel(Vw1)
由于采用内标法定量,在评定标准工作液引入的不确定度时,需同时评定标准工作液中的目标物和内标引入的不确定度。根据丁香酚含量结果计算的数学公式,结果仅与内标的响应值有关,而与内标实际浓度值无关。同时,由于标准溶液和样液中的内标都来源于10.0 μg/mL的内标中间液,因此,内标对检测结果不确定度的引入,与内标储备液配制和稀释到10.0 μg/mL内标中间液之前的过程无关。内标加入到标准工作溶液中的环节,是在标准工作液最终定容到10 mL前,加入1.00 μg/mL的内标稀释液1.00 mL。

urel(Vw1)=
=8.80×10-3

表1 标准溶液稀释量器校准引入的不确定度
注:稀释过程使用的分度吸量管和容量品均为A级。
Note:The graduated pipettes and volumetric flasks used in dilution process of standard solution are grade A.
(2)环境温度变化引起溶剂体积改变引入的相对标准不确定度urel(Vw2)
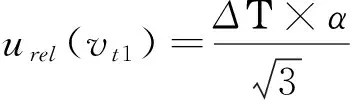

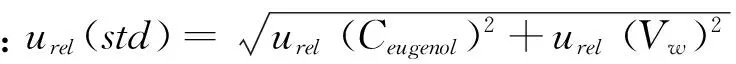
2.2.2样品称量引入的不确定度urel(m)

2.2.3样液定容引入的确定度urel(Vd)
由于采用内标法定量,样液定容不确定度来源于样液中加入的内标量。样液中内标引入是在样液进仪器分析前,加入0.50 mL浓度为0.40 μg/mL的内标稀释液。
1)量器校准引入的相对标准不确定度urel(Vd1)

urel(Vd1)=
=0.010 5

表2 内标稀释及加入样液过程量器校准引入的不确定度
注:稀释过程使用的分度吸量管和容量品均为A级。
Note:The graduated pipettes andvolumetric flasks used in process of standard solution diluted are grade A.
2)环境温度变化引起溶剂体积改变引入的相对标准不确定度urel(Vd2)

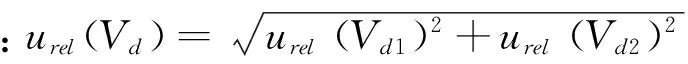
2.2.4仪器测定引入的不确定度urel(Y)

2.2.5样品前处理重复性引入的不确定度urel(rep)
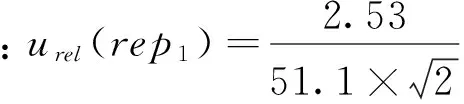
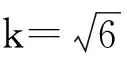



表3 加标水样平行检测结果
2.3合成相对标准不确定度及扩展不确定度
上述各项不确定度分量见表4,互相独立,养殖水体中丁香含量检测合成相对不确定度为:urel(X)=


表4 不确定度分量表
根据不确定度评定指南[8],在95%置信水平,推荐包含因子k=2。试样中丁香酚含量测定的扩展不确定度为:U(X)=k×u(X)=2×2.5=5.0 μg/L。因此,结果表述为:检测结果平均值及其不确定度为(50.2±5.0)μg/L。
2.4不同浓度点的不确定度差异对检测结果影响
本方法采用的定量方式为内标法单离子定量,选定浓度与样液相近的标准工作液,以峰面积比计算。由于不同浓度标准工作液稀释次数不同,浓度越低的标准工作液,相对标准不确定度越高,对结果引入的不确定度也相应增大。本方法标准工作液最高浓度点为1.00 μg/mL,最低浓度点为0.005 μg/mL,按照上述方法计算,对应的相对标准不确定度分别为urel(std1.00)=0.013 4和urel(std0.005)=0.016 7,检测结果的相对标准不确定度分别为urel(X1.00)=0.049和urel(X0.005)=0.050。因此,由标准工作液不确定度不同,而导致最终检测结果不确定度的差异可以忽略。
3 结论
本研究从标准溶液配制、样品称量、样液定容、仪器测定、样品前处理重复性等几方面对养殖水体中丁香酚残留检测结果的不确定度进行分析。由表4可知,检测结果不确定度主要来源于样品提取净化过程重复性和仪器测定。因此,要保证检测结果的准确可靠应注意以下四方面:1)严格控制样品前处理过程,特别强调操作的规范性;2)控制好气相色谱—质谱联用仪的工作环境条件及仪器中易污染部件的洁净,降低由仪器测定引入的不确定度;3)标准工作液和阳性样品的仪器测定值,必须以多次进样的算术平均值参与结果计算;4)阳性样品要以平行样品的算术平均值作为检测结果,单样的检测结果不确定度大。
[1]邱电,张魁华,方炳虎.丁香酚的药理作用[J].动物医学进展,2007,28(8):101-103.
[2]European Food Safety Authority.Conclusion on the peer review of the pesticide risk assessment of the active substance eugenol[J].EFSA Jorunal,2012,10(11):2914.
[3]梁政远,安丽娜,缪凌鸿,等.丁香油对鲤鱼和罗非鱼的麻醉作用[J].水产学杂志,2009,22(1):42-46..
[4]张志明,胡盼,姜志强,等.丁香酚对锦鲤麻醉效果的研究[J].水产科学,2014,33(1):40-45.
[5]吕海燕,王群,刘欢,等.鱼用麻醉剂安全性研究进展[J].中国渔质量与标准,2013,3(2):24-28.
[6]柯常亮,刘奇,陈洁文,等.气相色谱-串联质谱联用法测定水中丁香酚残留[J].中国渔业质量与标准,2014,4(4):49-53.
[7]杨媛,石磊,李文生,等.高效液相色谱法测定苹果中多菌灵残留量的测量不确定度分析[J].农药学学报,2010,12(3):349-354.
[8]中国合格评定国家认可委员会.CNAS-GL06:2006 化学分析中不确定度的评估指南[S].北京:中国计量出版社,2006.
[9]国家质量监督检验检疫总局.JJF1059.1-2012 测量不确定度评定与表示[S].北京:中国质检出版社,2013.
[10]张惠峰,綦天华.高效液相色谱法测定水产品中甲基睾酮残留量的不确定度评定[J].食品科学,2015,36,(18):199-203.
[11]顾晓俊,汤海青,欧昌荣.高效液相色谱法测定葡萄酒中山梨酸含量的不确定度评定[J].中国食品学报,2014,14,(12):143-147.
[12]国家质量监督检验检疫总局.JJG 196-2006 常用玻璃量器[S].北京:中国计量出版社,2006.
Uncertainty evaluation for detecting eugenol in aquaculture water by gas chromatography mass spectrometric
LIU Haixin,YU Ying,TANG Shuifen,WANG Lijuan,LUO Fangfang
(Key Laboratory of Cultivation and High-value Utilization of Marine Organisms in Fujian Province,Fisheries Research Institute of Fujian,Xiamen 361013,China)
According to the procedure for uncertainty assessment,we evaluated the measurement uncertainty of detecting eugenol in aquaculture water by GC-MS method which established in our lab.The components of uncertainty in the detecting process were studied and analyzed,including standard work solution,weighting sample,constant sample solution volume,instrument detection and sample preparation repeatability,then calculating and combining these components of uncertainty.At the 95% confidence level,the coverage factor k=2,expanding the method uncertainty.The results showed the major factors of uncertainty in this method were sample preparation repeatability and instrument detection.In order to insure that the detecting results are accuracy and reliable,we should standardize the operation,strictly control environmental condition and increase parallel sample.
uncertainty;eugenol;aquaculture water;gas chromatography mass spectrometric
2016-05-22
福建省属公益类科研院所基本科研专项(2016R1003-14);闽台重要海洋生物资源高值化开发技术公共服务平台(2014FJPT01);福建重要海洋经济生物种质库与资源高效开发技术公共服务平台(14PZY017NF17).
刘海新(1974-),男,副研究员,主要从事水产品安全检测技术研究.E-mail:liuhaixin303@163.com
O657
A
1006-5601(2016)04-0310-08
刘海新,余颖,汤水粉,等.气相色谱质谱法测定养殖水体中丁香酚含量不确定度评定[J].渔业研究,2016,38(4):310-317.

