华卟啉钠的光漂白性质研究
刘汉清,姜智焕,吴文涛,魏金峰,,靳洪涛,,,王爱平,,
华卟啉钠的光漂白性质研究
刘汉清1,姜智焕2,吴文涛3,魏金峰1,2,靳洪涛1,2,*,王爱平1,2,*
(1. 中 国医学科学院北京协和医学院药物研究所,北京100050;2. 北 京协和建昊医药技术开发有限责任公司,北京100176;3. 奥 溪利亚医药科技有限公司,天津300384)
目的: 观察华卟啉钠(DVDMS)在不同溶液中及动物皮肤中的光漂白性质。方法:采用微量分光光度计,测量不同浓度DVDMS(10、20、40 μg/mL)在生理盐水(NS)、RPMI-1640培养基(RPMI-1640)、含10%胎牛血清的RPMI-1640培养基(RPMI-FBS)和HaCaT细胞悬液中的吸收峰;设置DVDMS浓度1、2.5、5、10、20、40 μg/mL,采用酶标仪分别检测在激光照射3、6、10、20、40、50、60、120、180 min后DVDMS在上述4种溶液中的光漂白;正常和银屑病裸鼠均尾静脉注射DVDMS 2 mg/kg,采用小动物活体成像仪观察DVDMS在皮肤组织中的分布及激光照射后在银屑病模型动物皮肤组织中的漂白现象。结果:DVDMS 10、20、40 μg/mL在本实验设置的4种溶液中特征吸收峰明显;在前期药效学研究的条件下(激光照射3 min),DVDMS在4种溶液中发生了光漂白;在180 min内,DVDMS的光漂白呈现先快后慢的二相过程;DVDMS在正常和银屑病模型动物组织中分布均匀,在9.6 J/cm2激光照射后,DVDMS在银屑病模型动物皮肤组织中发生了明显光漂白。结论:DVDMS体外光漂白受光剂量、初始浓度、溶剂种类的影响,符合二级动力学模型,在银屑病模型动物皮肤组织中被激光照射后可发生光漂白。
华卟啉钠;激光;光漂白;银屑病
【ABSTRACT】OBJECTIVE: To observe the photobleaching characters of sinoporphyrin sodium (DVDMS) in different solutions and skins of animal. METHODS:Absorption peaks of DVDMS (10,20,40 μg/mL) in normal saline (NS),RPMI-1640 medium (RPMI-1640),RPMI-1640 medium containing 10% fetal calf serum (RPMI-FBS) and suspension of HaCaT cells were measured using micro-spectrophotometer. Using DVDMS solutions with concentrations of 1,2.5,5,10,20 and 40 μg/mL in the 4 solvents above,photobleaching of DVDMS after laser radiation for 3,6,10,20,40,50,60,120,180 min was observed using microplate reader. In vivo image acquisition system was used to study the distribution of DVDMS in animal skins,and the bleaching after irradiation in psoriasis-like animal skins were also observed. RESULTS:DVDMS with concentrations 10,20 and 40 μg/mL showed obvious characteristic absorption peaks in the 4 solutions. Photobleaching occurred in the 4 solutions under the irradiation conditions used in previous pharmacodynamics studies (laser radiation was 3 minutes). Two-phase processes photobleaching (fast first phase and second slow phase) of DVDMS were observed in 180 min. The distributions of DVDMS in skins of normal and psoriasis-like animal were uniform,obvious photobleaching occurred in skins of psoriasis-like animal after laser irradiation with dose of 9.6 J/cm2. CONCLUSION:In vitro photobleaching of DVDMS was influenced by light dose,initial concentrations and solvents. Secondary-dynamic model was suitable to describe the photobleaching progress. Photobleaching occurred in skins of psoriasis-like animal after laser irradiation.
【KEY WORDS】sinoporphyrin sodium;laser;photobleaching;psoriasis
光动力疗法(photodynamic therapy,PDT)是20世纪初兴起的一种新型治疗方法,对于肿瘤和非肿瘤性皮肤病具有良好的治疗效果[1-2]。光敏剂、激光和氧是PDT必备的3个要素。PDT的基本过程是:处于基态的光敏剂分子被特定波长的光照射后,吸收光能并跃迁为激发态,然后通过体系间跨越转变为三线态。三线态光敏剂分子可与生物分子直接发生氧化还原反应产生活性氧、超氧阴离子等,破坏细胞结构、抑制细胞核内DNA和RNA等从而发挥作用(Ⅰ型反应);也可与氧分子发生氧化还原反应形成单线态氧1O2,进而与生物分子发生反应(Ⅱ型反应)。Ⅰ型反应和Ⅱ型反应竞争发生,其中Ⅱ型反应被普遍认为是PDT的主要机制[3-4]。
光漂白是在光物理或光化学过程中光造成的发色团吸收强度或发射强度减少的现象。在PDT中,光漂白是指光敏剂被损耗的现象[3]。光漂白在PDT过程中伴随产生而产生,因而是不可避免的。大量研究表明,PDT治疗效果与光漂白的量和漂白速度有关[5-6]。在PDT治疗中,即便给予相同剂量的光敏剂、相同代谢时间及激光照射剂量,不同病人间的治疗效果仍可能有较大差异[7]。这是因为除以上因素外,PDT疗效还取决于病变组织、氧分压、光敏剂的光漂白和产率等因素。因此,精确量化给药量和激光照射条件,并根据患者的个体差异进行剂量的实时调整和优化,已成为亟待解决的难题。基于此,近年来提出了PDT剂量这一概念,定义为PDT治疗过程中的总产量。由于光漂白伴随的产生而发生,因此可以用光漂白量来估算PDT过程中光敏剂产生的量及PDT剂量[8]。
因此研究光敏剂的光漂白性质,对其治疗前景预测,PDT剂量设计等具有重要意义。华卟啉钠(sinoporphyrin sodium,DVDMS)是中国医学科学院药物研究所方起程教授创制的一种新型卟啉类光敏剂,具有结构明确、作用性强、毒性低等优点,可被630 nm激光特异性激发。本实验室系统评价了DVDMS的抗肿瘤药效学和毒理学作用,并确认了其抗银屑病疗效[9]。DVDMS的抗肿瘤药效学研究现已进入临床阶段,但其光漂白性质尚未测定,亦未见相关文献报道。本课题旨在观察DVDMS在不同溶液及动物皮肤组织中的光漂白性质,为后续抗银屑病药效学研究提供指导并为临床抗肿瘤药效学PDT剂量设计提供参考。
1 材料与方法
1.1材料
1.1.1仪器PDT-630激光肿瘤治疗仪,购自桂林市兴达光电医疗器械有限公司;Spectra Max Gemini XS荧光酶标仪,购自美国MD公司;Q5000微量分光光度计,购自美国Quawell公司;Caliper小动物活体成像仪,购自美国Caliper Life Sciences公司。
1.1.2试剂DVDMS由青龙高科技股份有限公司提供,由中国医学科学院新药安全评价研究中心供试品管理部门保管,供试品编号1108,用前领取。咪喹莫特乳膏(imiquimod cream,IMQ)购自湖北科益药业股份有限公司。RPMI-1640培养基,购自HyClone公司;胎牛血清(fetal bovine serum,FBS),购自浙江天杭生物科技有限公司;氯化钠注射液(0.9 % NaCl),购自石家庄四药有限公司。DVDMS溶液配制:取DVDMS冻干粉1瓶(10 mg),加入生理盐水 5 mL,配制为浓度为2 mg/mL的储备液,测量时稀释至所需浓度。
1.1.3动物Crl:NU-Foxn1nu免疫缺陷裸鼠,SPF级,雌雄各半,体质量18~22 g,由北京维通利华实验动物技术有限公司提供,生产许可证号SCXK(京)2006-0009,动物合格证号11400700079106。饲养于恒温恒湿的屏障环境,自由饮食、饮水。SPF级鼠料,制造单位为中国人民解放军军事医学科学院实验动物中心。饮水为自来水过滤、灭菌。
1.1.4细胞HaCaT细胞购自中国医学科学院基础医学研究所细胞资源中心。以含10% FBS的RPMI-1640培养基常规培养。取对数生长期细胞,制备细胞悬液,浓度为1×106/mL。
1.2方法
1.2.1吸收光谱测定前期体外抗肿瘤药效学研究中DVDMS体外给药浓度为0.001~10 μg/mL,体内药效学研究所用浓度为25、50、100 μg/mL。溶剂类型是影响光敏剂光漂白性质的重要因素[10]。在体内药效学研究中,配制光敏剂注射液所用溶液为生理盐水(normal saline,NS)而体外药效学所用溶剂为RPMI-1640培养基溶液。因此,设置NS,RPMI-1640培养基溶液(下称RPMI-1640),含10% FBS的RPMI-1640培养基溶液(下称RPMI-FBS)及HaCaT细胞悬液(下称细胞悬液)4种溶剂。以这4种溶剂配制DVDMS溶液,设置其终浓度分别为10、20、40 μg/mL,采用微量分光光度计测定其吸收光谱及最大吸收峰,上样量2.5 μL。
1.2.2标准曲线绘制配制DVDMS在上述4种溶剂中终浓度分别为0、0.1、0.25、0.5、1、2.5、5、10、20、40、80 μg/mL的溶液,加入到96孔板中,采用酶标仪以最大吸收峰为测定波长,测定在不同溶液中的吸光度并绘制吸光度-浓度曲线。
1.2.3DVDMS在不同溶液中光漂白性质测定前期体外抗肿瘤药效学研究中激光照射条件为:输出功率1.50 W,光斑直径8 cm,照射时间3 min,功率密度0.03 W/cm2,能量密度5.4 J/cm2,均在氧不饱和条件下进行测定。根据以上测定结果,DVDMS在浓度0.001~0.5 μg/mL范围内,激光照射前后吸光度变化较小,检测灵敏度较低,而在浓度过高时,DVDMS分子可能发生聚集。因此设置光敏剂浓度为1~40 μg/mL。
激光照射剂量(能量密度)主要受输出功率、光斑直径和激光照射时间的影响,由于在药效学研究中通常输出功率和光斑直径都是固定的,因此主要观察激光照射时间对光漂白的影响。为观察到发生光漂白的时间,固定输出功率为1.50 W,光斑直径为8 cm,设置激光照射时间分别为3、6、10、20、40、50、60、120、180 min,DVDMS浓度分别1、2.5、5、10、20、40 μg/mL。同时设置非激光照射对照组。将溶液加入96孔板中,测量吸光度并绘制吸光度-浓度曲线。此后,将96孔板置于激光肿瘤治疗仪下进行激光照射,照射结束后再次测量吸光度。对照组除不进行激光照射外,其余操作与激光照射组相同。根据吸光度-浓度曲线计算激光照射前后光敏剂浓度,按以下公式计算光漂白量、光漂白率及单位时间光漂白率。
光漂白量=激光照射前浓度-激光照射后浓度
光漂白率=[D(λ)0-D(λ)t] /D(λ)0×100%
单位时间光漂白率=累积漂白率/累积漂白时间
其中为D(λ)0激光照射前所测量吸光度,D(λ)t为 激光照射后所测量吸光度,λ为测量波长,t为照射时间。为消除测量因素和自然漂白的影响,用激光照射组测量值-对照组测量值作为光漂白量或光漂白率的真实值。
1.2.4DVDMS在动物组织中的吸收和光漂白为比较DVDMS在正常动物和银屑病模型动物组织中的分布,4只裸鼠随机分为正常组和DVDMS银屑病模型组,每组2只,雌雄各半。银屑病模型组动物背部皮肤涂抹5% IMQ,按每只约100 mg,每日1次,连续6 d制成银屑病模型,正常组动物不涂药。造模结束后,各组动物均尾静脉注射DVDMS 2 mg/kg,之后腹腔注射戊巴比妥钠60 mg/kg麻醉,分别采集给药后8、12、24 h背部及腹部的图像并进行比较。给药24 h后处死动物,解剖取心、肝、脾、肺、肾、皮肤等,采集图像并观察。
为观察DVDMS在银屑病模型动物皮肤组织内的光漂白,4只裸鼠随机分为激光照射组和非照射组,每组2只,雌雄各半。按上述方法制成银屑病模型。造模结束后,各动物尾静脉注射DVDMS 2 mg/kg,给药6 h后激光照射组进行激光照射(输出功率0.20 W,光斑直径4 cm,照射时间10 min,能量密度9.6 J/cm2),对照组不进行激光照射。麻醉后采集给药后8、12 h(激光照射后2、6 h)腹部和背部的图像。
光场校正后进行拍摄,拍摄同一视野下的X光和荧光图像。将采集的荧光图像添加RGB伪彩,按同一标尺调节至最佳显示效果后与X光图像叠加后输出。
1.2.5统计学方-法采用SPSS 17.0软件进行数据处理,计量数据以x±s表示,激光照射组和非照射组间光漂白量及光漂白率的差异分析采用单因素方差分析,以α=0.05为检验水准。
2 结 果
2.1DVDMS吸收光谱
根据质量标准,DVDMS水溶液(浓度2~4 μg/mL),应在(371.0±2)、437.0、518.0、580.0、632.0 nm处有吸收峰。吸收光谱测定显示,DVDMS在NS、RPMI-1640、RPMI-FBS和细胞悬液4种溶液中的吸收峰类似,特征明显,符合质量标准,见图1。在相同浓度下,DVDMS在4种溶液中的吸光度值为RPMIFBS﹥RPMI-1640﹥NS﹥细胞悬液,最大吸收峰波长为细胞悬液﹥RPMI-FBS﹥RPMI-1640﹥NS,见 表1。

表1 DVDMS在不同溶液中的最大吸收峰
2.2DVDMS在不同溶液中的吸光度-浓度曲线
采用表 1中平均值作为测量波长,测定并绘制DVDMS在上述4种溶液中的吸光度-浓度曲线。如图2所示,DVDMS在浓度为0~40 μg/mL范围内在4种溶液中浓度与吸光度符合郎伯比尔定律,主要以单体形式存在。当浓度提高到80 μg/mL时,DVDMS在4种溶液中的吸光度-浓度曲线R2值随之减小,特别是RPMIFBS的R2值明显减小,见图2。证明随浓度升高DVDMS在溶液中的聚集作用增加,在RPMI-FBS中,当浓度高于80 μg/mL时聚集明显。因此,在后续光漂白研究中采用40 μg/mL以下浓度。
2.3DVDMS在药效学研究条件下的光漂白
DVDMS在前期抗肿瘤药效学研究中所用光剂量(激光波长630 nm,输出功率1.50 W,光斑直径8 cm,照射时间3 min,功率密度0.03 W/cm2,能量密度5.4 J/cm2)下,在浓度为1~40 μg/mL范围内,在上述4种溶液中均发生了一定程度的光漂白。在RPMI-FBS中DVDMS光漂白率随浓度升高而降低,而在NS、RPMI-1640和细胞悬液中光漂白率随浓度升高呈现先升高后降低的现象,见图 3和图4。

图1 DVDMS在不同溶液中的吸收峰

图2 DVDMS在不同溶液中的吸光度-浓度曲线
2.4DVDMS在不同溶液中的光漂白动力学
DVMDS在浓度1~40 μg/mL范围内,照射时间10~180 min内(激光波长630 nm,输出功率1.50 W,光斑直径8 cm,功率密度0.03 W/cm2)在NS、RPMI-1640、RPMI-FBS内均发生了光漂白,见图 5和图6;在细胞悬液中,虽然DVDMS激光照射组吸光度随照射时间延长发生明显降低,但对照组吸光度亦随照射时间延长发生明显降低,因此未观察到明显的光漂白作用,见图7。说明DVDMS明显被HaCaT细胞吸收,且吸收速度较快。DVDMS在4种溶液中的光漂白速度为RPMI-FBS>NS>RPMI-1640>细胞悬液,见表2。

图3 DVDMS在不同溶液中光漂白量

图4 DVDMS在不同溶液中光漂白率比较
随着累积照射时间的延长,DVDMS每分钟漂白率逐渐降低,说明其漂白呈现先快后慢的二相过程,见图8。以时间为自变量对DVDMS在NS、RPMI-1640和RPMI-FBS中的光漂白率(%)进行线性回归分析(细胞悬液由于未检测到明显漂白,不进行拟合),经Pearson拟合度检验发现,DVDMS在3种溶液中的光漂白率与时间的对数呈线性相关,见表2。以激光照射时间和初始浓度为自变量对DVDMS的光漂白率(%)进行线性回归分析,在NS、RPMI-1640,RPMI-FBS中的拟合公式分别为Y=0.902+0.068X1+0.075X2(R=0.866,F=85.581,P=0.000),Y=2.620+0.071X1+0.006X2(R=0.914,F= 145.435,P=0.000),Y=2.929+0.165X1+0.247X2(R=0.737,F=33.962,P=0.000)。其中Y为漂白率(%),X1为激光照射时间,X2为初始浓度。进一步以溶剂类型、激光照射时间和初始浓度为自变量对DVDMS的光漂白率(%)进行线性回归分析,得到拟合公式分别Y=1.073+ 1.348Xi+ 0.079X2-0.008X3(R=0.520,F=29.195,P=0.000),其中Y为漂白率(%);Xi为 溶液类型,1代表NS,2代表RPMI-1640,3代表RPMI-FBS;X2为激光照射时间;X3为初始浓度。
2.5DVDMS在动物组织中的吸收和漂白

图5 DVDMS在不同溶液中的光漂白量比较(10~180 min)

图6 DVDMS在不同溶液中的光漂白率比较(10~180 min)

图7 DVDMS在细胞悬液中浓度和吸光度减少量

图8 DVDMS在不同溶液中单位时间漂白率的比较
进行荧光测定时,激发波长应大于发射波长。小动物活体成像仪的激发波长有430、590、610、630、670 nm,发射波长有535、600、790 nm。为确定最佳测量波长,裸鼠按2 mg/kg尾静脉注射DVDMS,1 h后腹腔注射戊巴比妥钠60 mg/kg麻醉,测量并比较不同波长组合下的荧光强度。DVDMS在激发波长430 nm,发射波长600 nm时荧光信号最强,但各位置信号无差异,不适合观察,在激发波长630 nm,发射波长790 nm处荧光强度高于激发波长590 nm,发射波长790 nm。因此选择荧光测量条件为激发波长630 nm,发射波长790 nm。
裸鼠按2 mg/kg尾静脉注射DVDMS,给药后8、12、24 h在银屑病模型组和正常组皮肤中含量无显著差异;在银屑病模型组皮损部位(背部皮肤)和非皮损部位(腹部皮肤)内含量无明显区别,模型组各动物在皮肤组织中的分布基本一致,差异较小,见图9。说明DVDMS在IMQ银屑病模型动物皮肤组织中分布较为均匀,荧光均一性较好。
DVDMS给药6 h后进行激光照射,照射后2、6 h(给药后8、12 h),激光照射动物背部皮肤组织中含量均明显低于非照射对照组动物,见图10。说明在能量密度为9.6 J/cm2的激光照射后,DVDMS在IMQ银屑病模型动物皮肤组织中发生了明显光漂白。
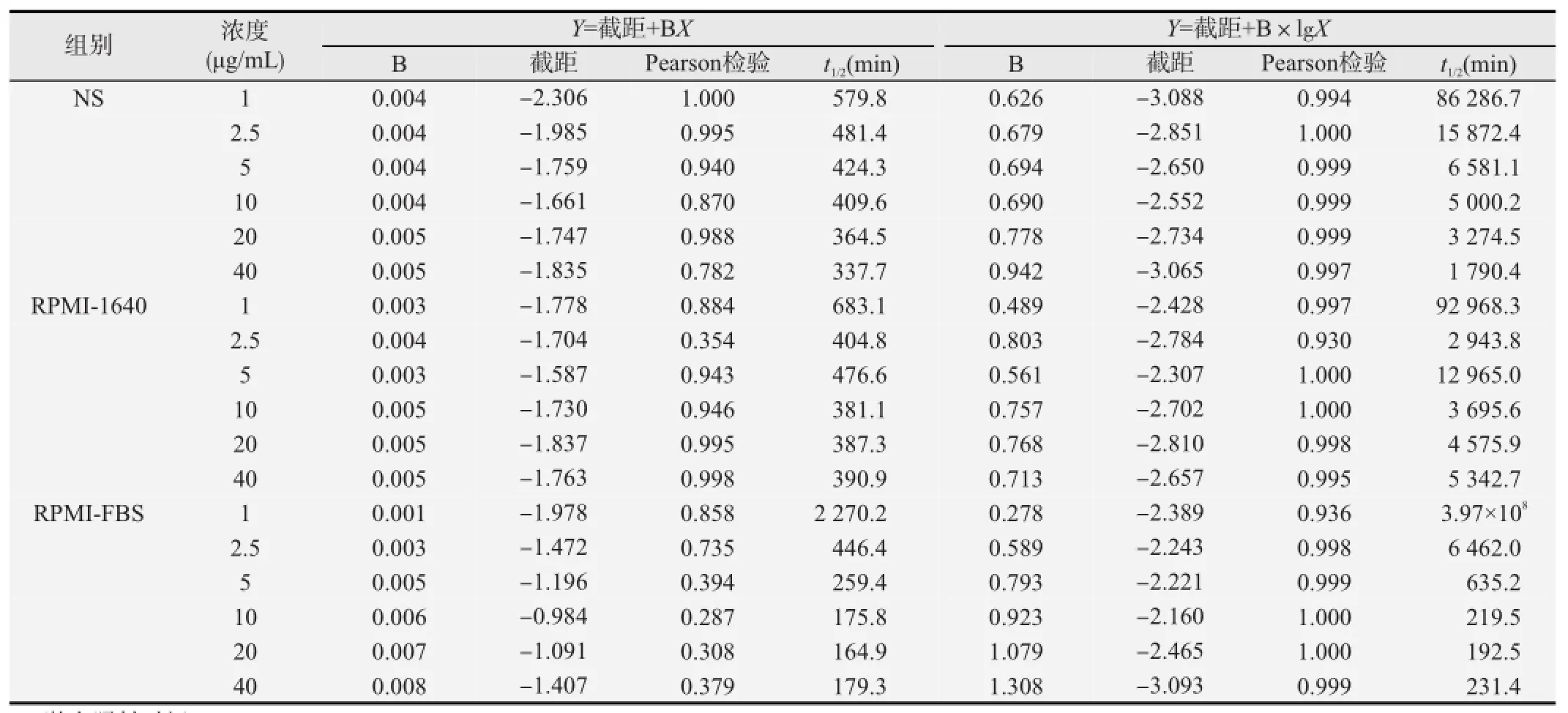
表2 DVDMS在不同溶液中的漂白动力学
3 讨论
光漂白的研究最早发生在染料性质和生物领域。相对于PDT治疗效果的研究,光敏剂光漂白性质的研究较少且缺乏相关的标准和指导原则。目前对于光敏剂光漂白性质的研究方法主要有荧光法和吸光度法两种。对于细胞及体内研究常采用荧光法,而对于体外溶液体系内的光漂白研究常采用吸光度法。如Zeng等[11]采用荧光光谱法测定了维替泊芬类似物QLT0074在BALB/c小鼠皮肤的光漂白性质,并提出3个新参数用于预测PDT引起的后果。王颖等[10]采用岛津UV-1601分光光度计测定吸收光谱,研究了HMME 在不同溶液中的光漂白反应动力学。
本研究采用全波长酶标仪为吸光度检测手段,构建光漂白检测系统。相对于分光光度计,酶标仪可同时检测多个样本,大大提高了通量并减少了供试品用量,极大地降低了研究的成本。研究发现,在一定浓度范围内,光敏剂在NS、RPMI-1640、RPMI-FBS和细胞悬液中的吸光度-浓度曲线线性良好且激光照射前后吸光度的变化比较敏感。为光敏剂体外溶液中的光漂白性质研究提供了参考。
许多研究表明光敏剂的光漂白与治疗效果有关。如Ascencio等[6]观察了荷瘤大鼠体内诱导原卟啉IX (protoporphyrin IX,PpIX)的光漂白和肿瘤组织坏死的关系,发现PpIX光漂白与肿瘤组织坏死之间呈直接线性相关,漂白率高的治疗效果好,而漂白率低的无效。Johansson等[7]对恶性胶质瘤病人进行5-氨基酮戊酸(5-aminolevulinic acid,ALA)间质性光动力治疗并测量治疗前后的PpIX荧光。结果3个病人治疗前在肿瘤组织中可检测到强荧光且激光照射后完全漂白,治疗效果好且稳定,而另外2个病人组织中检测不到PpIX荧光或荧光强度很低,治疗失败。但这种相关性并不是绝对的,也不能简单地认为光漂白越快越好或者漂白的量越多越好。如Baran等[12]对荷瘤小鼠给予酞菁类光敏剂Pc4后进行相同光剂量但不同光密度(光剂量100 J/cm2,光密度50或150 mW/cm2)的激光照射,发现不同光密度的两组之间肿瘤生长延迟无显著差别。Boere等[13]采用原位荧光计量学研究发现,在正常大鼠食管中,给予相同剂量ALA、相同激光照射条件下,PpIX荧光漂白差异显著。PpIX高漂白率导致高上皮损害,而漂白率低时食管组织对ALA-PDT无应答,在有反应组,PpIX光漂白呈先快后慢的两相衰减,而无反应的组缺乏快速漂白阶段,且第二阶段的漂白率更低,说明初始的快速漂白阶段对PDT治疗非常重要。

图9 DVDMS在正常和银屑病模型动物组织内分布比较

图10 DVDMS在IMQ模型动物皮肤中的光漂白
本研究发现,在前期的药效学研究条件下,DVDMS在浓度1~40 μg/mL范围内,在4种溶液中均发生了明显漂白,且其在180 min内的光漂白过程呈现一个先快后慢的两相过程,该特征提示DVDMS可能具有较好的作用效果。需要指出的是,Iinuma等[14]研究发现,在相同光剂量下,功率密度的高低对治疗效果无显著影响,光漂白率和功率密度之间亦无显著联系,当初始反应引起局部氧耗竭后,会抑制后续的光化学反应,而持续地反应对于杀伤肿瘤细胞是必须的。这种光漂白和光密度之间的独立性提示不依赖于氧浓度的光漂白机制的存在,推测光漂白率预测单线态氧和PDT治疗效果的作用受限。因此,在利用光漂白对1O2产量、光剂量和治疗效果的预测时,应充分考虑体内外药理毒理学的相关实验结果。
本研究发现DVDMS在NS、RPMI1640和RPMI-FBS中光漂白率与激光照射时间的对数呈现良好的线性关系;初始浓度可影响光漂白的速度,总体来说DVDMS在这3种溶液中的光漂白速度呈现随浓度增大而增大的趋势。但浓度对DVDMS初始光漂白速度的影响并不是简单的正比关系,在较高的浓度下,一方面随着光漂白增加,溶液中光敏剂单体浓度下降,会促进一部分聚集的光敏剂解聚成单体形式,造成吸光度测量的误差;另一方面,较大浓度在漂白过程中产生的单线态氧及漂白产物亦可能对测量造成影响。在细胞悬液中,DVDMS激光照射组的吸光度下降较大,但非照射对照组吸光度也有明显下降,提示HaCaT细胞对DVDMS 吸收较快。另外,同一浓度的DVDMS在相同照射条件下,在4种溶液中的光漂白量和漂白速度也存在明显差异,说明溶液体系对光漂白也有明显影响。
卟啉类光敏剂光漂白过程可用一级动力学模型表示。一级动力学模型便于计算,但只能满足部分实验数据。Braichotte等[15]在一级动力学基础上提出了二级动力学规律,即光敏剂的漂白速度取决于光敏剂的浓度、有效激发光敏剂的光剂量和底物浓度。本研究以激光照射时间、初始浓度和溶剂种类为自变量,以单位时间内的光漂白率作为因变量进行线性回归分析,得到拟合公式Y=1.073+1.348Xi+ 0.079X2-0.008X3(R= 0.520),证明DVDMS在单纯溶液体系中的光漂白受光剂量、初始浓度和底物的影响,其过程符合二级动力学模型。
研究表明,在采用PDT治疗银屑病时,光敏剂在体内,特别是皮肤组织中的分布对治疗结果有较大影响,银屑病皮损组织的荧光异质性是导致治疗效果较差的重要原因之一[16]。本研究采用小动物活体成像仪观察了DVDMS在正常动物和银屑病模型动物体内的分布,发现静脉注射给药后DVDMS在正常动物和银屑病模型动物皮肤组织中均有较高的分布,荧光均一性较好;模型动物被激光照射后,DVDMS在皮肤组织中发生了明显的光漂白,提示其可在皮肤组织发挥治疗作用。由于光敏剂自身发光的特性,采用小动物活体成像仪可以动态监测药物在同一动物组织中的分布随时间的变化,可大量减少动物的用量并消除不同动物个体差异造成的误差,对于光敏药物在体内分布的初步研究以及给药后PDT时间和条件的选择具有一定参考价值。
[1] Luksiene Z. Photodynamic therapy:mechanism of action and ways to improve the efficiency of treatment[J]. Mecicina:Kaunas,2003,39(12):1137-1150.
[2] Shackley DC,Whitehurst C,Clarke NW,et al. Photodynamic therapy[J]. J R Soc Med,1999,92(11):562-565.
[3] 黄乃艳,顾瑛,刘凡光. 卟啉类光敏剂漂白的动力学规律[J]. 中 国激光医学杂志,2005,14(1):31-34.
[4] 李步洪,谢树森,Huang Zheng,等. 光动力学疗法剂量学的研究进展[J]. 生物化学与生物物理进展,2009,36(6):676-683.
[5] Ascncio M,Collient P,Farine MO,et al. Protoporphyrin IX fluorescence photobleaching is a useful tool to predict the response of rat ovarian cancer following hexaminolevulinate photodynamic therapy[J]. Lasers Surg Med,2008,40(5):332-341.
[6] Johansson A,Faber F,Kniebühler G,et al. Protoporphyrin IX fluorescence and photobleaching during interstitial photodynamic therapy of malign antgliomas for early treatment prognosis[J]. Lasers Surg Med,2013,45(4):225-234.
[7] Hennig G,Stepp H,Johansson A. Photobleaching-based method to individualize individualize irradiation time during interstitial 5-aminolevulinic acid photodynamic therapy[J]. Photodiagnosis Photodyn Ther,2011,8(3):275-281.
[8] Jarvi MT,Patterson MS,Wilson BC,et al. Insights into photodynamic therapy dosimetry:simultaneous singlet oxygen luminescence and photosensitizer photobleaching measurements [J]. Biophys J,2012,102(3):661-671.
[9] 姜智换,史蕤,李超,等. 华卟啉钠介导的光动力疗法在体外和体内对肿瘤生长的抑制作用[J]. 癌变·畸变·突变,2013,25(3):163-167.
[10] 王颖,顾瑛,刘凡光,等. HMME在不同溶液中光漂白反应动力学规律[J]. 中国激光医学杂志,2007,16(2):73-78.
[11] Zeng H,Korbelik M,McLean DI,et al. Monitoring photoproduct formation and photobleaching by fluorescence spectroscopy has the potential to improve PDT dosimetry with a verteporfin-like photosensitizer[j]. Photochem Photobiol,2002,75(4):398-405.
[12] Baran TM,Foster TH. Fluence rate-dependent photobleaching of intratumorally administered Pc 4 does not predict tumor growth delay[J]. Photochem Photobiol,2012,88(5):1273-1279.
[13] Boere IA,Robinson DJ,de Bruijn HS,et al. Monitoring in situ dosimetry and protoporphyrin IX fluorescence photobleaching in the normal rat esophagus during 5-aminolevulinic acid photodynamic therapy[J]. Photochem Photobiol,2003,78(3):271-277.
[14] Iinuma S,Schomacker KT,Wagnieres G,et al. In vivo fluence rate and fractionation effects on tumor response and photobleaching:photodynamic therapy with two photo-sensitizers in an orthotopic rat tumor model[J]. Cancer Res,1999, 59 (24):6164-6170.
[15] Braichotte DR,Savary JF,Monnier P,et al. Optimizing light dosimetry in photodynamic therapy of early stage carcinomas of the esophagus using fluorescence spectroscopy[J]. Lasers Surg Med,1996,19(3):340-346.
[16] Kleinpenning MM,Smits T,Ewalds E,et al. Heterogeneity of fluorescence in psoriasis after application of 5-aminolaevulinic acid an immunohistochemical study[J]. Br J Dermatol,2006,155(3):539-455.
Research on photobleaching characters of sinoporphyrin sodium
LIU Hanqing1,JIANG Zhihuan2,WU Wentao3,WEI Jinfeng1,2,JIN Hongtao1,2,*,WANG Aiping1,2,*
(1. Institute of Materia Medica, Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100050; 2. Beijing Union-Genius Pharmaceutical Technology Development Co., Ltd., Beijing 100176; 3. Ocelean Pharmaceutical Technology Company, Tianjin 300384, China)
Q631;R758.63
A
1004-616X(2016)02-0081-11
1 0.3969/j.issn.1004-616x.2016.02.001
2015-07-10;
2015-12-19
国家重大新药创制资助项目(2013ZX09302302,2012ZX09J12203,2012ZX09301002-001-009)
作者信息: 刘汉清,E-mail:hanqingl@163.com。*
,靳洪涛,E-mail:jinhongtao@imm.ac.cn;王爱平,E-mail:wangaiping@imm.ac.cn

