内标法与外标法测定氨薄荷酊中薄荷脑含量的比较
吴松涛,段雪云
(1 湖北中医药大学药学院,湖北 武汉 430065;2 湖北省中医院,湖北 武汉 430061)
内标法与外标法测定氨薄荷酊中薄荷脑含量的比较
吴松涛1,段雪云2
(1 湖北中医药大学药学院,湖北武汉430065;2 湖北省中医院,湖北武汉430061)
为了对氨薄荷酊测量薄荷脑含量,用内标法和外标法对所得结果进行比较,并改进原有质量标准。用自动进样气相色谱对氨薄荷酊进行测定,通过内标法和外标法可得氨薄荷酊中待测物含量。内标法和外标法薄荷脑含量测定结果有显著性差异,在准确度和精密度上内标法优于外标法。实验人员根据实验条件,应尽量选择内标法。
氨薄荷酊;薄荷脑;气相色谱法;内标法;外标法
氨薄荷酊为湖北省中医院自制制剂,具有清热解毒,凉血止痛、止痒的功能,临床上用于蚊叮虫咬等[1]。现行氨薄荷酊质量标准中的NH3的含量测定为化学测定法,实验对氨薄荷酊的含量测定进行研究以更好的控制该制剂质量。薄荷脑的测定常用方法有外标法[2]、内标法[3]、一测多评法[4]和归一化法[5],但却并未找到相关方法比较的文献。为找到方便、准确的测定方法,实验对内标法和外标法进行比较。
1 实 验
1.1实验材料
自动进样气相色谱仪(PerkinElmerClarusGC580,氢火焰离子化检测器FID);电子分析天平(PrecisaES225SM-DR);薄荷脑对照品(110728-2005506);水杨酸甲酯对照品(110707-201413);氨薄荷酊(自制);氨水、无水乙醇为分析纯。
1.2实验方法
1.2.1色谱条件
固定相毛细管柱(交联键合聚乙二醇),30m×0.323mm×1.20μm;柱温:120 ℃;柱流量:高纯氮3.2mL/min(恒流) ;气体流量:氢气 45mL/min,空气 450mL/min,FID尾吹气30mL/min。进样口:250 ℃;检测器:250 ℃。进样方式:分流进样,分流比10:1[6-8]。
1.2.2溶液的制备
(1)内标溶液:向10mL量瓶中精密加入水杨酸甲酯[9]对照品0.1068g,加无水乙醇至刻度,作为内标储备液,向10mL容量瓶加入储备液1mL,加无水乙醇至刻度,得浓度为1.068mg/mL的内标液。
(2)供试品溶液:向25mL容量瓶精密加入氨薄荷酊1mL(批号20140710),稀释得1mg/mL供试品储备液。向10mL量瓶精密加入内标液和供试品储备液2mL,加无水乙 醇至刻度,既得供试品溶液。
(3)对照品溶液:于50mL容量瓶精密加入薄荷脑24.1mg,加无水乙醇至刻度得0.482mg/mL的对照品溶液。
1.2.3专属性试验
按照供试品溶液的制备方法取薄荷以外的其余药味,制得阴性对照溶液。如1.2.1所述设定色谱条件,发现在薄荷脑对照品相同保留时间处无干扰峰,可知薄荷含量脑测定不受其余药味的干扰,见图1。
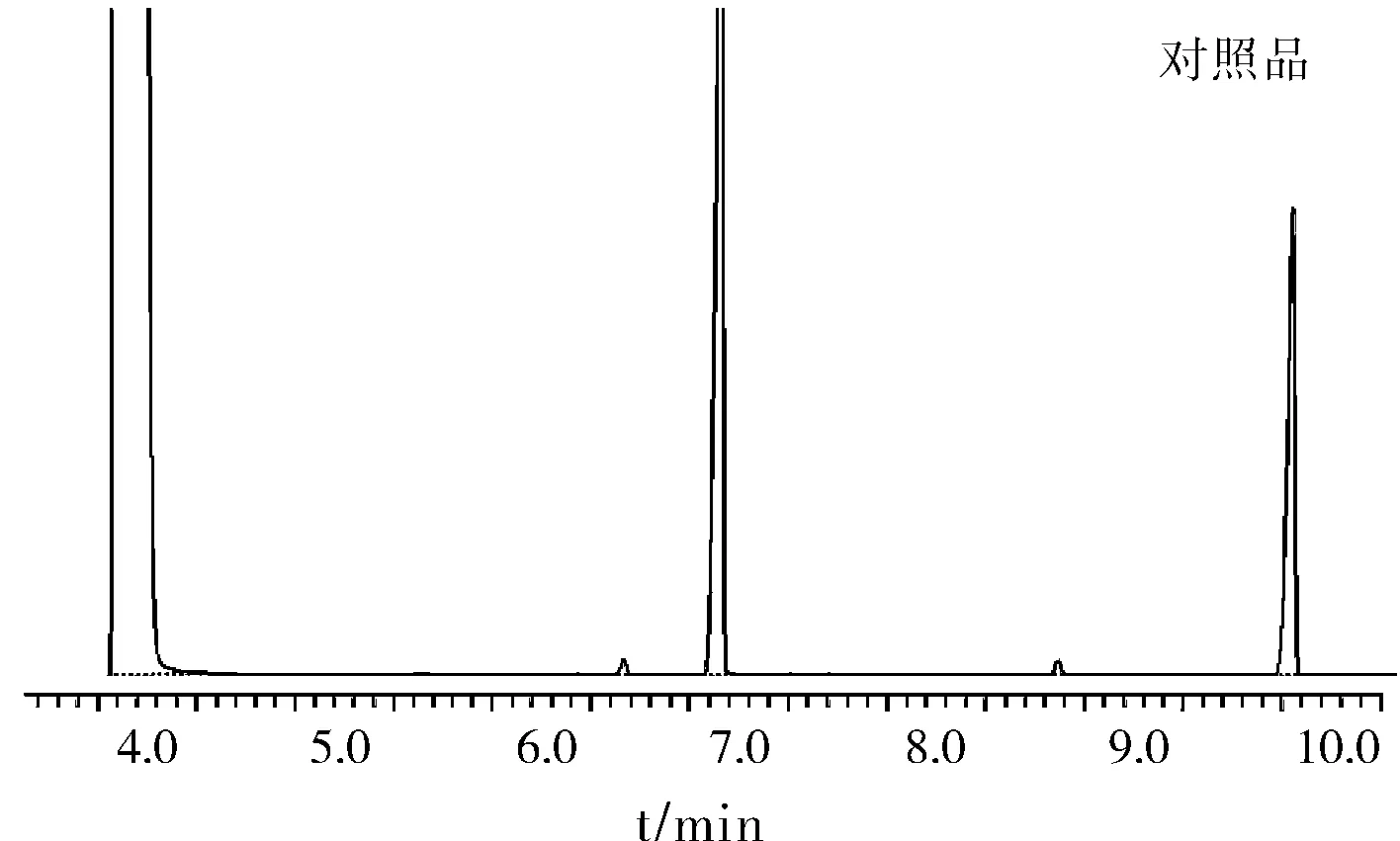

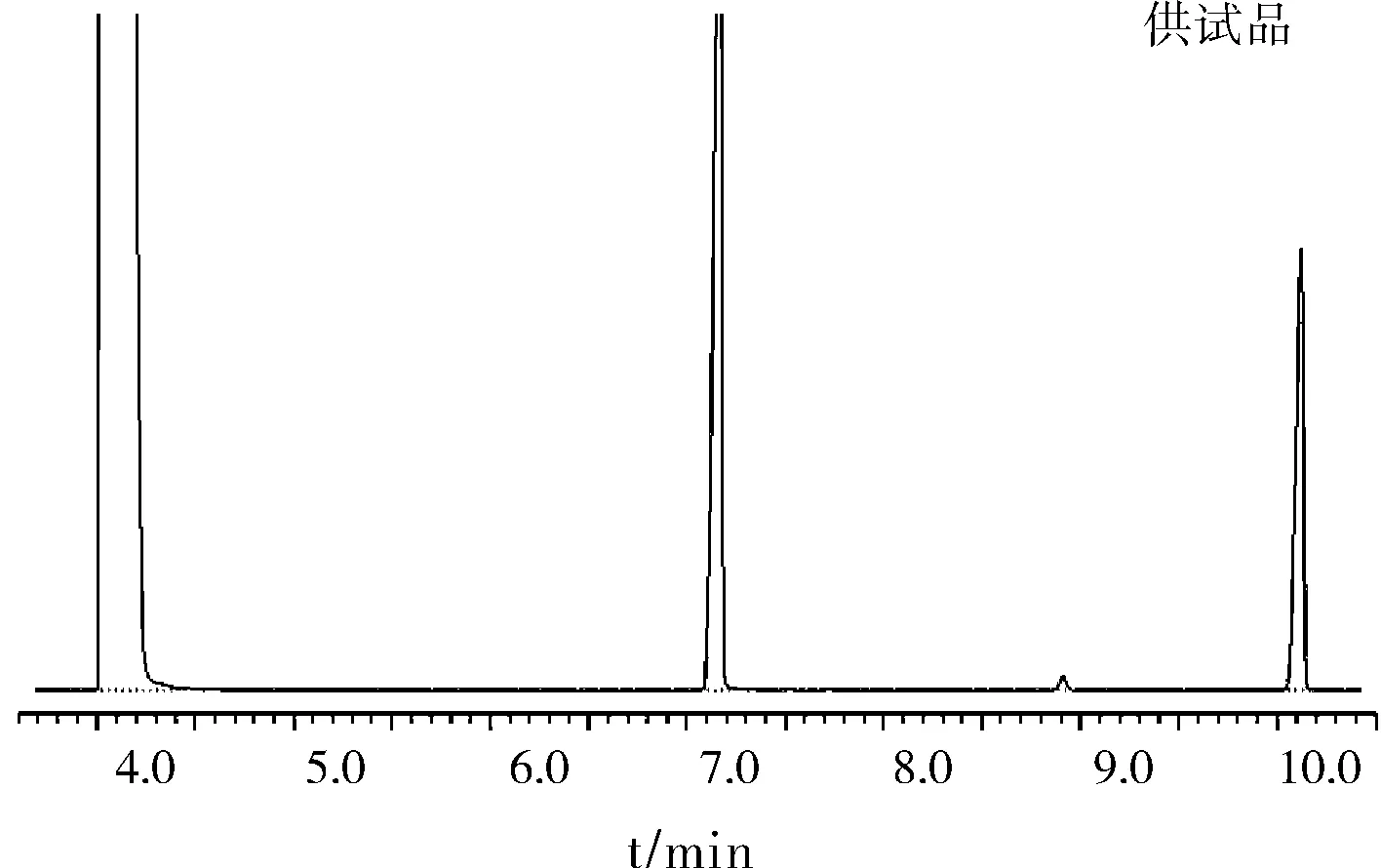
图1 HPLC色谱图
1.2.4线性关系考察
向10mL量瓶精密加入薄荷脑对照品溶液(482.0μg·mL-1)1、3、5、7、9mL,再分别加入2mL内标液,加无水乙醇至刻度,得浓度为48.2、144.6、241、337.4、433.8μg·mL-1的对照品溶液。按上述色谱条件,精密吸取配制好的不同浓度的对照品溶液1μL,进行测定。内标法:以薄荷脑与内标物的峰面积之比为因变量,以药物质量(μg)为自变量进行线性回归,求得线性回归方程。外标法:以薄荷脑峰面积为因变量,以药物质量 (μg)为自变量进行线性回归,求得线性回归方程。薄荷脑线性回归方程为:(外标法)y=0.7011x+4.7682,R2=0.9991(n=5),(内标法)y=0.8899x+0.7546,R2=0.9995(n=5),薄荷脑在0.0482~0.4338μg范围内线性关系良好。
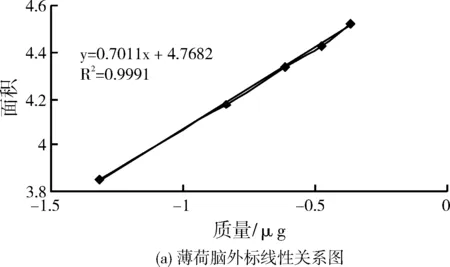

图2 线性关系图
1.2.5精密度试验
精取薄荷脑对照品溶液(433.80μg·mL-1),如1.2.1所述设定色谱条件,重复测定6次,进样量1μL。以测出的峰面积计算RSD值,可得内标法为0.63%,外标法为0.86%,可知仪器精密度良好。
1.2.6稳定性试验
配制后的0、2、4、6、8、12、24h测定氨薄荷酊供试品溶液薄荷脑与内标物峰面积,进样量1μL。以测出的峰面积计算RSD, 可得内标法为0.18%,外标法为1.14%,可知24h内供试品溶液稳定。
1.2.7重现性试验
按1.2.1所述设定色谱条件,精取本品(批号20140710)样品约1mL,共5份,按供试品溶液制备方法制备,进样量1μL,进行测定。薄荷脑含量RSD,内标法为0.20%,外标法为0.54%,表明方法重复性良好。
1.2.8加样回收试验
精取氨薄荷酊供试品溶液(含量为234.15μg·mL-1,批号20140610)4mL,共六份,加入薄荷脑对照品溶液(241.0μg·mL-1)2、4、6mL,进样量1μL,以测出的含量来计算回收率,结果见表1,得RSD值,外标法为2.3,内标法为1.1。
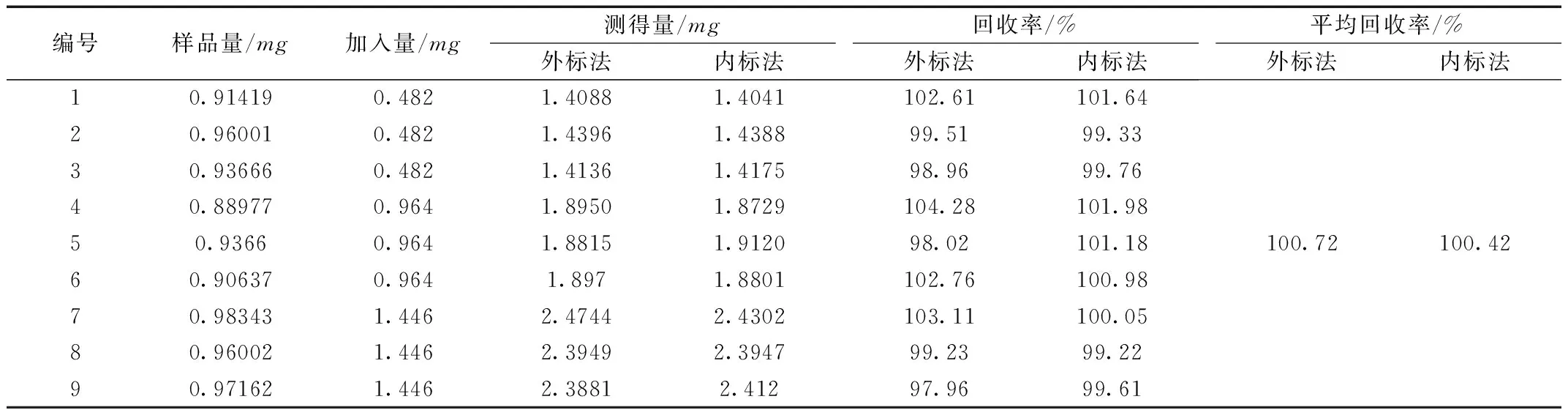
表1 薄荷脑加样回收率(n=6)Table 1 Recovery rate of menthol(n=6)
2 结果与讨论
2.1样品含量测定
依法精取6个不同批次的样品制成供试品溶液,自动进样程序设定进对照品溶液(433.8μg·mL-1和48.2μg·mL-1)1μL,供试品溶液1μL,如1.2.1所述设定色谱条件,每批样品测2份,分别用外标法和内标法计算薄荷脑含量,结果如表2所示。

表2 六批氨薄荷酊中薄荷的含量测定(n=6)Table 2 Content of mint elixirs in 6 batches of menthol(n=6)
续表2
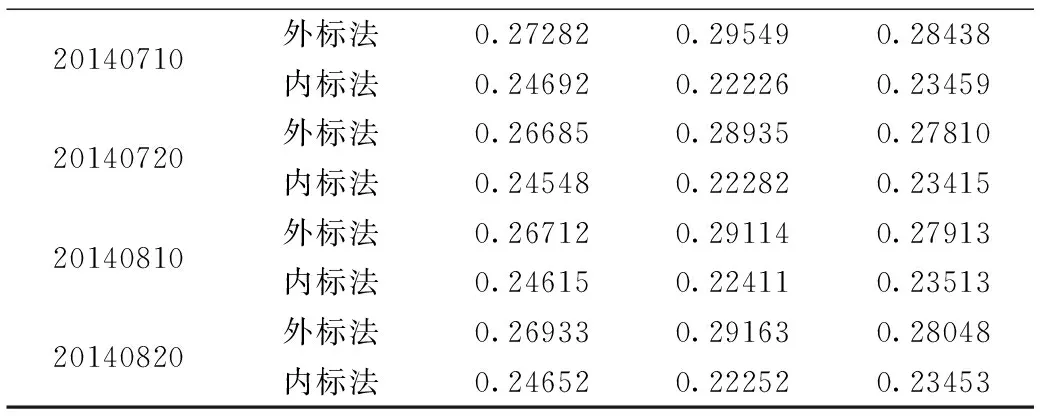
20140710外标法0.272820.295490.28438内标法0.246920.222260.2345920140720外标法0.266850.289350.27810内标法0.245480.222820.2341520140810外标法0.267120.291140.27913内标法0.246150.224110.2351320140820外标法0.269330.291630.28048内标法0.246520.222520.23453
2.2两种方法的比较及显著性差异分析
对内标法和外标法测得的薄荷脑含量数据进行统计分析(见表3),表明内标法在准确度和精密度两方面强于外标法。再对两法对氨薄荷酊中薄荷脑含量测定数据进行F,t检验,结果见表3。显然,内标法和外标法测得的各组数据在水平α=0.05下,F值大于F0.05(5,5)=5.05,t值大于t0.05,10=51.07,这说明薄荷脑含量测定中两种定量方法之间有显著性差异,分析人员在条件允许下应尽量选择内标法。

表3 内标法与外标法测定薄荷脑结果的分析Table 3 The analysis on determination of menthol with ISTD and ESTD
3 结 论
外标法可靠标准工作曲线直接算出含量,适于分析大量样品。但由于色谱条件很难保持一致,容易发生较大误差。且用标准样品来绘制标准曲线对前处理中待测组分的变化没有补偿。
以内标物及待测组分的峰面积的比值为因变量的内标法, 系统误差相对减少。待测组分在样品前处理时的损失由于前处理前加入内标物,得到部分补偿。操作程序较麻烦,有时寻找合适的内标物也有困难是内标法的缺点[10]。
本实验经对两法的比较及显著性差异分析,两法分析薄荷醑中薄荷时应首选内标法。
[1]湖北省卫生厅.湖北省医院制剂规范[M]. 武汉:武汉人民出版社,1999.
[2]曾惠芳,黄耀海,李湘力,等. 百草油中薄荷脑、肉桂醛、丁香酚的含量测定[J].中成药,2007, 29(4):558-560.
[3]李美琴,袁国平,宋辉. 气相色谱法测定止痒消炎水中薄荷脑、冰片和麝香草酚的含量[J]. 中国现代应用药学杂志,2007,24(6):505-507.
[4]黎梅桂,欧爱萍,卢嘉丽. 一测多评法同时测定狮马龙活络油中的薄荷脑与水杨酸甲酯含量[J]. 北方药学,2015,12(2):4-5.
[5]何翠薇. 正骨水化学成分气相一质谱分析[J]. 中国实验方剂学杂志,2010,16(6):93-96.
[6]黄丹萤.气象色谱外标法、内标法测定广藿香中百秋李醇含量的比较[J]. 中国药师杂志, 2010,13(9):1291-1292.
[7]孙萤,林大专,孙全乐,等.国内外标准测定依达拉奉注射液含量结果的对比研究[J]. 中国实用医药杂志,2014,9(14):254-256.
[8]汪凯莎,丁丽娜,刘建华,等.仙人掌超微粉挥发性成分研究[J]. 生物技术杂志,2009,19(5): 54-55.
[9]中国药典.一部[S].2010:528-529.
[10]汪正范.色谱定性与定量[M].北京:化学工业出版社,2000:169-172.
Comparison Analysis on Determination of Menthol in Mint ElixirswithISTDandESTD
WU Song-tao1, DUAN Xue-yun2
(1 School of Pharmacy, Hubei University of Traditional Chinese medicine, Hubei Wuhan 430065;2 Hubei provincial Hospital of traditional Chinese medicine, Hubei Wuhan 430061, China)
TocomparewhethertheresultsofInternalStandardMethod(ISTD)andExternalStandardMethod(ESTD)determiningthementholconcentrationaresignificantdifferentandimprovethequalitystandard,makinguseofthegaschromatographtodetectmentholwithISTDandESTD.TheaccuracyandprecisionofISTDwerebetterthanonesofESTD,simultaneouslytherewasasignificantdifferenceinthequantitativeresultsofmentholwithISTDandESTD.TheanalyzersshouldchooseISTDbasedontheirexperimentalconditions.
mintelixirs;menthol;gaschromatography;ISTD;ESTD
吴松涛(1991-),湖北中医药大学2014级研究生,研究方向:中药新制剂、新剂型的研究。
段雪云(1966-),主任药师,研究方向:中药新制剂、新剂型的研究。
R451
A
1001-9677(2016)013-0125-03

