小叶冷水花化学成分的研究
史莉莉,李洪攀,谭海波,邱声祥*
(1.长治学院,山西长治 046011;2.中国科学院华南植物园,广东广州 510650)
小叶冷水花化学成分的研究
史莉莉1,李洪攀1,谭海波2,邱声祥2*
(1.长治学院,山西长治046011;2.中国科学院华南植物园,广东广州510650)
采用硅胶色谱、Sephadex LH-20分子筛和RP-18反相硅胶色谱等技术,对小叶冷水花95%乙醇提取物的乙酸乙酯部位的化学成分进行分离纯化,并运用现代波谱技术(ESI,1HNMR,13CNMR)鉴定单体化合物结构.发现从其全草乙醇提取物的乙酸乙酯部位分离得到7个化合物,分别为:棕榈油酸(1),棕榈酸(2),乌苏酸(3),反式-植物醇(4),(-)-丁香烯氧化物(5),(+)-桉油烯醇(6),α-香树精(7).化合物1~7均为首次从该植物中分离得到.
小叶冷水花;化学成分;结构鉴定
小叶冷水花(Pileamicrophylla)系荨麻科(Urticaceae)冷水花属(PileaLindl.,nom.conserve.),广泛分布在亚洲、非洲热带,在我国台湾、江西、广东、广西、浙江等地较为常见[1].作为民间常用的药食同源植物,小叶冷水花以全草入药,具有清热、解毒、治疗臃肿疮疡等功效,其同属植物冷水花用于治疗黄疸、肺结核等疾病[2].现代药理活性研究表明,冷水花的乙酸乙酯提取部分具有明显的抗炎镇痛活性[3]及体外抑菌作用[4],但它的药理机理及活性成分还不明朗.
到目前为止,仅印度马尼帕尔大学(Manipal University)的Unnikrishnan课题组对小叶冷水花中的黄酮成分进行了初步研究,并从乙醇粗提物中分离到6个黄酮苷类化合物[5].国内仅对同属植物冷水花化学成分有研究[6-9],对小叶冷水花的研究尚未见报道.此外,小叶冷水花作为防腐和抗氧化的食品添加剂,在食品工业方面也具有潜在的经济价值[10-11].
为进一步开发利用该植物的化学资源,本文对小叶冷水花的化学成分进行了研究,从其全草乙醇提取物的乙酸乙酯萃取部共分离得到7个化合物,分别为棕榈油酸(1),棕榈酸(2),乌苏酸(3),反式-植物醇(4),(-)-丁香烯氧化物(5),(+)-桉油烯醇(6),α-香树精(7).所有化合物均为首次从该植物中分离得到.
1 仪器与材料
Eyela N-1100旋转蒸发仪(Tokyo Rikakai,日本);Eyela SB-1100水浴锅(Tokyo Rikakai,日本);Eyela Aspirator A-1000S循环水真空泵(Tokyo Rikakai,日本);DLSB-5/20低温冷却循环泵(郑州长城科工贸有限公司,中国);WFH-203三用紫外分析仪(上海精科仪器有限公司,中国);APCI 2000 LC-MS-MS(Applied Biosystems,美国);Bruker DRX-400 AVⅢ 500核磁共振仪(Bruker,瑞士).
柱色谱硅胶(80~100目、100~200目、200~300目,青岛海洋化工厂);柱层析反相硅胶RP-18(50 μm,70 μm Baker,美国);柱层析凝胶为Sephadex LH-20(Amersham Biosciences,瑞典);其他有机溶剂和化学药品均为国产分析纯.
植物采自中国科学院华南植物园,经中国科学院华南植物园邱声祥研究员鉴定为荨麻科冷水花属植物小叶冷水花(P.microphylla).样本保存于中国科学院华南植物园天然产物化学生物学实验室.
2 提取与分离
取小叶冷水花全草1.5 kg,充分粉碎,用95%的乙醇室温浸泡3次,每次约24 h,合并滤液减压浓缩至浸膏约200 g,然后加入1 500 mL水形成悬浊液,再用等体积的乙酸乙酯萃取3次,得乙酸乙酯部37.69 g.
将乙酸乙酯部进行硅胶(80~100目)柱层析,正己烷∶乙酸乙酯(100∶1→1∶1)梯度洗脱,各组分浓缩后采用TLC板检测,合并主点相同组分得Fr.1~Fr.6六个组分.
Fr.3(0.8 g)经Sephadex LH-20凝胶柱层析,用氯仿∶甲醇=1∶1进行洗脱得到组分Fr.3.1,再经硅胶(200~300目)柱层析,洗脱体系为正己烷∶乙酸乙酯(50∶1→10∶1),得化合物5(8.0 mg).
Fr.4(2.38 g)通过RP-18柱,用甲醇∶水(80%→100%)进行梯度洗脱,得到Fr.4.1~Fr.4.3三个亚组分.组分Fr.4.1(0.8 g)经Sephadex LH-20凝胶柱层析,用甲醇进行洗脱并合并主点相同流分;经硅胶(200~300目)柱层析,洗脱体系为正己烷∶乙酸乙酯(10∶1→2∶1);再经Sephadex LH-20凝胶柱层析,用氯仿∶甲醇=1∶3洗脱得化合物1(7.0 mg).组分Fr.4.2(0.5 g)经Sephadex LH-20凝胶柱层析,用甲醇进行洗脱并合并主点相同流分;再经硅胶(200~300目)柱层析,洗脱体系为正己烷∶乙酸乙酯(10∶1→2∶1)得到化合物6(5.0 mg).
组分Fr.5(4.24 g)通过RP-18柱,用甲醇∶水(80%→100%)进行梯度洗脱,得到三个亚组分Fr.5.1,Fr.5.2和Fr.5.3.组分Fr.5.2经Sephadex LH-20凝胶柱层析,用氯仿∶甲醇(8∶1→6∶1)梯度洗脱,再经硅胶(200~300目)柱层析,洗脱梯度为正己烷∶乙酸乙酯10∶1→1∶1,经过反复硅胶柱层析,得化合物4(23 mg).组分Fr.5.3经Sephadex LH-20凝胶柱层析,用氯仿∶甲醇(8∶1→6∶1)梯度洗脱,再经硅胶(200~300目)柱层析,洗脱梯度为正己烷∶乙酸乙酯=10∶1→2∶1,经过反复硅胶柱层析,得化合物7(16 mg).
Fr.6(4.1 g)通过RP-18柱,用甲醇∶水(90%→100%)进行梯度洗脱,得到8个亚组分Fr.6.1~Fr.6.8.组分Fr.6.7经Sephadex LH-20凝胶柱层析,用氯仿∶甲醇=1∶3进行洗脱,合并主点相同流分,得到Fr.6.7.1和Fr.6.7.2两个亚组分.Fr.6.7.1经硅胶(200~300目)柱层析,洗脱梯度为正己烷∶丙酮(10∶1→2∶1),经TLC点板检测,重结晶得到化合物2(5.0 mg).Fr.6.7.2经反复硅胶(200~300目)柱层析,洗脱梯度为正己烷∶乙酸乙酯=10∶1→2∶1,得到化合物3(15 mg).化合物1~7的结构见图1.
3 结构鉴定
化合物1.无色油状物,1HNMR(500 MHz,CDCl3)δ:5.34(2H,H-9,10),2.34(2H,t,J=7.5 Hz,H-2),2.01(4H,m,H-8,11),1.62(2H,m,H-3),1.33~1.28(16H,overlap,H-4~H-7,H-12~H-15),0.88(3H,t,J=6.6 Hz,H-16).以上数据与文献[12]基本一致,故鉴定化合物1为棕榈油酸.
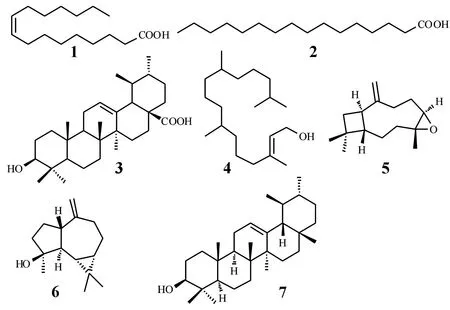
图1 化合物1~7的结构
化合物2.白色无定形粉末,1HNMR(500 MHz,CDCl3)δ:2.35(2H,t,J=7.5 Hz,H-2),1.62(2H,m,H-3),1.30~1.26(24H,overlap,H-4~H-15),0.88(3H,t,J=6.6 Hz,H-16);13CNMR(125 MHz,CDCl3)δ:179.5(C-1),34.1(C-2),32.1(C-14),29.9-29.2(C-4~C-13),22.8(C-15),14.3(C-16).以上数据与文献[13]基本一致,故鉴定化合物2为棕榈酸.
化合物3.白色无定形粉末,1HNMR(500 MHz, CDCl3)δ:5.48(1H,m,H-12),3.45(1H,m,H-3),2.63(1H,d,J=11.2 Hz,H-18),1.23,1.22,1.04,0.99,0.88(each 3H,s,5-Me),0.95(3H,d,J=6.0 Hz,30-Me),0.87(3H,J=6.0 Hz,29-Me);13CNMR(125 MHz,CDCl3)δ:181.1(C-28),140.5(C-13),126.8(C-12),79.3(C-3),57.0(C-5),54.7(C-18),49.3(C-9),43.8(C-17),41.3(C-14),40.8(C-20),40.7(C-19),40.7(C-8),40.4(C-1),40.3(C-4),38.6(C-22),38.4(C-10),34.8(C-7),32.4(C-21),30.1(C-23),30.0(C-15),29.3(C-2),26.0(C-16),25.1(C-27),24.9(C-11),22.6(C-30),20.1(C-6),18.8(C-29),18.7(C-26),17.7(C-25),17.0(C-24).以上数据与文献[14]基本一致,故鉴定化合物3为乌苏酸.
化合物7.无色针状结晶,13CNMR(125 MHz,CDCl3)δ:139.3(C-13),124.2(C-12),78.7(C-3),58.9(C-18),55.2(C-5),47.5(C-9),42.0(C-14),41.5(C-22),40.0(C-8),39.6(C-19),39.6(C-20),38.7(C-1),38.7(C-4),36.7(C-10),33.6(C-17),32.9(C-7),31.0(C-21),28.6(C-15),28.1(C-28),28.0(C-23),27.2(C-2),26.6(C-16),23.3(C-27),23.2(C-29),21.1(C-30),18.3(C-6),17.3(C-11),16.8(C-26),15.6(C-24),15.6(C-25).以上数据与文献[18]基本一致,故鉴定化合物7为α-香树精.
4 结束语
从药用植物中寻找发现具有良好活性的天然产物,是中药现代植物药研发的必经之路,也是天然药物研发的基本前提.近年来,无论是从正在研发的新药还是已获得批准的药物来看,天然产物在药物研发中一直占据着重要地位.尤其是在抗菌抗癌和免疫抑制等药物研发中,以天然产物为出发点的策略至今仍被认为是最有效的方法.本文对传统药用植物小叶冷水花的化学成分进行了研究,从其全草95%乙醇提取物的乙酸乙酯萃取部共分离得到7个化合物,分别为棕榈油酸(1)、棕榈酸(2)、乌苏酸(3)、反式-植物醇(4)、(-)-丁香烯氧化物(5)、(+)-桉油烯醇(6)、α-香树精(7).本实验所有化合物均为首次从该植物中分离得到,填补了小叶冷水花化学成分研究的空白.鉴于小叶冷水花的同属植物冷水花的乙酸乙酯部是其抑菌、抗炎、镇痛活性的主要部位,在以后的工作中将针对分离到的7种化合物进行生物活性测试,为小叶冷水花进一步的药效物质研究奠定基础.
[1]孙汉董.植物资源、植物化学与新药开发[J].国外医药植物药分册,1999,14(6):231.
[2]邱德文,杜江.中华本草:苗药卷[M].贵阳:贵州科技出版社,2005:311.
[3]孙春龙,郑庆霞,李洪庆,等.苗药冷水花提取物抗炎镇痛活性的研究[J].贵州大学学报(自然科学版),2009,26(6):67.
[4]孙春龙,杜文,李洪庆.苗药冷水花提取物的抑菌作用[J].山地农业生物学报,2009,28(5):468.
[5]BANSAL P,PAUL P,NAYAK P G,et al.Phenolic compounds isolated fromPileamicrophyllaprevent radiation-induced cellular DNA damage[J].ActaPharmaceuticaSinicaB,2011,1(4):226.
[6]梁志远,冉小燕,甘秀海.冷水花挥发油化学成分的GC-MS分析[J].贵州师范学院学报(自然科学版),2009,20(12):1.
[7]甘秀海,梁志远,杨小生,等.冷水花化学成分研究[J].中成药,2012,34(4):689.
[8]甘秀海,梁志远,赵超,等.RP-HPLC同时测定冷水花属3种植物中2种黄酮苷的含量[J].云南大学学报(自然科学版),2015,37(1):129.
[9]甘秀海,梁志远,姜金仲.冷水花抗菌活性成分研究[J].中国药学杂志,2014,49(23): 2069.
[10]MODARRESI C A,IBRAHIM D,FARIZA S S.Antioxidant,antimicrobial activity and toxicity test ofPileamicrophylla[J].IntJMicrobiol,2010,2010:1.
[11]PRABHAKAR K R,VEERAPUR V P,BANSAL P,et al.Antioxidant and radioprotective effect of the active fraction ofPileamicrophylla(L.) ethanolic extract[J].ChemBiolInteract,2007,165(1):22.
[12]郭盛,段金廒,赵金龙,等.滇枣仁化学成分研究[J].中药材,2014,37(3):432.
[13]谢威,李俊,李红梅.雪莲果化学成分的研究[J].中药材,2008,31(10):1510.
[14]路芳,巴晓雨,何永志.仙鹤草的化学成分研究[J].中草药,2012,43(5):851.
[15]SIMS J J,PETTUS J A J.Isolation of free cis and trans-phytol from the red algaGracilariaandersoniana[J].Phytochemistry,1976,15(6):1076.
[16]REINA M,NOLD M,SANTANA O,et al.C-5-substituted antifeedant silphinene sesquiterpenes fromSeneciopalmensis[J].JNatProd,2002,65(4):448.
[17]IWABUCHI H,YOSHIKURA M,KAMISAKO W.Studies on the sesquiterpenoids ofPanaxginsengC.A.MEYER.Ⅲ[J].ChemPharmBull,1990,38(5):1405.
[18]SEO S,TOMITA Y,TORI K.Carbon-13 NMR spectra of urs-12-enes and application to structural assignments of components of Isodon japonicas hara tissue cultures[J].TetrahedronLett,1975,16(1):7.
(责任编辑陆泉芳)
Chemical constituents from Pileamicrophylla
SHI Li-li1,LI Hong-pan1,TAN Hai-bo2,QIU Sheng-xiang2*
(1.Changzhi University,Changzhi 046011,Shaxi,China;2. South China Botanical Garden,Chinese Academy of Sciences,Guangzhou 510650,Guangdong,China)
The chemical constituents from ethyl acetate fraction of volume fraction 95% ethanolic extract ofPileamicrophyllaare isolated by various techniques including silica gel chromatographic,Sephadex LH-20 and RP-18 reversed-phasesilica gel chromatographic.Seven compounds are obtained and their structures are elucidated as palmitoleic acid(1),palmitic acid(2),ursolic acid(3),trans-phytol(4), 6,7-epoxy-3(15)-caryophyllene(5),(+)-spathulenol(6) and α-amyrin(7) by modern spectroscopic techniques(ESI,1HNMR,13CNMR).Compounds 1-7 are isolated from this plant for the first time.
Pileamicrophylla;chemical constituents;structure identification
10.16783/j.cnki.nwnuz.2016.04.014
2015-10-10;修改稿收到日期:2015-12-20
国家自然科学基金资助项目(81502949);广东省自然科学基金博士启动项目(2015A030310482)
史莉莉(1986—),女,山西永济人,讲师,博士.主要研究方向为天然产物全合成及天然产物化学.
E-mail:dandan986817@163.com
O 656
A
1001-988Ⅹ(2016)04-0064-04
*通讯联系人,男,研究员,博士研究生导师.主要研究方向为天然药物化学.E-mail:sxqiu@scbg.ac.cn

