首批肝素抗Ⅱa因子效价测定用国家标准品协作标定
李京,王悦,范慧红
(中国食品药品检定研究院,北京 100050)
首批肝素抗Ⅱa因子效价测定用国家标准品协作标定
李京,王悦,范慧红Δ
(中国食品药品检定研究院,北京 100050)
目的建立肝素抗Ⅱa因子效价测定用国家标准品。方法通过理化分析及效价测定,筛选出适合的标准品原料,溶解、分装、冻干后制备成肝素国家标准物质待标品(140817-201501)。以第6次肝素国际标准品07/328为标准品,分别采用《中国药典》2015年版和2010年版肝素钠效价测定方法测定待标品的抗Ⅱa因子效价、抗Ⅹa因子效价和抗凝效价,由13个实验室协作标定。为考察肝素国家标准品的延续性,上一批肝素钠国家标准品(150509-200912)在协作标定中使用。结果效价标化结果经统计学分析,实验室内及实验室间的几何变异系数(geometric coefficient of variation, gcv)均小于10%;以第6次肝素国际标准品07/328作为标准品,待标品抗Ⅱa因子效价为2011 IU/安瓿,抗Ⅹa因子效价为1998 IU/安瓿,抗凝效价为1992 IU/安瓿;对各实验室抗Ⅱa因子效价、抗Ⅹa因子效价、抗凝效价几何均值进行单因素方差分析,结果没有显著性差异;各实验室使用国际标准品测定待标品抗Ⅱa因子效价和使用上一批肝素钠国家标准品(150509-200912)测定的待标品抗凝效价几何均值进行welch检验,结果没有显著性差异,肝素国家标准品的延续性良好。结论经国家药品标准物质委员会审定后批准,待标品(140817-201501)用作肝素效价测定用国家标准品,效价为2011 IU/安瓿。
肝素;国家标准品;效价测定;协作标定;生色底物法;抗Ⅱa因子效价;抗Ⅹa因子效价; 抗凝效价
《中国药典》2015年版肝素钠、肝素钙效价测定方法由2010年版收载的血液凝固法测定抗凝效价改为生色底物法测定抗Ⅱa因子效价,因此急需建立肝素抗Ⅱa因子效价测定用国家标准品。传统的肝素效价测定方法是血液凝固法[1], 虽然能全面反映样品的抗凝活性,但专属性不强,在2009年肝素钠注射液全国评价性抽验中发现[2],有部分样品抗凝活性明显高于抗IIa因子活性,有关物质检查结果显示,上述样品的类肝素杂质超标。生色底物法[3]是肝素与纯化的凝血因子形成复合物,该复合物可以定量水解特异性生色底物,方法专属性强、操作简便,国际上已有使用生色底物法测定肝素效价替代血液凝固法的趋势。2009年第六次肝素国际标准品协作标定中[4],世界卫生组织(World Health Organization,WHO)已将抗Ⅱa因子和抗Ⅹa因子活性测定方法作为推荐使用的标定方法;美国药典(The United States Pharmacopeia,USP)于2010年USP33版中收载肝素抗Ⅱa因子效价测定方法[5]替代原来的羊血浆法[6];欧洲药典(European pharmacopoeia,EP)于2015年EP8.3版中收载肝素抗Ⅱa因子效价测定方法[7]替代原来的活化部分凝血酶时间法(activated partial thrombin time,APTT)[8];中国药典(Chinese pharmacopeia,CHP)于2015年CHP2015版中收载肝素抗Ⅱa因子效价测定方法[9]替代原来的血液凝固法[1]。
原有的肝素钠国家标准品(150509-200912,197 IU/mg)是采用血液凝固法[1]赋值的,为保证CHP2015版的顺利执行,决定换批制备新的肝素国家标准品(140817-201501),采用抗IIa因子效价测定法[9]赋值。中国食品药品检定研究院(中检院)通过理化分析及效价测定,筛选出适合的标准品原料,溶解、分装、冻干后制备成肝素国家标准物质待标品(140817-201501)。以第6次肝素国际标准品07/328为标准品,分别采用CHP2015和CHP2010年肝素钠效价测定方法测定待标品的抗Ⅱa因子效价、抗Ⅹa因子效价和抗凝效价,由13个实验室协作标定。为考察肝素国家标准品的延续性,上一批肝素钠国家标准品(150509-200912)在协作标定中使用。下面重点介绍协作标定的结果。
1 材料与方法
1.1 材料
1.1.1 国际标准品:WHO第六次肝素国际标准品,2009年建立,批号07/328,标示效价为2145 IU/安瓿,冻干品,包装为玻璃安瓿,-20 ℃避光保存,每个实验室1支。
1.1.2 国家标准品:肝素钠国家标准品,2009年建立,批号150509-200912,标示效价为197 IU/mg,白色粉末,包装为硬质玻璃管,避光冷藏保存,每个实验室1支。
1.1.3 待标品:肝素国家标准品待标品,批号140817-201501,估计效价为2 000 IU/安瓿,冻干品,包装为玻璃安瓿,-20 ℃避光保存,每个实验室4支。
1.2 方法
1.2.1 纳入实验室:在全国范围内作问卷调查,从有意愿参加协作研究的实验室中挑选了13家经验丰富的实验室,其中5家是药检所(中国食品药品检定研究院、上海市食品药品检验所、江苏省食品药品监督检验研究院、广东省食品药品检验所、天津市药品检验所),8家为制药企业(河北常山生化药业股份有限公司QC实验室、河北常山生化药业股份有限公司研发实验室、常州千红生化制药股份有限公司、南京健友生化制药股份有限公司、烟台东诚药业集团股份有限公司、东营天东制药有限公司、深圳市海普瑞药业股份有限公司、成都市海通药业有限公司)。
1.2.2 抗IIa因子效价:CHP2015二部肝素钠效价测定项下抗IIa因子效价测定法[9]。
1.2.3 抗Xa因子效价:CHP2015二部肝素钠效价测定项下抗Xa因子效价测定法[9]。
1.2.4 抗凝效价:CHP2010二部附录XII D肝素生物测定法[1]。
1.2.5 具体过程:每个实验室分别以国际标准品和国家标准品对4支待标品进行抗IIa因子、抗Хa因子、抗凝效价测定,提供4个有效数据。为考察日间差异,上述3种实验方法的4次测定应分别在4 d完成,填写结果报告表,报告实验所用试剂、仪器等基本信息,原始数据及效价计算结果。
要求每次测定均应将标准品(S)和供试品(T)稀释成4个或3个浓度,每个浓度平行作2管。以反应值(A)与浓度(C)的对数值作线性回归。基于量反应平行线法的测定原理[10],S和T的剂量与反应呈直线关系,并且S和T两条直线应平行。要首先对实验结果进行可靠性测验,回归关系应非常显著(P<0.01),偏离平行不显著(P>0.05),二次曲线、反向二次曲线不显著(P>0.05),实验可靠性测验通过者计算效价(PT)和95%概率水平的可信限率(FL%)。
对每个实验室提供的4个效价估计值进行合并计算,得到每个实验室效价测定的几何平均值,再对所有实验室的几何平均值汇总进行合并计算,得到所有实验室效价测定的几何平均值及95%均值置信区间。实验室内及实验室间的测定差异用几何变异系数(geometric coefficient of variation,gcv)表示,gcv的计算参照文献[11]中的公式。合并计算的方法与实验误差的表示参照第六次肝素国际标准品的效价计算方法[4]。
1.2.6 标准品使用说明:国际标准品和国家标准品按标准品附带说明书使用,待标品参考国际标准品说明书使用。标准品和待标品可复溶后制成母液分装保存,每次实验稀释液应新鲜制备。
1.3 统计学方法 除9号实验室使用了欧洲药典生物统计软件CombiStats(版本5.0)外,其余实验室均使用了中国药典生物检定统计程序BS2000(中国食品药品检定研究院编制)进行数据统计及效价计算。
2 结果
2.1 各实验室使用的试剂及仪器 13个实验室进行抗Xa因子和抗IIa因子效价测定,11个实验室进行了抗凝效价测定。各实验室抗Xa因子、抗IIa因子效价及抗凝效价测定使用的试剂及仪器见表1、表2。 从表1、表2的结果可以看出,各实验室使用了各自常用的试剂及仪器,来源、规格及生产厂商都不尽相同。在抗Xa因子、抗IIa因子效价测定实验中:除1个实验室使用人源的Xa因子外,其余实验室使用的Xa因子是牛源的;4个实验室使用了牛源FIIa,8个实验室使用人源IIa因子;所有实验室使用了人源ATIII;除两个实验室外,大部分实验室使用了Chromogenix公司的发色底物;在仪器方面,7个实验室使用了酶标仪,4个实验室使用分光光度计,2个实验室使用血凝仪。在抗凝效价测定实验中,有4个实验室使用血浆复钙法,2个实验室使用兔全血法,4个实验室使用APTT法,1个实验室使用USP羊血浆法;使用的底物包括兔血浆、兔全血、猪血浆、羊血浆;终点观察方法,4个实验室使用血凝仪、8个实验室使用肉眼观察。从实验结果看(见图1),不同厂商、不同来源的试剂、不同的仪器均可以使用,对效价测定没有显著影响。在以往多次的肝素与低分子肝素效价国际、国内协作标定中[4,12-13],各实验室也均使用了多种试剂及仪器,结果没有显著差异。
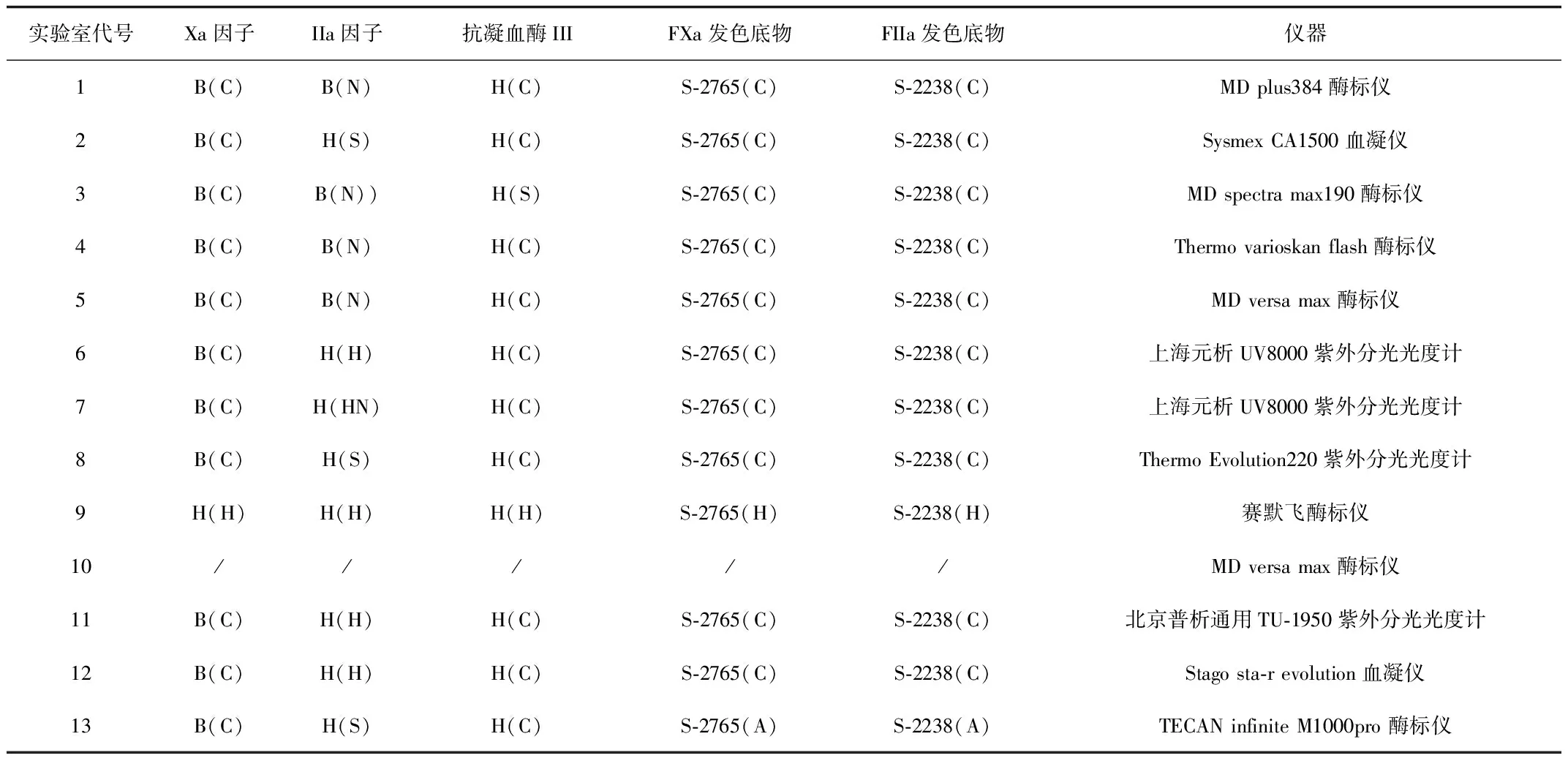
表1 抗Xa因子、抗IIa因子效价测定使用试剂及仪器Tab.1 The reagents and instruments used in anti-FXa and anti-FIIa chromogenic assays
B和H代表试剂的动物来源,B为牛源,H为人源。括号中字母代表试剂生产厂商,A: 北京艾德豪克国际技术有限公司,C:Chromogenix 公司,H:HYPHEN BioMed公司, HN:湖南一格制药有限公司,N:中国食品药品检定研究院,S:Sigma-Aldrich 公司。 “/”为企业未提供数据

表2 抗凝效价测定使用试剂及仪器
APTT法:活化部分凝血活酶时间测定法。括号中字母代表试剂生产厂商,U:unknown,N:南京新百药业有限公司,S:Siemens公司,ST:Stago公司,SD:山东苍山向阳生化助剂厂,G:广东蕊特生物科技有限公司;SH:上海铭睿生物科技有限公司
2.2 各实验室提交数据统计结果 各实验室提交的抗Xa因子效价测定结果共52个,抗IIa因子效价测定结果共52个,抗凝效价测定结果88个,均通过了可靠性测验,底物法、兔全血法APTT法FL%小于10%,血浆复钙法FL%小于5%,所有数据均为有效数据,可以参与合并计算。
2.3 抗IIa因子效价测定结果 各实验室抗IIa因子效价测定结果见表3。
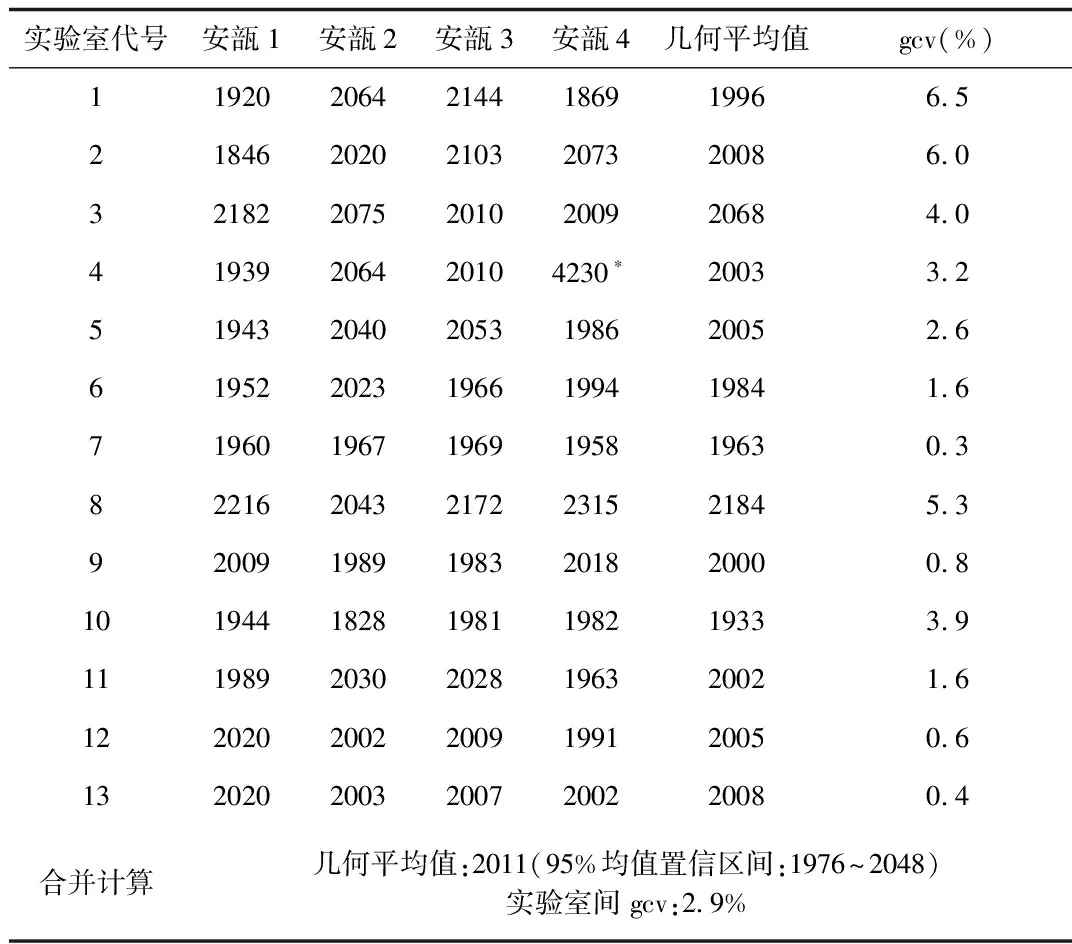
表3 以IS 07/328标定肝素标准品(140817-201501)抗IIa因子效价结果(IU/安瓿)Tab.3 The anti-FIIa potency of heparin national standard(140817-201501) determined by heparin international standard(07/328)(IU/ampoule)
带*数据为离群值,排除后计算;gcv为几何变异系数
2.4 抗Xa因子效价测定结果 各实验室抗Xa因子效价测定结果见表4。
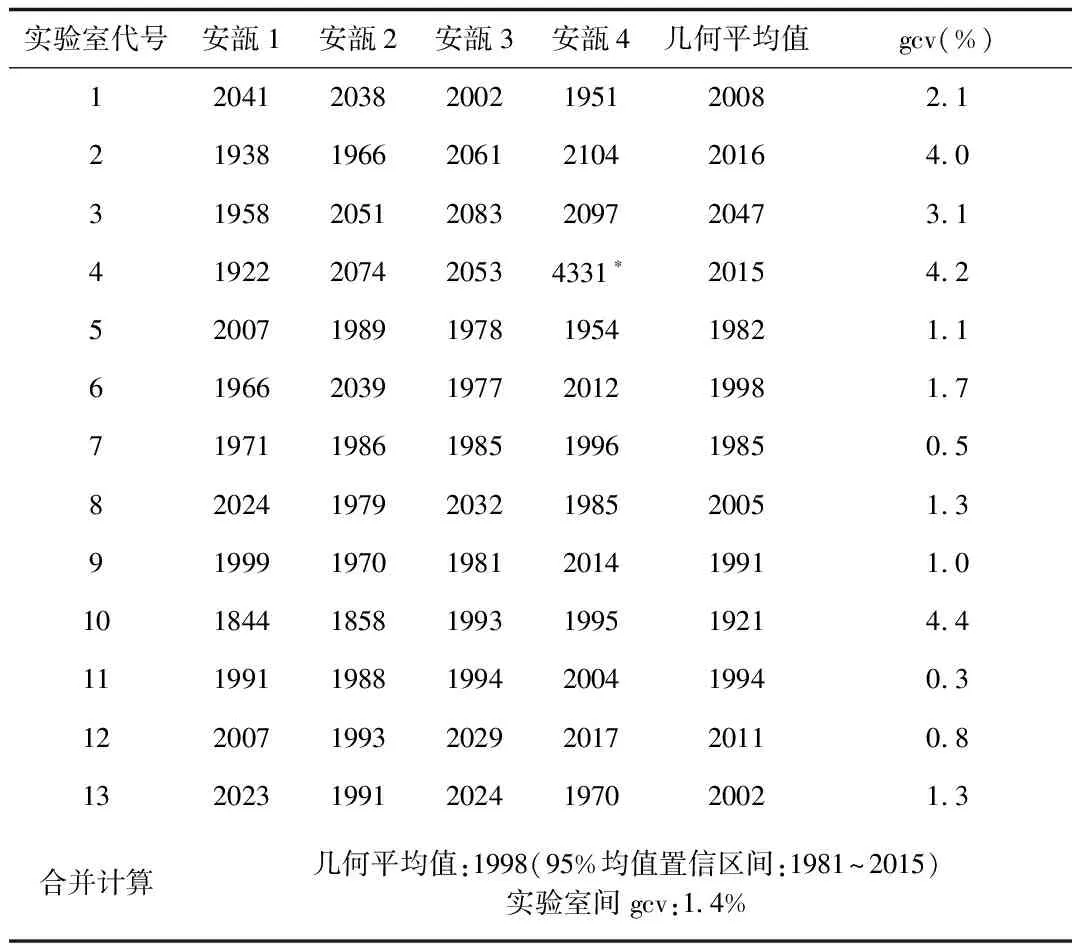
表4 以IS 07/328标定肝素标准品(140817-201501)抗Xa因子效价结果(IU/安瓿)Tab.4 The anti-FXa potency of heparin national standard(140817-201501) determined by heparin international standard(07/328) (IU/ampoule)
带*数据为离群值,排除后计算;gcv为几何变异系数
2.5 抗凝效价测定结果 各实验室抗凝效价测定结果,见表5、表6。
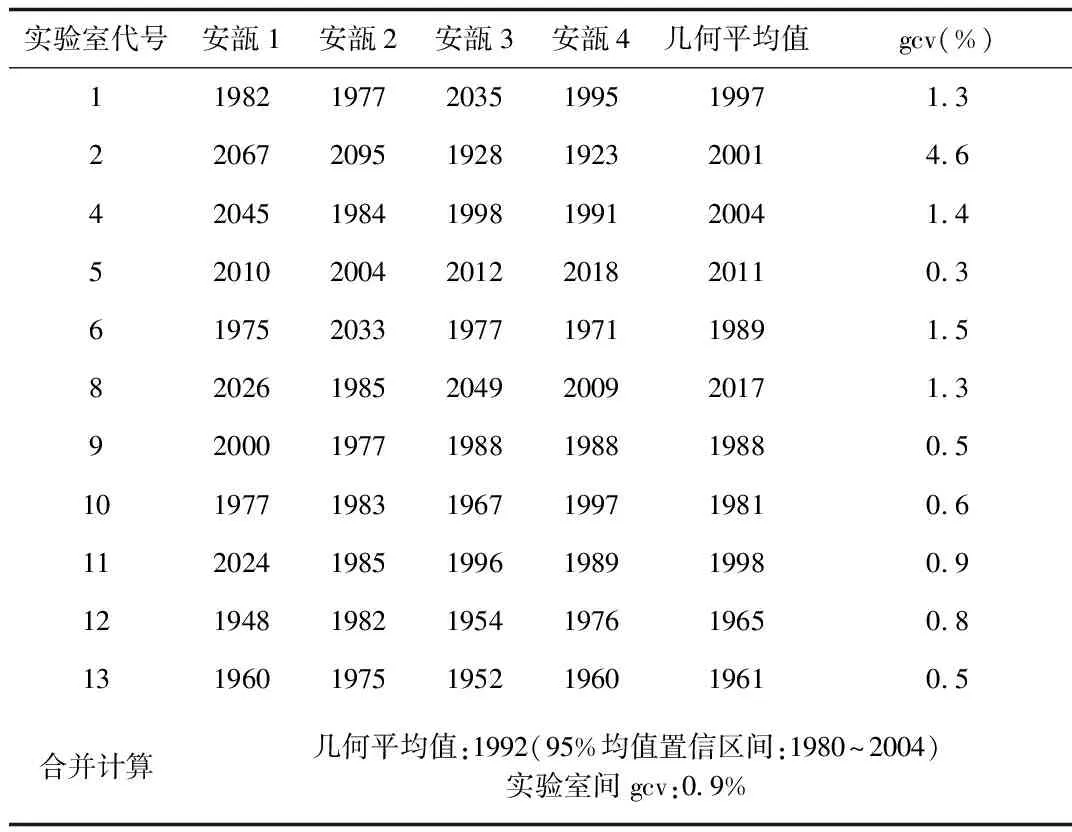
表5 以IS 07/328标定肝素标准品(140817-201501)抗凝效价结果(IU/安瓿)Tab.5 The anticoagulation potency of heparin national standard(140817-201501) determined by heparin international standard(07/328) (IU/ampoule)
gcv为几何变异系数

表6 以上一批肝素钠国家标准品((150509-200912)标定肝素标准品(140817-201501)抗凝效价结果(IU/安瓿)Tab.6 The anticoagulation potency of heparin national standard(140817-201501) determined by last heparin standard(150509-200912) (IU/ampoule)
gcv为几何变异系数
2.6 离群值处理结果 4号实验室安瓿4的抗IIa因子效价结果(见表3)和抗Xa因子效价结果(见表4)明显离群,但安瓿4的抗凝效价结果(见表5)在正常范围内,因此将4号实验室安瓿4的抗IIa因子效价和抗IIa因子效价作为离群值处理,不参与合并计算。
2.7 抗Xa因子与抗IIa因子效价比 肝素的抗Xa因子与抗IIa因子效价比应在0.9~1.1范围内,这是肝素活性的重要特征,肝素标准品(140817-201501)的抗Xa因子与抗IIa因子效价比值为1.0,符合规定。
3 讨论
3.1 方法比较 使用肝素国际标准品(07/328)对肝素标准品(140817-201501)进行抗IIa因子效价、抗Xa因子效价、抗凝效价测定,图1为3种方法测定结果的频数图,图2为箱线图。使用JMP10统计软件对各实验室几何均值进行单因子方差分析,F值为0.4554(大于0.05),结果没有显著性差异。3种测定方法中,抗IIa因子测定的误差较大,这是因为抗IIa因子的显色浓度范围较窄,反应浓度较低,加大了实验操作的难度。

图1 肝素国家标准品(140817-201501)效价测定结果频数图A-抗IIa因子效价,B-抗Xa因子效价,C-抗凝效价以肝素国际标准品(07/328)标定,图中每一个方块表示一次独立的测定结果,方块中的数字为实验室代号Fig.1 Frequency distribution of potency of national standard for heparin(140817-201501),A- anti-FIIa potency, B-anti-FXa potency, C-anticoagulation potency The potencies were determined against international standard of heparin(07/328).Each square represents an individual assay estimate. The number in the square denotes the laboratory code

图2 以肝素国际标准品(07/328)为标准品,采用不同方法测定的肝素国家标准品(140817-201501)效价厢线图Fig.2 Box plot of the potency of national standard for heparin(140817-201501)by different methods ,using heparin international standard(07/328) as standard
3.2 肝素国家标准品延续性考察 各实验室使用国际标准品测定肝素标准品(140817-201501)抗Ⅱa因子效价和使用上一批肝素钠国家标准品(150509-200912)测定肝素标准品(140817-201501)抗凝效价的几何均值进行welch检验,结果没有显著性差异,肝素国家标准品的延续性良好。图3为2种标准品测定肝素标准品(140817-201501)效价的箱线图。使用上一批肝素钠国家标准品(150509-200912)测定抗凝效价与使用国际标准品(07/328)测定抗IIa因子效价比较,实验间误差较大,原因可能是因为上一批肝素钠国家标准品为硬质玻璃管包装的固体粉末,使用时需称重,国际标准品为安瓿包装冻干品,使用时为整支溶解,称重后配制溶液的误差较大。

图3 以国际标准品测定抗IIa因子效价与以上批国家标准品测定的抗凝效价Fig.3 Box plot of the anti-FIIa potency by international standard and the anticoagulation potency by last national standard
3.3 实验注意事项 有部分实验室对标准品分装步骤不太清楚,可参考如下操作:取待分装标准品1支,放置至室温,小心开启安瓿,加水1 mL溶解,放置使充分溶解。用1 mL无菌注射器,取出安瓿中溶液,至25 mL量瓶中。在安瓿中加水1 mL,取出,重复至少8次,每次尽量将安瓿中溶液取尽。将25 mL量瓶加水至刻度,摇匀。将溶液分装至1.5 mL塑料离心管中,每支1 mL,将分装后的样品放在-20 ℃冻存,有效期为3个月。每天实验时取出1支复溶后使用,复溶后的样品不能再次冻存。分装后贮备的标准品溶液浓度不宜过低,应在80 IU/mL以上,浓度过低,标准品的稳定性无法保证。效价测定时的实验浓度通常在0.05 IU/mL以下,因此需要经过多个稀释步骤,正确的稀释步骤十分重要,应尽量保证标准品和供试品采用相同的稀释步骤。
3.4 标准品稳定性考察 肝素类标准品稳定性较好,国际标准品-20 ℃储存超过10年[4]。我们对肝素国家标准品(140817-201501)进行了初步稳定性考察,将其置于40 ℃、80%RH的恒温恒湿箱中,于第5天、第10天分别取样并存放于-20 ℃冰箱中,再同时进行效价测定,结果与-20 ℃冰箱保存样品比较,抗FXa效价与抗FIIa效价均在95%均值置信区间内,本品在40 ℃的储存条件下10 d内都是稳定的,因此本品的运输条件为常温,长期储存温度为-20 ℃。
3.5 赋值方式 中国药典2015年版与美国药典38版肝素标准效价测定方法类似,均以抗IIa因子效价表示肝素效价,同时测定抗Xa因子效价,计算抗Xa因子效价与抗II因子效价比值作为肝素鉴别试验。美国药典肝素效价测定用标准品(F0I187)的赋值方式是多个实验室使用国际标准品测定抗IIa因子效价,对抗IIa因子效价结果合并计算。因此肝素标准品(140817-201501)的赋值方式为采用13个实验室使用肝素国际标准品(07/328)测定的抗IIa因子效价合并计算。
综上,我国首批肝素抗IIa因子效价测定用国家标准品经13个实验室协作标定,结果接近,实验室间gcv小于10%,本批肝素国家标准品(140817-201501)效价定值为2011 IU/安瓿。2015年版中国药典肝素钠、肝素钙抗IIa因子与抗Xa因子效价测定实验中,均使用该值作为标准品赋值。
志谢衷心感谢参与协作标定实验室:上海市食品药品检验所、江苏省食品药品监督检验研究院、广东省食品药品检验所、天津市药品检验所、河北常山生化药业股份有限公司、常州千红生化制药股份有限公司、南京健友生化制药股份有限公司、烟台东诚药业集团股份有限公司、东营天东制药有限公司、深圳市海普瑞药业股份有限公司、成都市海通药业有限公司(上述实验室排序与文中实验室代号顺序不同)。
[1] 国家药典委员会.中华人民共和国药典:二部[S]. 2010年版,北京:中国医药科技出版社,2010:附录118-119.
[2] 李京,王悦,宋玉娟,等. 肝素质量评价与研究[J].中国药学杂志,2013,48(16):1412-1418.
[3] 李京,范慧红. 微量生色底物法测定肝素抗Ⅹa因子和抗Ⅱa因子活性[J].中国生化药物杂志,2010,31(1):45-47.
[4] 李京,邓利娟,李湛军,等.第六次肝素国际标准品协作标定[J].中国药学杂志,2010,45(24):1954-1958.
[5] USP33/NF28[S].2010.
[6] USP32/NF27[S].2009:2552-2554.
[7] EP 8.3[S].2015:4341-4343.
[8] EP 8.0[S].2014:2390-2391.
[9] 国家药典委员会.中华人民共和国药典:二部[S]. 2015年版,北京: 中国医药科技出版社,2015:517-519.
[10] 国家药典委员会.中华人民共和国药典:四部[S]. 2015年版,北京: 中国医药科技出版社,2015: 182-200.
[11] Kirkwood TBL.Geometric means and measure of dispersion[J].Biometrics,1975,35(10):908-909.
[12] 李京,王悦,范慧红.第3次低分子肝素国际标准品协作标定[J].药物分析杂志,2014,34(1):71-74.
[13] 李京,郝苏丽,范慧红,等.第一次低分子量肝素效价测定用国家标准品协作标定[J].2008,22(12):1077-1080.
(编校:吴茜)
Acollaborativestudytoestablishthenationalstandardforheparinwithanassignedvalueobtainedfromanti-FIIachromogenicmethod
LI Jing, WANG Yue, FAN Hui-HongΔ
(National Institutes for Food and Drug Control, Beijing 100050)
ObjectiveTo establish a national standard for heparin with an assigned value obtained from anti-FIIa chromogenic method.MethodsThrough physical, chemical and biological tests, one batch of heparin sodium was selected to prepare the national standard for heparin assay. The bulk material was dissolved with distilled water, distributed into ampoules and freeze-dried. The candidate sample(140817-201501) was assayed against the 6thinternational standard(07/328). Thirteen laboratories took part in the study. Three methods were used in the study, including anti-FIIa chromogenic assay, anti-FXa chromogenic assay and clot-based plasma assay. For the purpose of the continuity check between subsequent batch of national standard, the current heparin national standard for assay(150509-200912) was also included in the study.ResultsBased on the statistical analysis, the candidate gave low intra- and inter-laboratories variations, geometric coefficient variations were all less than 10%. Against the 6thinternational standard(07/328), Anti-FIIa potency of the candidate sample(140817-201501) was 2011 IU per ampoule, anti-FXa potency was 1998 IU per ampoule, anticoagulation potency was 1992 IU per ampoule. The results between three methods were not significant difference by statistics analysis. The results between international standard(07/328) and national standard(150509-200912) were not significant difference by statistics analysis. The continuity of the national standard of heparin is good.ConclusionAfter the examination of the expert committee on pharmaceutical standardization, the candidate(140817-201501) was approved as the national standard of heparin for assay with an assigned value 2011 IU per ampoule.
heparin; national standard; assay; collaborative study; chromogenic method; anti-FIIa potency; anti-FXa potency; anticoagulation potency
10.3969/j.issn.1005-1678.2016.10.003
李京,女,主任药师,研究方向:多糖类药物质量控制,E-mail:lijing317@nifdc.org.cn;范慧红,通信作者,女,博士,研究员, 研究方向:生化药物的质量控制,E-mail:shihuayaoshi@126.com。
R927
A

