紫青稞色素的热降解动力学研究
张娟,张留洋,王莉君,秦昌月,罗建,赵桃(上海工程技术大学化学化工学院,上海201620)
紫青稞色素的热降解动力学研究
张娟,张留洋,王莉君,秦昌月,罗建,赵桃*
(上海工程技术大学化学化工学院,上海201620)
为研究紫青稞色素的稳定性,在不同温度(70、80、90℃)和pH值(1、3、5、7)条件下检测其降解过程。结果发现该色素的降解速率与加热时间呈线性关系,符合一级动力学特征。该色素的稳定性同时受温度和pH影响,在较低温度和较低pH条件下稳定性较强。在70℃~90℃范围内,pH值为1,3,5和7时,紫青稞色素的半衰期t1/2分别为23.8 h~9.1 h、16.5 h~6.9 h、13.5 h~6.8 h、16.8 h~7.5 h,活化能Ea分别为49.68、45.37、35.55、41.84 kJ/mol。此外,紫青稞色素提取液的降解生成褐色物质,褐变指数随加热时间的延长、加热温度的升高、pH值的增大而增大。
花色苷;稳定性;动力学;青稞
花色苷类色素是植物中广泛存在的水溶性色素,不仅赋予植物鲜艳的颜色以利于授粉和种子传播、抵抗植物虫害以及预防植物的紫外线照射损伤,而且对于人类具有许多生理保健功能,如清除体内自由基、抗肿瘤、抗癌、预防糖尿病、保护视力等[1-4]。此外,花色苷还可用作抗氧化剂阻止或延缓油脂的自动氧化,防止食品在贮藏中因氧化而使营养损坏褐变褪色等[5]。
青稞(Hordeum vulgare ssp.Vulgare)即裸大麦,在我国主要分布西藏、青海、四川的甘孜州和阿坝州、云南的迪庆、甘肃的甘南等青藏高原地区。由于青稞含有大量可溶性纤维、β-葡聚糖、维生素、矿物质等营养成分,近年来受到广泛关注,种植面积日益增加[6]。青稞种皮色素属花色苷类色素,具有较好的抗氧化、去除自由基活性[7-8],但其稳定性还未得到深入研究。本试验主要研究紫青稞色素提取物在不同pH值和温度条件下的热稳定性及其降解动力学特征,为青稞色素的开发利用提供参考。
1 材料与方法
1.1材料与仪器
1.1.1材料
试验所用青稞材料:西藏农科所提供;试验所用试剂均为国产分析纯:购自国药集团化学试剂有限公司。1.1.2仪器
HH-数显恒温水浴锅:上海逸龙科技有限公司;pHB-4便携式pH计:上海精密科技仪器有限公司;SHZ-D型循环水式真空泵:巩义市英峪予华仪器厂;AB104-N型分析天平:梅特勒-托利上海有限公司;UV-7504型单光束紫外可见分光光度计:上海欣茂仪器有限公司;UV-1601PC型全波长扫描仪:岛津公司。
1.2色素提取
将去杂后的青稞种子置于含0.2%盐酸的甲醇溶液中[料液比1∶10(g/mL)],4℃避光浸提24 h。提取液过滤后,40℃减压旋转蒸发浓缩,并用3倍体积乙酸乙酯萃取3次脱脂,萃取液(水相)过滤后,40℃减压旋转蒸发干燥后,得到色素粗提物。
1.3色素纯化
利用Sp850型大孔树脂纯化色素粗提物。树脂用4倍体积无水乙醇浸泡24 h,充分溶胀,去除未聚合的单体、致孔剂、引发剂等杂质后过滤收集树脂。将2 g(干重)树脂湿法装柱,以2 BV/h上样,上样液质量浓度为22.0 mg/L,pH值为2.0。树脂吸附饱和后,结束上样,用蒸馏水冲洗,除去粗提物中糖和蛋白质等水溶性的杂质,待水洗流出液为无色后,用60%的乙醇溶液解吸色素,解吸流速为2 BV/h。解吸液于40℃减压旋转蒸发干燥后,得到纯化色素。
1.4光谱分析
将纯化的青稞花色素分别溶于pH为1、3、5、7的缓冲溶液,缓冲液配制方法见表1,以相应溶剂为参比,在波长400 nm~800 nm范围扫描其可见光谱特征。所有样品在测定前均避光平衡1 h。

表1 缓冲溶液的配置方法(体积比)Table 1 Solventproportion(v/v)of the buffer solutions
1.5色素质量浓度测定
色素质量浓度的测定采用pH示差法[9],由等量矢车菊素-3-葡萄糖苷(Cyd-3-G)表示,计算公式如下:
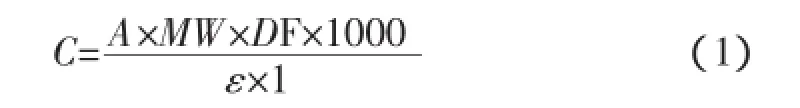
式中:C为花色苷质量浓度,mg/L;A为pH 1.0时花色苷在520 nm与700 nm的吸光值之差减去pH 4.5时花色苷在520 nm与700 nm的吸光值之差;MW为Cyd-3-G的分子量449.2 g/mol;DF为稀释倍数;1 000为将单位由g转化为mg的倍数;ε为摩尔消光系数26 900 L/(mol·cm);1为比色皿宽度,cm。
1.6热稳定性测定
取pH为1、3、5、7(表1)的青稞花色素15 mL溶液置于旋盖试管中,于70、80、90℃条件下水浴加热。每隔1 h测定其花色苷质量浓度变化。
1.7热降解模型
根据文献报道,花色苷类色素的热降解符合一级动力学特征,可用阿伦尼乌斯模型进行拟合,其基本公式如下:

式中:Y0为花色苷起始质量浓度,mg/L;Yt为加热t小时后的花色苷质量浓度,mg/L;T为绝对温度,K;k∞为指前因子,(/s);Ea为活化能,J/mol;R为气体常数[8.31 J/(mol·K)]。
1.8褐变指数测定
测定了加热9 h后,紫青稞色素样品的褐变指数(BI)的变化,计算公式如下:

式中:A420、A700、Amax分别代表样品在420、700 nm和最大可见吸收波长处的吸光值。
2 结果与分析
2.1紫青稞色素的可见吸收光谱
对紫青稞色素的可见吸收光谱分析结果如图1所示。

图1 不同pH条件下青稞色素的可见吸收光谱Fig.1 Visible spectra ofhulless barley extractatdifferentpH values
不同pH条件下,紫青稞色素在515 nm~580nm范围内出现特征吸收,符合花色苷类物质的2-苯基苯并吡喃母环的特征吸收波长范围。一般来说,在不同pH值的水溶液中,花色苷存在4种分子结构的平衡,包括红色花鎓阳离子,无色的甲醇假碱,蓝紫色醌式脱水碱和灰黄色查尔酮。因此,青稞色素在水溶液中,随着pH值变大,红色的花鎓阳离子结构逐步水解成为花鎓阳离子和甲醇假碱混合物(pH 1~5),醌式脱水碱和查尔酮混合物(pH 6~9),引起溶液颜色及光谱特征发生改变。根据实验确定的最大吸收波长,在相应波长位置测定并计算色素在不同pH条件下的褐变指数。
2.2紫青稞色素的热降解动力学研究
试验研究pH值为1、3、5、7,温度为70、80、90℃条件下紫青稞色素降解的动力学过程。结果表明,样品中青稞色素的质量浓度随加热时间的延长不断减小,样品液初始质量浓度C0和加热t min后的质量浓度Ct的比值与时间呈良好的线性关系,见图2,符合一级反应动力学规律,可通过下列公式进行拟合:
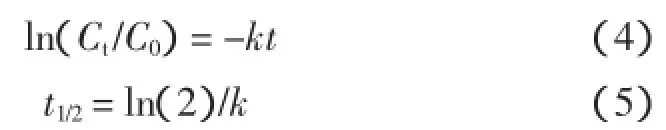
式中:C0为样品中花色苷的初始质量浓度,mg/L;Ct为加热t min后样品中花色苷质量浓度,mg/L;k(h-1)为一级反应速率常数(降解速率常数);t1/2(h)为半衰期,即花色苷降解50%所需时间,h。
青稞花色苷降解参数如表2所示。


图2 青稞色素在不同pH值条件下的热降解Fig.2 Degradation ofanthocyanins in hulless barley extracts during heating at various

表2 青稞花色苷的热降解参数Table 2 Thermaldegradation parameters of hulless barley anthocyanin extracts
由青稞色素的半衰期t1/2可知,在70℃~90℃条件下低pH值溶液中的青稞色素稳定性更强。如前所述,花色苷类色素由于其自身结构特点在不同pH值条件下存在4种分子结构的平衡,其中,花鎓阳离子的吡喃结构开环成为甲醇型假碱结构是花色苷降解的重要途径之一[10]。根据我们的结果,青稞色素在pH 1条件下热稳定性最好,在pH 5条件下热稳定性最差,与在大麦[11]、小麦[12]、土豆[13]、黑米[14]、萝卜[15]、玉米[16]等中的研究结果一致。
此外,动力学参数还表明青稞色素的降解随加热温度和加热时间的增加而增强。例如,在pH 1条件下,降解速率k由0.029 1 h-1(70℃)增加为0.075 9 h-1(90℃)。对紫土豆、红土豆、葡萄和紫萝卜的色素降解动力学研究发现,其半衰期t1/2(pH 3,80℃)分别为15、34、15和33 h[13]。而玫瑰茄花色苷在70、80、90℃条件下的半衰期t1/2分别为11.55、7.22和3.21 h[17]。不同物种花色苷降解速率的差异可能是由于其色素结构中的糖苷配基、糖残基组成和酰化程度不同所致,也可能与色素提取物中酚类化合物的含量和结构相关[10]。
青稞色素的降解对温度的依赖性由反应活化能(Ea)反映。根据阿伦尼乌斯(Arrhenius)模型(公式2),青稞花色苷的降解速率k(h-1)与活化能Ea间的关系可表示为:

式中:K0为频率因子,(h-1);Ea为活化能,kJ/mol;R为气体常数[8.31 J/(mol·K)];T为绝对温度,K。
由表2可知,青稞色素在pH 1、3、5、7的活化能分别为49.68、45.37、35.55、41.84 kJ/mol,即其对温度的敏感性随pH值变化而变化,在pH 5.0时对温度的敏感性较弱,可能主要受其甲醇假碱结构的影响。
2.3紫青稞色素的褐变指数
花色苷热降解过程中生成褐色化合物。可能的机制包括最初形成查耳酮,之后损失糖基部分和形成α-二元酮等,端产物有香豆苷衍生物、安息香酸衍生物和三羟基苯甲醛等。褐变指数是评价花色苷降解的又一有效量度,其值不仅反映了花色苷在降解过程中因形成无色醇型假碱而引起的在其最大可见吸光度的减小,也反映出由于生成褐色物质引起420 nm处吸光度的增加。根据公式(3)计算可知,紫青稞色素提取液在加热9 h后出现不同程度的褐变,其褐变指数随pH值的增加、加热温度的升高而增大(图3)。

图3 紫青稞色素提取液的褐变指数Fig.3 Brown indices of the extracts of purple hulless barley
3 结论
本研究表明,在70℃~90℃范围内,青稞色素的热降解过程符合一级动力学特征,降解率与加热时间呈线性关系,可用阿伦尼乌斯公式进行拟合和预测。青稞色素的热稳定性和褐变程度受溶液pH值、温度的影响,在较低的pH值和温度条件下稳定性更好,褐变程度较低。为提高青稞色素的稳定性,在对含青稞色素食品的加工或贮存过程中,应充分考虑温度及pH条件的影响。此外,需要对青稞色素提取物的具体化学组成及青稞花色苷的降解机理进行深入研究,进一步探索将青稞色素作为保健食品或食品添加剂的可行性。
[1]PHILPOTT M,GOULD K S,LIM C,etal.In situ and in vitro antioxidant activity of sweetpotato anthocyanins[J].Journal of agricultural and food chemistry,2004,52(6):1511-1513
[2]DAI J,PATEL J D,MUMPER R J.Characterization of blackberry extract and its antiproli ferative and anti-inflammatory properties[J]. Journalofmedicinalfood,2007,10(2):258-265
[3]WANG L S,STONER G D.Anthocyanins and their role in cancer prevention[J].Cancer letters,2008,269(2):281-290
[4]TOUFEKTSIAN M C,DE LORGERIL M,NAGY N,et al.Chronic dietary intake of plant-derived anthocyanins protects the ratheart againstischemia-reperfusion injury[J].The Journal of nutrition,2008, 138(4):747-752
[5]杨洋,韦小英,阮征.国内外天然食品抗氧化剂的研究进展[J].食品科学,2002,23(10):137-140
[6] 臧靖巍,阚建全,陈宗道,等.青稞的成分研究及其应用现状[J].中国食品添加剂,2004(4):43-46
[7]ZHAO T,YANG H,LI Y F,et al.In Vitro Studies on the Radical Scavenging Activity of Hulless Barley Pigment[J].Advanced Materials Research,2011,183:145-150
[8]赵桃,唐亚伟,单月琴,等.青稞紫色素的基本性质及其抗氧化能力[J].食品与发酵工业,2010,36(8):68-73
[9]LEE J,DURST R W,WROLSTAD R E.Determination of total monomeric anthocyanin pigment content of fruit juices,beverages, naturalcolorants,and wines by the pH differential method:Collabora tive study[J].Journal of AOAC international,2005,88(5):1269-1278
[10]CASTANEDA-OVANDO A,PACHECO-HERNANDEZ M L, PAEZ-HERNANDEZ M E,etal.Chemical studies of anthocyanins: A review[J].Food Chemistry,2009(4):859-871
[11]DEGUCHIT,SHOHARA S,OHBA R,etal.Effects of pH and light on the storage stability of the purple pigment,hordeumin,from uncooked barley bran fermented broth[J].Bioscience,biotechnology, and biochemistry,2000,64(10):2236-2239
[12]ABDEL-AAL E-S M,HUCL P.Composition and stability of anthocyanins in blue-grained wheat[J].Journal of Agricultural and Food Chemistry,2003,51(8):2174-2180
[13]REYES L F,CISNEROS-ZEVALLOS L.Degradation kinetics and colour of anthocyanins in aqueous extracts ofpurple-and red-flesh potatoes(Solanum tuberosum L.)[J].Food Chemistry,2007(3):885-894
[14]HOU Z,QIN P,ZHANG Y,etal.Identification of anthocyanins isolated from black rice(Oryza sativa L.)and their degradation kinetics [J].Food research international,2013,50(2):691-697
[15]SADILOVA E,CARLE R,STINTZING F C.Thermal degradation of anthocyanins and its impact on colorand in vitro antioxidant capacity[J].Molecular nutrition&food research,2007,51(12):1461-1471
[16]YANG Z,HAN Y,GU Z,et al.Thermal degradation kinetics of aqueous anthocyanins and visualcolor of purple corn(Zea mays L.) cob[J].Innovative Food Science&Emerging Technologies,2008,9 (3):341-347
[17]AURELIO D L,EDGARDO R G,NAVARRO-GALINDO S.Thermal kinetic degradation of anthocyanins in a roselle(Hibiscus sabdariffa L.cv.'Criollo')infusion[J].International Journalof Food Science&Technology,2008,43(2):322-325
Thermal Degradation Kinetics of Pigments from Purple Hulless Barley
ZHANG Juan,ZHANG Liu-yang,WANG Li-jun,QIN Chang-yue,LUO Jian,ZHAO Tao*
(College of Chemistry and Chemical Engineering,Shanghai University of Engineering Science,Shanghai 201620,China)
In the present study,thermalsta bility of anthocyanins from purple hulless barley was investigated at three temperatures(70,80,90℃)and four pH values(1,3,5,and 7).Results indicated that the degradation kinetics of hulless barley anthocyanins followed first-order reaction kinetics.The thermal degradation of hulless barley anthocyanins was temperature and pH dependent,and the anthocyanins were more stable during heating at lower temperature and pH.The calculated values ofhalf-lives t1/2were 23.8 h-9.1 h,16.5 h-6.9 h,13.5 h-6.8 h,16.8 h-7.5 h and the activation energies(Ea)were 49.68,45.37,35.55,41.84 kJ/molfor anthocyanins atpH 1,3,5 and 7,respectively.Besides,brown compounds appeared in the pigment extracts during heating,and the brown indices ofthe extracts increased with increasing oftime,temperature and pH.
anthocyanins;stability;kinetics;hulless barley
10.3969/j.issn.1005-6521.2016.12.006
上海工程技术大学高水平项目培育基金(2012gp10);上海市大学生创新活动计划项目(cs1404009);上海工程技术大学大学生创新活动计划项目(cx1404004)
张娟(1994—),女(汉),本科在读,制药工程专业。
赵桃(1982—),女(汉),副教授,博士,研究方向:天然产物。
2015-06-08

