甲酸根含量测定方法研究与讨论
王仲广,任奕,赵璐,逯学朝,王铁钢
(中海油能源发展有限公司工程技术分公司,天津300000)
甲酸根含量测定方法研究与讨论
王仲广,任奕,赵璐,逯学朝,王铁钢
(中海油能源发展有限公司工程技术分公司,天津300000)
甲酸钾、甲酸钠是甲酸盐钻完井液体系的主要材料,其优良的性能得到了大家的认可,但甲酸根在不同环境下检测的原理不同,检测方法及误差较大。该文细化了氧化还原法的反应原理,通过理论及实际验证确定了甲酸根的滴定条件:氢氧化钠0.5mol/L×7mL、高锰酸钾0.1mol/L× 25mL、浓硫酸2mol/L×5mL、碘化钾1.6g、反应温度75±5℃、反应时间为30min。
甲酸根;含量测定;钻完井液
甲酸盐钻完井液体系是一种环保型钻完井液,不仅满足海上施工过程中环保要求,而且具有抗温性强、流变性好、抑制性高、抗污染好、腐蚀速率低等良好的性能,尤其是与油层有良好的配伍性,倍受大家青睐。
1 甲酸盐的来源及生产工艺
1.1一氧化碳与氢氧化钾(氢氧化钠)反应,生成甲酸盐
CO+KOH(NaOH)→K(Na)COOH
主要生产方法有以下几种:一氧化碳气体与KOH或者NaOH溶液直接反应;转炉煤气与KOH或者NaOH溶液反应生成甲酸盐;以电石炉炉气或者尾气为原料制备甲酸盐等。主要生产工艺:净化后CO(纯度≥90%)与(3~5)molKOH(NaOH)溶液在170℃~220℃温度下合成甲酸钾溶液经过蒸发、浓缩、干燥制得相应的产品,此类产品中可能含:氢氧化钠、碳酸钠、碳酸氢钠等[1,2]。
1.2利用氯仿下脚料生产甲酸钠
氯仿的下脚料是白石膏,其主要成分是甲酸钙、石灰、氯化钙,通过对白石膏浸提、浓缩、热结晶等工艺过程将甲酸钙分离出来,然后再用碳酸钠与它反应,制得甲酸钠产品[3]。
1.3从多元醇母液副产物中回收甲酸钠
季戊四醇母液、新戊二醇母液、三羟甲基丙烷母液中回收得到甲酸钠。因得到的甲酸钠主要用来生产甲酸,且其中副产物多,故不作为重点研究其检测方法[4]。
2 甲酸盐的检测方法
2.1灼烧法
若甲酸盐中存在氢氧化钠、碳酸钠,则分别取两份相同重量样品A、B。A直接加蒸馏水溶解后用已知浓度的盐酸滴定,总碱量为氢氧化钠与碳酸钠的碱量之和;B经500℃焙烧3h后用盐酸滴定,通过计算得到甲酸钠、氢氧化钠、碳酸钠三者的含量。
2.2氧化法
在强碱性溶液中用过量的高锰酸钾定量地将甲酸根氧化,待反应完成后将溶液酸化;在酸性溶液中用还原剂硫代硫酸钠的标准溶液滴定溶液中所有的高价态的锰,使之还原为Mn2+计算出消耗还原剂的量,通过作空白实验从而测出甲酸根含量[5];高锰酸钾在强酸性条件下直接氧化甲酸盐,未反应的高锰酸钾采用碘量法进行滴定,从而间接计算出甲酸盐含量[6]。
灼烧滴定法,因高温灼烧过程中容易造成甲酸钠高温分解、沸腾等造成损耗,从而影响甲酸根浓度,因此该文只针对氧化还原法进行研究。
3 甲酸根测试方法的确立
3.1反应原理
高锰酸钾在酸性、中性、碱性条件下都有氧化性,区别在于H+浓度的差别使得它的氧化性强弱有所不同:在酸性条件下氧化性最强,还原产物是二价锰离子(Mn2+);在中性环境下次之,还原产物是二氧化锰(MnO2);在碱性环境下最弱,产物是锰酸钾(K2MnO4)
根据高锰酸钾与甲酸盐的反应可得出反应原理如下:
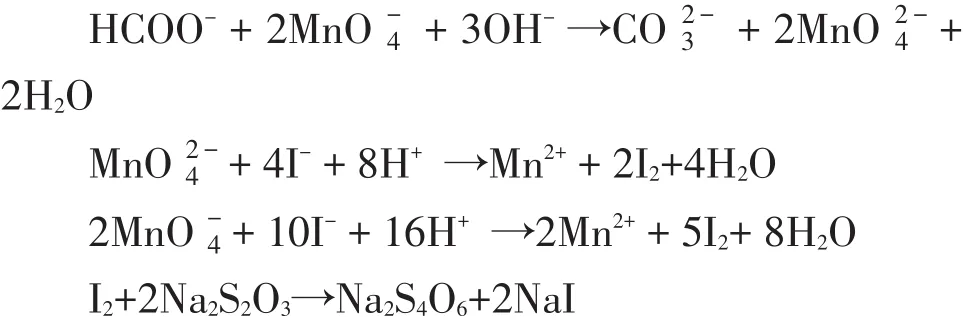
3.2测试条件的确立
根据反应原理可以先确定甲酸根的理论量,然后计算高锰酸钾、氢氧化钠(提供OH-,氢氧化钠在水溶液中完全解离,而碳酸钠解离成OH-与HCO3-)、硫酸(提供H+)、碘化钾(提供I-)以及硫代硫酸钠的使用量,根据检验过程中便于操作等因素确定各药剂的加量及使用浓度,确立试验过程。
准确称取甲酸钾0.84g(分析纯),称准至0.0001 g,置于100mL烧杯中,加蒸馏水溶解,然后转入250 mL容量瓶中加蒸馏水稀释至刻度,摇匀,用移液管量取25mL试液,注入碘量瓶中,准备进行测试;
通过计算得滴定甲酸钾的理论数据为:甲酸钾1mmol、氢氧化钠3mmol、高锰酸钾2mmol、浓硫酸8mmol、碘化钾8mmol、硫化硫酸钠8mmol。
根据计算结果可以确定(为保证各物质加量足够部分物料增加20%):氢氧化钠0.5mol/L×7mL;高锰酸钾0.1mol/L×25mL;浓硫酸2mol/L×5mL;碘化钾1.6g;硫代硫酸钠待定。
在滴定溶液中逐步加入氢氧化钠、高锰酸钾溶液在75±5℃水浴中恒温30min充分反应,反应结束后自然内冷却至室温,加入浓硫酸,碘化钾,充分摇匀,放在阴暗处5min,然后使用0.1mol/L的硫代硫酸钠溶液进行滴定,临近终点时加入1%的淀粉指示剂1mL,继续滴定至溶液蓝色消失。同时作空白试验,计算甲酸钠含量:
甲酸根含量计算公式如下:
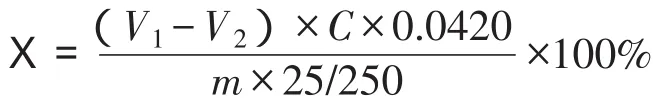
V1——空白试验硫代硫酸钠标准滴定溶液之用量,mL;
V2——滴定试样硫代硫酸钠标准滴定溶液之用量,mL;
C——硫代硫酸钠标准滴定溶液之浓度,mol/L;
m——试样的质量,g;
0.04200——0.5mmol甲酸钾质量g数。
25/250——取样比例。
根据上述计算和分析分别对分析纯的甲酸钾、甲酸钠进行滴定,以确定反应的准确性,实验数据见表1。

表1 分析纯甲酸根含量数据对照表
3.3甲酸根测定研究
根据上述甲酸根确立的测试试验的方法,主要要影响因素如下:OH-、高锰酸钾加入量、H+、I-、反应温度及反应时间的影响。
3.3.1氢氧化钠对甲酸根滴定的影响
固定高锰酸钾0.1mol/L×25mL、浓硫酸2mol/L× 5mL、碘化钾1.6g,改变氢氧化钠0.5mol/L加入量进行甲酸根含量的分析,试验结果见表2:
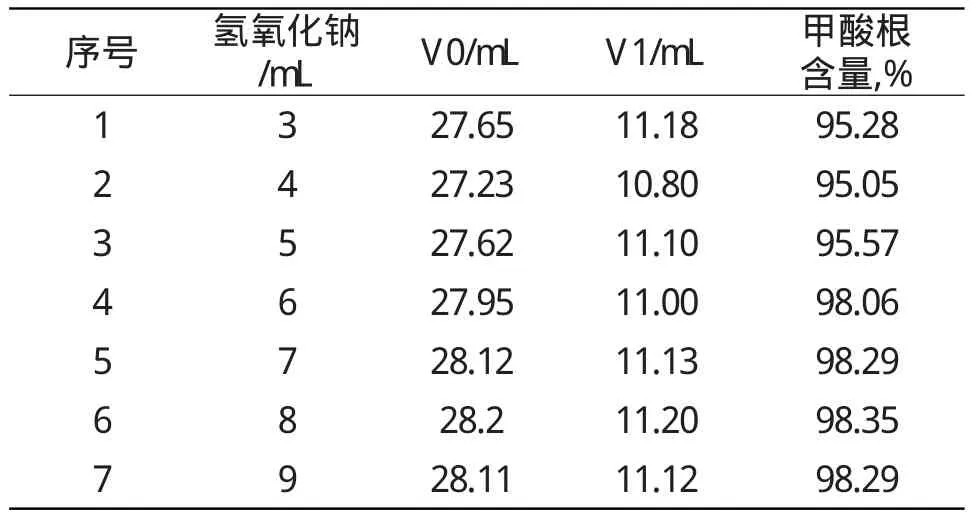
表2 氢氧化钠对甲酸根滴定影响数据表
3.3.2高锰酸钾对甲酸根滴定的影响
固定:氢氧化钠0.5mol/L×7mL、浓硫酸2mol/L× 5mL、碘化钾1.6g,改变高锰酸钾0.1mol/L加入量进行甲酸根含量的分析,试验结果见表3:
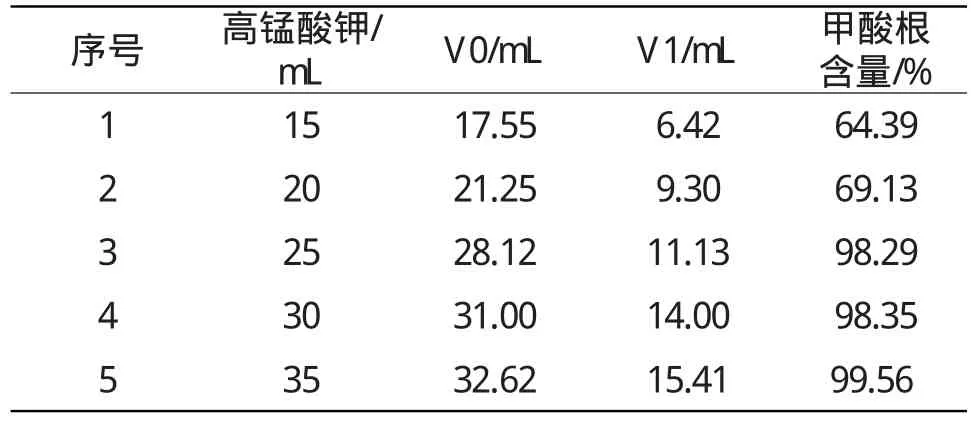
表3 高锰酸钾对甲酸根滴定影响数据表
3.3.3硫酸对甲酸根滴定的影响
固定:氢氧化钠0.5mol/L×7mL、高锰酸钾0.1mol/L×25mL、碘化钾1.6g,改变浓硫酸加入量进行甲酸根含量的分析,试验结果见表4:
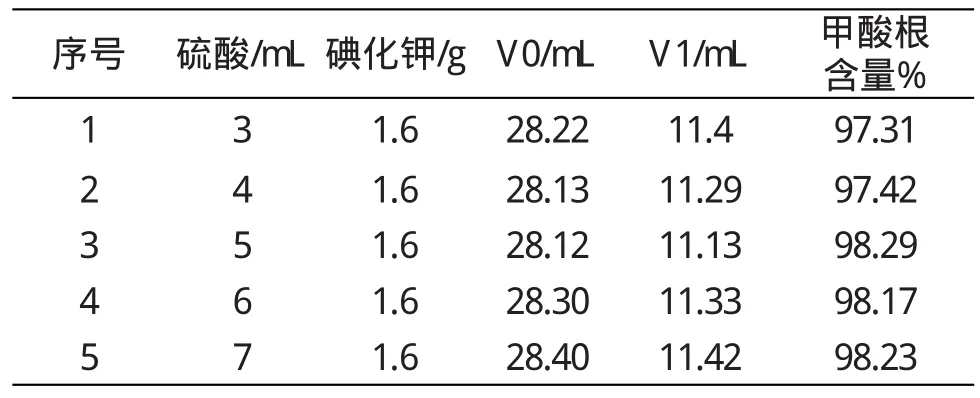
表4 硫酸对甲酸根滴定影响数据表
3.3.4碘化钾对甲酸根滴定的影响
固定:氢氧化钠0.5mol/L×7mL、高锰酸钾0.1mol/L×25mL、浓硫酸2mol/L×5mL,改变碘化钾加入量进行甲酸根含量的分析,试验结果见表5:

表5 碘化钾对甲酸根滴定影响数据表
3.3.5反应时间对甲酸根滴定的影响
固定:氢氧化钠0.5mol/L×7mL、高锰酸钾0.1mol/L×25mL、浓硫酸2mol/L×5mL、碘化钾1.6g,通过改变反应时间进行甲酸根含量的分析,试验结果见表6:

表6 加热反应时间对甲酸根含量的影响
3.3.6反应温度对甲酸根滴定的影响
固定:氢氧化钠0.5mol/L×7mL、高锰酸钾0.1mol/ L×25mL、浓硫酸2mol/L×5mL、碘化钾1.6g,通过改变反应温度进行甲酸根含量的分析,试验结果如表7:
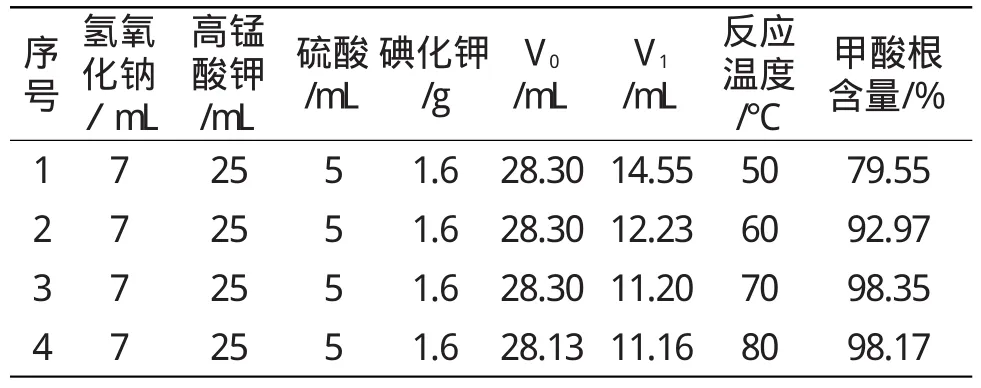
表7 反应温度对甲酸根含量的影响
4 结论
4.1通过试验验证了甲酸根滴定的原理;
4.2确定了氧化还原法中滴定甲酸根的测试条件:氢氧化钠0.5mol/L×7mL、高锰酸钾0.1mol/L×25mL、浓硫酸2mol/L×5mL、碘化钾1.6g、反应温度75±5℃、反应时间为30min。
[1]傅兵.《关于利用酒钢放散转炉煤气生产甲酸钠联产甲酸(钙)、六偏磷酸钠的建议》.酒钢科技,2001,3:12-15.
[2]苏品德.《甲酸钠浓缩、结晶的最佳工况》.云南化工,2000,27 (3):38-40.
[3]张少华,匡云飞,李薇.《新戊二醇副产甲酸钠回收利用工艺》.衡阳师范学院学报,2006,27(3):53-54.
[4]朱进春.《用季戊四醇下脚料甲酸钠生产草酸的新工艺》.湖南化工,2000,30(2):36-37.
[5]杨俊贞,黄达全,张波.甲酸盐含量测定方法研究.钻井液与完井液,2004,21(5):40-42.
[6]刘克清,闫长虹,王蕾,夏小春.钻井液用甲酸盐检测方法的研究,钻井液与完井液,2007,24(增刊):95-97.
10.3969/j.issn.1008-1267.2016.04.019
O657.31
A
1008-1267(2016)04-0055-03
2016-03-24
王仲广,男,工程师,2002年毕业于天津理工学院化工系,主要从事油田化学产品的研究与应用工作。
——硫代硫酸钠

